2. 中国食品药品检定研究院, 北京 100050
2. National Institutes for Food and Drug Control, Beijing 100050, China
辅料是药物制剂的重要组成部分, 其质量的好坏会直接影响到制剂的质量、稳定性和疗效。一致性评价的核心是研究制剂的工艺和处方, 在原料药相同时, 辅料的质量差异和制备工艺就成了仿制药与原研药药效差异的关键因素。因此, 辅料的性质研究对药物的一致性评价具有重要意义[1]。在片剂仿制药的一致性评价中, 不能只注重溶出曲线的一致, 崩解作用同样重要。片剂崩解不单是指崩解时限, 片剂崩解后的粒子形态同样会影响药物释放, 因此研究崩解剂的性质对一致性评价很有必要。羧甲淀粉钠(carboxymethyl starch sodium, CMS-Na)是一种淀粉羧基醚的钠盐, 是用氢氧化钠将淀粉处理成碱性淀粉, 再与氯乙酸反应制得[2], 具有较强的吸水溶胀作用, 是常用的超级崩解剂之一, 在固体制剂中得到广泛应用。目前, 国内外生产羧甲淀粉钠的厂家很多, 但各厂家产品质量不尽相同。Ao等[3]对不同厂家和型号的羟丙甲纤维素和两种羧甲淀粉钠的性能进行研究, 但并未见到对国内外多个厂家不同羧甲淀粉钠的性质比较研究。因此, 本文研究了不同厂家11种羧甲淀粉钠之间的性质差异, 并初步分析各性质差异对片剂崩解造成的影响, 旨在为一致性评价的辅料选择提供参考。
材料与方法材料与仪器 不同厂家羧甲淀粉钠1~11号; 乳糖(lactose, 批号: 20161207, 天津市恒兴化学试剂制造有限公司); 微晶纤维素(microcrystalline cellulose, MCC, 批号: 20170506)、硬脂酸镁(magnesium stearate, 批号: 20170908) (湖州展望药业有限公司); 盐酸(HCl, 批号: 20171220, 天津凯信化学工业有限公司); 磷酸二氢钾(KH2PO4, 批号: 20160713, 天津市科密欧化学试剂有限公司); 氢氧化钠(NaOH, 批号: 20160722, 天津市恒兴化学试剂制造有限公司); 蒸馏水(SZ-93型, 自动双重纯水蒸馏器, 上海亚荣生化仪器厂)。
扫描电子显微镜(Bruker D8 Advance型, Bruker科技有限公司); 激光粒度仪[HELOS (H3313) & RODOS, 德国新帕泰克有限公司]; 孔径检测仪及BET法比表面分析仪(V-Sorb2800型, 北京金埃谱科技有限公司); 智能崩解仪(ZB-1E型, 天津市天大天发科技有限公司)。
粒子形态 采用扫描电子显微镜观察CMS-Na的外观形态, 工作电压15 kV, 工作宽度12.9 mm。
粒径及其分布 采用激光粒度仪测定辅料粒径及其分布[4]。根据公式(1)计算粒径分布宽度(Sp)[5]。
| ${S_{\rm{p}}} = \frac{{\left( {{X_{90}} - {X_{10}}} \right)}}{{{X_{50}}}}$ | (1) |
式中, X90、X50和X10分别表示累计粒径分布图上累计分数90%、50%和10%所对应的粒子直径。
松密度及振实密度 精密称取一定质量的CMS-Na, 通过漏斗匀速倒入已称重的量筒中, 准确记录体积, 计算松密度(ρb); 将量筒以一定频率从一定高度落下, 直到粉末体积不再变化, 记录体积, 粉末质量除以此时体积, 即为振实密度(ρt)。平行测定3次, 并根据公式(2)和公式(3)计算Hausner比(H)和Carr's指数(C)[6]。
| $H = \frac{{{\rho _{\rm{t}}}}}{{{\rho _{\rm{b}}}}}$ | (2) |
| $C\left( {\rm{\% }} \right) = \frac{{{\rho _{\rm{t}}} - {\rho _{\rm{b}}}}}{{{\rho _{\rm{t}}}}} \times 100$ | (3) |
休止角 将干燥过的CMS-Na粉末, 经固定高度的漏斗匀速流至直径为5.8 cm的底座上, 形成对称的圆锥体, 直到圆锥体达到最高为止, 测量圆锥体高度, 计算休止角[7]。平行测定3次。
比表面积 采用BET法测定比表面积[8]。
pH值测定 25 ℃下1%浓度CMS-Na溶液pH值。
干燥失重 精密称取一定量待测粉末, 130 ℃中烘干90 min, 取出加盖放入保干器, 冷却后称重, 计算失重百分率。
取代度 采用铜盐沉淀法[9]测定。
吸湿性 称取适量干燥后的CMS-Na, 平铺在直径为40 mm的量瓶中, 精密称重, 将其放入装有饱和NaCl溶液的保干器中, 控制温度为25 ℃, 湿度为90%。分别在1、2、4、8、12、24、48和72 h取出, 精密称重。平行测定3次[10]。
吸水性 用橡胶软管将垂熔漏斗与移液管相连, 通过垂熔漏斗将水加入装置中, 使移液管中液面与垂熔漏斗底面平行, 再将润湿过的圆形滤纸铺在垂熔漏斗底部, 如图 1。精密称取一定质量的CMS-Na粉末, 均匀倒入垂熔漏斗内, 在相应时间点记录吸水量[11]。平行测定6次。
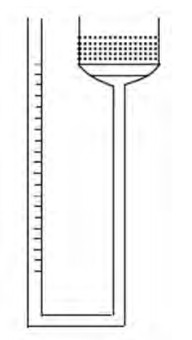
|
Figure 1 Apparatus of water uptake |
溶胀性 精密称取0.1 g样品倒入刻度试管中, 振实后记录体积(V0)。沿试管壁缓慢加入4 mL水, 在相应时间点记录样品溶胀后体积(V)。按公式(4)计算膨胀度(S)[12]。平行测定6次。
| $S = \frac{{V - {V_0}}}{{{V_0}}}$ | (4) |
崩解性能 分别以乳糖和微晶纤维素为填充剂, 按处方:填充剂97.5%、羧甲淀粉钠2%、硬脂酸镁0.5%, 采用单冲压片机, 粉末直接压片。乳糖片片重为200 ± 5 mg, 硬度为3.0 ± 0.5 kg; 微晶纤维素片片重为150 ± 5 mg, 硬度为10.0 ± 1.0 kg。按2015版中国药典规定, 采用吊篮法分别在37 ℃重蒸水、pH 6.8磷酸盐缓冲液(PBS)及0.1 mol·L-1 HCl溶液中测定片剂崩解时间。平行测定6次。
统计学分析 采用SPSS 21软件对松密度、振实密度、Carr's指数、Hausner比及休止角数据进行单因素分析, 所有数据用x ± s表示, 采用独立样本t检验将各产品与1号产品比较。
结果与讨论 1 粒子形态及粒径分布扫描电子显微镜具有分辨率高, 操作方法简单等优点, 能够观察样品表面的凹凸和形状, 以及样品表面的组成分布等。扫描电镜结果见图 2。

|
Figure 2 SEM micrographs of different sources of sodium carboxymethyl starch (CMS-Na). Magnification 400×. 1-11 mean the excipient No |
粒径分布表示不同粒径的粒子在粉体中的分布情况, 能够反映粒子大小的均匀程度, 是考察辅料粉体学性质的重要参数。粒径分布结果见表 1。
| Table 1 The particle size distribution of CMS-Na. X90, X50 and X10 represent the particle diameter corresponding to 90%, 50% and 10% of the cumulative fraction on the cumulative particle size distribution diagram respectively; SMD: Surface average particle diameter; VMD: Volume average particle diameter; Sp: Particle size span |
从显微镜照片和粒径分布可以看出, 1、3、4、9、10和11号粒径较大, 呈椭球形, 其中1、9、10和11号粒子表面光滑饱满, 而3号和4号粒子表面附有细小颗粒, 较粗糙。其余产品粒径较小, 表面粗糙, 且形状不规则, 棱角较多。一般情况下粒径较大, 表面光滑的粉体具有较好的流动性。从粒径分布宽度看, 粒径较大的6种产品粒径分布宽度在1~1.2之间, 粒径分布较均匀。其余5种粒径分布在1.48~1.98之间, 较宽。
粒子大小及形状是影响粉体流动性的重要因素之一。粒径分布较宽时, 小颗粒能够填充到大颗粒的缝隙之间, 空隙率较小, 而空隙率能够显著影响崩解剂的吸水溶胀性能, 致使崩解效果的改变。
2 粉体流动性影响粉体流动性的因素很多。粒子的粒径、密度、粒子形态、表面粗糙度及含水量都会影响粉体的流动[13]。本实验通过测定Carr's指数、Hausner比及休止角等参数评价羧甲淀粉钠粉体流动性, 结果见表 2。当Carr's指数小于20%, Hausner比小于1.2, 休止角小于40°时表示粉体流动性较好[14, 15]。结果显示, 1、3、4、9、10和11号粉体流动性较好, 结合粒子形态分析可知, 这6种产品粒度相对较大, 呈椭球型, 且表面较光滑, 便于流动。
| Table 2 The bulk density, tap density, Carr's index, Hausner ratio and angle of response of CMS-Na. n = 3, x ± s. **P < 0.01, ***P < 0.001 vs excipient No 1 |
1、3、4、9、10和11号产品松密度相对较大, 其余几种产品松密度较小。松密度较小说明相同质量的粉体体积较大, 在相同压力下压片时, 片剂会更致密, 孔隙率更小, 影响水分渗透进片剂内部, 从而影响崩解。
统计学分析结果显示, 在密度、Carr's指数及Hausner比等方面, 几种粒径相对较小的产品与1号相比具有显著性增加(P < 0.01);在休止角方面, 其他所有产品与1号相比均具有极显著性增加(P < 0.001)。
粉体流动性对制剂工艺的混合均匀度和压缩成形性等影响较大, 在片剂压制成形或填充时, 流动性差的粉体往往表面黏结不易分散而影响工艺进程。
3 pH值及干燥失重等理化性质不同来源CMS-Na的比表面积、pH值、干燥失重、取代度及吸湿性等理化性质测定结果见表 3及图 3。
| Table 3 Partial physicochemical properties of CMS-Na |
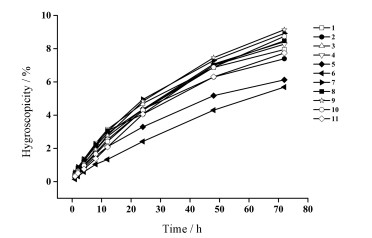
|
图 3 The profiles of hygroscopicity of different sources of CMS-Na |
2015版中国药典规定CMS-Na干燥失重不得超过10%, 1%浓度pH值应在5.5~7.5之间, 11种产品均符合规定。比表面积是表征粉体中粒子粒径的一种量度, 随着粒径的增大而减小。比表面积测定结果与粒径分布结果基本吻合。各CMS-Na产品的取代度不同, 取代度的高低会影响其吸水溶胀性能。取代度增大时, 亲水性基团-CH2COONa相应增多, 水合作用增强, 有利于水向CMS-Na网络结构中渗透, 从而增强吸水溶胀性[16]。
粉体的吸湿性是指固体表面吸附水分的现象。不同CMS-Na之间吸湿性相差较大。一般认为粉体的比表面积增大, 粉体与潮湿空气的有效接触面积也会随之增大, 吸湿速率同样增大。但结果显示比表面积与粉体吸湿性并无直接关系。CMS-Na吸湿后易结块, 且粒子间作用力增大, 影响产品流动性。因此含水量较大或吸湿性较强会直接影响产品质量。
4 吸水性与溶胀性CMS-Na的吸水性与溶胀性是评价其崩解性能的关键指标。本实验考察了不同来源的CMS-Na在重蒸水、pH 6.8 PBS缓冲液及0.1 mol·L-1 HCl溶液中的吸水性与溶胀性, 结果见图 4和图 5。由图可见, 不同来源的CMS-Na吸水溶胀性差异较大, 其中1、3、4、9、10和11号产品吸水性与溶胀性相对较好。
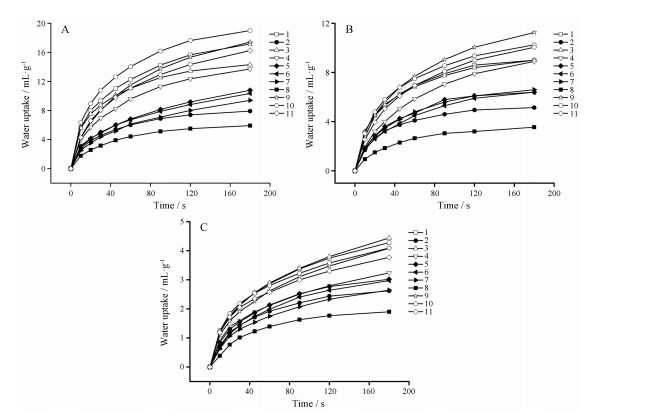
|
Figure 4 The profiles of water uptake over time in different mediums. A: H2O; B: pH 6.8 phosphate buffered solution (PBS); C: 0.1 mol·L-1 HCl solution |

|
Figure 5 The swelling of CMS-Na over time in different mediums. A: H2O; B: pH 6.8 PBS; C: 0.1 mol·L-1 HCl solution |
粒子形状不规则的产品可能是在合成过程中碱性溶液降低了淀粉分子组织的刚性与稳定性, 破坏了淀粉颗粒的结构, 从而导致其吸水溶胀性能降低[14]。
CMS-Na吸水溶胀性能受pH值影响较大, 在水中吸水溶胀性最好, pH 6.8 PBS中次之, 在0.1 mol·L-1 HCl溶液中最差, 这是因为CMS-Na在酸性条件下不稳定, 生成不溶于水的游离酸, 吸水膨胀作用均受到抑制。因此, 以CMS-Na为崩解剂的片剂在酸性条件下可能会崩解较慢。
5 含水量对羧甲淀粉钠吸水性和溶胀性的影响CMS-Na干燥失重在3%~8%之间, 说明其含水量较大, 因此比较烘干前后CMS-Na的吸水性与溶胀性, 考察含水量对其功能性的影响, 结果见图 6和图 7。由图可知, 大部分产品在烘干后的吸水性和溶胀性都要好于未烘干时所测结果, 因为在未烘干时CMS-Na粉末已因吸收少量水分而略微膨胀, 粒子体积变大, 导致其吸水溶胀能力略有下降, 因此在使用前先将CMS-Na烘干可能会有更好的崩解效果。
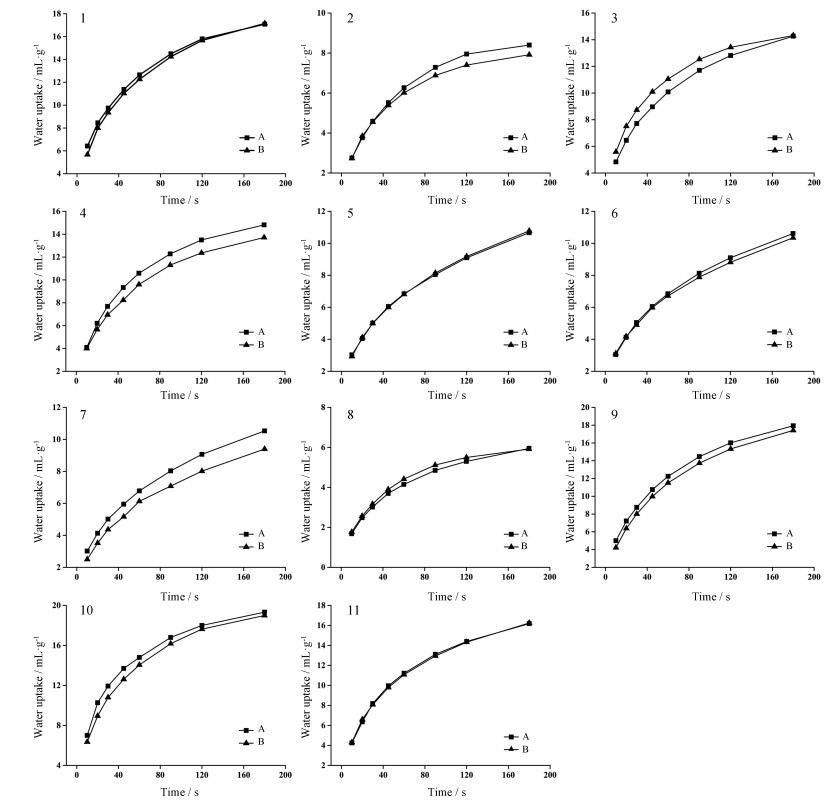
|
Figure 6 Effect of water content on the water uptake of CMS-Na. A: Dried; B: Not dried |

|
Figure 7 Effect of water content on the swelling of CMS-Na. A: Dried; B: Not dried |
分别以微晶纤维素和乳糖为填充剂, 考察不同来源CMS-Na的崩解性能, 结果见图 8。

|
Figure 8 The disintegration time of tablets. A: Microcrystalline cellulose; B: Lactose |
微晶纤维素片在0.1 mol·L-1 HCl溶液中崩解时间均超过4 min。在3种介质中的崩解由快至慢依次是水、pH 6.8 PBS和0.1 mol·L-1 HCl溶液, 与CMS-Na在3种介质中的吸水溶胀性相同。可见微晶纤维素片的崩解主要受CMS-Na功能性的影响。CMS-Na在0.1 mol·L-1 HCl溶液中吸水溶胀性很弱, 因此崩解较慢。不同产品之间比较, 4号与吸水溶胀性较差的2和8号等制备的微晶纤维素片崩解较慢, 而吸水溶胀性较好的产品崩解较快。
大部分乳糖片在3种介质中的崩解由快至慢依次是0.1 mol·L-1 HCl溶液、水和pH 6.8 PBS。而不同产品之间比较, 以吸水溶胀性能较差的5种CMS-Na为崩解剂的乳糖片崩解速度较快, 而用吸水溶胀性较好的1、9和10号等作为崩解剂的乳糖片崩解较慢。可能是因为乳糖亲水性较强, 易溶解, 与吸水性同样较强的CMS-Na混合后, 相互之间产生竞争性抑制, CMS-Na将水吸入自身粒子内部, 延缓了乳糖的溶解, 崩解较慢。CMS-Na在0.1 mol·L-1 HCl溶液中吸水溶胀性差, 对乳糖的竞争作用弱, 因此乳糖片在0.1 mol·L-1 HCl溶液中崩解最快。
由此可知, 片剂的崩解不仅与崩解剂性能有关, 各辅料间的相互作用也会对崩解造成影响。
结论所有产品的pH值和干燥失重均符合2015版中国药典要求; 1、3、4、9、10和11号因其粉体粒径较大, 粒子呈椭球型, 具有较好的粉体流动性, 并且表现出较强的吸水溶胀性能, 可见CMS-Na的粒子形态是影响其功能性的关键因素。但其吸水溶胀性受pH值影响较大, 且片剂崩解不仅与崩解剂性能有关, 辅料之间的配伍作用对片剂崩解影响也很大。
不同来源的CMS-Na性质差异较大, 且对片剂崩解有明显影响, 需要备受关注。其吸水溶胀性及与其他辅料间的相互作用是影响崩解的主要因素。一致性评价不仅只是生产出一批同原研药体内外释放相同的产品, 而是要保证在处方工艺一定的条件下, 能够长期稳定地生产出同原研药一致的产品。由此可见, 在制剂生产中对于崩解剂的选择要固定厂家, 才能保证批间的重现性, 同时这也要求同一厂家不同批次的辅料保证良好的批间重现性。
| [1] |
He ZG. The role of pharmaceutical excipients in the evaluation of the quality and efficacy of generic drugs[J]. China Food Drug Adm Mag (中国食品药品监管), 2018, 9: 44-46. |
| [2] |
Titi CS, Fachrudin R, Ruriani E, et al. Effect of agitation in alkalization process on the characteristics of sodium carboxymethyl sago and cassava starches[J]. IOP Conf Ser Earth Environ Sci, 2018, 147: 12-16. |
| [3] |
Ao LL, Zhang CF, Xu KM, et al. Physical and chemical properties and application effects of several commonly used disintegrants[J]. Guide Chin Med (中国医药指南), 2015, 13: 20-22. |
| [4] |
Yanli W, Wenyuan G, Xia L. Carboxymethyl Chinese yam starch:synthesis, characterization, and influence of reaction parameters[J]. Carbohydr Res, 2009, 344: 1764-1769. DOI:10.1016/j.carres.2009.06.014 |
| [5] |
Jiang JZ. Study on the method of particle size distribution width representation[J]. J Filtr Sep (过滤与分离), 2006, 16: 21-23. |
| [6] |
Yu LF, Hu RF, Su D, et al. Characterization of fluidity of microcrystalline cellulose and visualization of correlation of performance parameters[J]. Acta Pharm Sin (药学学报), 2018, 53: 154-159. |
| [7] |
Chen FC, Han P, Tu JS. Optimization of flow measurement method of microcrystalline cellulose and analysis of influencing factors of fluidity[J]. Prog Pharm Sci (药学进展), 2013, 37: 274-280. |
| [8] |
Han L, Zhang DF, Qin CF, et al. Determination of powder parameters of commonly used excipients in dispersible tablets and effects of micronized silica on disintegration performance of traditional Chinese medicine dispersible tablets[J]. Chin J Hosp Pharm (中国医院药学杂志), 2013, 33: 844-849. |
| [9] |
Zhang JL, Li ZF. Improvement of determination method of carboxymethyl starch substitution degree[J]. Petrochem Ind Appl (石油化工应用), 2006, 25: 30-32. |
| [10] |
Jiang F. Preliminary study on hygroscopic behavior of five kinds of starch-based excipients[J]. Strait Pharm J (海峡药学), 2018, 30: 13-16. |
| [11] |
Kawashima Y, Takeuchi H, Hino T, et al. Low-substituted hydroxypropylcellulose as a sustained-drug release matrix base or disintegrant depending on its particle size and loading in formulation[J]. Pharm Res, 1993, 10: 351-355. DOI:10.1023/A:1018975919598 |
| [12] |
Kowalski G, Ptaszek P. The effect of swelling time on rheological properties of hydrogels, consisting of high-amylose carboxymethyl corn starch and acrylic polymers[J]. Starch, 2016, 68: 381-388. DOI:10.1002/star.201400253 |
| [13] |
Cui FD. Pharmaceutics (药剂学)[M]. Beijing: People's Medical Publishing House, 2015: 99.
|
| [14] |
Lefnaoui S, Moulai-Mostefa N. Synthesis and evaluation of the structural and physicochemical properties of carboxymethyl pregelatinized starch as a pharmaceutical excipient[J]. Saudi Pharm J, 2015, 23: 698-711. DOI:10.1016/j.jsps.2015.01.021 |
| [15] |
Kumar V, Reus-Medina MDLL, Yang D. Preparation, characterization, and tableting properties of a new cellulose-based pharmaceutical aid[J]. Int J Pharm, 2002, 235: 129-140. DOI:10.1016/S0378-5173(01)00995-4 |
| [16] |
Wu KX, Li RQ. Semi-dry synthesis of carboxymethyl starch and discussion on sources of disintegration[J]. Northwest Pharm J (西北药学杂志), 1999, 14: 207-208. |
 2020, Vol. 55
2020, Vol. 55


