2. 呼吸疾病中医药防治省部共建协同创新中心, 河南 郑州 450046
2. Co-construction Collaborative Innovation Center for Chinese Medicine and Respiratory Diseases by Henan & Education Ministry of P. R. China, Zhengzhou 450046, China
姜皮为姜科多年生草本植物姜(Zingiber officinale Roscoe.)的干燥皮质部分[1]。干姜性热、味辛, 归脾、胃、心、肺经, 具有温经散寒, 回阳通脉, 温肺化饮之功[2]; 而姜皮性凉、味辛; 归脾、肺经, 具有行水消肿的功效, 主治水肿初起, 小便不利[3], 两者的性味归经和功效均有所差异[4], 因而干姜是否去皮入药应由病症需求而定。为了明确姜皮的药效物质, 需对姜皮中化学成分进行系统的研究, 本实验采用Diaion HP-20、MCI Gel CHP-20、Sephadex LH-20、ODS、硅胶和半制备高效液相等多种色谱分离技术从姜皮含水乙醇提取物中分离得到7个萜类化合物, 分别是(4R, 6S)-1-(羟甲基)-5, 5-二甲基二环[3.1.1]庚-2-烯-4-醇(1)、4-(羟甲基)-1-(异丙基)-2-烯-3, 4-二醇(2)、3, 5, 6-trihydroxy-7-megastigmen-9-one (3)、3-(3-hydroxybutyl)-2, 4, 4-trimethyl-2, 5-cyclohexadien-1-one (4)、angelicoidenol (5)、grasshopper ketone (6)和dihydrophaseic acid (7)。其中, 其中化合物1、2为新化合物, 化合物3~7均为首次从该植物中得到, 结构见图 1。

|
Figure 1 Structures of compounds 1-7 |
化合物1 黄色油状物。
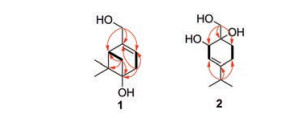
|
Figure 2 1H-1H COSY (  |
化合物2 白色油状物。
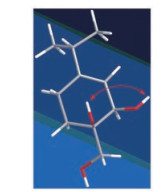
|
Figure 3 Key NOESY ( |
Bruker AVANCE Ⅲ 500型核磁共振仪(TMS内标); Bruker maxis HD型飞行时间质谱(德国布鲁克公司); AB SCIEX Qtrap 5500液质联用仪(美国AB SCIEX公司); Rudolph AP-Ⅳ型旋光仪(美国鲁道夫公司); 赛谱锐思LC50型高压制备液相色谱仪(赛谱锐思北京科技有限公司); Thermo Nicolet IS 10红外光谱仪(上海斯迈欧分析仪器有限公司); Thermo EV0300紫外分光光度计(美国热电公司); Agilent 1260 Infinity ⅡLC高效液相色谱仪(美国安捷伦科技公司); YMC-Pack ODS-A色谱柱(10 mm×250 mm, 5 μm, 12 μm, 日本YMC有限公司); Diaion HP-20、MCI Gel CHP-20 (日本三菱化学公司); Sephadex LH-20 (Pharmacia Biotech公司); GF254硅胶薄层板(青岛海洋化工厂)。分析纯和色谱纯试剂(天津四友精细化学品有限公司)。
姜皮购自于安徽亳州市, 2018年5月产于四川宜宾市, 经河南中医药大学董诚明教授鉴定姜皮为姜科多年生草本植物姜(Zingiber officinale Rosc.)的干燥皮质部分, 实验留样保存在BS630房间, 标本号: JP20180603。
1 提取与分离姜皮40 kg, 50%含水乙醇加热回流提取3次, 每次200 L、2 h, 提取液减压浓缩成稠浸膏状, 稀释到适当浓度后过滤, 上Diaion HP-20大孔吸附树脂柱, 依次用水、10%、30%、50%、70%、95%乙醇梯度洗脱得到6个洗脱组分。其中, 10%组分经乙酸乙酯萃取后得10%乙酸乙酯组分, 通过硅胶柱色谱, 梯度洗脱(二氯甲烷-甲醇)共得到5个组分(Fr.1~Fr.5)。Fr.1通过Sephadex LH-20柱色谱, 等度洗脱(纯甲醇), 得到Fr.1-1~Fr.1-3。Fr.1-3通过半制备液相分离纯化得到化合物1 (15.3 mg)。Fr.2通过半制备液相分离纯化得到化合物2 (4.5 mg)、5 (2.4 mg)、6 (3.5 mg)和7 (2.3 mg)。30%组分通过MCI柱色谱(甲醇-水)共得到6个组分(Fr.A~Fr.F)。Fr.D经硅胶柱色谱, 梯度洗脱(二氯甲烷-甲醇)共得到Fr.D-1~Fr.D-4。Fr.D-1通过Sephadex LH-20柱色谱, 等度洗脱(纯甲醇), 得到Fr.D-1-1~Fr.D-1-3。Fr.4-D-2通过半制备液相分离纯化得到化合物3 (3.7 mg)和4 (2.8 mg)。
2 结构鉴定化合物1 黄色油状物,
| Table 1 1H NMR (500 MHz in CD3OD) and 13C NMR (125 MHz in CD3OD) spectral data of compounds 1 and 2 |
化合物2 白色油状物,
化合物3 无色油状, 易溶于甲醇, ESI-MS [M-H]+ m/z: 241, 茴香醛-浓硫酸显色。1H NMR (500 MHz, CD3OD) δH 7.19 (1H, d, J = 16.0 Hz, H-8), 6.20 (1H, d, J = 16.0 Hz, H-7), 3.78 (1H, m, H-3), 2.30 (3H, s, H-10), 1.65, 2.33 (2H, m, H-4), 1.59, 1.30 (2H, m, H-2), 1.21 (3H, s, H-12), 1.20 (3H, s, H-11), 0.98 (3H, s, H-13); 13C NMR (125 MHz, CD3OD) δC34.7 (C-1), 46.2 (C-2), 63.0 (C-3), 40.0 (C-4), 67.4 (C-5), 69.4 (C-6), 144.0 (C-7), 132.4 (C-8), 198.8 (C-9), 23.7 (C-10), 28.4 (C-11), 26.0 (C-12), 18.6 (C-13)。以上数据与文献[6]报道的3, 5, 6-trihydroxy-7-megastigmen-9-one基本一致。
化合物4 无色油状, 易溶于甲醇, ESI-MS [M+H]+ m/z: 209, 茴香醛-浓硫酸显色。1H NMR (500 MHz, CD3OD) δH 6.95 (1H, d, J = 9.8 Hz, H-3), 6.16 (1H, d, J = 9.8 Hz, H-2), 3.83 (1H, m, H-9), 2.61, 2.40 (2H, m, H-7), 1.90 (3H, s, H-13), 1.60 (2H, m, H-8), 1.29 (6H, s, H-11, 12), 1.24 (3H, d, J = 6.3 Hz, H-10); 13C NMR (125 MHz, CD3OD) δC 187.1 (C-1), 124.6 (C-2), 158.7 (C-3), 40.8 (C-4), 164.1 (C-5), 130.9 (C-6), 26.5 (C-7), 37.3 (C-8), 67.4 (C-9), 21.9 (C-10), 24.5 (C-11), 24.7 (C-12), 10.1 (C-13)。以上数据与文献[7]报道的3-(3-hydroxybutyl)-2, 4, 4-trimethyl-2, 5-cyclohexadien-1-one基本一致。
化合物5 黄色固体, 易溶于甲醇, ESI-MS [M-H]+ m/z: 169, 茴香醛-浓硫酸显色。1H NMR (500 MHz, CD3OD) δH 3.83 (1H, m, H-5), 3.75 (1H, m, H-2), 1.65, 2.25 (2H, m, H-3), 1.30 (1H, s, H-4), 1.30, 1.65 (2H, m, H-6), 1.07 (3H, s, H-10), 0.89 (6H, s, H-8, 9); 13C NMR (125 MHz, CD3OD) δC 51.4 (C-1), 76.4 (C-2), 36.7 (C-3), 53.7 (C-4), 75.9 (C-5), 39.1 (C-6), 48.0 (C-7), 21.7 (C-8), 20.1 (C-9), 13.1 (C-10)。以上数据与文献[8]报道的angelicoidenol基本一致。
化合物6 黄色固体, 易溶于甲醇, ESI-MS [M-H]+ m/z: 223, 茴香醛-浓硫酸显色。1H NMR (500 MHz, CD3OD) δH 5.81 (1H, s, H-8), 4.20 (1H, m, H-3), 2.18, 2.21 (2H, m, H-4), 1.90, 2.18 (2H, m, H-2), 1.35 (9H, s, H-10, 11, 12), 1.14 (3H, s, H-13); 13C NMR (125 MHz, CD3OD) δC 37.0 (C-1), 50.0 (C-2), 64.4 (C-3), 49.7 (C-4), 72.4 (C-5), 120.0 (C-6), 211.5 (C-7), 101.1 (C-8), 200.9 (C-9), 26.5 (C-10), 29.3 (C-11), 32.3 (C-12), 30.8 (C-13)。以上数据与文献[9]报道的grasshopper ketone基本一致。
化合物7 白色固体, 易溶于甲醇, ESI-MS [M-H]+ m/z: 281, 茴香醛-浓硫酸显色。1H NMR (500 MHz, CD3OD) δH 7.98 (1H, d, J = 16.0 Hz, H-4), 6.52 (1H, d, J = 16.0 Hz, H-5), 5.75 (3H, s, H-2), 4.10 (1H, m, H-9), 3.69, 3.79 (2H, m, H-12), 2.08 (3H, s, H-15), 1.72, 2.03 (2H, m, H-8), 1.62 (2H, m, H-10), 1.13 (3H, s, H-14), 0.92 (3H, s, H-13); 13C NMR (CD3OD, 125 MHz) δC 169.6 (C-1), 119.2 (C-2), 151.5 (C-3), 131.8 (C-4), 135.2 (C-5), 83.2 (C-6), 87.8 (C-7), 46.0 (C-8), 66.0 (C-9), 44.5 (C-10), 49.4 (C-11), 77.3 (C-12), 16.4 (C-13), 19.7 (C-14), 21.3 (C-15)。以上数据与文献[10]报道的dihydrophaseic acid基本一致。
| [1] |
Pharmaceutical Administration of the People's Republic of China. National Chinese Medicine Processing Regulations (全国中药炮制规范)[M]. Beijing: People's Medical Publishing House, 1988: 32.
|
| [2] |
Lu CJ, Ou M, Wang NS, et al. Review on the study of chemical composition of ginger[J]. Tradit Chin Drug Res Clin Pharmacol (中药新药与临床药理), 2003, 14: 215-217. |
| [3] |
Liang QG, Zhao B, Meng J, et al. Study on the standardization of drying technology and quality standard of Zingiber officinale Peel[J]. China Pharm (中国药房), 2017, 28: 3106-3109. |
| [4] |
Li TS, Sha FF, Lu XH, et al. DAD-HPLC method for simultaneous determination of gingerols of ginger peel[J]. Food Ind (食品工业), 2016, 37: 281-285. |
| [5] |
Miyazawa M, Suzuki Y, Kameoka H. Biotransformation of (-)-nopol by Glomerella cingulata[J]. Phytochemistry, 1995, 39: 337-340. DOI:10.1016/0031-9422(94)00843-I |
| [6] |
Sun Y, Zhan YC, Sha Y, et al. Norisoprenoids from Ulva lactuca[J]. J Asian Nat Prod Res, 2007, 9: 321-325. DOI:10.1080/10286020600727491 |
| [7] |
Alejandro F, Enrique J, Rachid C, et al. Synthesis of natural oxygenated monocarbocyclic sesquiterpenoids from 6, 7-epoxygeranyl acetate[J]. Tetrahedron, 2000, 56: 6099-6113. DOI:10.1016/S0040-4020(00)00560-3 |
| [8] |
Mahmood U, Singh SB, Thakur RS. Angelicoidenol, a bicyclicmonoterpene from the seeds of Pleurospermum angelicoides[J]. Phytochemistry, 1983, 22: 774-776. DOI:10.1016/S0031-9422(00)86984-8 |
| [9] |
Yan ZH, Han ZZ, Hu XQ, et al. Chemical constituents of Euonymus alatus[J]. Chem Nat Compd, 2013, 49: 340-342. DOI:10.1007/s10600-013-0598-9 |
| [10] |
Cai L, Liu CS, Fu XW, et al. Two new glucosides from the pellicle of the walnut (Juglans regia)[J]. Nat Prod Bioprospect, 2012, 2: 150-153. DOI:10.1007/s13659-012-0009-0 |
 2020, Vol. 55
2020, Vol. 55


