2. 山西广誉远国药有限公司, 山西 太谷 030800;
3. 山西省食品药品检验所, 山西 太原 030006
2. Shanxi Guang Yuyuan Traditional Chinese Medicine Co., Ltd., Taigu 030800, China;
3. Shanxi Food and Drug Inspection Institute, Taiyuan 030006, China
衰老是人机体各组织、器官功能随年龄增长而发生退行性变化的过程[1]。伴随衰老会逐步出现精力不济、抵抗力减弱、行动力迟缓等表现[2, 3]。研究衰老的生理病理变化及抗衰老药物的作用机制可以帮助人们减少或减缓衰老引起的疾病, 提高生活质量。目前研究者从多方面阐释衰老, 主要包括自由基学说、遗传学说、端粒学说、代谢学说等[4], 其中代谢学说越来越得到人们的关注。液质联用(LC-MS)代谢组学技术因其能快速识别生物系统的小分子代谢物而被广泛应用于代谢疾病的研究[5, 6]。
龟龄集始于明代嘉靖年间, 是一种补肾填精、壮阳培本的传统中药制剂, 素有“养生国宝”的美誉[7]。龟龄集全方有28味药组成, 《中国药典》 (2015版)公开了其中的20味药材, 包括红参、鹿茸、海马、枸杞子、丁香、穿山甲、雀脑、牛膝、锁阳、熟地黄、补骨脂、菟丝子、杜仲、石燕、肉苁蓉、甘草、天冬、淫羊藿、大青盐、砂仁, 涵盖植物药、动物药和矿物药。龟龄集具有强身补脑, 固肾补气, 增进食欲的功效。用于肾亏阳弱, 记忆减退, 夜梦精溢, 腰酸腿软, 气虚咳嗽, 五更溏泻, 食欲不振。龟龄集20多味药材中, 有皂苷类、黄酮类、甾体类、挥发油等多种物质成分发挥治疗疾病的作用。其中人参皂苷类Re可以保护中枢神经系统, 改善衰老引起的学习记忆功能障碍; 甘草中的甘草酸及黄酮类化合物能保护神经元、改善神经功能, 促进脑功能恢复。淫羊藿苷及黄酮类可减轻衰老大鼠睾丸生殖细胞DNA损伤, 保护睾丸组织延缓生殖功能衰退; 肉苁蓉可通过调节激素水平改善性功能作用。现代药理研究表明龟龄集能明显改善衰老导致的记忆功能障碍和生殖功能障碍[8, 9]等, 但是其作用机制尚需进一步研究探讨。
课题组前期采用自然衰老大鼠模型证明了龟龄集具有延缓衰老的作用, 为了更全面的探究龟龄集延缓衰老的机制, 采用不同模型相互应证, 本研究选用D-半乳糖致衰老大鼠模型, 并采用旷场实验考察龟龄集的延缓衰老作用, LC-MS代谢组学技术结合多元统计方法分析模型大鼠血清中代谢产物的变化律, 探寻龟龄集延缓衰老的潜在生物标志物, 为龟龄集的作用机制研究提供新的思路。
材料与方法仪器与试剂 Dionex UltiMate 3000超高效液相相色谱及四级杆-静电场轨道阱高分辨质谱联用仪、Xcalibur工作站(美国Thermo Fisher Scientific公司); MX-S可调式混匀仪(美国Scilogex公司); Neofuge13R高速冷冻离心机(力康公司); 大鼠旷场测试箱(100 cm×100 cm×80 cm), 黑色, 25格, 实验室自制; BSA124S电子天平(赛多利斯科学仪器有限公司)。
龟龄集(每粒0.3 g, 批号: 103170714, 山西广誉远国药有限公司, 临用前溶于0.5% CMC-Na中); CMC-Na (批号: 20170915, 国药集团化学试剂有限公司); D-半乳糖(批号: WXBC6583V, Sigma公司); 乙腈(LC-MS级)、甲酸(HPLC级)均购自Thermo Fisher Scientific公司; 纯化水(屈臣氏集团有限公司)。
动物 成年雄性SD大鼠40只, SPF级, 体质量(220 ± 20) g, 购自中国食品药品检定研究院, 动物生产许可证号SCXK (京) 2014-0013, 质量合格证号: 11400500031232。动物饲养温度(23 ± 2) ℃, 相对湿度(50 ± 10) %, 自然昼夜节律光照, 适应1周后进行实验。动物实验获得山西大学伦理委员会批准(SXULL2014032)。
动物分组、造模及给药 40只大鼠按体质量随机分为5组, 每组8只, 分别为空白对照组, 模型组, 龟龄集高(GLJ-H, 150 mg·kg-1)、中(GLJ-M, 75 mg·kg-1)、低(GLJ-L, 37.5 mg·kg-1)剂量组。除空白对照组外其余各组大鼠每日皮下注射300 mg·kg-1的D-半乳糖溶液, 连续8周。造模的同时, 从第5周开始各给药组灌胃给予相应剂量的龟龄集, 5 mL·kg-1, 连续4周, 对照组和模型组同时给予等体积的0.5% CMC-Na。
旷场实验 旷场实验是评价大鼠在新异环境中的自主行为与探究行为的一种常用检测方法[10]。通过分析大鼠空间自主活动及探索能力, 可以反映大鼠的衰老情况。大鼠在给予D-半乳糖8周后进行旷场实验, 将大鼠轻放入旷场箱的中央格中让其自由活动, 先适应1 min, 接着观察大鼠在4 min内的活动情况, 记录大鼠逃离中央格时间, 穿越方格总数和直立次数。同时考虑到旷场实验的3个评价指标之间并非完全独立, 而是有内在联系的, 存在时间的唯一性和排它性, 即同一动物个体在同一时间内只能具有其中的一种行为, 采用秩和比法进行综合得到旷场指数。将大鼠的穿越格数和直立次数从小到大排序并进行编号, 将逃离中央格时间从大到小排序并进行编号, 各大鼠的编号加和得到相应的旷场指数。指数越大表示对应大鼠状态越年轻, 指数越小表示相应大鼠越衰老。
样本收集与制备 样本的收集:实验过程结束后, 用10%的水合氯醛按4 mL·kg-1的剂量对大鼠腹腔注射进行麻醉。经腹主动脉采血, 静置30 min后, 于4 ℃、3 500 r·min-1离心15 min, 吸取上层血清, 分装后, 储存于-80 ℃冰箱备用。
样本的处理:将收集的血清样本置于冰水混合物中解冻, 精密吸取血清100 μL于1.5 mL EP管中, 加入0.1%甲酸乙腈200 μL后涡旋振荡30 s, 在4 ℃下以13 000 r·min-1高速离心15 min, 取上清液于液相小瓶中, 供分析。
质控(QC)样本的制备:分别取上述各大鼠血清样本10 μL进行混合, 按照以上备样方法制备, 作为质控样本。在样本进样分析过程中, 每进8针样品进2针QC样品, 用PCA对QC样本数据进行聚类分析并对8针QC样品分别提取10个离子, 分别计算10个离子的保留时间(tR)和质荷比(m/z)的RSD值, 以监测LC-MS系统稳定性。
LC-MS分析条件
LC-MS分析的液相条件 使用Dionex UltiMate 3000 UHPLC-Q Exactive Orbitrap MS进行数据采集, 采用的色谱柱为Waters ACQUITY UPLC HSS T3色谱柱, 流动相为A (水, 含0.1%甲酸)-B (乙腈, 含0.1%甲酸), 流动相梯度为0~2 min, 2% B; 2~3 min, 2%~35% B; 3~15 min, 35%~70% B; 15~20 min, 70% B; 20~27 min, 70%~98% B; 27~31 min, 98% B; 31~32 min, 98%~2% B; 32~35 min, 2% B。体积流量为0.2 mL·min-1, 进样量为5 μL, 柱温为40 ℃。
LC-MS分析的质谱条件 采用HESI电喷雾离子化方式, 喷雾电压大小为正极3.5 kV, 负极2.5 kV。毛细管温度为320 ℃, 加热器温度为300 ℃, 鞘气体积流量为35 arb, 辅助气体积流量为10 arb。扫描模式为Full Scan/dd-MS2, 采集范围为m/z 100~1 500, 正负离子切换采集模式。分辨率设定为MS Full Scan 35000 FWHM以及MS/MS 17500 FWHM, 碰撞能量为12.5、25和37.5 eV。
LC-MS数据处理 将采集所得的LC-MS/MS数据原始文件导入Compound Discoverer 2.0软件(Thermo Fisher公司, 美国), 以获取匹配和对齐的峰值数据, 设置的参数如下:质量范围100~1 500, 质量偏差5×10-6; 保留时间偏差0.05 min; 信噪比阈值1.5。将峰面积归一化后的数据导入SIMCA-P 14.1 (Umetrics公司, 瑞典)进行分析。
数据统计 旷场数据采用统计学软件SPSS 16.0进行统计分析, 结果以x ± s表示, 通过t检验比较组间差异。液质数据结果运用SIMCA-P 14.1 (Umetrics公司, 瑞典)进行偏最小二乘判别分析(PLS-DA)和正交偏最小二乘判别分析(OPLS-DA)。同时结合S-plot图中的VIP > 1和独立样本t检验的P < 0.05筛选贡献最大的差异性变量并对差异性变量进行鉴定指认, 将得到的差异代谢物数据运用Metabo Analyst 4.0数据库进行代谢通路富集分析。旷场指数和差异代谢物的峰面积通过Metabo Analyst 4.0绘制相关性热图, 采用统计学软件SPSS 16.0进行皮尔森相关系数的计算。
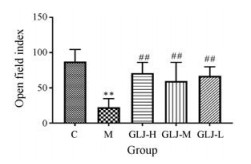
结果 1 龟龄集改善衰老大鼠的旷场测试与空白对照组相比, 模型组大鼠脱毛现象严重, 毛无光泽, 大鼠背部皮肤松弛, 出现倦怠、精神萎靡的状态, 反应力和行动力迟缓, 敏捷性降低。结果显示, 与空白对照组比较, 模型组大鼠穿越格数和直立次数均显著减少(P < 0.01), 逃离中央格时间明显增加, 提示大鼠的运动能力和探索能力下降, 表现出了衰老特征, 造模成功; 给予龟龄集后, 与模型组比较, 龟龄集高剂量组和低剂量组可以显著增加大鼠穿越格数和直立次数, 缩短逃离中央格时间; 龟龄集中剂量组可以显著增加大鼠的穿越格数(表 1)。旷场指数结果表明龟龄集能明显改善D-半乳糖致衰老大鼠的自发运动行为(图 1)。
| Table 1 Effects of Guilingji on open field of D-galactose induced aging rats (n = 8, x ± s). The results of the open field test of control (C), model (M), high dose Guilingji (GLJ-H), medium dose Guilingji (GLJ-M), low dose Guilingji (GLJ-L). **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
|
Figure 1 Open field index results of rats in each group. n = 8, x ± s. **P < 0.01 vs control group; ##P < 0.01 vs model group |
通过QC样本监测LC-MS系统稳定性, 结果显示, QC样品聚集在一起, 10个提取离子tR的RSD为(0.1%~1.64%), m/z的RSD为(3.24×10-7~1.73×10-3)。结果表明本次实验建立的LC-MS分析方法的重复性和稳定性符合大批量血清样本代谢组学的分析要求。
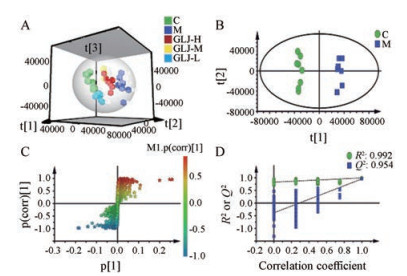
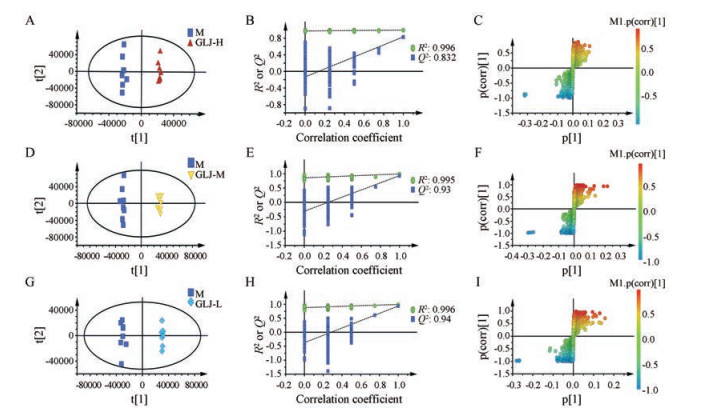
采用UHPLC-Q Exactive Orbitrap MS方法对空白对照组、模型组、不同剂量给药组大鼠血清样品进行检测, 得到各组大鼠的血清代谢数据。运用PLS-DA对各组大鼠血清数据进行代谢轮廓分析(图 2A), 表明衰老使大鼠体内血清代谢轮廓发生了改变。通过对模型组和空白组大鼠血清数据进行OPLS-DA分析, 可见两组明显分离(图 2B)并得到相应的S-plot图(图 2C)以便寻找空白组与模型组的组间内源性差异代谢物。进一步对模型数据进行200次随机排列实验以进行模型验证, 结果表明, R2与Q2参数接近, 模型的斜率稍大且与纵轴的截距为负值, 表明模型未产生过分拟合, 模型可靠(图 2D)。通过OPLS-DA分析对各给药组分别和模型组的血清样本数据进行代谢轮廓分析(图 3), 表明与模型组相比, 给予龟龄集后使大鼠体内血清代谢轮廓发生了改变。
|
Figure 2 PLS-DA scatter plot of serum from all rats (A) and OPLS-DA scatters plot (B), corresponding S-plot (C), corresponding validation plot of serum of rats in control and model groups (D) |
|
Figure 3 OPLS-DA scatters plot (A), corresponding validation plot (B) and corresponding S-plot (C) of serum of rat serum from model and GLJ-H; OPLS-DA scatters plot (D), corresponding validation plot (E) and corresponding S-plot (F) of serum of rat serum from model and GLJ-M; OPLS-DA scatters plot (G), corresponding validation plot (H) and corresponding S-plot (I) of serum of rat serum from model and GLJ-L |
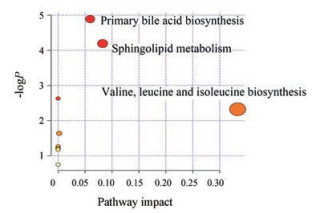
通过对模型和空白组代谢物数据进行OPLS-DA分析, 参考HMDB数据库并结合二级碎片离子进行鉴定指认, 找到与衰老相关的23个差异变量(表 2)。使用回调率(regulatory ratio)来表示龟龄集对衰老大鼠的回调效果, 回调率= (给药组的平均峰面积-模型组的平均峰面积) / (空白组的平均峰面积-模型组的平均峰面积)×100%。龟龄集高剂量组可以回调其中的16个物质, 回调率超过40%的有7个物质; 龟龄集中剂量组可以回调16个物质, 回调率超过40%的有8个物质; 龟龄集低剂量组对16个物质有回调, 回调率超过40%的有9个物质; 给药组与模型进行OPLS-DA分析并筛选与药效相关的显著回调的有神经鞘氨醇、胆酸、棕榈酰鞘磷脂和大麻隆4个物质。表明龟龄集对衰老大鼠的血清代谢轮廓具有一定的调控作用。采用Metabo Analyst数据库对差异代谢物进行代谢通路分析(图 4), 结果显示衰老主要涉及了原发性胆汁酸生物合成(primary bile acid biosynthesis)、鞘脂代谢(sphingolipid metabolism)和缬氨酸, 亮氨酸和异亮氨酸的生物合成(valine, leucine and isoleucine biosynthesis)。其中龟龄集主要回调其中的胆汁酸合成和鞘脂代谢两条通路。
| Table 2 Differential metabolites in serum of aging rats induced by D-galactose. ↑-up-regulated metabolite ↓-down-regulated metabolite; *P < 0.05 |
|
Figure 4 MetPA analysis of metabolic pathway |
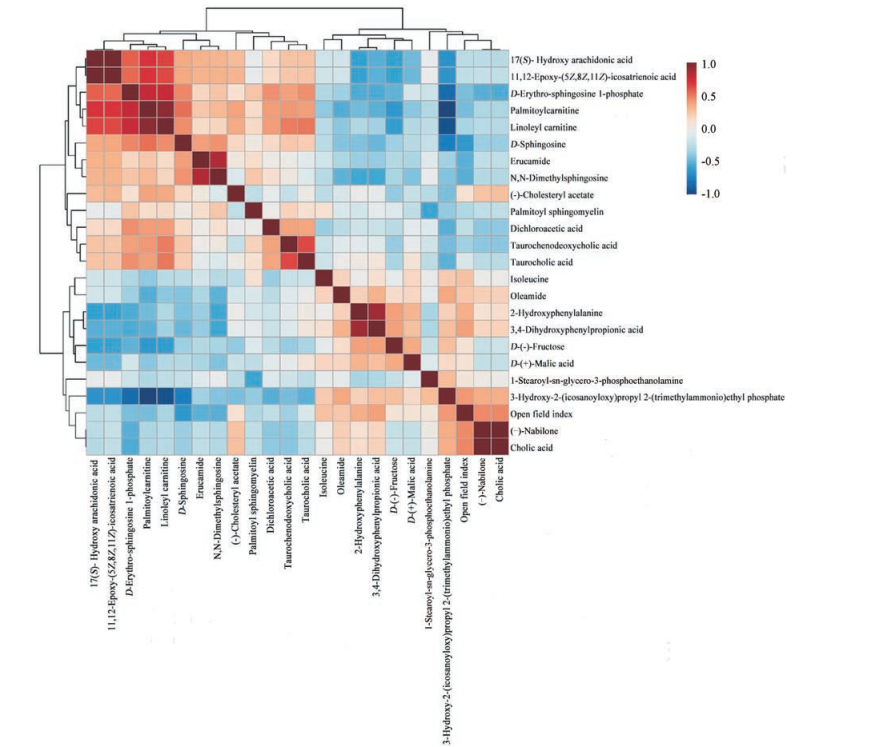
对旷场指数和差异代谢物进行皮尔森相关性分析(图 5), 比较相关系数r得到相关性最大的前两个物质是神经鞘氨醇(r = -0.511 9; P = 0.000 7)和胆酸(r = 0.501 7; P = 0.000 9)。这两种物质是龟龄集可显著回调的物质, 进一步验证了龟龄集可以通过影响鞘氨醇和胆酸来延缓衰老。
|
Figure 5 Correlation analysis between open field index and differential metabolites in rats |
随着年龄的增长, 机体功能逐渐发生退行性改变。本次实验通过连续给大鼠注射大剂量的D-半乳糖致衰老模型来研究龟龄集延缓衰老的药理作用机制, 该模型机制是使机体的细胞内半乳糖浓度增高, 在醛糖还原酶的催化下, 还原成半乳糖醇, 这种物质不能全部被细胞进一步代谢, 而堆积在细胞内, 影响了正常渗透压, 细胞发生膨胀, 引起机体多器官、多系统的功能障碍, 最终导致了衰老的发生[11]。该模型的特点是造衰老模型时间短、操作简单、重复性好, 表现出与自然衰老动物相似的衰老体征, 已成为国内较公认的衰老动物模型[12]。因此, 本次实验采用了D-半乳糖致衰老模型、旷场实验及代谢组学技术来探究龟龄集延缓衰老的机制。
旷场实验是用于评价实验动物自主活动及探索能力的经典方法。穿越格数可以用于反映大鼠自主活动能力, 直立次数可以反映大鼠的空间探索能力及好奇心的强弱, 逃离中央格时间反映大鼠对新环境的恐惧程度[13-15]。除此还构建了旷场指数来对大鼠自主活动行为进行综合评价[16]。通过分析大鼠空间自发运动, 来反映大鼠的衰老情况。代谢组学是对某一生物或细胞内所有低分子量代谢产物同时进行定性和定量分析的一门学科[17]。和基因组学和蛋白质组学相比, 代谢组学可以告诉我们确实发生了什么。代谢组学的整体性优势可以对内源性代谢物进行整体评价, 全面反映机体代谢物的变化。本次代谢结果显示衰老主要涉及的途径有鞘脂代谢、原发性胆汁酸生物合成和缬氨酸、亮氨酸和异亮氨酸的生物合成。
鞘脂包括鞘磷脂、脑苷脂以及神经节苷脂。鞘磷脂及其代谢产物如神经酰胺、鞘氨醇、1-磷酸鞘氨醇是一类重要的具有生物活性的信号分子, 它们参与调节细胞的生长、分化、衰老和死亡等许多重要信号转导过程[18]。鞘脂代谢开始于内质网, 由丝氨酸和棕榈酸缩合产生3-酮-二氢鞘氨醇, 进一步生成神经鞘氨醇, 并继续通过连续的酶促反应导致神经酰胺的合成。神经酰胺减少的累积是致病的, 有研究发现降低的神经酰胺水平与自噬和细胞内α-突触核蛋白积累受损有关, 而自噬受损和细胞内α-突触核蛋白积累会导致衰老的发生[19, 20]。鞘氨醇可以抑制细胞存活、促进细胞凋亡。而经鞘氨醇激酶催化鞘氨醇磷酸化生成的1-磷酸鞘氨醇则可以促进细胞的存活和增殖。给予D-半乳糖后, 鞘氨醇含量显著增加, 促进细胞凋亡造成了衰老模型。给予龟龄集后通过调节鞘氨醇含量调控鞘脂代谢通路来延缓衰老。龟龄集可能通过增加自噬减少核蛋白积累延缓衰老。
胆汁酸是肝细胞内胆固醇的转化产物, 由肝细胞分泌并经胆道系统排入肠内。胆汁酸作为一种信号分子通过激活肝、肠道和外周组织中的胆汁酸受体影响体内葡萄糖和脂质的代谢平衡, 对于调节肥胖、非酒精性脂肪肝等代谢性疾病具有非常重要的意义[21, 22]。过氧化物酶体有助于胆汁酸、胆固醇和缩醛磷脂生物合成。目前研究表明过氧化物酶体功能随着衰老而下降, 过氧化物酶体功能障碍与多种年龄相关疾病(包括神经退行性疾病)的早期发病有关, 过氧化物酶功能障碍可能会阻碍胆汁酸的合成。胆汁酸的合成有两条途径, 分别是经典合成途径和替代途径。有研究者提出机体-胆汁酸-肠道微生物-代谢性疾病间形成的网络是胆汁酸对代谢性疾病调控的重大突破[23]。因此, 龟龄集通过调节胆酸含量调控胆汁酸代谢紊乱。提示龟龄集可能对体内的葡萄糖和脂质的代谢以及肠道菌群代谢的平衡有调控作用。
支链氨基酸包括亮氨酸、异亮氨酸、和缬氨酸, 是人体内重要的必需氨基酸。支链氨基酸(BCAAs)对运动来说是最重要和最有效的营养补充剂[24]。支链氨基酸(缬氨酸、亮氨酸、异亮氨酸)组成几乎1/3的肌肉蛋白[25]。由D-半乳糖致衰老大鼠血清中异亮氨酸的含量显著降低, 体内氨基酸含量降低, 这可能会使机体肌肉生成来源不足, 机体出现旷场穿越格数减少, 直立次数减少。给予龟龄集后, 体内氨基酸含量增加, 大鼠自主活动能力增强。提示龟龄集可以调节氨基酸代谢延缓衰老。
本次实验通过分析旷场实验, 采用LC-MS技术对龟龄集延缓衰老的机制进行了研究, 结果显示龟龄集能显著改善衰老大鼠的自主活动能力, 并通过代谢组学分析共找到23个潜在生物标志物, 主要涉及3条代谢通路, 分别为原发性胆汁酸生物合成、鞘脂代谢和缬氨酸、亮氨酸和异亮氨酸的生物合成。本次实验只采用了代谢组学技术, 下一步关于衰老的机制深入研究将考虑通过多技术, 多组学综合分析进行解释, 也考虑引用同位素示踪法定位体内物质来追踪代谢过程[26-29]。借助稳定同位素示踪技术, 对生物体内所有代谢物的定量分析, 进一步寻找代谢物与疾病的对应关系, 深入解释疾病的发生及药物的作用路径。
| [1] |
Chang YF, Gong WX, Zheng YH, et al. Urinary metabolomics study of the effects of Scutellaria baicalensis Georgi ethanol extract on D-galactose-induced rats[J]. Acta Pharm Sin (药学学报), 2016, 51: 86-92. |
| [2] |
Cheng ZH, Dun YY, Liu J, et al. Effect of total saponins of Panax japonicus on improving colon inflammation in aged rats[J]. Chin Tradit Pat Med (中成药), 2019, 41: 678-681. |
| [3] |
Miao MS, Peng MF, Liu BS, et al. Effect of Schisandrae Chinensis Fructus powder on D-galactose-induced aging model mice[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 3074-3081. |
| [4] |
Pang YY, Qin XM, Du GH, et al. Research progress on pharmacological effects and mechanisms of flavonoids from Scutellaria baicalens based on aging hypotheses[J]. Chin Tradit Herb Drugs (中草药), 2019, 50: 3207-3216. |
| [5] |
Du K, Gao XX, Feng Y, et al. Effects of Guilingji on Kidney-Yang Deficiency syndrome in rats based on serum metabolomics[J]. Acta Pharm Sin (药学学报), 2019, 54: 1476-1483. |
| [6] |
Liang ML, Zhao F, Fang Y, et al. Hippocampus metabolomic research on antidepressant mechanism of petroleum ether fraction of Bupleuri Radix by LC-MS in rats[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 2291-2301. |
| [7] |
Shi JC, Zhang JJ, Gao XX, et al. Construction of inorganic elemental fingerprint and principal component analysis of Guilingji Capsule[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 3619-3624. |
| [8] |
Zhao SJ, Zhao XZ, Liu HL, et al. Effects of Guilingji on improving learning and memory dysfunction caused by aging[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 5352-5357. |
| [9] |
Zhao XZ, Zhao SJ, Tian JS, et al. Research progress on material basis of Guilingji based on pharmacodynamical effect[J]. Chin Tradit Herb Drugs (中草药), 2017, 48: 1424-1431. |
| [10] |
Zhang T, Zhao F, Zhang X, et al. Antidepressant effect of Compound Chaigui prescription and its mechanism of regulating 5-HT metabolic pathway[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 1338-1344. |
| [11] |
Zhao FF, Zhou YZ, Gao L, et al. Advances in the study of the rat model of aging induced by D-galactose[J]. Acta Pharm Sin (药学学报), 2017, 52: 347-354. |
| [12] |
Zhao FF, Li X, Gao Li, et al. Liver metabolomics study of effects of Glycyrrhizae Radix et Rhizoma extracts on D-galactose-induced rats[J]. Chin Tradit Herb Drugs (中草药), 2017, 48: 3545-3553. |
| [13] |
Song J, Pang YY, Gao L, et al. Effects of Scutellaria baicalensis Georgi flowers on D-galactose induced aging in rats based on serum metabolomics[J]. Acta Pharm Sin (药学学报), 2019, 54: 533-539. |
| [14] |
Zhang T. Study on the Anti-Depression Mechanism of Extract of Chaiguifang (柴归方提取物抗抑郁作用机制研究)[D]. Taiyuan: Shanxi University, 2018. http://cdmd.cnki.com.cn/Article/CDMD-10108-1018312204.htm
|
| [15] |
Lu TF, Yu ZS, Yao L, et al. Behaviour on effect of herb pair of Bupleuri Radix and Paeoniae Alba Radix in chronic unpredictable mild stress depression model of rats[J]. Chin Tradit Herb Drugs (中草药), 2016, 47: 2137-2141. |
| [16] |
Qu P. Intervention of Different Xiaoyao Pills on Rat Model of Liver Depression and Spleen Deficiency Syndrome (不同处方逍遥丸对肝郁脾虚证大鼠的干预效果研究)[D]. Taiyuan: Shanxi Medical University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10114-1013224147.htm
|
| [17] |
Liu SB, Xu T, Gao Y, et al. 1H-NMR metabolomics analysis of changes of serum metabolites in rats with depression induced by Compound Chaigui Prescription[J]. Chin Tradit Herb Drugs (中草药), 2019, 50: 97-103. |
| [18] |
Huby E, Napier JA, Baillieul F, et al. Sphingolipids:towards an integrated view of metabolism during the plant stress response[J]. New Phytol, 2019. DOI:10.1111/nph.15997 |
| [19] |
Indellicato R, Trinchera M. The link between Gaucher disease and Parkinson's disease sheds light on old and novel disorders of sphingolipid metabolism[J]. Int J Mol Sci, 2019. DOI:10.3390/ijms20133304 |
| [20] |
Snider JM, Luberto C, Hannun YA, et al. Approaches for probing and evaluating mammalian sphingolipid metabolism[J]. Anal Biochem, 2019, 575: 70-86. DOI:10.1016/j.ab.2019.03.014 |
| [21] |
Gual-Grau A, Guirro M, Mayneris-Perxachs J, et al. Impact of different hypercaloric diets on obesity features in rats:a metagenomics and metabolomics integrative approach[J]. J Nutr Biochem, 2019, 71: 122-131. DOI:10.1016/j.jnutbio.2019.06.005 |
| [22] |
Zhang DY, Zhu L, Liu HN, et al. The protective effect and mechanism of the FXR agonist obeticholic acid via targeting gut microbiota in non-alcoholic fatty liver disease[J]. Drug Des Dev Ther, 2019, 13: 2249-2270. DOI:10.2147/DDDT.S207277 |
| [23] |
Zhang J, Deng ZY, Wu X. Regulation of bile acids on metabolic diseases[J]. Chin J Biochem Mol Biol (中国生物化学与分子生物学报), 2019, 35: 399-403. |
| [24] |
Directo D, Wong MWM, Elam ML, et al. The effects of a multi-ingredient performance supplement combined with resistance training on exercise volume, muscular strength, and body composition[J]. Sports (Basel), 2019. DOI:10.3390/sports7060152 |
| [25] |
Gil Hernández Á. Muscle, metabolic paradigm in nutritional recovery[J]. Nutr Hosp, 2019, 36: 4-11. |
| [26] |
Fan TWM, Bruntz RC, Yang Y, et al. De novo synthesis of serine and glycine fuels purine nucleotide biosynthesis in human lung cancer tissues[J]. J Biol Chem, 2019, 294: 13464-13477. DOI:10.1074/jbc.RA119.008743 |
| [27] |
Engelen MPKJ, Ten Have GAM, Thaden JJ, et al. New advances in stable tracer methods to assess whole-body protein and amino acid metabolism[J]. Curr Opin Clin Nutr Metab Care, 2019, 22: 337-346. DOI:10.1097/MCO.0000000000000583 |
| [28] |
Cordes T, Metallo CM. Quantifying intermediary metabolism and lipogenesis in cultured mammalian cells using stable isotope tracing and mass spectrometry[J]. Methods Mol Biol, 2019, 1978: 219-241. |
| [29] |
Ling HT, Liu SB, Gao Y, et al. Applications progress of stable isotopic tracer technique in metabolic regulation of endogenous substances[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 2678-2685. |
 2020, Vol. 55
2020, Vol. 55


