2. 河南中医药大学药学院, 河南 郑州 450046;
3. 陕西中医药大学, 陕西省中医药管理局中药配伍重点研究室, 陕西 西安 712046
2. Henan University of Chinese Medicine, Zhengzhou 450046, China;
3. Key Laboratory of Shaanxi Administration of Traditional Chinese Medicine for TCM Compatibility, Shanxi University of Chinese Medicine, Xi'an 712046, China
血瘀证临床表现各异, 涉及病种很多, 如心脑血管疾病、外周血管疾病等, 但一般均有血液“浓黏凝聚”的倾向, 这些表现主要与常规检测指标如血液流变学、凝血功能和血小板功能等密切相关。近年来, 随着血瘀证的研究不断深入, 人们对血瘀证的认识也在不断深化, 发现血瘀证与血管内皮细胞产生的多种血管活性物质(如花生四烯酸代谢物、抗凝系统、纤溶系统指标等)和表达于内皮细胞上的黏附分子即内皮细胞黏附分子的表达等也有密切关系[1, 2]。现代学者对血瘀的诊断标准除血液流变学异常外, 还有纤溶活性降低或血液凝固性增高等。而血瘀则血液运行不畅, 易导致血栓形成和血管栓塞等。
当归-川芎配伍是临床常用理血药类活血药对, 课题组前期已经基于急性血瘀大鼠模型, 研究了该药对对急性血瘀大鼠血液流变学、凝血功能和血小板聚集的影响, 发现当归-川芎配伍可协同增强活血化瘀功效[3, 4]。有研究者对活血化瘀药的药理作用进行归纳发现, 该类药物除具有改善血流动力学和凝血功能外, 还可抗血栓形成, 其可能通过对血小板聚集、纤溶酶活性和黏附分子表达等多个环节相关指标的调节发挥作用[5-7]。在对血瘀证发病机制和活血化瘀药的药理作用深入认识的基础上, 为了更全面认识当归-川芎药对治疗血瘀证过程中对血管活性物质(花生四烯酸代谢物、抗凝-纤溶系统指标)和内皮细胞黏附分子表达的影响, 本文采用偏最小二乘判别法(partial least squares discrimination analysis, PLS-DA)结合多指标综合指数法研究该药对对急性血瘀大鼠血清中花生四烯酸代谢物、纤溶系统指标和黏附分子表达等的影响, 为进一步深入探讨该药对及其相关方药治疗和血瘀相关疾病的药效和作用机制奠定扎实基础。
材料与方法动物 SPF级雌性SD大鼠, 体质量180~220 g, 购自北京维通利华实验动物技术有限公司, 许可证号: SCXK (京) 2016-0011。动物实验前适应性饲养1周。实验方案经河南中医药大学第一附属医院动物实验伦理委员会批准, 所有程序均严格按照动物使用和护理的伦理原则进行。
试剂与仪器 大鼠前列环素(prostacyclin I2, PGI2)、6酮前列腺素F1α (6-keto-prostaglandin F1α, 6-keto-PGF1α)、血栓素A2 (thromboxane A2, TXA2)、血栓素B2 (thromboxane B2, TXB2)、蛋白C (protein C, PC)、纤溶酶原(plasminogen, PLG)、组织型纤溶酶原激活剂(tissue-type plasminogen activator, t-PA)、纤溶酶原激活物抑制因子1 (plasminogen activator inhibitor type-1, PAI-1)、抗凝血酶Ⅲ (antithrombin III, AT-Ⅲ)、细胞间黏附分子1 (intercellular adhesion molecule-1, ICAM-1)和血管内皮细胞黏附分子1 (vascular cell adhesion molecule 1, VCAM-1)试剂盒均购自上海酶联生物科技有限公司(批号均为201708)。酶标仪(型号Multiskan FC, 赛默飞世尔科技公司)。
药物及其制备 当归为伞形科植物当归Angelica sinensis (Oliv.) Diels的干燥根(甘肃, 批号16120104);川芎为伞形科植物川芎Ligusticum chuanxiong Hort的干燥根茎(四川, 批号16110201)。当归、川芎饮片均购自郑州瑞龙制药股份有限公司, 经检测, 均符合《中国药典》 2015年版一部项下标准。按照前期样品制备方法[3]得到当归-川芎药对(Danggui-Chuanxiong herb pair, GX)不同配比(1︰0、3︰2、1︰1、2︰3、0︰1)的水提物(water extract, W)、醇提物(alcohol extract, A)和先水提后醇提物(water-alcohol extract, WA)样品, 其中, W浸膏生药含量分别为1.09、0.97、0.83、0.97和0.89 g·g-1, A浸膏生药含量分别为1.22、1.13、1.28、1.45和1.34 g·g-1, WA浸膏生药含量分别为0.98、1.13、0.92、1.21和1.37 g·g-1。
急性血瘀大鼠模型制备[8] 将大鼠皮下(subcutaneous injection, sc)给予盐酸肾上腺素注射液0.8 mg·kg-1后2 h, 将大鼠置于0~2 ℃冰水中游泳4 min, 第一次给予盐酸肾上腺素注射液后4 h再次进行皮下注射盐酸肾上腺素注射液0.8 mg·kg-1, 造成大鼠急性血瘀模型。
动物分组及给药 将大鼠随机分为17组, 每组8只。正常组、模型组和归芎药对5个配比(1︰0、3︰2、1︰1、2︰3、0︰1)的3种提取物给药组。给药组均按照临床等效量的5倍量(8.10 g·kg-1)进行灌胃(ig)给药。正常组和模型组大鼠ig给予等体积的生理盐水。每日早晚8:00各灌胃给药1次, 于第3天4:00 pm将模型组和给药组按照急性血瘀大鼠模型制备方法造模。
样品采集和指标检测 造模结束后将大鼠禁食不禁水饲养12 h, 最后一次灌胃给药, 30 min后用10%水合氯醛进行麻醉, 腹主动脉取血, 室温静置1 h后3 000 r·min-1离心10 min, 分装上层血清8份, 每份200 μL。将各指标按照ELISA试剂盒说明书进行操作, 最后采用酶标仪进行吸光度(A)值检测。
数据统计与分析 实验数据采用SPSS v20.0软件中的描述性分析(descriptives)进行统计, 实验结果采用均值±标准差(x ± s)表示; 与模型组比较, 采用软件中方差分析(analysis of variance, ANOVA)中Dunnett法进行比较, P < 0.05表示差异具有统计学意义; 采用斯皮尔曼相关性分析方法(Spearman)对各指标的相关性进行分析。
效应整合 首先对花生四烯酸代谢物、抗凝-纤溶系统指标和内皮细胞黏附分子相关指标进行标化, 当模型组指标值(value, V)高于正常组值时, V标化= (V模型-V给药)/V模型; 当V模型低于V给药时, V标化= (V给药-V模型)/V模型。然后将所有指标的源数据导入SIMCA v13.0软件中, 采用帕雷托(Pareto)规格化处理模式进行PLS-DA分析, 得到各样品的得分图(score plot)、各指标的S-plot载荷图(loading plot)和变量重要性投影值(variable importance in projection, VIP), 依据各指标的VIP值大小, 结合查阅到的各指标在血瘀相关报道文献数量累积值综合赋予权重系数, 总效应值即为各指标的标化值乘以权重系数后的加和值。
结果 1 当归-川芎药对对急性血瘀大鼠血清中花生四烯酸主要代谢物的影响与正常组比较, 模型组的大鼠血清中PGI2和6-keto-PGF1α与TXB2的比值(PGF/TXB2)均显著降低(P < 0.01), TXB2和TXA2均显著升高(P < 0.05), 6-keto-PGF1α降低, 但无统计学意义。与模型组比较, GX 1︰1_W组、GX所有配比_A组和GX (1︰0、3︰2、2︰3、0︰1)_WA组的大鼠血清中PGI2含量均显著升高(P < 0.05); GX 1︰1_W组、GX (1︰0、3︰2、1︰1、2︰3)_A组和GX所有配比_WA组中TXA2均显著降低(P < 0.05); GX (1︰0、2︰3)_W组、GX (3︰2、1︰1、0︰1)_A组和GX (1︰0、3︰2、2︰3、0︰1)_WA组中6-keto-PGF1α含量均显著升高(P < 0.05); GX 1︰1_W组、GX (1︰0、3︰2、2︰3、0︰1)_A组和GX (1︰0、3︰2、1︰1)_WA组中TXB2均显著降低(P < 0.05); GX (1︰0、1︰1、0︰1)_W组、GX所有配比_A组及WA组中PGF/TXB2均显著升高(P < 0.05)。结果见表 1。
| Table 1 Effect of Danggui-Chuanxiong (GX) herb pair on the main metabolites of arachidonic acid in the serum of acute blood stasis in rats (x ± s). #P < 0.05, ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs model group. W: Water extract; A: Alcohol extract; WA: Water-alcohol extract; PGI2: Prostacyclin I2; TXA2: Thromboxane A2; 6-keto-PGF1α: 6-Keto-prostaglandin F1α; TXB2: Thromboxane B2 |
与正常组比较, 模型组的大鼠血清中PC、PLG、t-PA和AT-Ⅲ的含量均显著降低(P < 0.05); PAI含量显著升高(P < 0.05)。与模型组比较, GX 2︰3_W组和GX (1︰0、3︰2、2︰3)_A组的大鼠血清中PC含量均显著升高(P < 0.05); GX (3︰2、2︰3)_A组和GX (1︰0、3︰2、1︰1、0︰1)_WA组大鼠血清中PLG均显著升高(P < 0.05); GX (1︰0、3︰2、1︰1、0︰1)_W组、GX (1︰0、1︰1)_A组和GX 2︰3_WA组中t-PA含量均显著升高(P < 0.05); GX 2︰3_A组和GX 1︰1_WA组中PAI含量均显著降低; GX (1︰0、0︰1)_W组、GX (1︰0、1︰1)_A组和GX所有配比_WA组中AT-Ⅲ含量均显著升高(P < 0.05)。结果见表 2。
| Table 2 Effect of GX herb pair on anticoagulation and fibrinolysis indicators in the serum of acute blood stasis in rats (x ± s). #P < 0.05, ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs model group. PC: Protein C; PLG: Plasminogen; t-PA: Tissue-type plasminogen activator; PAI: Plasminogen activator inhibitor type; AT-Ⅲ: Antithrombin Ⅲ |
与正常组比较, 模型组的大鼠血清中ICAM-1和VCAM-1含量均显著升高(P < 0.05)。与模型组比较, GX (1︰0、0︰1)_W组、GX (1︰1、2︰3)_A组和GX (3︰2、1︰1、2︰3)_WA组的大鼠血清中ICAM-1含量均显著降低(P < 0.05); GX 1︰1_A组和GX (2︰3)_WA组中VCAM-1含量均显著降低(P < 0.05)。结果见图 1。

|
Figure 1 Effects of GX herb pair on the expressions of adhesion molecules intercellular adhesion molecule-1 (ICAM-1) and vascular cell adhesion molecule 1 (VCAM-1) in acute blood stasis rats. n was same as Table 1. *P < 0.05 vs M. M: Model group; C: Control group; • Represents outlier values |
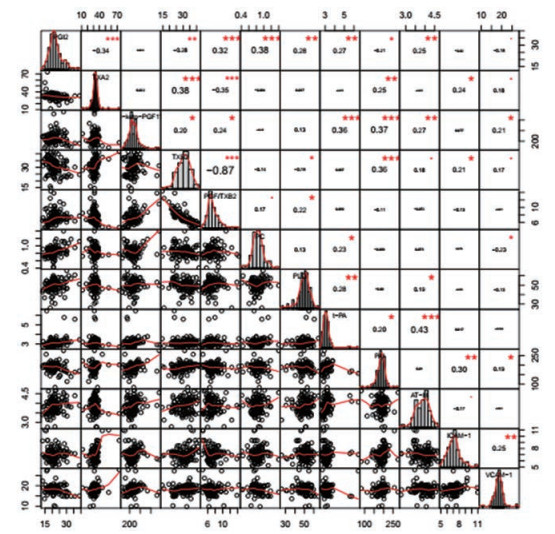
采用Spearman方法将12个指标的相关性进行分析(图 2), 由结果可知, PGI2与TXA2、TXB2、PAI和VCAM-1呈负相关(P < 0.05), 与PGF/TXB2、PC、PLG、t-PA和AT-Ⅲ呈正关(P < 0.01); TXA2与TXB2、PAI、ICAM-1和VCAM-1呈正相关(P < 0.05), 与PGF/TXB2呈负相关(P < 0.001); 6-keto-PGF1α与TXB2、PGF/TXB2、t-PA、PAI、AT-Ⅲ和VCAM-1呈正相关(P < 0.05); TXB2与PGF/TXB2和PLG呈负相关(P < 0.05), 与PAI、AT-Ⅲ、ICAM-1和VCAM-1呈正相关(P < 0.05); PGF/TXB2与PC和PLG呈正相关(P < 0.05); PC与t-PA呈正相关(P < 0.05), 与VCAM-1呈负相关(P < 0.05); PLG与t-PA和AT-Ⅲ呈正相关(P < 0.05); t-PA与PAI和AT-Ⅲ呈正相关(P < 0.05); PAI与ICAM-1和VCAM-1呈正相关(P < 0.05); AT-Ⅲ与ICAM-1呈负相关(P < 0.05); ICAM-1和VCAM-1呈正相关(P < 0.05)。由于相关系数值越接近1或-1, 说明相关性越强, 其中只有TXB2和PGF/TXB2的相关系数值为-0.87 (< -0.5), 具有较强相关性; 其余指标间的相关系数值均在-0.5~0.5之间, 相关性较弱。
|
Figure 2 Correlation plot rectangle of arachidonic acid metabolites, anticoagulation and fibrinolysis indicators and adhesion molecules in acute blood stasis rats after administration of GX herb pair extracts. *P < 0.05, **P < 0.01, ***P < 0.001. All imply that there is a correlation between the two indicators, but their correlation intensity should be judged according to the value of correlation coefficient |
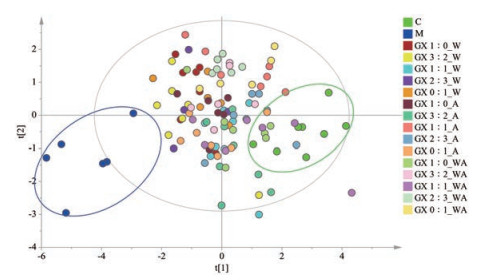
由PLS-DA的score plot得分图(图 3)可知, 正常组中心值约为(2.73, -0.51), 模型组的中心值约为(-4.52, -1.32), 两组得到较好分离, 提示急性血瘀模型大鼠造模成功。当归-川芎药对给药组分布在正常组和模型组中间。从整体可以看出, 当归-川芎不同配比WA组和A组距离正常组较近, W组距离模型组较近。
|
Figure 3 PLS-DA score plot of GX herb pair with different proportions and different preparations on vasoactive substances and adhesion molecules in acute blood stasis rats |
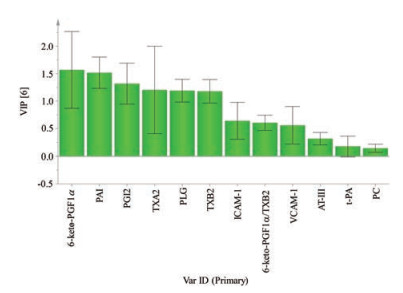
由PLS-DA分析得到的VIP值结果(图 4)可知, 6-keto-PGF1α、PAI、PGI2、TXA2、PLG、TXB2的VIP值均 > 1, ICAM-1、PGF/TXB2和VCAM-1的VIP值在 > 0.5~ < 1, AT-Ⅲ、t-PA和PC的VIP值均 < 0.5。依据VIP值> 1对分类的贡献可知, 花生四烯酸代谢物中6-keto-PGF1α、PGI2、TXA2、TXB2和纤溶系统指标中PAI、PLG共6个指标对本实验各组差异的贡献较大, 可作为急性血瘀模型大鼠和当归-川芎药对对急性血瘀大鼠活血化瘀效应评价的主要指标。
|
Figure 4 The VIP values of arachidonic acid metabolites, anticoagulant-fibrino system indexes and adhesion molecules in the serum of acute blood stasis rats after administration of GX herb pair by using PLS-DA method. n was same as Table 1 |
分别以“血瘀”和花生四烯酸代谢物、纤溶系统、黏附分子及各指标的中文和英文为主题词在中国知网(China National Knowledge Infrastructure, CNKI)和PubMed中检索相关文献, 得到与t-PA、TXB2、ICAM-1、PAI-1、6-keto-PGF1α、AT-Ⅲ、TXA2、PGI2、VCAM-1、PC和PLG相关的血瘀文献分别有88、58、49、43、24、21、15、13、10、6和6篇。结合各指标的VIP值, 综合给出6-keto-PGF1α、PAI-1和TXB2的权重系数为3 (标化值设为Va), PGI2、TXA2、PLG、ICAM-1、PGF/TXB2、VCAM-1和t-PA的权重系数为2 (标化值设为Vb), AT-Ⅲ和PC的权重系数为1 (标化值设为Vc)。将各指标的标化值分别乘以相应的权重系数, 得到当归-川芎药对对急性血瘀大鼠血清中和黏附分子指标改善的总效应值(表 3), 大小排序为GX 1︰1_WA > GX 0︰1_WA > GX 1︰0_WA > GX 3︰2_A > GX 2︰3_A > GX 1︰1_A > GX 1︰1_W > GX 0︰1_A > GX 3︰2_WA > GX 2︰3_WA > GX 1︰0_A > GX 0︰1_W > GX 1︰0_W > GX 3︰2_W > GX 2︰3_W。
| Table 3 The total effect values of arachidonic acid metabolites, anticoagulant-fibrin system indexes and adhesion molecules in the serum of acute blood stasis rats after administration of GX herb pair. Va, Vb and Vc represent the normalized values of the indicators with a weight coefficient of 3, 2 and 1, respectively |
近年来, 在与血栓形成有密切联系的血瘀证研究中, 多认为血瘀证是内外致病因素下机体在形态、结构、代谢和机能诸方面改变多个病理过程的综合所导致的血流动力学、血凝-纤溶系统和血小板功能等的紊乱, 从而使“血行失度”、“血脉瘀阻”, 其病理改变基础则可能与血管内皮细胞损伤密切相关。
花生四烯酸通过环氧酶途径, 生成不稳定的环内过氧化物, 在多种酶的作用下, 生成前列腺素类和血栓素类化合物。PGI2是前列腺素类化合物的代表, 可抑制血小板聚集而呈现抗血栓形成作用, 而PGI2可经水解生成无活性的6-keto-PGF1α, 再经β-氧化由尿排出; TXA2是血小板中花生四烯酸的主要代谢产物, 具有生理性的、强大的促进血小板聚集和释放作用, 是常用的血管收缩剂, TXA2可水解为TXB2。故通常也通过测定6-keto-PGF1α和TXB2以表示PGI2和TXA2的含量或活性。本文结果显示, 与正常组比较, 急性血瘀模型组的大鼠血清中PGI2含量显著降低, 抗血栓形成作用减弱; TXA2和TXB2含量显著升高, 使血小板活化, 聚集作用增强, 进而诱导血栓形成, 造成血瘀[9]。而当归-川芎药对不同配比的醇提物和先水提后醇提物及当归-川芎1︰1水提物给药后对模型组的大鼠血清中上述指标有显著改善作用, 且当归-川芎药对的醇提物和先水提后醇提物对急性血瘀大鼠血清中花生四烯酸代谢物的调节作用强于水提物。有研究报道, 当归中的挥发油成分和阿魏酸能抑制TXA2的生成, 并通过改善TXA2和PGI2的平衡来抑制血小板聚集, 产生良好的抗血栓作用[10, 11]; 川芎注射液可通过抑制以TXA2生产为主的多环节发挥抗血小板活化作用[12], 或与其所含的川芎总酚具有扩张冠状动脉, 抑制TXA2的生成和活性有密切关系[13]。本课题组前期通过代谢组学研究发现, 当归-川芎药对能够调节急性血瘀大鼠血浆中内源性生物标志物花生四烯酸的含量[14], 本文研究结果初步揭示了该药对作用于花生四烯酸代谢通路的分子机制。
凝血和纤溶的平衡在维持机体正常的血液运行和组织修复中发挥重要作用, 纤溶酶原激活系统是体内防止血栓形成的重要机制, 其中心环节是PA系统将纤溶酶原转化成纤溶酶从而发挥纤溶作用。纤溶活性下降是形成血管内凝血、血栓和动脉硬化的重要因素[5]。纤溶系统包括PLG、t-PA、纤溶酶和PAI-1等。t-PA和PAI是由血管内皮细胞合成和释放的活性物质, 两者之间的平衡对调节纤溶的功能具有重要意义; 同时, t-PA可以激活PLG, 促进纤溶, 防止血栓形成。PC系统是具有抗凝作用的血浆蛋白系统, 血管内皮细胞合成或释放PC是体内重要的抗凝因子, 其生成的活化PC (activated protein C, APC)可以增强纤溶活性, 刺激PLG激活物释放。PC的缺乏会使凝血、抗凝和纤溶系统发生紊乱, 从而引发血栓性疾病。AT是主要的生理性血浆抗凝物质, 正常情况下, AT-Ⅲ与肝素结合后抑制凝血酶、纤溶酶及多种凝血因子的活性, 维持血液平衡, 是防止血栓形成的主要生理物质。本文结果显示, 与正常组比较, 急性血瘀模型大鼠血清中PAI显著升高, 而PC、t-PA、PLG和AT-Ⅲ显著降低, 说明急性血瘀模型大鼠机体抗凝和纤溶系统受到抑制; 给予当归-川芎药对后, 对凝血和纤溶指标有一定改善作用。可能与当归、川芎中阿魏酸钠可降低PAI含量、升高t-PA含量有密切关系[15]; 也有文献显示, 川芎嗪对凝血系统中酶的抑制作用和对纤溶系统中酶的促进作用在川芎的活血化瘀机制中起着重要作用[16]; 与已报道[17]的川芎提取物可使脑缺血再灌注损伤大鼠血浆中t-PA活性升高, PAI活性下降, 具有提高纤溶活性、溶栓、消栓的作用相一致。
细胞黏附分子(cell adhesion molecules, CAMs)是一种广泛分布于细胞表面和细胞外基质的糖蛋白, 在凝血和血栓形成、组织损伤修复等生理和病理过程中发挥着重要作用。内皮细胞黏附分子主要有ICAM和VCAM等。国内外有研究初步表明, ICAM-1、VCAM-1、血小板-内皮细胞黏附分子(platelet endothelial cell adhesion molecule 1, PECAM-1)和诱生型一氧化氮合酶(inducible nitric oxide synthase, iNOS)均与血瘀证和(或)具有血瘀征象的病种有不同程度的关系。本文结果显示, 急性血瘀模型大鼠血清中的ICAM-1和VCAM-1均显著升高, 而给予当归-川芎药对不同配比、不同制法样品后, 两者均有不同程度的降低。有研究报道[18], 当归抑制ICAM-1的表达可能与M型胆碱能受体兴奋有关; 川芎内酯及其主要成分Z-藁本内酯可能通过抑制细胞核因子(nuclear factor kappa B, NF-κB)的表达进而减少ICAM-1和VCAM-1的分泌[19]。
PLS是集主成分分析(principal component analysis, PCA)、典型相关分析和多元线性回归于一体的多元线性统计分析方法; PLS-DA算法是一种基于PLS回归的、常用的多变量数据分析方法之一。而多指标综合指数法可把不同性质、不同类别和不同计量单位的指标经过标化, 按照同类指标相乘, 异类指标相加的方法得到总效应值, 从而更便于观察药效的强弱[20-22]。本文结果显示, 当归-川芎1︰1_WA组对急性血瘀模型大鼠血清中花生四烯酸代谢物、抗凝-纤溶系统指标和黏附分子改善的总效应最强; 当归-川芎配比相同时, WA组和A组的总效应比W组的总效应强; 提取方法相同时, 当归-川芎药对1︰1给药组的总效应相对较好。与课题组前期比较评价当归-川芎配伍对急性血瘀大鼠血液流变学及凝血功能药效评价结果[3]基本一致。
血瘀证的发生是多因素的结果, 黏附分子表达、凝血-纤溶系统和花生四烯酸代谢物等血管活性物质表达的检测分别与本课题组前期研究的当归-川芎药对对血瘀大鼠血液流变学(全血黏度、血浆黏度)、凝血四项[3]和血小板聚集[4]的结果相呼应, 均从血液“黏、凝、聚”的角度整合分析了当归-川芎药对协同增强活血化瘀的功效。但由于目前灌胃给药的是当归-川芎药对提取物, 而药效和作用机制的发生离不开成分的作用, 同一配比的当归-川芎药对, 其醇提物中芳香酸类(阿魏酸、绿原酸和咖啡酸)和苯酞内酯类(洋川芎内酯I、洋川芎内酯H、Z-藁本内酯和Z-正丁烯基苯酞)的总含量均高于先水提后醇提样品, 水提样品的含量最低, 由于配比、制法不同, 成分的溶出亦存在差异[23], 可能是造成其功效差异的根本。故尚需根据研究结果进一步选取该药对中主要活性成分和与上述检测指标密切相关的作用通路, 深入探讨当归-川芎药对活血化瘀的作用机制。
| [1] | Gao Y, Yang LF, Zhai Y, et al. Research progress of pharmacologic action and mechanism of blood-activating and stasis-resolving medicine[J]. Chin J Tradit Chin Med Pharm (中华中医药杂志), 2018, 33: 5053–5056. |
| [2] | Yang YH, Wang JN, Han X, et al. A review on relevance between Xueyu syndrome and objective indexes[J]. Clin J Chin Med (中医临床研究), 2014, 6: 142–144. |
| [3] | Li WX, Tang YP, Guo JM, et al. Comparative assessing the effects of Angelica Root and Chuanxiong on the hemorheology and the blood coagulation function in acute blood stasis rats[J]. Chin J Integr Trad West Med (中国中西医结合杂志), 2012, 32: 806–811. |
| [4] | Wang H, Tang YP, Guo JM, et al. Effect of Radix Angelica and Rhizoma Ligusticum with different proportions and preparation methods on platelet aggregation and prothrombin[J]. Chin J Exp Trad Med Form (中国实验方剂学杂志), 2010, 16: 73–77. |
| [5] | Li DX, Yang JH, Deng YH. Relativity discuss of each stlbscriber set of coronary artery disease blood stasis syndrome and fibrinolytic system activity[J]. Chin Med Modern Distance Edu China (中国中医药现代远程教育), 2007, 5: 8–10. |
| [6] | Zhao JH, Lin L, Zhu FH, et al. Effect of Chinese herbs with activiting blood circulation to remove stasis on coagulation-fibrinolysis in rat with vascular endothelial cell injured[J]. Chin J Trad Med Sci Technol (中国中医药科技), 2001, 8: 303–304. |
| [7] | Chen YB, Wang Q, Lai SL. Progress in the application of modern hematology in the study of blood stasis syndrome and promoting blood circulation to remove blood stasis[J]. J Guangzhou Univ Trad Chin Med (广州中医学院学报), 1993, 10: 238–241, 243. |
| [8] | Li WX, Huang MY, Tang YP, et al. Establishment and optimization of acute blood stasis rat model[J]. Chin Pharm Bull (中国药理学通报), 2011, 27: 1761–1765. |
| [9] | Zhang JX, Feng Y, Li SD, et al. Microvascular pathological features and changes in related injury factors in a rat acute blood stasis model[J]. J Trad Chin Med, 2017, 37: 108–115. DOI:10.1016/S0254-6272(17)30034-1 |
| [10] | Yang CC, Han Y, Zhang AS, et al. Effect of Huangqi, Danggui and Ligustrazine as medicines activating blood and eliminating stasis on the expression of plasminogen activator inhibitor 1 in HepG2 hepatocarcinoma cell strain[J]. Chin J Clin Rehab, 2005, 9: 210–212. |
| [11] | Xu LN, Yu WG, Tian JY, et al. Effect of sodium ferulate on arachidonic acid metabolism[J]. Acta Pharm Sin (药学学报), 1990, 25: 412–416. |
| [12] | Lai FS, Shi YM, Zheng HM, et al. Study on antiplatelet mechanism of Ligusticum Wallichii injection[J]. Chin J Integr Trad West Med (中国中西医结合杂志), 1995, S1: 84–86. |
| [13] | Liu JG, Xu FQ, Shi DZ, et al. Effect of the extracts from Rhizoma Chuanxiong and Radix Paeoniae Rubra in different proportions on promoting blood circulation and removing blood stasis[J]. Tradit Chin Drug Res Clin Pharmacol (中药新药与临床药理), 2005, 16: 315–317. |
| [14] | Li WX. Study on the Bio-active Components and Compatibility Action Mechanism of Danggui-Chuanxiong Herb Pair (当归-川芎药对功效物质与配伍作用机制研究)[D]. Nanjing: Nanjing University of Chinese Medicine, 2014. http://cdmd.cnki.com.cn/article/cdmd-10315-1014416320.htm |
| [15] | Wen W, Yang J, Yao Y. Effect of sodium ferulate injection on superoxide dismutase, lipid peroxide, and fibrinolysis system in patients with coronary disease[J]. China Pharm (中国药师), 2002, 5: 555–556. |
| [16] | Yang R, Wei WN. Effect of ligustrazine on activation of coagulation and fibrinolysis[J]. Acta Univ Med Tongji (同济医科大学学报), 1995, 24: 362–364. |
| [17] | Yang JH, Bai HB, Wan HT, et al. Effects of acupoint application with extract of Rhizoma Ligustici Chuanxiong on activities of t-PA and PAI in rat with cerebral IR injury[J]. Chin J Tradit Chin Med Pharm (中华中医药杂志), 2004, 19: 526–528. |
| [18] | Yan XH, Ouyang JP, Tu SZ, et al. Effects of Angelica Sinensis on OLDL-induced decrease of NO release from human endothelial cells and increase of ICAM-1 expression on the surface of human endothelial cells[J]. Chin J Pathophysiol (中国病理生理杂志), 2000, 16: 57–59. |
| [19] | Wang YC. Mechanism of Anti-atherosclerotic Effect of Lactone Components from Ligusticum chuanxiong Hort. and Z-ligustilide (川芎内酯及其主要成分Z-藁本内酯抗动脉粥样硬化作用机制研究)[D]. Hangzhou: Zhejiang University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10335-1013147451.htm |
| [20] | Zhang J, Shi XQ, Zhou GS, et al. Comparative study on the effects of different proportions of ginkgo ketoester and donepezil on anti-dementia based on principal component analysis and multi-attribute comprehensive index methods[J]. Acta Pharm Sin (药学学报), 2019, 54: 660–669. |
| [21] | Li SJ, Li WX, Tang YP, et al. Comparative analysis of the promoting blood effects of the combination of different proportions of Danggui and Honghua by the principal component analysis and multi-attribute comprehensive index methods[J]. Acta Pharm Sin (药学学报), 2014, 49: 1304–1309. |
| [22] | Qu C, Tang YP, Shi XQ, et al. Comparative study on promoting blood effects of Danshen-Honghua herb pair with different preparations based on chemometrics and multi-attribute comprehensive index method[J]. China J Chin Mater Med (中国中药杂志), 2017, 42: 3017–3025. |
| [23] | Li WX, Wang H, Tang YP, et al. The quantitative comparative analysis for main bio-active components in Angelica sinensis, Ligusticum chuanxiong, and the herb pair Gui-Xiong[J]. J Liq Chrom Rel Technol, 2012, 35: 2439–2453. DOI:10.1080/10826076.2011.633678 |
 2019, Vol. 54
2019, Vol. 54


