2. 神威药业集团有限公司, 河北 石家庄 051430
2. Shenwei Pharmaceutical Group Co., Ltd., Shijiazhuang 051430, China
茵陈为菊科植物滨蒿(Artemisia scoparia Waldst.et Kit.)或茵陈蒿(Artemisia capillaris Thunb.)的干燥地上部分, 始载于《神农本草经》, 列为上品, 之后历代本草均有记述, 具有清利湿热、利胆退黄的功效[1, 2]。茵陈标准汤剂系遵循中医药理论, 按照临床汤剂的煎煮方法规范化煎煮, 固液分离, 经适当浓缩制得或经适宜方法干燥制得, 作为一种标准参照物, 用于标化临床用药, 保障用药的准确性和剂量的一致性。茵陈标准汤剂所含成分复杂、功效多样, 《中国药典》 2015年版以含量较高的绿原酸作为茵陈的检测指标, 难以体现茵陈多成分、多功效的特点, 且仅以单一成分控制质量, 不能较好的说明茵陈标准汤剂的内在质量, 因此多指标的含量测定显得更为科学可靠[3-7]。Wang等[8, 9]提出的一测多评法(QAMS)用于多指标的测定, 近年来已经用于多种中药的质量评价, 其中黄连一测多评的含量测定方法已经收入《中国药典》 2015年版, 具有重要的指导意义[10-13]。本文采用QAMS实现茵陈标准汤剂多指标的含量测定, 以绿原酸作为内参物, 计算出新绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸与内标绿原酸的相对校正因子, 从而计算得出新绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸的含量。并采用外标法和QAMS同时测定12批茵陈标准汤剂中8种成分的含量, 比较其结果以验证QAMS的可行性和准确性, 最终建立茵陈标准汤剂中8种成分的一测多评方法, 为茵陈标准汤剂的全面质量控制提供新的方法和思路。
材料与方法仪器 安捷伦公司Agilent 1290超高效液相色谱仪(包括四元泵、在线脱气机、自动进样器、DAD检测器和色谱工作站); Waters Cortecs T3色谱柱(2.1 mm×100 mm, 2.7 μm)
试剂与样品 对照品新绿原酸(批号CHB170828, 含量以98%计)、绿原酸(批号CHB170713, 含量以98%计)、隐绿原酸(批号CHB170828, 含量以98%计)、3, 4-二咖啡酰奎宁酸(批号CHB160725, 含量以98%计)均购自成都曼斯特生物科技有限公司, 对照品咖啡酸(批号MUST-17032010, 含量以99.48%计)、1, 3-二咖啡酰奎宁酸(批号MUST-17022608, 含量以99.69%计)、3, 5-二咖啡酰奎宁酸(批号MUST-17030621, 含量以98.82%计)、4, 5-二咖啡酰奎宁酸(批号MUST-17021603, 含量以99.8%计)均购自成都克洛玛生物科技有限公司。乙腈(色谱纯, 美国Sigma公司), 甲醇(色谱纯, 山东禹王公司), 磷酸(色谱纯, 天津市科密欧化学试剂有限公司), 其他试剂(分析纯, 市售), 水(杭州娃哈哈集团有限公司)。共收集不同产地的茵陈饮片12批, 经沈阳药科大学中药学院王东教授鉴定为菊科植物滨蒿Artemisia scoparia Waldst.et Kit.或茵陈蒿Artemisia capillaris Thunb.的干燥地上部分。来源见表 1。
| Table 1 The source of all the samples |
UHPLC色谱条件 色谱柱: Waters Cortecs T3 (2.1 mm×100 mm, 2.7 μm); 流动相: 0.05%磷酸水(A) -乙腈(B)梯度洗脱(0~5 min, 3%~10% B; 5~6 min, 10%~11% B; 6~7 min, 11%~13% B; 7~8 min, 13% B; 8~10 min, 13%~18% B; 10~14 min; 18%~23% B); 流速: 0.5 mL·min-1; 检测波长: 327 nm; 柱温: 30 ℃; 进样量: 2 μL。
混合对照品溶液的制备 精密称取各对照品适量, 加入甲醇配制成含新绿原酸79.84 μg·mL-1, 绿原酸402.0 μg·mL-1, 咖啡酸16.06 μg·mL-1, 隐绿原酸100.6 μg·mL-1, 1, 3-二咖啡酰奎宁酸16.06 μg·mL-1, 3, 4-二咖啡酰奎宁酸79.84 μg·mL-1, 3, 5-二咖啡酰奎宁酸200.4 μg·mL-1, 4, 5-二咖啡酰奎宁酸100.8 μg·mL-1的混合溶液, 作为混合对照品储备溶液。精密量取混合对照品储备溶液2.0 mL, 置10 mL量瓶中, 加入甲醇稀释至刻度, 摇匀, 制成新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸浓度分别为15.97、80.4、3.213、20.12、3.213、15.97、40.08和20.16 μg·mL-1的混合对照品溶液。
供试品溶液的制备 取茵陈饮片100 g, 加入12倍量水搅拌浸泡5 min, 加热回流30 min, 200目筛趁热过滤, 向药渣中加入10倍量水, 加热回流20 min, 200目筛趁热过滤, 合并两煎液后65 ℃减压浓缩至160 mL, 即得茵陈标准汤剂浓缩液。取浓缩液1 mL加水稀释至50 mL, 摇匀, 离心, 取上清液, 0.22 μm微孔滤膜过滤, 弃去初滤液, 取续滤液即得。
线性与范围 精密量取混合对照品储备溶液0.1、0.5、1.0、2.5、4.0和5.0 mL, 分别置10 mL量瓶中, 用甲醇定容, 摇匀, 即得系列浓度的混合对照品溶液。
精密度 精密量取同一批茵陈标准汤剂0.5、1.0和1.5 mL, 按“供试品溶液的制备”项下的方法制备低、中、高3个浓度的供试品溶液, 每一种浓度平行操作3份, 按上述UHPLC色谱条件进样分析, 测定峰面积, 计算各待测物的浓度, 作为重复性实验。精密量取同一批茵陈标准汤剂1.0 mL, 按“供试品溶液的制备”项下方法制备相同浓度的标准汤剂供试品溶液3份, 按上述UHPLC色谱条件连续3天进样分析, 测定峰面积, 计算各待测物的浓度, 作为日间精密度实验。
准确度 取已知含量的茵陈标准汤剂, 精密称取9份, 每份约0.5 mL, 分别按已知含量的50%、100%、150% 3个水平加入对照品, 按“供试品溶液的制备”项下的方法制备低、中、高3个不同浓度的供试品溶液, 每个浓度平行制备3份。
稳定性 精密量取同一批茵陈标准汤剂1.0 mL, 按“供试品溶液的制备”项下方法操作, 室温放置, 按上述UHPLC谱条件分别在0、2、4、6、8和10 h进样分析。
相对校正因子的测定 以绿原酸为内参物, 根据相对校正因子计算公式(fsi = fs/fi = As·Ci/Ai·Cs, 其中As为内参物绿原酸的峰面积, Cs为内参物绿原酸的浓度, Ai为待测物i的峰面积, Ci为待测物i的浓度), 精密吸取一系列不同浓度的混合对照品溶液, 按上述UHPLC谱条件进样测定, 记录各浓度对照品峰面积。
系统适用性实验 分别取混合对照品溶液和供试品溶液, 按上述UHPLC色谱条件进样分析, 新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸与相邻色谱峰的分离度均大于1.5。理论塔板数以绿原酸计不低于9 000, 拖尾因子均在0.80~1.1之间。取混合对照品溶液, 连续进样6次, 计算的新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸峰面积的RSD值分别为0.86%、0.93%、1.16%、0.96%、1.05%、0.94%、0.95%和1.07%, 取混合对照品溶液, 配制一系列不同浓度的灵敏度试验用溶液, 测定新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸的信噪比均大于10, 表明系统适用性良好。
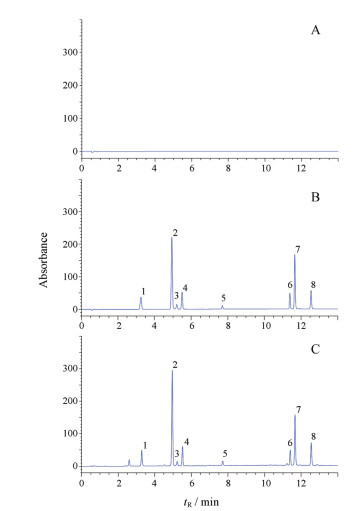
结果 1 方法学考察 1.1 专属性通过对比空白溶剂(水)、混合对照品溶液和供试品溶液色谱图, 考察方法专属性。典型色谱图如图 1所示。结果表明, 该方法专属性良好。
|
Figure 1 The UHPLC chromatograms of blank solvent (A), mixed standard solution (B) and sample solution (C); 1: Neochlorogenic acid; 2: Chlorogenic acid; 3: Caffeic acid; 4: Cryptochlorogenic acid; 5: 1, 3-O-Dicaffeoylquinic acid; 6: 3, 4-O-Dicaffeoylquinic acid; 7: 3, 5-O-Dicaffeoylquinic acid; 8: 4, 5-O-Dicaffeoylquinic acid |
以峰面积(X)为横坐标, 进样浓度(Y)为纵坐标, 绘制标准曲线。回归方程及相关系数见表 2。结果表明8个成分在各自的线性范围内线性关系良好。
| Table 2 Criteria curves, correlation coefficients, and linearity ranges of reference substances |
新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸浓度的RSD分别为0.74%、0.67%、0.80%、0.56%、1.2%、0.58%、0.72%和1.3%, 表明本方法重复性良好。
新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸浓度的RSD分别为2.4%、2.2%、2.8%、2.3%、3.8%、2.2%、2.6%和2.2%, 表明日间精密度良好。
1.4 准确度结果表明, 各成分的回收率均在95.7%~103.0%内, RSD值均 < 2.0%, 方法准确度良好。
1.5 稳定性新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸的RSD分别为0.3%、0.04%、2.3%、0.5%、1.3%、2.1%、1.0%和0.7%, 表明供试品溶液在10 h内稳定。
2 相对校正因子 2.1 相对校正因子的测定新绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸的相对校正因子分别为0.928 0、0.546 2、1.099 8、0.872 1、1.086 8、0.739 2、1.056 6。
2.2 相对校正因子重现性考察分别考察了三台不同的Agilent 1290超高效液相色谱仪, 两个不同批号的Waters Cortecs T3色谱柱(批号分别为01093731716707和01093731716607)按上述UHPLC色谱条件进样分析, 计算相对校正因子, 所有结果RSD值均 < 2.0%, 表明不同的液相色谱仪和色谱柱对相对校正因子没有显著影响。
2.3 待测组分色谱峰的定位取一系列不同浓度的混合对照品溶液, 在不同液相色谱仪上分别采用不同色谱柱, 测定并计算了各待测成分与内参物绿原酸的相对保留时间和保留时间差, 见表 3。结果显示不同仪器和不同色谱柱下, 各待测成分的相对保留时间的波动较小, RSD < 2.0%。咖啡酸和隐绿原酸的保留时间差波动较大, RSD值分别为8.55%、5.04%。结果表明, 相对保留值法适用于茵陈标准汤剂中待测成分QAMS的定位。
| Table 3 Investigation on relative retention time and retention time difference |
取12批不同来源的茵陈饮片, 采用QAMS对茵陈标准汤剂中的新绿原酸、绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸进行含量测定, 并与外标法含量测定结果进行比较, 结果见表 4。
| Table 4 Determination results of eight components by external standard methods (ESTD) and quantitative analysis of multi-components with a single-marker (QAMS) |
常规外标法实测含量值与QAMS计算的含量经成组t检验比较。结果显示, 2种方法所得新绿原酸、咖啡酸、隐绿原酸、1, 3-二咖啡酰奎宁酸、3, 4-二咖啡酰奎宁酸、3, 5-二咖啡酰奎宁酸和4, 5-二咖啡酰奎宁酸含量的P值分别为0.951、0.919、0.935、0.788、0.975、0.896和0.986, 均不存在显著性差异, 表明2种方法测得含量没有显著差异。可见, QAMS在茵陈标准汤剂多指标成分定量分析中的应用是准确可靠的。
讨论茵陈标准汤剂以水为提取溶媒, 提取出的成分主要为绿原酸类成分。该类成分含量较高, 性质稳定, 是茵陈水提物中的代表性物质, 也是茵陈具有抗氧化、抗菌、抗肿瘤和免疫调节作用的主要有效物质, 因此对该类的多成分进行含量测定。其中绿原酸是茵陈标准汤剂中含量最高的成分, 也是《中国药典》 2015年版茵陈中规定的指标成分, 其对照品也容易获得, 因此选其作为一测多评的内参物。
中药所含成分较多, 多成分测定已经成为中药质量评价的发展趋势, QAMS运用所测各组分间存在的内在函数关系, 以其中一个易得且性质稳定的成分作为内参物, 通过建立内参物与其他所测组分间的fsi, 实现多组分的同时测定, 大大地降低了检验成本, 已广泛得以应用。本实验采用UHPLC-DAD建立了一测多评法, 对来自不同产地的12批茵陈标准汤剂中的8种成分进行了同时含量测定。所得结果与外标法进行比较, 结果无显著性差异。检测方法快速、简便、准确, 为茵陈标准汤剂的全面质量控制提供新的方法和思路。
| [1] | Chinese Pharmacopoeia Commission. The Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2015 ed. Part Ⅰ. Beijing: China Medical Science Press, 2015: 239-240. |
| [2] | Chinese Herbs Editorial Committee. State Administration of Traditional Chinese Medicine. Herba Sinica (中华本草)[M]. Shanghai: Shanghai Science and Technology Press, 1999: 687-693. |
| [3] | Tan XJ, Li Q, Chen XH, et al. Simultaneous determination of 13 bioactive compounds in Herba Artemisiae Scopariae from different harvest seasons by HPLC-DAD[J]. J Pharm Biomed, 2008, 47: 847–853. DOI:10.1016/j.jpba.2008.04.010 |
| [4] | Zhang Q, Zhang JY, Dong LY, et al. Determination of chlorogenic acids in Qingkailing Injection by a multi-evaluation method[J]. Chin Tradit Pat Med (中成药), 2014, 36: 768–772. |
| [5] | Zhang Q, Zhang JY, Gao FY, et al. Simultaneous determination of seven phenolic acids in Qingkailing injection by HPLC-DAD[J]. China J Pharm Anal (药物分析杂志), 2013, 33: 73–77. |
| [6] | Zhao Y, Zhao J, Li YP, et al. Research progress in caffeoylquinic acid compounds[J]. China J Chin Mater Med (中国中药杂志), 2006, 31: 869–874. |
| [7] | Zhen R, Jia ZW, Wang K, et al. Determination of six organic acids in honeysuckle extract[J]. Chin Tradit Pat Med (中成药), 2013, 35: 560–564. |
| [8] | Wang ZM, Gao HM, Fu XT, et al. Methodological study on the quality evaluation model of traditional Chinese medicine in "quantitative analysis of multi-components with a single-marker"[J]. China J Chin Mater Med (中国中药杂志), 2006, 31: 1925–1928. |
| [9] | Wang ZM, Qian ZZ, Zhang QW, et al. A technical guide for the quantitative analysis of multi-components with a single-marker method[J]. China J Chin Mater Med (中国中药杂志), 2011, 36: 657–658. |
| [10] | Kuang YH, Zhu JJ, Wang ZM, et al. Determination of berberine, palmatine, coptisine, epipodamine and jatrorrhizine in Rhizoma Coptidis by QAMS[J]. Chin Pharm J (中国药学杂志), 2009, 44: 390–394. |
| [11] | Ding LY, Zhou L, Wang LN, et al. Multi-components quantitation by one marker for simultaneous content determination of four components in Psoralea corylifolia[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2013, 19: 152–154. |
| [12] | Fan L, Yan D, Li S, et al. Simultaneous quantitative analysis of polygonin, resveratrol, archen and emodin monomethyl ether in Polygoni Cuspidati Rhizoma et Radix by multi-components assay and single marker[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2013, 19: 103–107. |
| [13] | Meng J, Lu GY, Cheng XX, et al. Quantitative analysis of four gingerol components in Zingiberis Rhizoma by QAMS[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2012, 18: 77–80. |
 2019, Vol. 54
2019, Vol. 54


