2. 上海中医药大学中药现代制剂技术教育部工程研究中心, 上海 201203
2. Engineering Research Center of Modern Preparation Technology of Traditional Chinese Medicine, Ministry of Education, Shanghai University of Traditional Chinese Medicine, Shanghai 201203, China
中药挥发油具有抑菌及抗耐药性、抗病毒、抗炎作用, 调节心血管、消化系统和中枢神经系统等药理活性[1], 在临床中被广泛应用。2015年版《中国药典》一部收载的常用中药固体制剂中, 近20%成方制剂含有中药单提挥发油。而挥发油几乎不溶于水, 具有刺激性大、生物利用度低、挥发性强、稳定性差, 易受光、氧、热等环境因素影响的缺点, 在很大程度上限制了其在口服制剂开发及临床应用等方面的发展[2, 3]; 在含有中药单提挥发油的成方制剂中, 近80%挥发油以液体的形式直接喷洒在颗粒表面, 而为提高挥发油制剂的稳定性, 16%中药挥发油被制成环糊精包合物。包合技术已广泛应用于挥发油粉末化研究, 但该技术仍存在辅料用量较大、包封率低等问题[3]。近年来, 针对挥发油自身的特性, 一些现代制剂新技术如微囊化[4, 5]、微球化[6, 7], 新型载药系统如脂质体、纳米乳[8, 9]也被应用于中药挥发油, 增加溶解度、提高制剂稳定性、提高生物利用度、缓解刺激性和液体药物固体化。然而, 这些新技术的应用存在有机溶剂残留、载药量低、存放稳定性差、毒副作用不明确、对制备工艺有特殊要求和不利于工业化放大生产等问题, 其制剂工业化生产可能性低[2, 3]。
有研究表明, 以固体材料如吸收剂[10-13]、多孔材料[14-17]为载体, 通过简单的搅拌工艺, 将载体与挥发油混合均匀, 即通过吸附法实现液体物料固体化的目的, 且避免了热与湿对物料的影响, 在一定程度上提高制剂的稳定性, 具有制备工艺简单、方便、成本低廉和便于制剂成型加工的特点, 有较好的应用前景。目前常用的吸收剂如微晶纤维素、磷酸氢钙[10]、交联聚维酮[11]、羟基磷灰石[12]和氧化石墨烯[13]等的吸收能力一般, 固化粉末热稳定性差, 且载药后粉末粉体特性差异较大, 限制了该技术在油性药物固体化方面的应用。多孔材料因具有较高的比表面积和较大的空隙率, 药物分子吸附到孔隙后处于非晶态, 可提高药物溶出速率从而提高疏水药物分子生物利用度, 常被作为高效的药物载体广泛应用。二氧化硅是研究最广泛的辅料, 通常被认为是安全的, 常作为一种润滑剂、载体、增稠剂、吸附剂和防腐剂等已被应用于食品和医药领域。此外, 它也是生产多孔材料的常用无机组分[18]。介孔二氧化硅Sylysia 350FCP (mesoporous silica Sylysia 350FCP, Sylysia 350FCP)是一种高纯度、非晶形和多孔结构亲水性的二氧化硅, 其平均粒径为3.9 μm, 平均孔径为25 nm, 空隙容积为1.9 mL·g-1, 比表面积为294 m2·g-1, 由于其表面含有许多硅烷醇基团, 较高的孔隙容积和安全性, 良好的水润湿性和分散性[19], 常被作为制备固体分散体、固体脂质纳米粒、自微乳化药物输送系统等有效固体载体, 是有潜能的低水溶性药物载体[20, 21]。
连翘和柴胡是常用解表类中药, 含有挥发油成分。本课题组前期研究发现, 连翘和柴胡共提混合挥发油(以下简称柴翘挥发油)的主要成分为α-蒎烯和β-蒎烯, 总相对含量为70%左右, 其中β-蒎烯的相对含量近50%。现代药理学研究表明, 连翘和柴胡挥发油具有抑菌、抗病毒、抗氧化和解热抗炎等药理活性[22-24], 具有较好的临床应用价值。因此, 本研究以柴翘挥发油为研究对象, 以Sylysia 350FCP为载体, 对其进行固化研究, 并对其挥发油固化粉末(volatile oil drug-loading powder, VO-DLP)进行粉体学性质考察、热稳定性及机械稳定性研究, 采用扫描电镜(scanning electron microscopy, SEM)、粉末X-射线衍射(powder X-ray diffraction, PXRD)和同步热分析(synchronous thermal analysis, STA)等方法对粉末进行表征, 为以多孔材料为载体进行挥发油固化研究提供理论和实践依据。
材料与方法仪器 气相色谱仪(7890A, 美国Agilent公司); 转矩流变仪(MTR3, 英国Caleva公司); 环境扫描电子显微镜(QUANTA FEG 250, 美国FEI公司); 粉末X-射线衍射仪(Bruker Advanced D8, Bruker AXS GMBH); 同步热分析仪(STA449F3, 德国耐驰公司); 粉体综合特性测试仪(BT 1000型, 丹东市百特仪器有限公司); 真密度测定仪(Accupyc Ⅱ 1340, 美国Micromeritics公司); 激光粒径测定仪(Mastersizer-2000, 英国Marlven公司); 感应压片机(XP1, 德国Korsch公司); 智能片剂硬度仪(YD-20KZ, 天津市天大天发科技有限公司)。
药品与试剂 柴翘挥发油(批号: T180724, β-蒎烯含量为52.0%, 安徽济人药业有限公司); β-蒎烯对照品(批号: G139678, 纯度: 99.5%, 德国Dr.Ehrenstorfer公司); Sylysia 350FCP (批号: RL-0162, 富士硅化学有限公司); 微晶纤维素MCC-102 (批号: 5610264526, 上海昌为医药辅料技术有限公司); Tween-80 (批号: ZY181210, 上海谱振生物科技有限公司)。
挥发油固化粉末的制备 分别称取适量Sylysia 350FCP置于转矩流变仪的搅拌槽中, 并按照挥发油(volatile oil, VO):辅料(excipient, Ex) 1:4、1:2、1:1和3:2的质量比均匀加入适量柴翘挥发油, 于60 r·min-1条件下, 搅拌12 min, 使柴翘挥发油被介孔二氧化硅充分吸收并混合均匀, 制得挥发油固化粉末, 密封保存于铝箔袋中, 备用。
气相色谱条件及方法验证 以(5%苯基)-甲基聚硅氧烷为固定相的毛细管柱(内径为0.32 mm, 柱长为30 m, 膜厚度为0.25μm); 柱温为程序升温:初始温度为40 ℃, 然后以7 ℃·min-1的速率升温至85 ℃, 保持6 min, 接着以10 ℃·min-1速率升温至100 ℃, 最后以15 ℃·min-1速率升温至220 ℃, 保持2 min; 进样口温度为250 ℃; 检测器(FID)温度为280 ℃; 载气(高纯氮气)流速为0.5 mL·min-1; 空气流速为400 mL·min-1; 氢气流速为40 mL·min-1; 尾吹气流速为40 mL·min-1; 分流进样, 分流比为55:1;进样体积为1.0 μL。对该方法的专属性、线性范围、精密度、重复性、回收率及稳定性进行方法学验证。
β-蒎烯吸附率的计算 取VO-DLP适量, 精密称定, 置具塞锥形瓶中, 精密加入无水乙醇25 mL, 称定重量, 超声处理10 min后, 放冷, 再次称重, 用无水乙醇补足减失的重量, 摇匀, 滤过, 取续滤液, 按气相色谱条件测定其中β-蒎烯的量并记为实际检测量; 另取挥发油110 mg于25 mL棕色量瓶中, 用无水乙醇定容, 摇匀, 通过色谱分析及相关计算求得固化粉末中β-蒎烯理论含有量, 并按公式(1)计算β-蒎烯吸附率[13-15]。
| $ \beta - {\rm{蒎烯吸附率 = }}\frac{{{\rm{固化粉末中}}\beta - {\rm{蒎烯实际检测量}}}}{{{\rm{固化粉末中}}\beta - {\rm{蒎烯理论含有量}}}} \times 100\% $ | (1) |
热稳定性考察 分别取不同载药量的VO-DLP, 于60 ℃下放置10 h, 定时取样, 测定并计算β-蒎烯的吸附率, 考察其热稳定性。
样品表征 扫描电镜:样品粉末分散固定于电镜载物台上, 采用高真空镀膜仪进行喷金处理, 实验加速电压为10 kV; 粉末X-射线衍射: Cu-Kα辐射(λ=1.540 6), 管压为40 kV, 管流为40 mV, 连续扫描步长为0.02°; 同步热分析:称取适量样品于Al2O3坩埚内, 在60 mL·min-1 N2环境下以5 ℃·min-1加热速率由室温升至600 ℃。
粉体学性质考察 粒径及粒径分布和比表面积:采用马尔文2000激光粒径测定仪干法测定样品的粒径(d0.5)、粒径分布Span和比表面积(specific surface area, SSA); 休止角(angle of repose, AR):采用固定漏斗法测定样品的休止角, 将样品在固定高度以自由落体的方式通过固定内径的漏斗, 落至圆形底座中心, 直至形成对称的直径与底座相同的圆锥体, 并按公式(2)计算休止角(AR), 式中r和h分别表示固定的底座半径和圆锥形的高度; 堆密度(bulk density, ρb)、振实密度(tap density, ρbt)、Carr's index (CI)和Hausner ratio (HR):采用BT-1000粉体综合特性测定仪测定样品ρb和ρbt, 并按公式(3)和(4)计算其CI和HR; 真密度(true density, ρt)及孔隙率(total porosity, εt):利用氦气置换法, 使用真密度测定仪测试样品在0.14 MPa压强下真密度, 每个样品测试为5个循环, 计算其平均值和标准差, 并按公式(5)计算其孔隙率。
| $ {\rm{tan}}\theta = \frac{h}{r} $ | (2) |
| $ {\rm{CI}} = \frac{{{\rho _{bt}} - {\rho _b}}}{{{\rho _{bt}}}} \times 100{\rm{\% }} $ | (3) |
| ${\rm{HR}} = \frac{{{\rho _{bt}}}}{{{\rho _b}}} $ | (4) |
| $ {\varepsilon _t} = 1 - \frac{{{\rho _b}}}{{{\rho _t}}} $ | (5) |
体外溶出度考察 以β-蒎烯为指标, 考察挥发油固化粉末的体外溶出情况。精密称取含0.5 g挥发油的VO-DLP, 按溶出度测定方法测定(《中国药典》 2015年版四部附录0931项下桨法), 以经脱气处理的3% Tween-80水溶液(600 mL)为溶出介质, 转速为50 r·min-1, 温度为37 ± 0.5 ℃, 经0.8 μm纤维素滤膜, 分别于10、20、30、45、60、90和120 min取样5 mL (同时补加同温度等量溶出介质), 按照气相色谱法测定不同时间点药物释放量。
压缩成型性 粉体的压缩性指在一定压力下粉体体积减小的能力[25], 反映了粉体在压缩过程中发生不可逆形变的能力, 是评价粉体是否适于压片的重要参数。本研究采用塑性常数(net energy per unit of quality, ESP)、快速弹性松弛即快速弹性复原率(fast elastic stretch, FES)、摩擦功(friction energy, E1)、解压缩后保留能即净功(energy retained during unloading, E2)、出片力(ejection force, EF)和中模壁力(middle die wall force, MDWF)表征粉体的压缩过程。粉体的成形性指粉体能够形成具有一定机械强度的压缩物的能力[26], 反映了实际压缩过程中粉体粒子的结合能力, 是衡量压片是否成功的关键因素。本研究采用压缩物抗张强度(tensile strength, TS)与压力曲线图评价粉体的成形性[25]。
以微晶纤维素MCC-102为研究对象, 分别以1%介孔二氧化硅及VO-DLP作为润滑剂, 采用8.5 mm圆形冲头单冲压片机, 分别在1、2、3、4和5 kN的上冲压力下压片, 片重(m) 240 mg。测定片剂的硬度(F)、直径(D)和厚度(T), 并由压片机数据分析系统记录E1、E2、EF和MDWF, 按公式(6)、(7)、(8)计算ESP、TS和FES。
| $ {E_{{\rm{SP}}}} = \frac{{{E_2}}}{m} $ | (6) |
| $ {\rm{TS}} = \frac{{2F}}{{{\rm{ \mathsf{ π} }}DT}} $ | (7) |
| $ {\rm{FES}} = \frac{{{H_1} - {H_2}}}{{{H_2}}} \times 100{\rm{\% }} $ | (8) |
机械稳定性 为考察挥发油固化粉末的机械稳定性, 以微品纤维素MCC-102为研究对象, 分别以1%介孔二氧化硅及VO-DLP作为润滑剂, 采用8.5 mm的圆形冲头Korsch XP1单冲压片机, 分别在1、2、4、6和8 kN上冲压力下压片, 观察片子的表面是否有油溢出, 并避光密封保存于室温一段时间, 观察片子是否有油斑出现。
固化粉末的应用——工业化生产 采用8.5 mm圆形冲头Korsch XP1单冲压片机, 在2 kN上冲压力下, 每分钟10片的压速下全自动连续压片, 分别按照2015年版《中国药典》第四部0101片剂项下重量差异检查法和0923片剂项下脆碎度检查法对片子分别进行重量差异和脆碎度的检查。
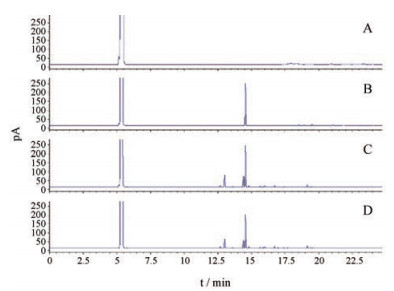
结果与讨论 1 β-蒎烯含量测定分析方法验证由气相色谱图谱(图 1)可知, 该色谱条件下, β-蒎烯色谱峰与其他组分色谱峰可达到基线分离, 其他组分对测定无干扰, 说明该方法专属性良好。以对照品β-蒎烯溶液的浓度(C)为横坐标, 对应的峰面积(A)为纵坐标, 绘制标准曲线, 得回归方程为A = 282.29C - 3.977 5 (r = 0.999 8), 表明β-蒎烯在0.092 1~9.206 7 mg·mL-1内与峰面积线性关系良好。质量浓度为2.762 0 mg·mL-1的β-蒎烯对照品溶液连续进样6次, RSD值为1.06%;配置6份样品溶液, 进样分析, RSD值为1.19%;样品溶液于25 ℃避光放置0、2、4、6、8、10和12 h, 定点取样测定, RSD值为0.48%。结果表明, 该方法的准确度、精密度和重复性等均符合要求, 且样品溶液在12 h内稳定, 可用于β-蒎烯的含量测定。
|
Figure 1 Gas chromatogram of blank solvent (A), standard solution of beta-pinene (B), volatile oil (C) and volatile oil drug-loading powder (D) |
应用不同用量的多孔载体制得VO-DLP, 其挥发油中β-蒎烯吸附率及其60 ℃条件下放置10 h的热稳定结果见表 1。由表 1可知, 当挥发油与载体的质量比为1:1时, 制得的固化粉末其中β-蒎烯吸附率较高、受热前后β-蒎烯含量变化较小、热稳定性较好, 而挥发油与载体的质量比为3:2时, 挥发油的加入量超出Sylysia 350FCP的最大负荷量, VO-DLP粉末的质量稳定性有所降低。
| Table 1 Adsorption rate and thermal stability of volatile oil drug-loading powder (VO-DLP) (n = 3, x ± s). Ex: Excipient (Sylysia 350FCP) |
不同载体用量制得的挥发油固化粉末外观见图 2。结果表明, 当挥发油与载体的质量比在1:4~1:1之间时, 挥发油均能被较好吸附, 且粉体分散较为均匀, 无黏连现象, 器壁无残留, 制得的VO-DLP表面比较干爽。当挥发油与载体的质量比为3:2时, 出现结块现象, 器壁有残留, 制得的VO-DLP表面有油腻感, 表明挥发油的添加量已超出多孔载体的吸附能力。

|
Figure 2 Appearance of mesoporous silica Sylysia 350FCP (Sylysia 350FCP) (a), VO:Ex 1:4-DLP (b), VO:Ex 1:2-DLP (c), VO:Ex 1:1-DLP (d), VO:Ex 3:2-DLP (e) |
借助环境扫描电子显微镜对载体及挥发油固化粉末进行表征, 结果见图 3。由图可知, 载体Sylysia 350FCP辅料为类球形结构, 表面比较粗糙, 布满褶皱; 载药后依然保持类球形的结构, 且随着挥发油添加量的增多, 固化粉末表面粗糙程度有所缓和, 但表面没有明显的油膜形成, 且粒子大小无显著变化, 表明挥发油可能以液体的形式被吸附进入多孔载体的空腔内而非分布于粒子表面。

|
Figure 3 The scanning electron micrograph of Sylysia 350FCP (a), VO:Ex 1:4-DLP (b), VO:Ex 1:2-DLP (c), VO:Ex 1:1-DLP (d), VO:Ex 3:2-DLP (e) (40 000 ×, 10 000 ×) |
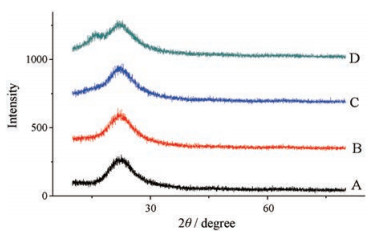
载体载药前后粉末X-射线衍射图见图 4。从图中可见, 当挥发油与载体的质量比为1:4和1:2时, VO-DLP的X-射线衍射图谱与载体Sylysia 350FCP基本一致, 都仅有1个包峰, 表明挥发油以无定型形态完全装载于载体的孔道内, 且装载过程不会破坏载体的结构[27]; 当挥发油与载体的质量比为1:1时, VO-DLP的X-射线衍射图谱与载体Sylysia 350FCP相比多出1个特征峰, 表明挥发油的投料量过大, 超出载体的吸附能力, 有少部分挥发油未被吸附进入多孔载体的孔道内, 而以油状液体的形式存在于粒子表面。
|
Figure 4 The powder X-ray diffraction pattern of Sylysia 350FCP (A), VO:Ex 1:4-DLP (B), VO:Ex 1:2-DLP (C), VO:Ex 1:1-DLP (D) |
挥发油、介孔二氧化硅和挥发油固化粉末同步热分析结果见图 5。由热重力(thermal gravity, TG)曲线图可知, 在30 ℃~115 ℃内未固化挥发油的质量损失迅速, 其质量损失近48%, 而VO-DLP在此温度范围内质量损失缓慢, 其质量损失仅为5%左右。由DTG (differential thermogravimetry)曲线可知, 未固化挥发油在30 ℃~120 ℃内出现了1个向下延伸的特征峰, 并于115 ℃时达到峰值, 而VO-DLP在此温度范围内则未出现此特征峰。此外, 在30 ℃~115 ℃内未固化挥发油的DSC (differential scanning calorimetry)曲线图出现了向下延伸的吸热峰, 并于100 ℃达到峰值, 同时在其DDSC (differential of DSC)曲线图相应位置也出现了特征峰, 而VO-DLP的DSC和DDSC曲线图在此范围内均未出现相应的特征峰, 与TG和DTG结果一致。说明在30 ℃~115 ℃内未固化挥发油内的水分和易挥发性物质受温度的影响, 吸热气化而损失, 热不稳定性特征较为明显; VO-DLP因挥发油装载于介孔二氧化硅的孔道内, 而非游离于载体表面, 并且纳米孔道的毛细管作用力限制了挥发油的气化损失[28], 所以在DSC和DDSC曲线图中挥发油特征峰消失, 表明介孔二氧化硅固化挥发油可显著提高挥发油的热稳定性且其固化机制为可逆的物理吸附过程。

|
Figure 5 Thermal gravity (TG), differential thermogravimetry (DTG), differential scanning calorimetry (DSC) and differential of DSC (DDSC) curves of volatile oil (A), mesoporous silica (B) and volatile oil drug-loading powder (VO:Ex 1:2-DLP as C and VO:Ex 1:1-DLP as D). a: TG curve; b: DTG curve; c: DSC curve; d: DDSC curve |
各粉末的粉体物理学参数测定结果见表 2。由表可知, 与载药前相比, 载药后Sylysia 350FCP的粒径、总孔隙率减小, 比表面积、休止角、堆密度和振实密度增大, 且随着挥发油投料量增大, VO-DLP的堆密度、振实密度逐渐增大, 真密度逐渐减小, 总孔隙率逐渐减小。挥发油的密度小于Sylysia 350FCP的真密度, 挥发油与多孔载体搅拌混合时, 挥发油进入多孔介质的孔道内, 当挥发油的投料量增大, 伴随着更多的挥发油进入载体的孔道内, 从而使VO-DLP的堆密度、振实密度增大, 真密度、总孔隙率减小; 载药前, Sylysia 350FCP的休止角大于40°, 压缩性指数CI大于28%, HR大于1.5[28], 说明粉体流动性极差; 与载药前比, 当VO-DLP的VO:Ex质量比为1:4、1:2时, CI和HR逐渐减小, 表明Sylysia 350FCP载药后流动性有所改善, 可能是由于多孔载体吸附挥发油后, 粒子表面粗糙程度有所缓解, 降低粒子间的凝聚性, 改善了粉体的流动性; 当VO-DLP的VO:Ex质量比为3:2时, CI和HR均有所增大, 表明VO-DLP流动性变差, 可能是由于挥发油的投料量超出多孔载体的吸附能力, 使部分挥发油以液体油状物存在于粒子表面, 使粒子间的黏附性增大, 降低了粉体的流动性。
| Table 2 The physical properties of powders (n = 3, x ± s). ρb: Bulk density; AR: Angle of repose; ρbt: Tap density; ρt: True density; CI: Carr's index; HR: Hausner ratio |
因挥发油几乎不溶于水, 选择亲水性的表面活性剂Tween-80水溶液作为溶出介质, 进行挥发油固化粉末体外溶出度的考察。将不同时间点药物释放量的气相测定结果代入标准曲线计算β-蒎烯的质量, 并换算成累积溶出率。以时间为横坐标, 累积溶出率为纵坐标, 作VO-DLP中β-蒎烯的溶出曲线图, 其结果如图 6所示。由图可知, VO-DLP在30 min内其累积释放量达到70%以上, 且VO:Ex 1:2-DLP的药物释放速率明显高于VO:Ex 1:1-DLP, 表明柴翘挥发油被吸附进入介孔二氧化硅的孔道内, 随着VO-DLP载药量的增大, 其孔隙率降低, 与溶出介质的接触面积减小。因此, 其溶出速率减慢。

|
Figure 6 The cumulative release percentage of VO-DLP with different drug loads (n = 6, x ± s) |
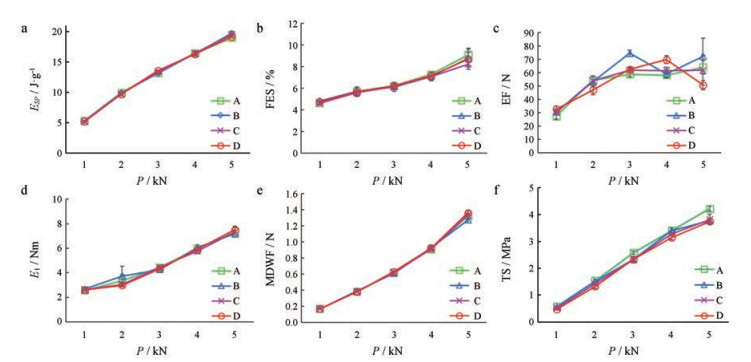
载体介孔二氧化硅载药前后在1~5 kN内压缩成型性结果如图 7所示。由图 7a、b可知, 在1~5 kN压力内, Sylysia 350FCP在载药前后, 其与微晶纤维素的混合粉末的塑性常数和快速弹性松弛情况几乎没有变化, 说明Sylysia 350FCP在吸附挥发油后几乎不影响物料的可压缩性; 由图 7c可知, 不同混合物料的出片力稍有波动, 但在可接受的范围内, 总体趋势为同等质量的不同混合物料在同一压力下压制成的片子其表面光滑程度基本一致, 即Sylysia 350FCP在吸附固化挥发油后不影响其作为润滑剂的特性, 与其他结果一致; 由图 7d、e可知, 不同物料在压缩过程中模壁力及摩擦功基本一致, 说明不同物料的压缩性基本一致, 即Sylysia 350FCP在吸附固化挥发油后不影响其压缩过程, 与上述结果一致; 由图 7f可知, 在1~5 kN压力内, 不同混合物料的抗张强度基本一致, 说明Sylysia 350FCP在吸附固化挥发油后不影响粉末的成型性。
|
Figure 7 The compressibility and compactibility of blended powder under different pressure: MCC-102+1% Sylysia 350FCP (A), MCC-102+1% VO:Ex 1:4-DLP (B), MCC-102+1% VO:Ex 1:2-DLP (C), MCC-102+1% VO:Ex 1:1-DLP (D). a: Esp - pressure curve; b: FES - pressure curve; c: EF - pressure curve; d: E1-pressure curve; e: MDWF-pressure curve; f: TS-pressure curve (n = 5, x ± s). ESP: Net energy per unit of quality; FES: Fast elastic stretch; EF: Ejection force; E1: Friction energy; MDWF: Middle die wall force; TS: Tensile strength |
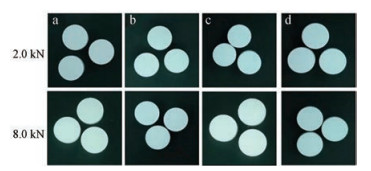
载体介孔二氧化硅载药前后在8.0 kN高压力下呈现的机械稳定性见图 8。由图可知, 按照不同药-辅质量比制得的挥发油固化粉末在8.0 kN高压力下压制成的片子均未见油溢出, 且放置两个月后片子表面依然光洁未出现油斑, 说明由Sylysia 350FCP制得的挥发油固化粉末, 机械稳定性较高, 可应用于工业化生产。
|
Figure 8 Appearance characteristics of tablets of blended powder under 8.0 kN high pressure: MCC-102+1% Sylysia 350FCP (a), MCC-102+1% VO:Ex 1:4-DLP (b), MCC-102+1% VO:Ex 1:2-DLP (c), MCC-102+1% VO:Ex 1:1-DLP (d) |
挥发油固化粉末作为润滑剂, 在连续生产过程中, 片剂的质量情况见表 3。由表可知, Sylysia 350FCP作为润滑剂及固化挥发油的载体, 在载药前后, 其片重及脆碎度无明显差异, 且均符合《中国药典》相关要求, 与物料压缩成型性结果一致, 可应用于工业化连续生产。
| Table 3 Quality inspection of tablets prepared under 2.0 kN pressure |
本文通过简单的搅拌工艺, 采用介孔二氧化硅为载体, 以柴翘挥发油为研究对象, 制得挥发油固化粉末, 具有制备工艺简单、易行, 避免了湿和热对挥发油稳定性的影响。通过对挥发油固化粉末热稳定性考察及载体载药前后其粉体学性质、压缩成型和机械稳定性等关键属性研究, 发现以介孔二氧化硅为载体固化挥发油具有载药量大、高热稳定性和高机械稳定性等优点, 且载药后不影响其作为固体润滑剂、助流剂的优良特性, 对物料的压缩过程及压缩成型性无显著影响, 并能够满足连续化生产的需求。此外, 采用SEM、PXRD、STA等方法对固化粉末进行表征。结果显示, 以Sylysia 350FCP为载体固化挥发油, 其固化机制为物理吸附; 通过对固化粉末体外溶出度的考察, 发现挥发油被吸附进入介孔二氧化硅的孔道内, 并可快速释放出来, 不会显著影响药物的吸收。将介孔二氧化硅用于液体物料的固化具有良好的应用前景, 值得进一步深入研究。
| [1] | Wang YQ, Yang YZ, Wu ZF, et al. Traditional function and modern research progress on volatile oil in Chinese materia medica[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 455–461. |
| [2] | Wu GT, Zhang XH, Li FQ. Advances in pharmaceutical studies on improvement of stability of volatile oils of Chinese materia medica[J]. Pharm Care Res (药学服务与研究), 2008, 8: 197–200. |
| [3] | Zhang JJ, Zhu Y, Yu JN, et al. Advances in novel carrier systems of chemical constituents from spice volatile oils[J]. Chin J Chin Mater Med (中国中药杂志), 2015, 40: 3932–3936. |
| [4] | Wang LX, Wang WW, Zhao SH, et al. Preparation and properties of ginger volatile oil microcapsules[J]. J Tianjin Univ Sci Tech (天津科技大学学报), 2017, 32: 15–19. |
| [5] | Ding L, Lin JH, Shen Y, et al. Preparation and in vitro release properties of Brucea javanica oil microcapsules[J]. China Pharm (中国药业), 2017, 26: 8–11. |
| [6] | Li ZJ, Yang W, Chen YM, et al. Preparation and characterization of peppermint oil-β-cyclodextrin polymer microsphere inclusion compound[J]. Chin Tradit Herbal Drugs (中草药), 2011, 42: 271–274. |
| [7] | Zhang H, Zhang B, Wang XJ, et al. Preparation, characterization and in vitro drug release of tea tree oil microspheres using β-cyclodextrin as framework material[J]. Int J Pharm Res (国际药学研究杂志), 2018, 45: 144–149. |
| [8] | Shi F, Zhao JH, Guo T, et al. Research progress on nano-drug delivery system of volatile oil from traditional Chinese medicine[J]. J China Pharm (中国药房), 2013, 24: 1429–1431. |
| [9] | Piao LM, Jin Y, Cui YL, et al. Preparation of Oenothera biennis oil solid lipid nanoparticles based on microemulsion technique[J]. Chin Med Mat (中药材), 2015, 38: 1290–1294. |
| [10] | Tang RQ, Xie H, Wu YC, et al. Effect of calcium hydrogen phosphate with different powder properties on adsorption and desorption characteristics of paeonol[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2018, 24: 26–31. |
| [11] | Zhang ZH, Li SX, Lv HX. Solidification of volatile oil of Cinnamomum cassia with polyvinylpolypyrrolidone[J]. Chin Pharm J (中国药学杂志), 2014, 49: 1913–1916. |
| [12] | Qian JM. The Study on Hydroxyapatite as Absorbent (羟基磷灰石作为吸收剂的研究)[D]. Changchun: Jilin University, 2014. |
| [13] | Yan HM, Jia XB, Zhang ZH, et al. Solidification of volatile oil with graphene oxide[J]. Acta Pharm Sin (药学学报), 2015, 50: 222–226. |
| [14] | Ning Q, Jiang YR, Zhang ZH, et al. Investigation of solidifying volatile oil from Cinnamomum cassia with porous starch[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2013, 19: 29–32. |
| [15] | Jiang YR, Zhang ZH, Ding DM, et al. Study on porous maize starch preparation and powdering coix seed oil[J]. China J Chin Mater Med (中国中药杂志), 2013, 38: 2287–2291. |
| [16] | Liu S, He DD, Liu Y, et al. Comparative study oil colloidal silica dioxide and β-cyclodextrin solidifying clove volatil oil[J]. J Nanjing Univ Tradit Chin Med (南京中医药大学学报), 2018, 34: 77–80. |
| [17] | Ye BN, Wang Z, Feng NP. Solidification of patchouli oil with fumed silica AEROPERL 300 Pharma[J]. Chin New Drug J (中国新药杂志), 2015, 24: 107–111. |
| [18] | Wei QH, Keck CM, Müller RH. Oral hesperidin-amorphization and improved dissolution properties by controlled loading onto porous silica[J]. Int J Pharm, 2017, 518: 253–263. DOI:10.1016/j.ijpharm.2016.11.005 |
| [19] | Miura H, Kanebako M, Shirai H, et al. Influence of particle design on oral absorption of poorly water-soluble drug in a silica particle-supercritical fluid system[J]. Chem Pharm Bull, 2011, 59: 686–691. DOI:10.1248/cpb.59.686 |
| [20] | Mai K, Al-Nimry S. Stabilization and amorphization of lovastatin using different types of silica[J]. AAPS PharmSciTech, 2017, 18: 2358–2367. DOI:10.1208/s12249-017-0717-1 |
| [21] | Zhou Y, Quan G, Wu Q, et al. Mesoporous silica nanoparticles for drug and gene delivery[J]. Acta Pharm Sin B, 2018, 8: 165–177. DOI:10.1016/j.apsb.2018.01.007 |
| [22] | Tian D, Shi MQ, Wang Y. Volatile oil from Forsythia suspense:chemical constituents and pharmacological effects[J]. Nat Prod Res Dev (天然产物研究与开发), 2018, 30: 1834–1842. |
| [23] | Xiao HM, He Y, Wang SW, et al. Component analysis of forsythia essential oil and study on their anti-viral activity[J]. Chin Med Her (中国医药导报), 2011, 8: 31–33. |
| [24] | Huo MY, Liu X, Lin Y, et al. Study of antipyretic active ingredients in Bupleurum Chinense volatile oil[J]. Chin J Pharm Anal (药物分析杂志), 2013, 33: 1202–1209. |
| [25] | Ilic I, Kása P Jr, Dreu R, et al. The compressibility and compactability of different types of lactose[J]. Drug Dev Ind Pharm, 2009, 35: 1271–1280. DOI:10.1080/03639040902932945 |
| [26] | Yap SF, Adams MJ, Seville JPK, et al. Single and bulk compression of pharmaceutical excipients:evaluation of mechanical properties[J]. Powder Technol, 2008, 185: 1–10. DOI:10.1016/j.powtec.2007.09.005 |
| [27] | Wu BY, Zhou YX, Pan X, et al. Improving the dissolution rate of water-insoluble diflunisal by γ-cyclodextrin metal-organic framework[J]. Acta Pharm Sin (药学学报), 2019, 54: 29–35. |
| [28] | Yu LF, Hu ZF, Su D, et al. Characterizing flowability of microcrystalline cellulose and its visualizing the correlation of the performance parameters[J]. Acta Pharm Sin (药学学报), 2018, 53: 806–811. |
 2019, Vol. 54
2019, Vol. 54


