2. 陕西中医药大学, 陕西省中医药管理局中药配伍重点研究室, 陕西 西安 712046
2. Key Laboratory of Shaanxi Administration of Traditional Chinese Medicine for TCM Compatibility, Shaanxi University of Chinese Medicine, Xi'an 712046, China
阿尔茨海默病(Alzheimer's disease, AD)即老年性痴呆, 是老年人群中最为常见的一种病症。随着全球人口的老龄化发展, 阿尔茨海默病的患病率逐年攀升[1,2]。临床症状一般表现为进行性记忆力减退和获得性知识丧失, 直至日常活动能力丧失为特征, 给社会和家庭带来沉重负担, 成为严重的社会和医疗卫生问题[3]。AD的病因并不明确, 一般认为与老化基础上的遗传、生化、神经内分泌、免疫和环境等因素有关。此外, 氧化损伤、铝中毒和铁中毒等均可导致胆碱能神经系统损害, 进而产生意识障碍[4]。目前, AD尚无法彻底治愈, 而常用的治疗药物主要包括:胆碱酯酶抑制剂、胆碱能受体激动剂、谷氨酸受体阻断剂、抗氧化类药物、抗自由基药物和雌激素等, 但均属于单靶向药物, 有效性和特异性显得尤为不足, 只能改善或者缓解患者的症状, 且这些药物有着较为严重的不良反应, 限制了其临床应用[5,6]。中药因其多靶点、多系统、多环节和多途径的特征在治疗AD上表现出独特的优势[7], 文献[8]报道人参、天麻、黄芪、银杏、吴茱萸和雷公藤等可用于治疗AD。因此, 目前越来越多的临床实践研究发现, 中西医联合用药治疗阿尔茨海默病的疗效显著, 不良反应少, 在很大程度上改善了老年患者的学习认知能力。
经过临床调查发现, 银杏酮酯-多奈哌齐(GD)联合用药最引人注目, 其治疗AD效果显著、不良反应低, 因而在临床实践中应用广泛[9,10]。中药银杏中最主要的成分即黄酮类和萜内酯类成分, 通过提高脑胆碱能神经功能, 增加脑血流量从而来保护脑神经细胞改善脑神经损害[11]。多奈哌齐是经美国FDA批准上市的属于第二代特异的可逆性中枢胆碱酯酶(acetyl cholinesterase, AChE)抑制剂, 可以选择性抑制AChE的活性, 使突触间隙乙酰胆碱(acetylcholine, ACh)分解减慢, 提高ACh的含量, 广泛用于轻、中度阿尔茨海默病和血管性痴呆治疗, 可以改善患者认知功能和全脑功能[12,13]。文献[8]研究发现, 在AD动物模型上, 银杏酮酯和多奈哌齐联用明显提高ACh, 改善脑部ACh缺乏现状, 优于单独使用。但是临床上对于两药的应用仍停留在临床医生经验用药的层面, 对其量效关系和配伍比例未见报道。
药物的剂量与临床效应之间存在正比的关系, 即在“一定的”范围内, 当一种药物的含量/浓度增加或减少时, 药物的效应也会随之增强或减弱, 这就是药物量效关系[14], 是确定临床用药的基础。而药物联用是按病情需要和药性特点, 有选择地将两药及不同配比同用, 从而起到协同增效的治疗作用。因此, 在本实验中采用多因素损伤法进行造模, 先以临床常用配比(1:1)为基础设计不同剂量(0.5、1、2、4、6、8和10 mg·kg-1·d-1)来探讨银杏酮酯-多奈哌齐联用时的最佳治疗剂量, 接着基于最佳剂量选择银杏酮酯-多奈哌齐不同配比(1:0、2:1、3:1、4:1、8:1、1:1、1:8、1:4、1:3、1:2和0:1)为研究对象, 观察两药不同配比联用后对痴呆小鼠Morris水迷宫行为学、神经递质、相关酶指标及脑组织损伤的影响。本文采用主成分分析联合多指标综合指数法评价银杏酮酯-多奈哌齐不同剂量及配比抗AD的活性, 从而筛选出银杏酮酯和多奈哌齐联用的最佳剂量和配比。进而为临床上二者合理联用提供实验依据, 同时对中西医结合联合用药治疗AD的研究提供参考。
材料与方法药物 银杏酮酯分散片(国药准字Z20050670), 购自江苏神龙药业股份有限公司; 盐酸多奈哌齐(批准文号:国药准字H20070181)购自卫材(中国)药业有限公司。
动物 SPF级雄性ICR小鼠, 体质量18~22 g, 购自于南京市江宁区青龙山动物繁殖场, 合格证号: SCXK (苏) 2017-0001。将所有小鼠随机分笼饲养, 室内温度(22±2) ℃, 相对湿度(50±5) %, 提供12 h光照且明暗交替。保证每笼小鼠自由进食和饮水。实验方案经南京中医药大学动物实验伦理委员会批准, 所有程序均严格按照动物使用和护理的伦理原则进行。动物实验前适应性饲养1周。
试剂与仪器 无水氯化铝(10000862)购自国药集团化学试剂有限公司; 盐酸东莨菪碱(S113892)、硫酸亚铁七水合物(F116340)和D-半乳糖(G100366)均购自阿拉丁试剂有限公司; 小鼠AChE elisa试剂盒(YFXEM00765)、小鼠ACh elisa试剂盒(YFXEM00564)、小鼠单胺氧化酶(monoamine oxidase, MAO) elisa试剂盒(YFXEM00076)和小鼠乙酰胆碱转移酶(choline acetyltransferase, ChAT) elisa试剂盒(YFXEM00769)均购自南京翼飞雪生物科技有限公司; 生理盐水(lw17-09-20-1)购自南京良玮生物科技有限公司。Morris水迷宫视频跟踪分析系统购自上海吉量软件科技有限公司; 酶标仪(Inspire)购自Perkins Elmer公司。
药物制备 将银杏酮酯分散片和多奈哌齐研磨至粉状, 称取适量粉末溶于0.5%羧甲基纤维素钠溶液中。动物给药剂量按体表面积换算系数计算:人临床用量×0.002 6/20×1 000×临床等效量的倍数, 银杏酮酯分散片人临床剂量为450 mg·d-1, 多奈哌齐人临床剂量为5 mg·d-1。根据公式所得银杏酮酯的临床等效量为58.5 mg·kg-1·d-1, 多奈哌齐的临床等效量为0.65 mg·kg-1·d-1。
多因素损伤痴呆模型的建立 适应性饲养1周后, 小鼠随机分为正常组和模型组。模型组小鼠每日灌胃无水氯化铝(3.3 mg·kg-1)和硫酸亚铁七水合物(50 mg·kg-1)及腹腔注射东莨菪碱(0.33 mg·kg-1)和D-半乳糖(120 mg·kg-1), 连续4周[15], 复制小鼠痴呆模型; 正常组小鼠用0.9%生理盐水重复相同操作。
基于银杏酮酯-多奈哌齐临床常用量(1:1)优选抗痴呆作用的最佳剂量 将模型小鼠随机分为10组, 每组10只, 即模型组(M1)、多奈哌齐组(D)、银杏酮酯组(G)、0.5倍量组(0.5×)、1倍量组(1×, 即临床等效量)、2倍量组(2×)、4倍量组(4×)、6倍量组(6×)、8倍量组(8×)和10倍量组(10×)。造模结束后, 除正常组(C1)和模型组(M1)小鼠灌胃给予0.2 mL·d-1生理盐水, 各组小鼠分别灌胃给予各自剂量的药物治疗, 连续给药10天。
基于最佳剂量优选银杏酮酯-多奈哌齐抗痴呆作用的最佳配比 将模型小鼠随机分成12组, 每组10只, 分别为模型组(M2)和银杏酮酯-多奈哌齐不同配比给药组(即1:0、2:1、3:1、4:1、8:1、1:1、1:8、1:4、1:3、1:2、0:1)。造模结束后, 除正常组(C2)和模型组(M2)小鼠灌胃给予0.2 mL·d-1生理盐水, 各组小鼠分别灌胃给予各自配比的药物治疗, 连续给药10天。给药剂量换算同上。
Morris水迷宫行为学测试 为了评价药物的治疗效果, 在给药4天后, 进行持续6天的Morris水迷宫行为学实验, 测试各组小鼠空间学习记忆能力。水迷宫水温控制在(20±1) ℃, 站台位置(固定于第三象限)及水池外固有参照物如桌子、窗帘和门等保持固定不变, 且水面高出站台0.5 cm。实验时将小鼠面向池壁放入水中, 自由游泳60 s。录像系统自动记录小鼠找到平台的时间和游泳路径。若小鼠未在1 min内找到平台, 将其引导至平台上, 并停留10 s。每天从2个不同象限对小鼠进行训练, 连续4天。在第5天进行定位航行实验, 1 min内小鼠找到平台的时间即为潜伏期, 未找到平台的按1 min计。第6天撤除平台进行空间探索实验, 于站台位置对角象限为起始点, 将小鼠面向池壁放入水中, 记录小鼠在1 min内游泳轨迹全过程。分别记录小鼠潜伏期、穿越站台次数、第三象限占总路程百分比、第三象限游泳时间对小鼠空间学习和记忆能力进行评价。
检测指标 Morris水迷宫实验结束后, 立即脱颈处死小鼠并在冰上快速分离出小鼠的大脑皮层和海马组织, 液氮迅速冷冻。称取一定质量脑组织在冰上匀浆, 按照说明书要求测定ACh含量和AChE、ChAT和MAO活性。
苏木精-伊红(hematoxylin-eosin, HE)染色 各组小鼠处死后, 每组中选取2只小鼠在冰上快速取出脑组织, 于4 ℃生理盐水中漂洗去除血渍, 滤纸拭干, 置于福尔马林(4 ℃)中固定, 进行病理切片的考察。
数据统计与分析 将所有数据导入SPSS 19.0中用Descriptives进行统计, 结果采用均数±标准差(x±s)表示; 与正常组和模型组比较采用ANOVA中的Dunnett法进行组间两两比较, P < 0.05表示有统计学意义。
效应整合 根据多指标综合指数法, 对潜伏期、穿越站台次数、第三象限占总路程百分比、第三象限时间、ACh、AChE、MAO和ChAT多个指标进行标化和效应整合。多指标综合指数法就是对实验过程中各指标数据进行标准化, 当模型组的相应指标数值(value, V)与正常组相比升高时, V标化 = (V模型-V给药)/V模型; 当模型组的相应指标与正常组相比降低时, V标化 = (V给药-V模型)/V模型。查阅近10年来阿尔茨海默病模型相关文献160余篇, 其中检测潜伏期(QFQ)的有107篇, 检测穿越站台次数(No.)的有57篇, 检测AChE的有43篇, 检测病理切片(HE)的有38篇, 检测ChAT的有20篇, 检测第三象限时间(tⅢ)的有17篇, 检测第三象限占总路程百分比(Ⅲ%)的有14篇, 检测ACh的有10篇, 检测MAO的有8篇。此外还需要结合同行专家对各指标进行评分, 最后根据直观的变量重要性投影值(variable importance in the projection, VIP)处理结果分别独立给出各指标的权重系数, 该总效应值即为各指标标化值乘以权重的加和值[16-18]。各个指标的VIP的计算是将所测得的所有指标数据导入MassLynx v4.1 (Waters公司)软件的EZ info中, 采用主成分分析法(principal components analysis, PCA)中的Pareto进行规格化处理, 得到各指标的得分图, 然后采用软件中的偏最小二乘法(partial least squares method, PLS)分析得到各指标VIP值, 依据VIP值的大小判断各指标对分类的重要程度, 一般VIP > 1的指标认为其对分类的贡献比较大[19]。最终确定各指标的权重系数:潜伏期的权重系数为3, 穿越站台次数、AChE和病理切片得分的权重系数为2, ChAT、MAO、ACh、第三象限时间和第三象限路程百分比的权重系数为1。此外, 对不同剂量、配比的联用组和的相应药效的指标数据进行PCA分析, 计算各给药组到正常组的相对距离来评价不同配比联用给药组抗痴呆的效应。
结果 1 外观形态经过持续4周造模后, 模型小鼠表现出食欲不振、皮毛粗糙失去光泽且伴有不同程度的脱毛等现象。正常组小鼠行动矫健、皮毛光洁、饮食活动正常。各给药组小鼠的情况较模型组有不同程度的改善。
2 不同给药组小鼠Morris水迷宫行为学考察 2.1 银杏酮酯-多奈哌齐不同剂量对多因素神经损伤小鼠学习记忆能力的影响持续10天给药后, 进行水迷宫行为学测试, 于训练第5天进行定位航行实验, 结果表明(表 1)多因素造模后的小鼠潜伏期较正常组小鼠明显延长且有显著性差异(P < 0.01), 不同剂量组治疗后除单用多奈哌齐、联用4倍量(GD 4×)和6倍量(GD 6×)无显著性缩短外, 其余剂量组均可以显著地降低潜伏期的时间, 其中联用1倍量(GD 1×)和2倍量(GD 2×)潜伏期与正常组接近。次日进行空间探索实验发现模型组无论是穿越站台次数(P < 0.01)还是在目标象限停留的时间(P < 0.05)及其第三象限路程百分比(P < 0.01)均较正常组显著降低, 不同剂量给药后均有不同程度地提高, 表明不同给药剂量均可改善痴呆小鼠的记忆学习能力。
| Table 1 Effects of behavioral indicators of Morris water maze in dementia mice after ginkgo ketoester tablet - donepezil (GD) combinations. After administration, the orientation navigation and space exploration tests were conducted. The latency to reach the platform, swim distance and the number of platform location crossing were film recorded by a camera, mounted above the center of the water maze. The results showed that the ability of spatial learning and memory of model mice had dramatically decreased and recovered after administration. n = 6-10, x±s. #P < 0.05, ##P < 0.01 vs C; *P < 0.05, **P < 0.01 vs M. C1: Normal group in different dose experiment; M1: Model group in different dose experiment; C2: Normal group in different proportion experiment; M2: Model group in different proportion experiment |
造模结束后, 连续给药10天开始进行Morris水迷宫测试。结果如表 1所示, 与正常组小鼠相比, 模型组小鼠潜伏期明显延长且有显著性差异(P < 0.01)。撤除平台后进行空间探索实验发现, 模型小鼠穿越站台次数(P < 0.01)、第三象限时间(P < 0.05)和第三象限路程百分比(P < 0.01)均明显小于正常组。说明每日灌胃和注射无水氯化铝、硫酸亚铁七水合物、东莨菪碱和D-半乳糖对小鼠学习和记忆能力造成损失, 表明多因素神经损伤痴呆小鼠模型成功。给予不同配比的银杏酮酯-多奈哌齐治疗后, 与模型组小鼠相比, 发现GD 2:1 (P < 0.05)、GD 3:1 (P < 0.05)、GD 1:2 (P < 0.05)、GD 1:1 (P < 0.01)和GD 0:1 (P < 0.01)这5个配比治疗组小鼠的潜伏期均明显降低。在空间探索实验中, GD 2:1 (P < 0.05)、GD 1:1 (P < 0.01)、GD 1:4 (P < 0.05)、GD 1:2 (P < 0.05)和GD 0:1 (P < 0.05)配比组穿越站台次数较模型组小鼠显著增加。此外, 由第三象限路程百分比可以看出GD 2:1、GD 3:1、GD 1:1和GD 1:2这4个配比组均高于模型组(P < 0.05)。其余各配比给药组有一定的治疗作用, 但不显著。
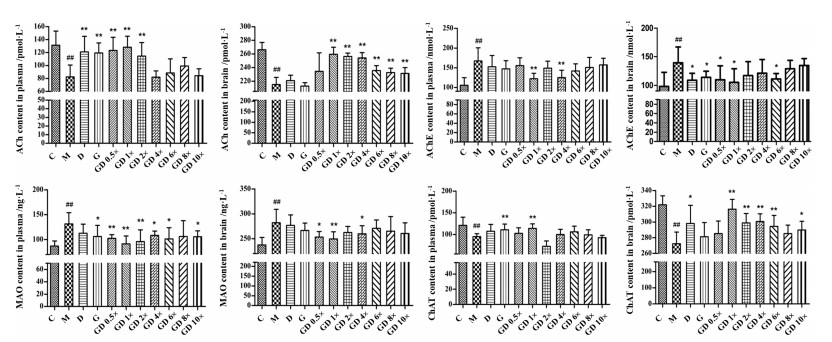
3 不同给药组小鼠对血浆及大脑中神经递质及其相关酶的影响 3.1 银杏酮酯-多奈哌齐不同剂量对多因素神经损伤痴呆小鼠血浆和大脑中ACh、AChE、ChAT和MAO的影响多因素损伤造模后, 模型小鼠各指标较正常小鼠均有显著差异(P < 0.01)。在血浆中, 单用银杏酮酯和GD 1×对降低的ACh含量和ChAT活性有显著升高(P < 0.01), 而单用多奈哌齐、GD 0.5×和GD 2×仅回调降低的ACh含量(P < 0.01);对于造模后升高的AChE和MAO, GD 1×和GD 4×均有显著降低作用(P < 0.05或P < 0.01)。单用银杏酮酯、GD 0.5× (P < 0.01)、GD 2× (P < 0.01)、GD 6× (P < 0.05)和GD 10× (P < 0.05)对MAO也有显著降低。GD 1×、GD 2×、GD 4×、GD 6×和GD 10×可提高脑组织中ACh含量和ChAT的活性(P < 0.05或P < 0.01); GD 0.5×和GD 1×对升高的AChE和MAO均有显著降低, 此外, 其余各剂量组均有一定程度治疗作用。结果见图 1。
|
Figure 1 Effects of different doses of GD administration on neurotransmitters and related enzymes in dementia mice. Immediately after the completion of behavioral tests, the animals were sacrificed. The cerebral cortex and hippocampus were rapidly isolated on ice and rapidly homogenized with 10 volumes of ice-cold physiological saline, and then centrifuged at 4℃. The supernatants were collected for the further analysis. Acetylcholine (ACh), acetyl cholinesterase (AChE), choline acetyltransferase (ChAT) and monoamine oxidase (MAO) were measured by commercial available kits. All procedures were carried out according to the manufacturer's protocol using a microplate reader to measure the absorbance at their respective absorption wavelengths. n = 6-10, x±s. ##P < 0.01 vs C; *P < 0.05, **P < 0.01 vs M |
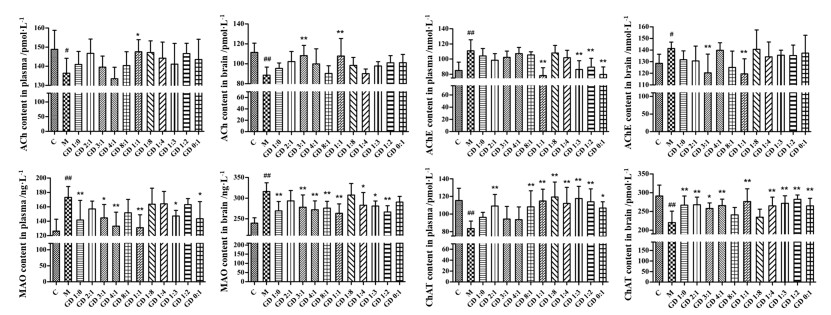
本研究结果发现, 造模后的小鼠无论是血浆还是脑组织中ACh含量和ChAT活性与正常组小鼠相比均显著降低(P < 0.05或P < 0.01), 而MAO和AChE的活性较正常小鼠显著升高。说明模型小鼠胆碱能神经递质遭到破坏且有老化现象, 表明造模成功。经不同配比药物治疗后, 与模型组比较发现, 在血浆样品中, 仅GD 1:1对降低的ACh (P < 0.05)和ChAT (P < 0.01)均有显著升高, GD 8:1 (P < 0.01)、GD 1:8 (P < 0.01)、GD 1:2 (P < 0.01)、GD 2:1 (P < 0.01)、GD 1:4 (P < 0.01)、GD 1:3 (P < 0.01)和GD 0:1 (P < 0.05)仅对ChAT有回调的作用; 而GD 1:1、GD 1:3和GD 0:1对升高的MAO和AChE均有显著降低(P < 0.05), GD 1:0 (P < 0.01)、GD 3:1 (P < 0.05)和GD 4:1 (P < 0.01)仅回调了升高的MAO活性。而在脑组织中, GD 3:1和GD 1:1 ACh含量和ChAT活性均不同程度升高(P < 0.05), ChAT中, GD 8:1和GD 1:8有一定的回调趋势但未表现出显著性差异; GD 3:1和GD 1:1均显著降低MAO和AChE (P < 0.01), 脑组织MAO, GD 2:1、GD 1:8和GD 0:1有一定的回调趋势但没有显著性差异。具体结果见图 2。
|
Figure 2 Effects of different GD combination on neurotransmitters and related enzymes in dementia mice. The animals were sacrificed after the completion of Morris water maze. The cerebral cortex and hippocampus were rapidly isolated on ice and rapidly homogenized with 10 volumes of ice-cold physiological saline, and then centrifuged at 4 ℃. The supernatants were collected to determine the ACh, AChE, MAO and ChAT kits. All procedures were carried out according to the manufacturer's protocol using a microplate reader to measure the absorbance at their respective absorption wavelengths. n = 6-10, x±s. #P < 0.05, ##P < 0.01 vs C; *P < 0.05, **P < 0.01 vs M |
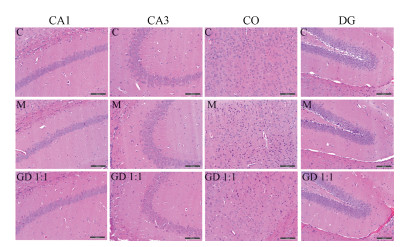
脑组织病理切片染色显示, 正常组小鼠脑组织细胞形态完好, 细胞膜、核膜清晰, 未出现细胞核固缩、深染、老年斑等情况。而模型组小鼠大脑组织中可见大量细胞核固缩、深染、较多老年斑、少量空泡样病变和局部细胞核淡染。不同配比给药组有一定改善作用, 图 3列出评分最低给药组(即GD 1:1)病理切片图, 可见其大脑损伤不严重, 仅表现出较少细胞核固缩深染, 并未出现老年斑与空泡样病变。该病理切片表明两药联用临床剂量1:1时对脑部病理损伤最小。
|
Figure 3 Hematosylin-eosin staining (HE) of brain tissue (×200) |
将所测指标的源数据导入MassLynx v4.1中EZ info生成PCA图。其中, 每一个点表示1个样品, 且药效相似的点会被聚到一起。本实验采用相对距离的方法计算PCA中模型、给药组与正常组之间的距离, 从而评判不同给药组抗痴呆作用的程度。从图 4可以看出, 正常组中心大约是(4.22, -0.90), 模型组中心大约是(-4.28, -0.65), 可见正常组与模型组之间获得较好分离, 其他各不同剂量给药组散落在正常组与模型组之间, 其中两药联用1倍量与正常组最为接近, 中心大约是(2.84, 0.21)。结果表明多因素损伤痴呆小鼠模型复制成功, 不同给药组对痴呆小鼠有不同程度改善作用, 其中联用药组1倍量改善作用最好。

|
Figure 4 PCA score plot of anti-dementia indexes after different doses of GD administration. Data of measured indicators were imported into EZ info in MassLynx v4.1 to generate a PCA map. Each point represented a sample. Results showed that normal and model groups got a better separation. The other different dose groups were scattered between the normal and model groups in which the combination of two drugs at the dose of 1 time had the best separation with the model group |
同上操作得到不同配比的PCA图(图 5), 图中可以看出正常组中心大约(4.01, 0.76), 模型组中心大约是(-3.94, 0.74), 两组得到较好分离, 提示痴呆小鼠造模成功。不同给药组散落在正常组与模型组之间, 且GD 1:1、GD 1:2和GD 1:3的中心离正常组较近, 说明抗痴呆效果较好, 其中GD 1:1中心离正常组最近, 表示该配比组对痴呆小鼠改善作用最好。GD 1:8和GD 8:1组中心离模型组最近, 表示它们对痴呆小鼠改善作用最弱。

|
Figure 5 PCA score plot of anti-dementia indexes after different GD combination. Data of measured indicators were imported into EZ info in MassLynx v4.1 to generate a PCA map. Each point represented a sample. Results showed that normal and model groups got a better separation. The groups of GD 1:1, GD 1:2 and GD 1:3 were closer to the normal group indicating that they had a better effect on anti-dementia. However the group of GD 1:1 was closest to the normal group, which indicated that it had the best effect on dementia mice |
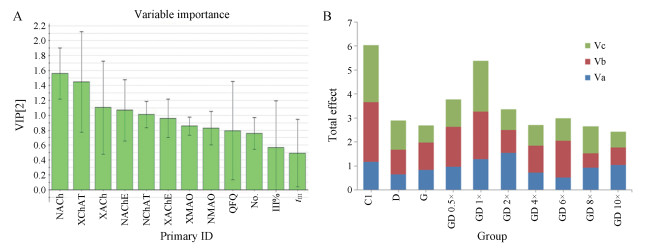
将所有指标数据导入MassLynx v4.1 EZ info中, 采用偏最小二乘法分析得到各指标的VIP值, 如图 6A所示, 指标对分类的贡献度与VIP值大小呈正比关系。结果发现脑组织中ACh、AChE和ChAT, 血浆中ACh和ChAT的VIP值均大于1, 而其余各指标的VIP值较小。采用多指标综合指数法对各个指标进行归一化处理, 得到总的效应值(表 2), 最后得到不同剂量的银杏酮酯-多奈哌齐抗痴呆总效应值(图 6B), 其大小顺序为: GD 1× > GD 0.5× > GD 2× > GD 6× > D > GD 4× > G > GD 8× > GD 10×, 说明银杏酮酯-多奈哌齐临床剂量1倍量时, 抗痴呆效应最好。实验结果表明基于临床常用配比的不同剂量中, 1倍量抗阿尔茨海默症效果最佳, 0.5倍量总效应值仅次于1倍量。当两药剂量在0.5~6倍量时, 效应值大于两药单用, 而增至8~10倍量时效应值最低, 治疗效果最差, 提示两药联用在一定剂量范围内(0.5~6倍量)表现出增效的作用, 其中1倍量效果最好, 而8~10倍量内可能表现出一定的拮抗作用。
|
Figure 6 The VIP plot of anti-dementia indexes (A) and total effect (B) after different doses of GD administration. In picture A, all indicator data were imported into EZ info in MassLynx v4.1 to obtain the VIP value by partial least squares analysis. And then each indicator was normalized by multi-attribute comprehensive index method. QFQ: Escape latency; No.: Platform crossing; tⅢ: Third quadrant time; Ⅲ%: Third quadrant distance percent; N: Brain tissue; X: Plasma. In picture B, total effect values were represented as column diagram for intuitive comparison. Va: Standardized values a; Vb: Standardized values b; Vc: Standardized values c |
| Table 2 Standardized indexes and total effect values of GD combination. TE: Total effect |
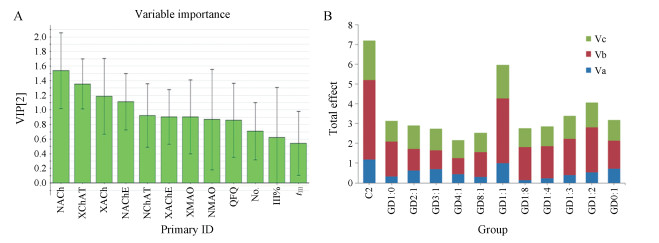
VIP图(图 7A)可得出不同配比治疗后各指标的VIP值。结果发现, 血浆中ChAT、AChE和MAO及脑组织中MAO的VIP值大于1, 其余各指标的VIP值均较小。通过多指标综合指数法归一化处理, 得到各指标效应值(表 2), 最后得到不同配比的总效应值(图 7B)。其大小顺序为: GD 1:1 > GD 1:2 > GD 1:3 > GD 0:1 > GD 1:0 > GD 2:1 > GD 1:4 > GD 1:8 > GD 3:1 > GD 8:1 > GD 4:1, 表明GD 1:1治疗效果最佳。这些研究结果表明, 在两药不同比例配伍时, 随着多奈哌齐所占比例增加时(GD 1:1~GD 1:3), 两药联用效果远大于银杏酮酯和多奈哌齐单用, 表现出两药联用的协同增效作用, 但随着多奈哌齐所占比例进一步增加时, 两者配伍后的总效应值逐渐降低, 说明两药在一定配比范围内协同增效。
|
Figure 7 The VIP plot of anti-dementia indexes (A) and total effect (B) after different GD combination. In picture A, all indicator data were imported into EZ info in MassLynx v4.1 to obtain the VIP value by partial least squares analysis. And then each indicator was normalized by multi-attribute comprehensive index method. In picture B, total effect values were represented as column diagram for intuitive comparison |
结合PCA法和多指标综合指数法的结果可知, 两药联用1倍量的抗痴呆效果最好, 两种分析方法所得结果相一致。在0.5~6倍量时, 两者联用表现出增效作用, 且在1倍量时达到顶峰。提示银杏酮酯-多奈哌齐比例为1:1时, 即小鼠用药剂量(银杏酮酯分散片58.5 mg·kg-1·d-1, 多奈哌齐0.65 mg·kg-1·d-1)为临床用量的1倍量时对多因素损伤小鼠的学习记忆改善最好。
7.2 银杏酮酯-多奈哌齐不同配比抗痴呆总效应值由PCA图和多因素指标综合指数法均可知GD 1:1组总效应值最大。在两者配比GD 1:1~GD 1:3时, 总效应值是远大于单用两药的, 而随着多奈哌齐的所占比例进一步增加时, 其效应值小于两单味药。提示GD 1:1组对于改善多因素损伤痴呆小鼠的学习记忆能力最强, 这与临床上银杏酮酯和多奈哌齐使用相一致。
讨论AD是病因复杂机制尚不完全明确的疾病, 本实验通过给小鼠腹腔注射D-半乳糖(加速动物衰老)、东莨菪碱(阻断胆碱受体)和灌胃三氯化铝、硫酸亚铁溶液(进行铝、铁中毒)造模, 模拟乙酰胆碱分泌不足、金属元素摄入体内和加速颅内老化等多种因素损伤致AD的发生, 避免单一损伤造模的偏颇[20]。Morris水迷宫通常用于研究与空间学习和记忆功能评估相关的大脑区域, 因此通过该行为学来评价不同药物对痴呆小鼠的影响。早在1982年就有研究报道胆碱能神经递质系统的破坏是与年龄相关的中枢神经系统功能障碍和认知丧失的主要原因[21], 而AChE和ChAT分别是水解和合成ACh的相关酶。此外, 研究发现MAO-B被认为是老化的标志, 称之为老化相关酶。因此本实验还选择了ACh、AChE、MAO和ChAT等多个效应指标来综合评价其药效, 但各指标的评价标准和药物对各指标的反应灵敏度往往不一致, 需从一个整体的、直观的角度对这些不同指标进行标准化, 统一计量单位, 从而形成整合效应来进行综合评价。
综合指数是编制总指数的基本形式, 把不同性质、不同类别和不同计量单位的指标经过指数化, 按照同类指标相乘、异类指标相加的方法进行指标综合, 然后比较总效应值, 进而便于观察药物发挥效应的强弱[22]。PCA是考察多个变量间相关性的一种多元统计方法, 通过恰当的数学变换, 使新变量主成分成为原变量的线性组合, 并选取少数几个在总信息量中比例较大的主成分来分析事物的一种方法[23,24], 主要作用在于揭示数据集中观测变量的分组、趋势及离群值[25]。此外, 对各指标权重的确定还参考专家评分, 即同行专家依据指标模型涉及的药物干预环节, 独立给出各指标权重系数。两者相结合在一定程度上弥补各自不足, 并采用PLS-DA中VIP值对各个指标进行评分。因此, 本文采用多种方法对银杏酮酯-多奈哌齐不同量比各指标评分, 避免单一评分的偏颇, 为确定权重系数提供客观的理论依据。
综合多指标综合指数法和PCA对银杏酮酯、多奈哌齐单用和1:1联用的7个剂量总效应值进行比较, 结果发现两药联用0.5~1倍量时呈量效关系, 在1倍量(即临床等效量)时治疗效果最佳, 2~6倍量时治疗效果虽然弱于1倍量但明显优于两药单用, 当剂量进一步增大至8~10倍量时, 治疗效果不及两药单用, 提示两药在一定剂量范围内随着剂量增加效应增加。而后基于优选的最佳剂量进一步评价银杏酮酯-多奈哌齐不同配比的总效应, 结果发现两药配伍随着银杏酮酯或多奈哌齐的所占比例增大, 总效应值呈下降趋势。综上, 本研究结果表明, 当银杏酮酯―多奈哌齐配伍比例1:1, 剂量为临床常用量时抗痴呆效果最好。
| [1] | Cheng XR, Zhou WX, Zhang YX. The behavioral, pathological and therapeutic features of the senescence-accelerated mouse prone 8 strain as an Alzheimer's disease animal model[J]. Ageing Res Rev, 2014, 13: 13–37. DOI:10.1016/j.arr.2013.10.002 |
| [2] | Romberg C, McTighe SM, Heath CJ, et al. False recognition in a mouse model of Alzheimer's disease: rescue with sensory restriction and memantine[J]. Brain, 2012, 135: 2103–2114. DOI:10.1093/brain/aws074 |
| [3] | Selkoe DJ. Alzheimer's disease: genes, proteins, and therapy[J]. Physiol Rev, 2001, 81: 741–766. DOI:10.1152/physrev.2001.81.2.741 |
| [4] | Wang WZ. Neurology[M]. Beijing: People's Medical Publishing House, 2001: 249-251. |
| [5] | Ma XW, Li JZ, Zhang TT, et al. Recent development of non-steroidal anti-inflammatory drugs on the neuro-inflammation of Alzheimer's disease[J]. Acta Pharm Sin (药学学报), 2014, 49: 1211–1217. |
| [6] | Peng Y, Li PP, Li L, et al. Progress of clinical trials in Alzheimer's disease drugs[J]. Acta Pharm Sin (药学学报), 2016, 51: 1185–1195. |
| [7] | Zang CX, Bao XQ, Sun H, et al. Research progress of traditional Chinese medicine compound in the treatment of Alzheimer's disease[J]. Pharm Clin Chin Mater Med (中药药理与临床), 2016, 32: 157–161. |
| [8] | Wang SS, Zhang Z, Zhang X, et al. Advances in immunotherapy of Alzheimer's disease with traditional Chinese medicine[J]. Acta Pharm Sin (药学学报), 2018, 53: 1023–1029. |
| [9] | Stein C, Hopfeld J, Lau H, et al. Effects of Ginkgo biloba extract EGb 761, donepezil and their combination on central cholinergic function in aged rats[J]. J Pharm Pharm Sci, 2015, 18: 634–646. DOI:10.18433/J3WC8V |
| [10] | Yancheva S, Ihl R, Nikolova G, et al. Ginkgo biloba extract EGb 761®, donepezil or both combined in the treatment of Alzheimer's disease with neuropsychiatric features: a randomised, double-blind, exploratory trial[J]. Aging Ment Health, 2009, 13: 183–190. DOI:10.1080/13607860902749057 |
| [11] | Xie CM, Zheng GL, Zhong ZY, et al. Effect of ginkgo leaf on learning and memory in Alzheimer's disease mice[J]. Chin J Comp Med (中国比较医学杂志), 2010, 20: 26–29. |
| [12] | Richard JL, Cosman KM, Porsteinsson AP. Donepezil in the treatment of severe Alzheimer's disease[J]. Aging Health, 2007, 3: 419–435. DOI:10.2217/1745509X.3.4.419 |
| [13] | Liu DM, Zhang M, Jiang XM, et al. Protective effects and the mechanisms of donepezil and galantamine on neuronal injury induced by glucose deprivation/reoxygenation[J]. Acta Pharm Sin (药学学报), 2017, 52: 928–935. |
| [14] | Li SJ, Tang YP, Li WX, et al. Comparing tonifying blood effects of Danggui-Honghua with different proportions on blood deficiency mice[J]. Chin Pharmacol Bull (中国药理学通报), 2014, 30: 874–879. |
| [15] | Wei W, Wu XM, Li YJ. Experimental Methodology of Pharmacology (药理实验方法学)[M]. 4th ed. Beijing: People's Medical Publishing House, 2010: 320-321. |
| [16] | Li WX, Tang YP, Guo JM. Comparative assessing the effects of angelica Root and Chuanxiong on the hemorheology and the blood coagulation function in acute blood stasis rats[J]. Chin J Integr Tradit Chin West Med (中国中西医结合杂志), 2012, 32: 806–811. |
| [17] | Li SJ, Li WX, Tang YP, et al. Comparative analysis of the promoting blood effects of the combination of different proportions of Danggui and Honghua by the principal component analysis and multi-attribute comprehensive index methods[J]. Acta Pharm Sin (药学学报), 2014, 49: 1304–1309. |
| [18] | Li WX, Tang YP, Shang EX, et al. Analysis on correlation between general efficacy and chemical constituents of Danggui-Chuanxiong herb pair based on artificial neural network[J]. China J Chin Mat Med (中国中药杂志), 2012, 37: 2935–2942. |
| [19] | Li WX, Huang MY, Tang YP, et al. Metabolomic study of the action mechanism of nourishing blood effect of Fo-Shou-San on blood deficiency mice[J]. Acta Pharm Sin (药学学报), 2013, 48: 1301–1306. |
| [20] | Shi YW, Chen Y, Liu MQ, et al. Research of Jiawei Kaixin San on improving learning and memory abilities of multiple neuronal damage induced dementia mice[J]. J Nanjing Univ Tradit Chin Med (南京中医药大学学报), 2017, 33: 44–48. |
| [21] | Bartus RT, Dean RL 3rd, Beer B, et al. The cholinergic hypothesis of geriatric memory dysfunction[J]. Science, 1982, 217: 408–414. DOI:10.1126/science.7046051 |
| [22] | Ma RJ, Miao MS. A new method for evaluating the efficacy of Chinese medicine: the comprehensive weight coefficient method[J]. Tradit Chin Drug Res Clin Pharm (中药新药与临床药理), 2011, 22: 569–572. |
| [23] | Li YS, Zeng ZX, Zhang M, et al. Application of primary component analysis in the methods of comprehensive evaluation for many indexes[J]. J Hebei Univ Technol (河北工业大学学报), 1999, 28: 94–97. |
| [24] | Nie L, Hu Z, Luo GA, et al. Generation of reference fingerprint using principal component analysis[J]. Chin Tradit Pat Med (中成药), 2005, 27: 621–625. |
| [25] | A JY, He J, Sun RB. Multivariate statistical analysis for metabolomic data: the key points in principal component analysis[J]. Acta Pharm Sin (药学学报), 2018, 53: 929–937. |
 2019, Vol. 54
2019, Vol. 54


