肠易激综合征是一种常见的以腹部不适、腹痛、排便习惯和大便性状改变为特征的功能性肠道疾病, 同时伴有焦虑、抑郁等临床症状。现代药理学研究表明, 该病是一种多因素疾病, 具有慢性、反复发作且与其他功能胃肠道疾病重叠的特点, 会严重影响患者的生活质量[1]。目前其病因和发病机制尚未完全阐明, 可能的影响因素主要包括社会心理因素、遗传、感染、食物、药物等。发病机制可能与脑-肠轴调节异常、肠黏膜屏障功能紊乱、低度炎症、内脏痛觉高敏性、免疫系统异常、肠道微生态失衡等有关。中医理论认为, IBS多属于中医“泄泻”、“腹痛”等范畴。病机的关键在于脾胃的功能障碍, 肝脾不和, 脾失健运, 而致肠道传导失常, 多属肝脾不调症, 治疗IBS以疏肝理气、调理肝脾为治疗原则[2]。
固肠止泻丸(Gu-Chang-Zhi-Xie pills, GCZX)是我国传统医药宝库中有代表性的中药复方制剂之一, 为国家中药保护品种, 《中华人民共和国药典》 (2015年版)收录, 源自医圣张仲景经典名方“乌梅丸”化裁而成, 由乌梅、黄连、干姜、木香、元胡、罂粟壳等六味药材组成的复方中药, 其中乌梅用醋制, 增加其收涩之性, 黄连用吴茱萸炮制, 降低其苦寒之性。该中药复方制剂可从整体上对消化系统的功能进行调节, 乌梅、罂粟壳涩肠止泻, 黄连燥湿清热, 兼有解毒功效, 延胡索、木香行气活血, 干姜温中散寒。木香和黄连同用可以舒气行滞除里急后重, 乌梅和罂粟壳同用可固气涩肠止泻, 干姜和黄连同用, 寒热并用。各种药物共同作用可以达到调和肝肾、行气止疼、涩肠止泻的疗效, 近年来在IBS治疗方面展现出良好的应用前景。
本课题组对服用固肠止泻丸的IBS患者进行约诊或随访, 发现患者腹痛腹胀、低度炎症等症状得到改善, 临床疗效确切, 推测固肠止泻丸可能降低内脏痛觉的高敏感、抑制结肠黏膜炎症因子的过表达。虽然, 近年来固肠止泻丸或乌梅丸组方治疗IBS的临床相关研究多见报道[3, 4], 但是其药效物质基础及分子作用机制尚不明确, 有效判定其关键药效成分及核心作用靶标, 对该方的阐明作用机制与指导临床用药具有重要意义。本文以固肠止泻丸中具有抗IBS作用的药效成分为研究对象, 应用网络药理学的研究方法, 建立“药效成分−疾病靶标−生物学通路”之间的关系, 探究该方治疗IBS的多成分、多靶点和多途径作用机制, 为创新药物研究奠定基础。
材料与方法化学成分的获取与活性成分的筛选 从传统中药系统药理学数据库TCMSP (http://sm.nwsuaf.edu.cn/lsp/tcmsp.php/)、中国中药整合数据库TCMID (http://www.megabionet.org/tcmid/)、传统中药化合物数据库CHEM-TCM (http://www.chemtcm.com)、台湾中医药资料库TCM database@Taiwan (http://tcm.cmu.edu.tw/)等四大中药化学成分数据库, 收集固肠止泻丸中每味中药含有的全部化学成分, 并结合现有文献资料进行数据挖掘、整理, 以TCMSP数据库中收录的化学成分为基础, 统一化学名称及编号, 删除重复分子。利用ChemOffice2016软件制作固肠止泻丸药效成分的分子结构式, 其中ChemDraw模块进行化合物2D结构的绘制, ChemBio3D模块进行3D结构的转换, 保存为MOL2 (.mol2)格式文件。采用加拿大ACD/Labs公司ADME_Suite软件包对固肠止泻丸所含的所有化学成分的药代动力学参数进行相关预测, 主要涉及口服生物利用度、类药性、Caco-2细胞单层模型表观渗透系数、血浆蛋白结合率等4个方面, 过滤掉不符合ADME标准的化合物。
活性成分的化学空间主成分分析 利用Discovery Studio v3.5软件中Calculate Molecular Properties模块, 进一步计算候选活性分子的40个重要描述符, 用这些描述符来刻画其药效性质, 借助主成分分析(principal component analysis, PCA)进行活性成分二次筛选。PCA是运用统计学方法进行海量数据信息简化的技术。通过计算矩阵对角特征向量, 再将特征向量矩阵转换为数据。随后将数据信息转换为坐标系统的第一新坐标(称为第1主成分)中, 使得全部数据均映射到第一新坐标的第一方差上, 随后全部数据均再映射到第二新坐标(称为第2主成分)的第二方差上, 依次类推, 将多维分子描述符的数值映射到三维主成分分析图上, 最后筛查到加权累加贡献率超过85%的3个主成分, 因为85%的阈值标准, 说明3个主成分涵盖了所有指标具有的分子描述符信息。简而言之, 在确保原有数据丢失量最小的准则下, 主成分分析用一组简化数据特征作为新变量, 以此描述繁杂的海量数据, 新变量已经整合原有的数据信息特征, 具有极强的数据代表性。在构建3个主成分的化学多维空间中, 将候选活性分子对应放置到多维化学空间的一个坐标点上, 建立其在化学空间中的分布状态, 每个点代表一个候选化合物, 分子的相似性用两点间的距离来表示, 因此可以有效预测两个化合物的理化性质近似度。从Drug Bank数据库中收集整理了FDA已批准上市的IBS治疗药效分子(截止2017年12日31日, 共23个, 表 1), 作为FDA药效分子集, 将固肠止泻丸候选分子集与FDA药效分子集平行计算, 进行理化参数的相似性筛选[5]。
| Table 1 Twenty three drugs approved by FDA for irritable bowel syndrome (IBS) treatment |
药效分子潜在靶标预测与分子对接验证 药效分子的靶标通过PharmMapper Server数据库(http://59.78.96.61/pharmmapper/)预测得到[6], 采用23个FDA已批准上市的IBS治疗药效分子作为训练集, 对于每个分子, 保留300个匹配分数≥3.00的匹配靶标。在设置靶标集合库时, 仅保留人源性靶标, 共计2 214个, 其余所有参数均采用默认值。收集治疗IBS相关靶标, 通过Therapeutic_Target_Database、PharmGkb_Database及DrugBank_Database三大数据库来验证这些靶标集合库与IBS的关系。最后从PDB数据库中获取相应靶标蛋白晶体结构文件用于下一步实验, 靶标详细信息如表 2所示。为了筛选及验证治疗IBS潜在疾病靶标和固肠止泻丸活性化合物之间是否具有相互作用的关系, 利用分子对接模拟软件AutoDock_Vina, 对每个药效分子与预测靶标进行受体-配体对接模拟计算。完成全部的对接模拟后, 根据打分函数的评价, 对所有药效活性分子与疾病靶标互作的强弱依次进行排序。若打分函数低于阈值, 且结合能不高于-8.5 kcal·mol-1, 则判定为有效对接, 二者之间可形成较强的相互作用。
| Table 2 Information of potential target proteins related to IBS therapy |
“药效分子-疾病靶标”网络构建与分析 为了深度分析对接结果, 将固肠止泻丸的药效分子和抗IBS作用靶标导入高度可视化的网络构建程序Cytoscape3.4.0软件, 通过将药效分子、疾病靶标相连, 绘制成一个宏观的互作网络, 较为直观地明确特定药效分子的疾病靶标, 从整体水平上解析中药复方治疗疾病的分子机制。选取两个关键的拓扑参数, 即网络度(degree)和介数(betweenness), 借助Network Analyzer插件[7]对已构建的互作网络进行拓扑学分析, 计算这两个网络拓扑参数。这两个参数综合衡量, 可较好地反映药效分子及疾病靶标的药理学价值。
KEGG通路富集分析 借助CluoGO_v2.1.5插件, 将靶标元素映射到相关生物学通路中, 进一步构建“关键靶标-生物学通路”网络, 在通路水平上阐释关键靶标与固肠止泻丸治疗PI-IBS作用机制的潜在联系。ClueGO[8]是Cytoscape软件的一款插件, 可对基因或蛋白进行注释, 本研究需要对PI-IBS关键靶标进行KEGG pathway注释及GO富集注释。KEGG pathway涵盖多种细胞生化途径, 如信号分子转导、生物大分子代谢、信号跨膜转运、细胞周期调控等细胞生化过程; GO全称为Gene Ontology, 指基因本体论, 这里用于基因功能的系统评价, 用于衡量基因功能, 诸如该基因在代谢、信号转导等通路中的作用等。需要说明的是, 在本研究中, KEGG pathway的数据采用2017.10.07上传共享开源的数据信息(该数据库目前共涉及9 606个基因)。除物种类别设置为人源性选项之外, 其余参数选项值均为默认值。
结果 1 活性成分的ADME筛选与主成分分析前期得到395个化合物, 其中乌梅、干姜、黄连、罂粟壳、木香、延胡索分别含有41、149、49、25、107、78个。进行ADME药代动力学参数的预测, 主要涉及口服生物利用度、类药性、Caco-2细胞单层模型表观渗透系数、血浆蛋白结合率等4个关键指标的筛选, 过滤后得到102个符合条件的候选活性化合物。
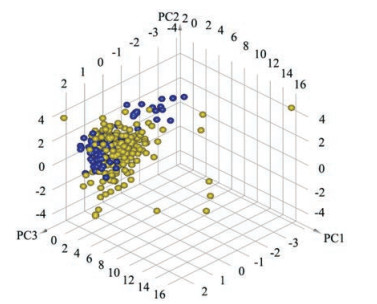
计算固肠止泻丸所含102个化合物的40个相关理化性质描述符, 并对计算结果进行主成分分析, 结果显示其物理化学性质差异显著, 呈多样性分布, 提示病灶的多个靶标均有药效分子与其产生药效作用, 呈现多种药理活性。同时进行平行实验, 对23个FDA认证的IBS药效分子做主成分分析, 进而比较两种药效分子集合的空间分布差异。结果表明两种分子集合(固肠止泻丸所含候选活性化合物、FDA批准可用于IBS适应症的西药)在空间位置的重叠性较高, 说明固肠止泻丸的类药性较强。但是也发现个别活性化合物的重叠性越低, 推测其类药性较弱, 需要从固肠止泻丸候选活性成分集合中剔除。因此固肠止泻丸候选活性分子集的主成分分析结果均转化为三维空间坐标数值, 计算得到一对一空间坐标距离共8 640个(96×90);本研究将固肠止泻丸候选活性成分与FDA认证的治疗IBS药效分子的空间距离近似度设定为1.0, 超过这个数值化合物分子全部剔除(共计6个化合物), 如图 1所示, 最终得到96个固肠止泻丸的药效分子。
|
Figure 1 Principal component analysis with PC3-PC2-PC1 diagram. The yellow ball represents the candidate active compounds in Gu-Chang-Zhi-Xie pills, and the blue ball represents the FDA approved western medicines for IBS indications |
利用反向药效团筛选技术结合数据库验证及文献挖掘, 确定与IBS适应症相关的68个靶标蛋白, 由于其中7个没有PDB蛋白晶体数据或者配体小分子结构数据, 其余的61个靶标蛋白数据文件可以从PDB数据库中获取, 用于药效分子与疾病靶标的分子对接计算, 如表 2所示。
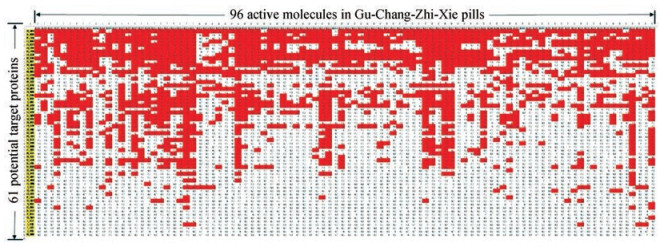
完成全部的对接模拟后, 根据打分函数的评价, 对固肠止泻丸96个活性分子与61个疾病靶标互作的强弱依次进行排序。为了更好地区分疾病靶标与活性分子之间是否发生强相互作用, 参照前人的研究思路[9, 10], 将原配体小分子与靶标蛋白的对接得到的结合能作为参照阈值, 若打分函数低于阈值, 且结合能不高于-8.5 kcal·mol-1, 则判定为有效对接, 二者之间可形成较强的相互作用, 进行红色标注。由于篇幅有限, 详细的对接模拟结果略去, 图 2仅提供61个靶标蛋白与96个活性分子对接模拟的聚类分析热图。如图 2所示, 绝大多数的GCZX活性分子均集中作用于某些靶标蛋白, 提示这些靶标可能是治疗PI-IBS的关键靶标。
|
Figure 2 The heat map of cluster analysis for molecular docking results. Abscissa represents 96 active molecules in Gu-Chang-Zhi-Xie pills, ordinates represent 61 potential target proteins for IBS therapy, red dots at the crossbar represent strong interactions between target proteins and active molecules |
由于本节参照文献[11], 并结合自身研究的特点, 减少后期分析的不确定性, 明确“关键药效分子”、“主要疾病靶标”、“核心疾病靶标”, 所以将活性分子与靶标蛋白相关联整合, 构建关键药效分子C-T型互作网络(打分排名前5的关键药效分子与靶标蛋白互作, 见图 3), 模型显示了固肠止泻丸药效分子与疾病靶标之间存在着复杂关系, 这个复杂关系网络同样印证了固肠止泻丸作用于“多成分、多靶标”来发挥其治疗IBS的论断。

|
Figure 3 Compound-target network containing top 5 ingredients for each target. Red circles represent target, blue purple triangle icon represents compound, each connection represents the interaction between a compound and a target, green circle icon represents six kinds of Chinese medicinal materials |
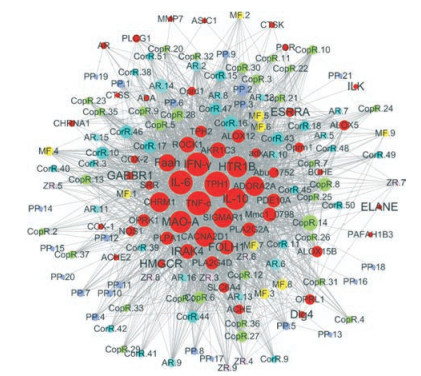
借助插件Network Analyzer, 计算网络模型的拓扑学参数, 其中靶标蛋白也被作为网络节点, 从网络节点重要性的角度进行分析。由于网络度(degree)是指该节点相关联的边的条数, 节点的degree值越大, 往往表示节点在网络的重要性越大。因此研究选取degree作为节点重要性的衡量指标。分析结果筛选出11种关键药效分子, 如表 3所示, 依次为盐酸药根碱_M001463、绿原酸_M010839、姜酮_M013352、6-姜辣素_M000762、延胡素乙素_M004199、左旋荷包牡丹碱_M000791、盐酸小檗碱_M004225、药根碱_M001474、黄连碱_M001458、甲基黄连碱_M002668、罂粟碱_M004230, 这些药效分子不仅与靶标的网络度较好(degree均大于10), 并且其与靶标具有较强相互作用(结合能均低于-9.0 kcal·mol-1)。进一步筛选出39个主要疾病靶标, 其degree值均大于12, 说明这些靶标与12个以上的药效分子可能发生互作, 如图 4与表 4所示, 即为39个主要疾病靶标的网络节点的网络特征信息。然后, 进一步提高阈值到70, 即degree≥70, 筛选出靶标蛋白TPH1、TNF-α、IL-6、IFN-γ、MAO-A、IL-10等, 这些靶标作用的活性化合物均超过70个, 此处被定义为核心疾病靶标。
| Table 3 Network characteristics of key component-target network nodes |
|
Figure 4 Compound-target network contains all the effective components in Gu-Chang-Zhi-Xie pills. Green nodes represent components, red nodes represent targets. Degree is positively related to node size in network model, and the size of node corresponds to the core degree indirectly. Six different colors are used to distinguish between six different Chinese medicinal materials; yellow: Mume Fructus, MF; pink: Zingiberis Rhizoma, ZR; green: Coptidis Rhizoma, CopR; purple: Papaveris Pericarpium, PP; bright blue: Aucklandiae Radix, AR; dark blue: Corydalis Rhizoma, CorR |
| Table 4 The network characteristics of the nodes of 39 main targets |
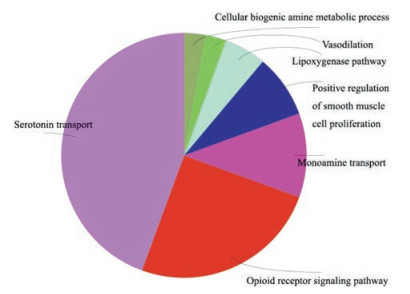
基于39个主要疾病靶标, 本节使用Cytoscape3.4.0的插件ClueGO进行KEGG通路富集分析, 结果如图 5、6和表 5所示。其中, 图 5是基于分组的39个主要疾病靶标的KEGG信号通路富集分析图, 图 6是KEGG通路富集饼形图, 表 5是基于显著性的39个交集靶标的KEGG信号通路显著性分析, 该插件对通路条目根据参数Kappa Score进行了分组, 阈值设定为0.4, 判定大于该阈值的两个条目属于同一分组。从KEGG通路富集分析中可以看出, 基于39个高显著性疾病靶标涉及29个相关KEGG通路, 富集于7个分组, 5-HT信号通路(serotonin transport)、阿片受体信号通路(opioid receptor signaling pathway)、单胺递质转运(monoamine transport)、平滑肌细胞增殖(smooth muscle cell proliferation)、脂氧合酶降解途径(lipoxygenase pathway)、血管舒张(vasodilation)、细胞内生物胺代谢过程(cellular biogenic amine metabolic process)等, 并将29条信号通路按P值进行排序, 如表 5所示。其中5-HT信号通路的P值最小, 为1.9E-6, 在KEGG通路富集饼形图中占据近乎1/2的面积, 推断固肠止泻丸药效分子可能主要通过作用于5-HT信号合成或转运通路发挥药效作用。

|
Figure 5 KEGG signal pathway enrichment analysis of 39 main disease targets based on grouping. Different biological pathways were divided into different groups according to Kappa Score and the dots with different colors represent different groups of biological pathways. If a dot is made up of several colors, it belongs to multiple groups at the same time. Edges represent the links between pathways, which are based on the similarity of pathway related targets. The size of a dot represents the statistical significance between pathways, which is inversely proportional to the P value of the path. 1: Serotonin transport; 2: Regulation of behavior; 3: Eating behavior; 4: Circadian behavior; 5: Monoamine transport; 6: Regulation of neurological system process; 7: Amine transport; 8: Regulation of amine transport; 9: Protein kinase C-activating G-protein coupled receptor signaling pathway; 10: Opioid receptor signaling pathway; 11: Regulation of sensory perception; 12: Catecholamine transport; 13: Catecholamine secretion; 14: Regulation of catecholamine secretion; 15: Regulation of sensory perception of pain; 16: Adenylate cyclase-inhibiting G-protein coupled receptor signaling pathway; 17: Nitric oxide biosynthetic process; 18: Regulation of chemokine production; 19: Regulation of epithelial cell apoptotic process; 20: Regulation of cation channel activity; 21: Regulation of calcium ion transmembrane transporter activity; 22: Smooth muscle cell proliferation; 23: Regulation of smooth muscle cell proliferation; 24: Positive regulation of smooth muscle cell proliferation; 25: Lipoxygenase pathway; 26: Arachidonic acid metabolic process; 27: Vasodilation; 28: Cellular biogenic amine metabolic process |
|
Figure 6 Pie chart of KEGG biological pathway |
| Table 5 Significance analysis of biological pathways involved in major disease targets. *Path name is the most significant KEGG biological pathway in each group |
生物碱类化合物是存在于生物体(主要为植物)中的一类含氮的碱性有机化合物, 是中草药的常见有效成分, 大多数具有复杂的环状结构, 其中氮元素多包含在环内, 发挥显著的生物学活性。现有研究结果证实, 大多数生物碱具有抗肿瘤、降血压、强心、镇痛、消炎、抗菌等功效[12]。本研究分析了关键药效分子C-T型网络的节点特征, 发现打分排名前11位关键药效分子大部分属于异喹啉类生物碱, 其中包括盐酸药根碱_M001463、右旋荷包牡丹碱_M000791、盐酸小檗碱_M004225、药根碱_M001474、黄连碱_M001458、甲基黄连碱_M002668、罂粟碱_M004230等, 共7种生物碱, 占较大权重(7/11), 且作用于4种靶标蛋白, 实现其药效作用, 如TPH1、TPH2、5-HT受体1B、TNF-α、INF-γ。究其原因, 主要是异喹啉类生物碱在中草药及天然产物中分布广泛, 具有抗炎镇痛活性的生物碱种类较多。如盐酸小檗碱_M004225就很有代表性, 也称为黄连素, 从中药材黄连中天然提取, 在临床上具有抑菌、抗炎的疗效, 相关实验证明盐酸小檗碱可有效修复大鼠结肠黏膜的损伤。以葡聚糖硫酸钠(dextran sulfate sodium salt, DDS)诱导大鼠为例, Yan等[13]成功构建结肠黏膜损伤的动物模型, 随后进行肠道黏膜完整性、临床生理生化指标、嗜铬细胞数量、促炎因子表达量等指标检测确认。DSS诱导效应, 导致结肠促炎因子分泌量升高; 通过盐酸小檗碱干预后, 有效下调了细胞因子IL-17、INF-γ、TNF-α等表达水平; 通过有效控制结肠组织嗜铬细胞、肥大细胞的数量, 可以抑制促炎因子分泌量过剩的状态, 加速结肠巨噬细胞凋亡, 缓解DDS诱导大鼠模型结肠黏膜的炎症反应。因此推测盐酸小檗碱潜在的治疗机制是其有效遏制DSS诱导模型大鼠体重降低的趋势, 上调MAO-A催化活性, 从而有效控制炎症的加剧及结肠黏膜的损伤[13]。其次, 右旋荷包牡丹碱_M000791、罂粟碱_M004230, 这两个化合物同属异喹啉类生物碱。右旋荷包牡丹碱是一种GABA-A受体的竞争性拮抗剂, 有镇痛、镇静、抗癌及肠平滑肌解痉作用[14-16]; 而罂粟碱可作为一种平滑肌松弛药或平滑肌解痉剂, 缺乏高度选择性, 临床上内、外科广泛使用, 同样具有显著的镇痛作用[17]。文献报道, 李惠兰等[15]采用大鼠胃底肌条的离体实验法, 右旋荷包牡丹碱、罂粟碱对5-HT诱发的大鼠胃底肌条收缩均有显著的对抗作用, 呈现出非竞争性拮抗, 提示这两种药效成分均可缓解胃肠道痉挛, 降低痛觉敏感。本文运用计算机模拟实验预测, 分析得到GCZX关键药效成分, 与上述相关药理学研究结果基本吻合, 相互印证, 推断GCZX中此类异喹啉类生物碱为关键药效分子, 分别主要作用于炎症、痛症两类靶标, 对IBS均有不同程度抗炎镇痛的疗效。
网络药理学计算结果还明确了若干核心疾病靶标。在固肠止泻丸的91个活性成分中, 89个化合物均与靶标蛋白色氨酸羟化酶1 (TPH1)产生较强相互作用, 在选定的核心疾病靶标中排名处于第1位。TPH1是5-HT合成的限速酶, 单胺氧化酶A (MAO-A)是5-HT主要代谢酶, 二者均是5-HT代谢途径中的关键酶。TPH分为TPH1、TPH2两种亚型, 其中TPH1是胃肠道内生物合成5-HT的关键限速酶, 能够催化L-色氨酸生成5-羟色氨酸, 然后进一步脱羧为5-HT, 储存在细胞内的囊泡内, 约95% 5-HT来源于肠道黏膜层的嗜铬细胞。随着兴奋性信号的传导, 神经元被激活, 5-HT从囊泡被释放到突触间隙, 并与突触后膜5-HT受体结合, 产生相应的生理学效应。随后, 5-HT经MAO-A降解, 生成5-HIAA。目前有相关临床试验表明[18], IBS人群在外周血与胃肠道黏膜的5-HT分泌量均超出正常值范围, 推测IBS患者长期腹泻及内脏痛觉敏感是肠道5-HT含量异常升高所造成的。因此, 有科学家与医疗工作者均提出抑制5-HT合成或降低5-HT释放, 用于治疗IBS患者。目前, 从5-HT合成为突破口, 开发的TPH抑制剂LX1031已进入Ⅱ期临床研究, 该药物可显著缓解IBS患者临床症状[19]。因此, TPH1、MAO-A靶标排名均处于非常重要的位置(即第1位、第5位), TPH1对胃肠道5-HT的合成具有重要意义, MAO-A对催化5-HT的氧化脱氨也起到了关键作用, 都属于治疗IBS的核心疾病靶标。由此推测固肠止泻丸所含的多种药效分子协同作用于TPH1、MAO-A两种酶, 干预5-HT合成与分解的生物学过程, 最终有效调节胃肠道内5-HT浓度。
近些年来发现, 在IBS患者肠黏膜层中, 其他细胞因子也有不同程度的改变[20]。本研究除了关注5-HT代谢途径中的关键酶TPH1、MAO-A之外, 还分析了C-T型网络模型的节点关联度, 发现炎症细胞因子TNF-α、IL-6、IFN-γ、IL-10等作为疾病作用的核心靶标蛋白, 同样具有较高的网络度。炎症细胞因子是一类具有广泛生物学活性的小分子蛋白质, 由淋巴细胞、单核细胞等免疫细胞合成及分泌而来, 可调节免疫细胞的分化和激活, 主要参与细胞间信号转导、炎症反应调节、免疫相关细胞分化、免疫应答调节等生物学过程。按其作用效应不同, 大体划分为抗炎因子、促炎因子两类。抗炎因子主要包括IL-23、IL-10、IL-4、TGF-β, 而促炎因子主要包括IL-6、IL-1、TNF-α、IL-12、IL-18、INF-γ、IL-2。其中, IL-6、INF-γ、TNF-α为主要促炎因子, IL-10为主要抗炎因子。TNF-α和IL-6能够有效增强炎症效应, 并促进巨噬细胞或淋巴细胞增殖, 而IL-10主要抑制促炎因子释放, 有效阻遏单核细胞、巨噬细胞发挥的免疫应答[21]。本研究从C-T互作网络中的靶标节点入手, 深入分析其节点的网络特征参数。结果表明, TNF-α (degree = 84)、IL-6 (degree = 83)、IFN-γ (degree = 82)、IL-10 (degree = 74)等疾病靶标具有较高的节点度值, 均与70个以上药效成分发生相互作用。提示IBS患者肠道中的这些炎症因子表达异常, 导致抗炎因子与促炎因子之间相互拮抗的平衡状态被打破。由此推断, 在IBS肠道炎症过程中, 上述4种炎症细胞因子扮演着重要角色, 而固肠止泻丸的药效成分可能作用于这些疾病靶标蛋白, 以此调控免疫系统趋于恢复正常。
生物学通路富集分析[22]结果表明, 39个靶标基因关联29个相关KEGG通路, 且29条KEGG通路富集于7个分组。其中5-HT信号通路分组(即serotonin transport通路分组)在KEGG通路富集饼形图中占据近乎1/2的面积, 提示该通路在固肠止泻丸治疗肠易激综合征中扮演着举足轻重的角色。现有研究表明, 在5-HT信号通路中, 5-HT及其受体、转运体均与IBS发病机制密切相关。血清素不仅存在于中枢神经系统, 而且存在于胃肠消化道黏膜组织中, 参与胃肠道动力、内脏痛觉感应等生理功能, 这些应激反应又形成负反馈, 促使肠黏膜局部血清素的进一步释放。许多临床试验已证实, 在IBS患者肠道中发现5-HT合成通路、转运信号通路均发生了变化, 推测这条生物学通路包含合成、存储、释放及再摄取等诸多关键环节, 某一个节点相关基因、蛋白、酶、信号分子的变化均可引起IBS相关症状, 如内脏痛觉高敏感、胃肠道动力不足等, 可能与IBS发病机制密切相关。并且在外周组织中, 5-HT也是潜在的致敏源。相关生物学实验显示[23], 大鼠皮下注射低剂量5-HT前体物质5-羟色氨酸后, 诱发肠道内脏痛觉扩张敏感度显著增高, 说明外周组织5-HT分泌异常同样参与了IBS患者内脏痛觉高敏恶变的病理发展过程。临床试验研究也有报道[24], 采用治疗IBS常用药帕罗西汀, 作为一种血清素再摄取抑制剂, 可改善胃肠动力不足, 降低内脏痛觉阈值过低, 推测其机制为帕罗西汀下调了神经细胞突触间隙内5-HT的浓度。因此, 从KEGG生物学通路富集分析中可以看出, 固肠止泻丸的药效分子可能主要通过作用于5-HT信号合成或转运通路来发挥药效, 外周5-HT分泌量异常升高、内脏痛觉阈值降低, 二者之间可能存在密切联系。
需要补充说明两点。第一, 既然帕罗西汀已经成为IBS治疗的常用药物了, 那么本研究的创新性发现是什么?这也是正是本研究的亮点, 西药单体帕罗西汀、中药复方固肠止泻丸二者的药效作用机制截然不同。帕罗西汀为TPH酶活特异性抑制剂, 而TPH在整个5-HT合成过程中扮演关键限速酶的角色, 所以帕罗西汀干预PI-IBS大鼠模型的机制是基于“单一药效分子(帕罗西汀)、单一靶标蛋白(TPH1)”作用途径。然而中药复方固肠止泻丸的计算药理学研究发现了96种活性化合物、11种IBS关键药效分子、6种IBS关键靶标蛋白, 因此固肠止泻丸通过“多药效分子、多靶标蛋白”途径、“加性效应”干预治疗IBS。多组分的固肠止泻丸与帕罗西汀的单组分作用单个靶标蛋白的药效机制相比较, 给药干预效果趋于一致, 但药效作用机制却截然不同。本文的创新性就在于阐明固肠止泻丸治疗IBS的药效物质基础与分子作用机制, 发现其与等同疗效的西药帕罗西汀的作用分子机制是有相同之处通路, 但是是“多药效分子、多靶标蛋白”途径。第二点需要强调的是, 本文根据生物信息学方法, 初步判定5-HT信号通路具有关键性作用。本研究目的并不是发现IBS的发病分子机制的相关重要信号通路, 而是挖掘中药复方固肠止泻丸治疗IBS信号通路是否与西医治疗IBS的信号通路不谋而合。
综上所述, ADME药代动力学参数筛选、化学空间主成分分析、分子对接模拟、网络互作模型构建等计算机模拟多种手段, 确定固肠止泻丸药效分子, 探索其作用的疾病靶标, 以及相关生物学通路, 最终从“核心药效分子-关键疾病靶标-相关生物学通路”角度来揭示固肠止泻丸治疗IBS的作用机制。由于此项对于中药复方的研究仍存在一些需要深耕细作才能解决的问题, 因此本课题组正在开展后续的生物学验证实验。
| [1] | Mearin F, Lacy BE, Chang L, et al. Bowel disorders[J]. Gastroenterology, 2016, 150: 1393–1407. DOI:10.1053/j.gastro.2016.02.031 |
| [2] | Zhang SS, Xu WJ, Chen Z, et al. Curative effect of dispersing stagnated liver-qi ang invigorating spleen versus invigorating spleen for eliminating dampness on diarrhea predominant irritable bowel syndrome[J]. China J Tradit Chin Med Pharm (中华中医药杂志), 2010, 25: 127–130. |
| [3] | Gu YM. Clinical study on treatment of irritable bowel syndrome with Gu Chang Zhixie pill[J]. Chin J Gastroenterol (胃肠病学), 2003, 8(supple 1): A23. |
| [4] | Guo XL, Wang ZK, Guo Y, et al. Clinical observation on 896 cases of ulcerative colitis treated with Chinese medicine Gu Chang Zhixie pills[J]. J Shanxi Coll Tradit Chin Med (陕西中医学院学报), 2000, 23: 19–23. |
| [5] | Zhou RR, Zhang M, Zhu Y, et al. Data mining of the prescription containing Codonopsis and study on the molecular mechanism of prevention and treatment of gastrointestinal disease[J]. Acta Pharm Sin (药学学报), 2018, 53: 1422–1428. |
| [6] | Shi Y, Yao YJ, Lin Y, et al. Mechanism of Kai Xin San in the treatment of Alzheimer's disease based on network pharmacology[J]. Acta Pharm Sin (药学学报), 2018, 53: 1458–1466. |
| [7] | Assenov Y, Ramirez F, Schelhorn SE, et al. Computing topological parameters of biological networks[J]. Bioinformatics, 2008, 24: 282–284. DOI:10.1093/bioinformatics/btm554 |
| [8] | Bindea G, Mlecnik B, Hackl H, et al. ClueGO:a Cytoscape plug-in to decipher functionally grouped gene ontology and pathway annotation networks[J]. Bioinformatics, 2009, 25: 1091–1093. DOI:10.1093/bioinformatics/btp101 |
| [9] | Li B, Xu X, Wang X, et al. A systems biology approach to understanding the mechanisms of action of Chinese herbs for treatment of cardiovascular disease[J]. Int J Mol Sci, 2012, 13: 13501–13520. DOI:10.3390/ijms131013501 |
| [10] | Liu ZZ, Liang JP, Nie YC, et al. Network pharmacology study of compound Xueshuantong capsule based on the targets related to blood circulation and hemostasis[J]. Acta Sci Nat Univ Sun Yat-sen (中山大学学报-自然科学版), 2013, 52: 97–100. |
| [11] | Wang X, Wang GC, Rong J, et al. Identification of steroidogenic components derived from Gardenia jasminoides Ellis potentially useful for treating postmenopausal syndrome[J]. Front Pharmacol, 2018, 9: 390. DOI:10.3389/fphar.2018.00390 |
| [12] | Tao B, Zhang A, Lan R. Advances in studies on analgesic cukaloids and their analgesic mechanism[J]. Lishizhen Med Mater Med Res (时珍国医国药), 2011, 22: 957–960. |
| [13] | Yan F, Wang L, Shi Y, et al. Berberine promotes recovery of colitis and inhibits inflammatory responses in colonic macrophages and epithelial cells in DSS-treated mice[J]. Am J Physiol Gastrointest Liver Physiol, 2012, 302: G504–G514. DOI:10.1152/ajpgi.00312.2011 |
| [14] | Ge ZJ, Dai TJ, Zeng YM, et al. Protective effect of L-dicentrine on acute myocardial ischemia and anoxia lesion[J]. Chin J Pharmacol Toxicol (中国药理学与毒理学杂志), 2005, 19: 35–38. |
| [15] | Li HL, Zhang RP, Ye HT, et al. Effect of L-dicentrine on contraction of rat stomach muscle strips[J]. China J Chin Mater Med (中国中药杂志), 2000, 25: 42–44. |
| [16] | Li M, Shu SG, Shu YH, et al. Protective effect of L-dicentrine on acute myocardial ischemia and anoxia lesion[J]. J Kunming Med Univ (昆明医学院学报), 1997, 18: 66–67. |
| [17] | Ng A, Habib A, Swami A, et al. Randomized controlled trial investigating the effect of transcervical papaverine and bupivacaine on postoperative analgesia following laparoscopic sterilization[J]. Eur J Anaesthesiol, 2002, 19: 803–807. DOI:10.1097/00003643-200211000-00005 |
| [18] | Zhang YC, Shao YY, Zuo X, et al. Therapeutic effect of Donglingcao Tablet on post-inflammatory irritable bowel syndrome in rats[J]. Chin J Mod Appl Pharm (中国现代应用药学), 2016, 33: 1235–1239. |
| [19] | Brown PM, Drossman DA, Wood AJ, et al. The tryptophan hydroxylase inhibitor LX1031 shows clinical benefit in patients with nonconstipating irritable bowel syndrome[J]. Gastroenterology, 2011, 141: 507–516. DOI:10.1053/j.gastro.2011.05.005 |
| [20] | Liebregts T, Adam B, Bredack C, et al. Immune activation in patients with irritable bowel syndrome[J]. Gastroenterology, 2007, 132: 913–920. DOI:10.1053/j.gastro.2007.01.046 |
| [21] | Matricon J, Meleine M, Gelot A, et al. Review article:associations between immune activation, intestinal permeability and the irritable bowel syndrome[J]. Aliment Pharmacol Ther, 2012, 36: 1009–1031. DOI:10.1111/apt.12080 |
| [22] | Wu D, Gao Y, Xiang H, et al. Exploration into mechanism of antidepressant of Bupleuri radix based on network pharmacology[J]. Acta Pharm Sin (药学学报), 2018, 53: 210–219. |
| [23] | Oliveira MC, Pelegrini-da-Silva A, Parada CA, et al. 5-HT acts on nociceptive primary afferents through an indirect mechanism to induce hyperalgesia in the subcutaneous tissue[J]. Neuroscience, 2007, 145: 708–714. DOI:10.1016/j.neuroscience.2006.12.021 |
| [24] | Masand PS, Gupta S, Schwartz TL, et al. Paroxetine in patients with irritable bowel syndrome:a pilot open-label study[J]. Prim Care Companion J Clin Psychiatry, 2002, 4: 12–16. DOI:10.4088/PCC.v04n0105 |
 2019, Vol. 54
2019, Vol. 54


