中医药在治疗妇科疾病方面表现出独特的优势, 随着大规模临床观察的开展, 有关中药毒副作用的报道日趋增多, 引起人们的关注[1, 2]。有些中药不良反应事件出现与中药应用脱离中医药理论指导有关[3], 以中医辨证论治理论为指导, 可在一定程度上降低中药的妊娠毒性, 进而发挥中医药的特色和提高中医药的疗效[4]。目前对于中药毒性的研究主要集中于生理状态下中药毒性成分对机体脏器组织结构和功能的损害, 而忽视了中药对病理状态下机体的毒性效应[5]。传统中医药理论特别强调机体病证状态对药物疗效和安全性的影响, “有故无殒, 亦无殒”是指导中药在妊娠期临床应用的重要原则之一[6]。采用正常动物评价中药妊娠毒性, 评价结果往往与临床实际需求脱节, 限制了中药的临床应用[7]。瘀血是妇科疾病常见的致病因素, 活血化瘀法是中医治疗妇科疾病的常用方法, 但孕妇一般慎用活血化瘀类中药[8]。妇科妊娠期用药, 除可能对其自身造成不利影响外, 还可能危及到子代健康。核因子E2相关因子2 (transcription factor NF-E2-related factor 2, Nrf2)是增强机体抗氧化功能最重要的转录因子, 氧化应激是有毒中药的重要毒性机制, 谷胱甘肽及生物合成相关基因(Gclc和Gclm)是机体重要的抗氧化酶。本研究采用寒凝血瘀小鼠模型, 旨在探讨莪术神经发育毒性的“有故无殒”现象及其机制。
材料与方法仪器 ELX800全自动酶标仪(BioTek公司), Stratagene Mx3005P实时荧光定量PCR仪(Agilent公司)。
药物及试剂 蓬莪术由江西樟树国康中药饮片有限公司提供(批号: 170301), 蓬莪术中莪术醇含量为1.774 mg·g-1[9]。莪术按照传统中医煎药的方法制成含生药2 g·mL-1汤剂, 4 ℃冰箱中保存备用。2, 5-二叔丁基氢醌(tert-butylhydroquinone, tBHQ, No: 112976, 美国Sigma-Aldrich公司); 还原型谷胱甘肽(glutathione, GSH)试剂盒(Cat No: 703002, Cayman公司)。SYBR® Premix Ex Taq试剂盒和PrimeScript RT Reagent Kit (cade: RR420A和DRR037A, 宝生物工程大连有限公司); TRIzol Reagent (REF: 15596026)、谷氨酸半胱氨酸连接酶催化亚基(glutamate cysteine ligase catalytic subunit, GCLc, No: ab153967)抗体和GCL修饰亚基(GCL modifier subunit, GCLm)抗体(No: ab55435) (Abcam公司); 甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase, GAPDH)抗体(No: 2118S, Cell Signaling公司)。
动物 SPF级C57BL/6雌性鼠120只, 雄性鼠60只, 体重(21~23) g, 由南京生物医药研究院提供, 动物许可证号: SCXK (苏) 2015-0001, Nrf2基因敲除(knockout, KO)纯合子(Nrf2-/-)近交系小鼠由南京生物医药研究院制作, 经繁育获得24只雌性和12只雄性小鼠用于实验, 小鼠饲养于齐齐哈尔医学院实验动物中心SPF实验室。本实验遵守国家有关实验动物保护与使用准则。
寒凝血瘀证小鼠模型制备[10-12] 小鼠放入冰水中冷浴20 min, 1次/天, 连续14天。
动物分组 雌性小鼠随机分为正常对照组、血瘀证对照组、正常+莪术(2.5、5、10 g·kg-1)组、血瘀证+莪术(2.5、5、10 g·kg-1)组、血瘀证Nrf2敲除组、血瘀证Nrf2敲除+莪术(10 g·kg-1)组、正常+ tBHQ (Nrf2的激动剂)组和正常+莪术(10 g·kg-1) + tBHQ组, 共12组, 每组10只。
染毒剂量和时间 以雌雄比为2:1将雌鼠随机与雄鼠合笼饲养, 次日清晨观察雌鼠有无阴栓, 如有阴栓则定为妊娠第0天, 小鼠受孕后第5~18天为莪术暴露期。莪术设低、中、高3个灌胃染毒实验组, 剂量分别为2.5、5.0和10.0 g·kg-1·d-1。正常+莪术+tBHQ组和Nrf2-KO+莪术组小鼠按照10.0 g·kg-1·d-1给予莪术水煎液。对照组给予等体积生理盐水。tBHQ通过饲料添加1% tBHQ (w/w)喂养给药。出生后每窝保留4只仔鼠, 多余仔鼠剔除。
断崖回避检测[13] 仔鼠出生后第5天开始测试, 将仔小鼠放于桌子边缘, 15 s内仔鼠从平台边缘处退回或转身为达标。
GSH检测 取子代小鼠大脑组织, 放入冰冷生理盐水中制备组织匀浆, 离心, 取上清液。按照Cayman公司的Glutathione Assay Kit说明书采用分光光度法检测匀浆上清液中GSH含量。
实时定量PCR检测Nrf2、GCLc和GCLm mRNA表达 按TRIzol试剂盒说明书提取总RNA, 取适量总RNA为模板, 采用PrimeScript™ RT Reagent kit逆转录成cDNA。实时定量PCR按照SYBR® Premix Ex Taq™试剂盒说明书进行。反应条件如下: 95 ℃预变性30 s, 共1个循环; 95 ℃变性5 s, 60 ℃退火31 s, 共40个循环。采用2-ΔΔCt进行Nrf2、GCLc和GCLm mRNA相对表达分析。引物由生工生物工程(上海)股份有限公司合成, 引物序列见表 1。
| Table 1 Primers used for real-time PCR detection of gene expression |
蛋白质印迹法检测Nrf2、GCLc和GCLm蛋白表达 细胞浆蛋白与核蛋白抽提试剂盒提取浆蛋白和核蛋白。100 ℃水浴中加热使蛋白变性, 10% SDA-PAGE电泳, 胶中蛋白质在75 V恒压状态下2 h电泳转移至硝酸纤维素膜, 脱脂奶粉封闭, 加一抗(1:1 000)孵育, 加二抗(1:4 000)孵育, 加Super Signal West Pico Chemiluminescent Substrate显影、拍照, 用AlphaEaseFC凝胶图像处理系统分析目的条带的积分光密度。
统计学方法 采用SPSS 19.0进行统计分析, 数据以均数±标准差(x± s)描述。均数组间比较采用单因素方差分析, 两两比较采用SNK-q检验或LSD检验, 检验水准α = 0.05, 双侧检验。
结果 1 莪术对正常和血瘀证的孕鼠子代反射行为功能的影响与野生(wild type, WT)小鼠正常对照组比较, 正常小鼠(WT) +10.0 g·kg-1莪术组子代断崖回避的达标日龄显著延长(P < 0.05), 而血瘀证小鼠(WT) +10.0 g·kg-1莪术组子代断崖回避的达标日龄显著差异(P > 0.05)。与Nrf2-KO小鼠血瘀证对照组比较, 血瘀证Nrf2-KO小鼠+10.0 g·kg-1莪术组子代断崖回避达标日龄显著延长(P < 0.05)。与野生小鼠正常对照组比较, 正常小鼠(WT) + 10.0 g·kg-1莪术+ tBHQ组子代断崖回避的达标日龄无显著差异(P > 0.05)。结果见表 2。
| Table 2 Effect of Rhizoma Curcumae (RC) on the positive occurring time of avoidance precipice reflex tests of the offspring mice (n= 40, x ± s).*P < 0.05 vs WT mice + NS group; #P < 0.05vs model Nrf2-KO mice + NS group. NS: Normal saline; WT: Wild type; KO: Knockout |
与野生小鼠正常对照组比较, 血瘀证小鼠(WT)对照组子代脑组织GSH含量显著增加(P < 0.05), 正常小鼠(WT) +10.0 g·kg-1莪术组子代脑组织GSH含量显著减少(P < 0.05), 而血瘀证小鼠(WT) +10.0 g·kg-1莪术组子代脑组织GSH含量无显著差异(P > 0.05)。与血瘀证Nrf2-KO小鼠对照组比较, 血瘀证Nrf2-KO小鼠+10.0 g·kg-1莪术组子代脑组织GSH含量显著减少(P < 0.05)。与正常小鼠(WT) +10.0 g·kg-1莪术组比较, 正常小鼠(WT) + 10.0 g·kg-1莪术+ tBHQ组子代脑组织GSH含量显著增加(P < 0.05)。结果见表 3。
| Table 3 Effect of RC on glutathione (GSH) levels in brain of offspring mice (n = 6, x ± s).*P < 0.05 vs WT mice + NS group; #P < 0.05 vs model Nrf2-KO mice + NS; ΔP < 0.05vs WT mice + RC (10 g·kg-1) |
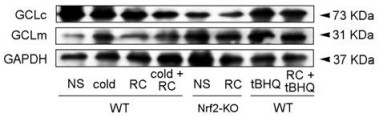
GCLc的Western blot和PCR结果显示, 与野生小鼠正常对照组比较, 血瘀证小鼠(WT)对照组、血瘀证小鼠(WT) +10.0 g·kg-1莪术组和正常小鼠(WT) +莪术+ tBHQ组子代脑组织GCLc蛋白和mRNA表达显著增加(P < 0.05), 而正常小鼠(WT) +莪术组子代脑组织GCLc蛋白和mRNA表达无显著差异(P > 0.05)。与Nrf2-KO血瘀证小鼠对照组比较, Nrf2-KO血瘀证小鼠+10.0 g·kg-1莪术子代脑组织GCLc蛋白和mRNA表达无显著差异(P > 0.05)。与正常小鼠(WT)对照组比较, 正常小鼠(WT) +莪术+ tBHQ组子代脑组织GCLm蛋白和mRNA表达显著增加(P < 0.05)。与Nrf2-KO血瘀证小鼠对照组比较, Nrf2-KO血瘀证小鼠+莪术子代脑组织GCLm蛋白和mRNA表达无显著差异(P > 0.05)。结果见图 1和表 4。
|
Figure 1 Western blot analysis of GCLc and GCLm proteins expression in brain of offspring mice |
| Table 4 Effect of RC on GCLc and GCLm proteins and mRNA expression in brain of offspring mice (n = 5, x ± s).*P < 0.05 vs WT mice + NS group |
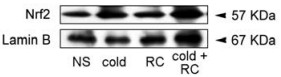
Nrf2的Western blot和PCR结果显示, 与野生小鼠正常对照组比较, 血瘀证小鼠(WT)对照组和血瘀证小鼠(WT) +莪术组子代脑组织Nrf2蛋白和mRNA表达显著增加(P < 0.05);与血瘀证小鼠(WT)对照组比较, 血瘀证小鼠(WT) +莪术组子代脑组织Nrf2蛋白和mRNA表达无显著差异(P > 0.05)。结果见图 2和表 5。
|
Figure 2 Western blot analysis of Nrf2 proteins expression in brain of offspring mice |
| Table 5 Effect of RC on Nrf2 mRNA and protein expression in brain of offspring mice (n = 5, x ± s).*P < 0.05 vs WT mice + NS group |
中药毒性并不是孤立一成不变的, 人体体质可能是影响中药毒性的重要因素之一[14]。在病理状态下, 由于证候不同, 机体的药物代谢能力和酶系统则存在差异。因此, 对药物的敏感度和耐受力等有差别[15]。方证相应则中药表现出治疗作用, 方不对证就可能出现毒性反应。《黄帝内经·素问》“黄帝问曰:妇人重身, 毒之何如……有故无殒, 亦无殒也”。古代医家认为, 体质对于中药毒性表达起决定性作用, 在不同的病证状态下中药具有不同的毒性表达[16]。莪术临床成年人煎服用量为5~15 g, 本研究按体表面积将成年人临床莪术剂量换算成小鼠妊娠期莪术暴露的低剂量[约为2.5 g(生药)·kg·d-1]。莪术主要成分是倍半萜类等20多种有机成分和多种微量元素。药理研究表明, 莪术原料药中莪术醇是莪术的活性/毒性成分。研究发现, 蓬莪术中莪术醇含量最高[9]。前期研究也发现莪术醇是具有抑制神经突起生长的作用。本研究发现, 10.0 g·kg-1莪术孕期暴露可导致正常小鼠子代断崖回避达标日龄显著延长, 而在寒凝血瘀证小鼠子代则没有观察到反射行为功能异常, 提示中药毒性研究不能脱离中医理论, 应以辨证论治为基础。
妊娠禁忌中药分为慎用药、忌用药与禁用药3大类。慎用药虽然没有毒性, 但药性猛烈, 容易损伤胎气, 慎用药多属活血祛瘀药、温里药、行气药和攻下药类中药; 禁用药大多服用后可导致滑胎或死胎, 多属剧毒药或药性比较剧烈的中药; 忌用药是指避免使用或最好不用的药物[17]。2015年版《中国药典》收录妊娠禁用、忌用和慎用药材99种, 其中莪术是37种禁用药之一。莪术是姜科植物蓬莪术、广西莪术和温郁金的干燥根茎, 始载于《药性论》, 中医理论认为莪术味苦辛、性温、无毒, 入肺脾二经, 开胃消食、行气破血、止痛。动物实验表明, 莪术根茎的醇浸膏及其有效成分具有抗早孕作用和抗着床效果, 莪术油有止孕作用[18]。本研究发现, 莪术对正常孕小鼠子代反射行为功能具有不良影响, 此结果与其他学者的研究结果为莪术的妊娠禁忌提供了实验数据[19]。
谷胱甘肽是一个由谷氨酸、甘氨酸和半胱氨酸组成的非蛋白巯基化合物。在谷氨酸的侧链的羧基组和半胱氨酸的氨基组之间以肽键相连。谷胱甘肽是细胞内抵御氧化应激的主要内源性抗氧剂, 维持自由基的产生与清除的动态平衡, 减少活性氧对组织造成损伤[20]。GSH可保护细胞免遭氧化损伤, 解除药物代谢产物的毒性, 抑制细胞凋亡[21]。本研究发现, 血瘀证小鼠子代脑组织GSH含量较正常小鼠子代显著升高, 血瘀证小鼠莪术(10.0 g·kg-1)暴露子代脑组织GSH含量与正常小鼠子代无显著差异, 子代小鼠脑组织GSH含量变化和行为学结果相似。γ-谷氨酰半胱氨酸合成酶(γ-glutamylcysteine synthetase, γ-GCS)是GSH生物合成的限速酶, 是由GCLc和GCLm构成的异二聚体[22]。本研究发现, 血瘀证小鼠子代脑组织GCLc蛋白和mRNA表达较正常组小鼠子代显著上调, 但莪术对GCLc表达无显著影响。而寒凝血瘀证和莪术均对GCLm表达无显著性影响。研究提示GCLc可能与莪术的有故无殒现象有关。
Nrf2是具有抗氧化功能的核心转录因子, 通过识别并结合抗氧化反应元件调控一系列抗氧化酶和Ⅱ相解毒酶的转录, 清除多余的自由基, 在减少神经发育毒性中起到重要作用[23]。本研究发现, 血瘀证组小鼠和血瘀证小鼠(WT) +莪术组小鼠子代脑组织Nrf2表达较正常小鼠子代显著升高, 莪术对小鼠子代脑组织Nrf2表达无显著性影响。Nrf2基因敲除增加了母源性莪术暴露子代断崖回避的达标日龄, 减少了GCLc基因表达, 而Nrf2激活剂tBHQ减少了正常野生小鼠子代的莪术神经发育毒性。这些结果表明, Nrf2蛋白在正常和血瘀证小鼠子代莪术神经发育毒性选择性表达中发挥了一定作用。
| [1] | Yang YH, Liu YL, Li H, et al. Thinking on the method of Chinese medicine attenuation based on prescription theory[J]. Lishizhen Med Mater Medic Res (时珍国医国药), 2018, 29: 648–650. |
| [2] | Guo YS, Lu J, Qiao L, et al. Clinical application of Chinese patent medicines with toxic herbs[J]. Pharm J Chin PLA (解放军药学学报), 2018, 34: 263–265. |
| [3] | Zhang YH, Zhao KW, Liu LX, et al. Zhou Chaofan talking about potential adverse reactions of non-toxic Chinese Medicine[J]. Chin J Basic Med Tradit Chin Med (中国中医基础医学杂志), 2017, 23: 544–545. |
| [4] | Wang JB, Cui HR, Bao ZF, et al. Precision medicine-oriented safety assessment strategy for traditional Chinese medicines:disease-syndrome-based toxicology[J]. Acta Pharm Sin (药学学报), 2016, 51: 1681–1688. |
| [5] | Song YG, Miao YY, Miao MS. Analysis on toxicity of traditional Chinese medicine containing aristolochic acid[J]. China J Tradit Chin Med Pharm (中华中医药杂志), 2018, 33: 1950–1954. |
| [6] | Zhou YP, Li XY. LI Xiang-yun's experience in using activating blood circulation to dissipate blood stasis herbsduring pregnancy:a report of three proven cases[J]. China J Tradit Chin Med Pharm (中华中医药杂志), 2017, 32: 3537–3540. |
| [7] | Song J, Zhong RL, Xia Z, et al. Research and application of hepatotoxicity evaluation technique of traditional Chinese medicine[J]. China J Chin Mater Med (中国中药杂志), 2017, 42: 41–48. |
| [8] | Wang YG, Jin R, Kong XW, et al. Safety grade of application of traditional Chinese medicines during pregnancy[J]. China J Chin Mater Med (中国中药杂志), 2016, 41: 150–153. |
| [9] | Xie Y, Hang TJ, Zhang ZX, et al. Comparison of curcumol contents in essential oil from four species of Rhizoma Curcumae L[J]. Chin Tradit Herb Drug (中草药), 2001, 32: 600–602. |
| [10] | Cheng XM, Du HL, Li D. Establishment of syndrome model of blood stasis due to cold accumulation in rats[J]. Chin J Basic Med Tradit Chin Med (中国中医基础医学杂志), 2005, 11: 604–605. |
| [11] | Zhou HM, Guo Y. Building of mice's models with blood stasis due to cold syndrome and evaluation[J]. Chin J Tradit Med Sci Technol (中国中医药科技), 2010, 17: 1–2. |
| [12] | Liang YN, Tang SQ, Li XM, et al. Normal and blood-stasis pregnant rats prenatal exposure to Rhizoma Curcumae inhibit ST8Sia Ⅱ and focal adhesion kinase expression in hippocampus of the offspring rats[J]. Lishizhen Med Mater Medic Res (时珍国医国药), 2016, 27: 1066–1068. |
| [13] | Bo CX, Zhang ZL, Sai LL, et al. Effects of 2, 4-dichlorophenoxyacetic acid on offsprings' development and oxidative stress[J]. Carcinogen, Teratogen Mutagen (癌变·畸变·突变), 2015, 27: 221–224. |
| [14] | Ling J, Wang M, Chen Y, et al. Analysis of Folium Epimedium toxicity in combination with Radix Morindae Officinalis based on zebrafish toxicity/metabolism synchronization[J]. Acta Pharm Sin (药学学报), 2018, 53: 74–83. |
| [15] | Liu JX, Ding XS. Research progress in hepatotoxicity assessment of traditional Chinese medicine under different pathological conditions[J]. Prog Pharm Sci (药学进展), 2017, 41: 619–623. |
| [16] | Wang J, Wang XD, Wu CY, et al. Origin and development of concept of toxicology in herbalism[J]. Chin Tradit Herb Drug (中草药), 2017, 48: 197–202. |
| [17] | Yu C, Sun X, Niu Y. An investigation of the developmental neurotoxic potential of curcumol in PC12 cells[J]. Toxicol Mech Methods, 2016, 26: 635–643. |
| [18] | Li Y, Wu JH, Xie YH. Research progress of zedoary turmeric oil[J]. J Shaanxi Coll Tradit Chin Med (陕西中医药大学学报), 2017, 40: 118–121. |
| [19] | Zhou NN, Miao XJ, Zhang J, et al. Pharmacological study of Rhizoma Curcumae contraindication of pregnancy[J]. Chin Arch Tradit Chin Med (中医药学刊), 2004, 22: 2291–2292. |
| [20] | Bains VK, Bains R. The antioxidant master glutathione and periodontal health[J]. Dent Res J (Isfahan), 2015, 12: 389–405. DOI:10.4103/1735-3327.166169 |
| [21] | Ren X, Zou L, Zhang X, et al. Redox signaling mediated by thioredoxin and glutathione systems in the central nervous system[J]. Antioxid Redox Signal, 2017, 27: 989–1010. |
| [22] | Lin LC, Chen CF, Ho CT, et al. γ-Glutamylcysteine synthetase (γ-GCS) as a target for overcoming chemo-and radio-resistance of human hepatocellular carcinoma cells[J]. Life Sci, 2018, 198: 25–31. DOI:10.1016/j.lfs.2018.02.015 |
| [23] | Silva-Islas CA, Maldonado PD. Canonical and non-canonical mechanisms of Nrf2 activation[J]. Pharmacol Res, 2018, 134: 92–99. DOI:10.1016/j.phrs.2018.06.013 |
 2019, Vol. 54
2019, Vol. 54


