2. 南开大学药学院, 药物化学生物学国家重点实验室, 天津 300353;
3. 天津药物研究院, 释药技术与药代动力学国家重点实验室, 天津 300193
2. College of Pharmacy, Nankai University/State Key Laboratory of Medicinal Chemical Biology, Tianjin 300353, China;
3. State Key Laboratory of Drug Delivery Technology and Pharmacokinetics, Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
中药质量是中药临床疗效的保障, 是中药产业发展的生命线。中药质量研究历来是行业关注的焦点, 中药质量标准和质量控制研究和应用是关系到中医药科学和产业发展的国家战略问题。刘昌孝院士针对中药生物属性、制造过程及配伍理论等自身医药体系的特点, 于2016年提出中药质量标志物(Q-marker)的新概念[1], 中药质量标志物概念提出后, 引起学术界、产业界的高度重视, 国家自然科学基金委员会于2017年1月17日和18日在天津组织召开了中药质量战略与方法学研究研讨会, 业内学者纷纷开展了相关研究, 中药质量标志物成为质量研究的前沿和焦点, 在研究模式、方法和示范性研究等方面进行广泛的探讨[2-34]。在此情况下, 有必要在剖析解读质量标志物概念科学内涵的基础上, 提出和形成中药质量标志物的核心理论, 总结凝练研究思路、方法和研究模式, 指导中药质量标志物研究。鉴于此目的, 本文概述中药质量标志物的概念、科学内涵、理论框架和研究方法, 以期为中药质量标志物研究提供有益的借鉴。
1 中药质量标志物的定义和科学内涵 1.1 背景和定义近年来, 我国中药科技工作者为中药质量控制做了大量的工作, 中药质量研究水平也有了长足的进步, 但仍未能满足日益提高的质量控制的要求。特别是中药药效物质基础研究薄弱, 致使质量控制指标与中药的有效性关联性不强; 质量控制指标专属性差。虽然业内科技工作者做了大量的研究工作, 但由于缺少系统的思路统领, 大多数研究都是针对某个局部或点的问题, 致使研究工作呈现碎片化, 重复性研究现象严重, 不能有效的解决行业发展的共性问题。
为提升我国中药产品质量和质量控制水平, 刘昌孝院士针对中药生物属性、制造过程及配伍理论等自身特点, 于2016年提出中药质量标志物的新概念。明确了质量标志物的基本条件: ①存在于中药材和中药产品中固有的次生代谢物, 或加工制备过程中形成的化学物质; ②来源某药材(饮片)特有的而不是来源于其他药材的化学物质; ③有明确的化学结构和生物活性; ④可以进行定性鉴别和定量测定的物质; ⑤按中医配伍组成的方剂“君”药首选原则, 兼顾“臣”、“佐”、“使”药的代表性物质。中药质量标志物概念的提出, 针对中药生物属性、制造过程及配伍理论等中医药体系的自身特点, 整合多学科知识, 提出核心质量概念, 以此统领中药质量研究, 进一步密切中药有效性-物质基础-质量控制标志性成分的关联度; 所建立的思维模式和研究方法着眼于全过程的物质基础的特有、差异、动态变化和质量的传递性、溯源性, 有利于建立中药全程质量控制及质量溯源体系。实现了中药质量控制理论、思路和方法的质的飞跃。
1.2 内涵解析质量标志物的核心内容是基于有效、特有、传递与溯源、可测和处方配伍的“五要素”, 既反映了与有效性(和安全性)的关联关系, 又体现中药成分的专属性、差异性特征, 特别是基于方-证对应的配伍环境, 使质量研究回归到中医药理论, 体现针对疾病的中药有效性表达方式及其物质基础的客观实质。质量标志物核心概念有利于反映中药治疗疾病的本质特征、有利于建立专属性、针对性的质量评价方法和质量标准、有利于建立可传递和溯源的全程质量控制体系。
1.2.1 质量标志物的“有效性”内涵质量控制的根本目的是对中药有效性的控制, 因此, “有效”是质量标志物的核心要素。在中医药理论体系中, “药性”与“药效” (功效)均是中医药理论的核心概念, 是中药特有的功效属性, 是从不同侧面、不同角度对中药治疗疾病性能的客观描述, 反映中药有效性的本质特征, 并作为临证治法、遣药组方的重要依据。“药味(性)”和“药效”体现中药的“物质基础”作用人体疾病主体的不同层面、不同方式的生物效应表达形式, 二者呈现复杂的离合关系[2-6]。“性-效-物”的表征、相关性规律研究是阐释中药的药效物质基础、作用原理以及配伍规律、指导临床实践的重要依据和研究路径, 将“药性”和“药效”均纳入中药质量评价, 才能反映中药质量的完整性。
入血成分及其代谢产物是中药功效表达的最终物质基础, 中药复杂体系的体内释放暴露及其动力学规律研究以及方药指纹-代谢指纹-药效靶标活性三者之间的关系研究是揭示中药有效性客观表达的有效路径。也是质量标志物发现和确定的重要依据。
1.2.2 质量标志物的“特有性”内涵“特有性”是中药鉴别、质量评价和质量控制的重要条件, 中药种类繁多、成分复杂, 不同药材含有同一成分频见。一个“好的”质量评价方法或质量标准应具有对特定药材的“针对性”、“专属性”, 才能避免“张冠李戴”、“以假乱真”。但现行的质量标准中还有很多药材均以普遍存在的成分(如绿原酸、芦丁等)作为含量测定指标, 显然难以反映不同药材的“特质”, 不能准确的评价不同药材的各自特有的质量特点, 也给掺假和掺伪留有可乘之机。
“特有性”体现在两个不同层次: ①能代表和反映同一类药材的共有性并区别于其他类药材的特征性成分; ②能反映同一类、不同种药材之间的差异性成分。由于很多中药基原亲缘接近, 成分类似, 药效和药性等方面差异和倾向可能反映在成分的种类、含量或不同成分之间的相对比例等不同方面。
成分“特有性”的形成具有植物亲缘学及其次生代谢产物生物合成途径的依据, 又与药材的组织部位(组织化学)、生长时期(采收期)、地理分布(植物区系地理)和生态条件(化学性状环境饰变)等密切相关。
1.2.3 质量标志物的“传递与溯源”内涵质量标志物的应用价值在于建立全程质量控制体系。中药不同于化学药物, 其形成的产业链长, 药物成分经历了采收加工-炮制-提取精制及制剂工艺-药物传输和体内代谢等多环节的传递与变化, 最终体内的“效应成分”与原料中的“原有成分”的构成已大不相同, 按照质量内涵的“效应物质”与“源头质控”的要求, 必须辨识和阐明中药形成全过程中各环节的化学物质组及其传递与变化规律, 提炼质量标志物, 并建立以质量标志物统领的全程质量控制体系。
① 植物中的生物合成成分:中药原料为天然生物有机体, 其中, 绝大多数来源于植物(约占87%), 中药的有效成分多为植物的次生代谢产物, 不同植物具有不同遗传物质基础和生物合成途径, 因而形成特异的次生代谢产物, 故称之为“植物中的生物合成成分”。次生代谢产物的种类、含量及各成分之间的相对比例是决定中药有效性和质量优劣的核心内涵。从质量要素的传递与溯源角度, 植物中的生物合成成分是第一环节, 是优质药材选育、产地选择及栽培技术规范化重点关注的环节, 因此, 又有中药生产“第一车间”之称, 是“药材好, 药才好”的根本保证。
② 药材中的原有成分:根据药用目的, 对植物的器官(根、茎、叶、花、果实、种子等)进行采收和产地加工, 才能形成药材, 相对于加工炮制后的饮片和提取制备后的制剂, 药材是初始原料, 故将药材中的成分称之“原有成分”。植物的不同物候期其次生代谢产物的合成和积累差异很大, 采收时间直接决定成分的含量; 产地加工方式方法也会对成分产生影响, 干燥方式等都会影响药材中的成分种类和含量。大多数含挥发性成分的药材, 在干燥凉晒的过程中有效成分挥发散失; 根茎类药材切制时需浸润, 水溶性成分容易损失; 一些苷类成分在适当的条件下(如一定的温度、湿度)会酶解成苷元。
③ 饮片中的转化成分:饮片是中药临床运用的原料, 药材通常需要一定的加工炮制形成饮片后才能临床运用或作为制药工业原料投料生产, 饮片加工炮制后成分发生变化, 产生减毒增效、改变药性、有助煎出等作用, 使其更能符合配伍的需要, 达到临床治疗疾病的目的。炮制过程中成分的变化非常普遍, 相对于药材, 对饮片中的成分称之为“转化成分”。
④ 制剂中的原形成分:中药材经提取纯化等制备工艺制成中药复方制剂, 因此, 中药制备过程既有有效性(药效物质基础)的获取, 又有去粗取精去伪存真的过程, 是中药质量传递与溯源的重要环节。制剂中的成分既是饮片原料化学成分的获取和传递的结果, 又是入血成分及其代谢产物的来源, 故称之为“原形成分”。制剂中的原形成分是质量控制的主要指标, 其上溯药材源头, 下延体内的最终效应物质。
⑤ 血中的效应成分:药物经一定的传输途径, 入血、代谢、分布并产生特异性的生物效应, 因此, 入血成分及其代谢产物才是最终的“效应成分”。从质量传递与溯源的角度, 血中的效应成分是质量传递体系的最终环节, 也是质量标志物确定的重要依据。
1.2.4 质量标志物的“配伍环境”内涵中医理论是中药的理论基础, 中药配伍理论是中医药理论的核心内容。中药配伍理论面向临床, 以辨证论治、方-证对应的方式遣药组方、临床施治。复方是中药临床运用的主要形式, 复方中药的“系统质”具有“非加和性”。同时, 同一中药材在不同复方中发挥的作用及其药效物质基础也可能不同: ①外源性药物对不同疾病有不同的生物效应, “汝之良药, 彼之毒方”即此之意; ②不同疾病的治则和用药目的不同, 因此, 同一药材在不同处方中的有效成分亦不尽相同; ③不同配伍环境中药物之间的交互作用不同, 既反映在不同作用靶点、通路之间的关联串扰、协同与拮抗, 又涉及吸收、代谢等体内过程的交互多用。
中药质量标志物的确定, 必须延伸到中药临床运用的层面, 针对具体疾病病因病机和治法治则, 从处方配伍环境出发, 基于中药临床运用时最终效应成分及其功效的临床表达形式, 确定质量标志物。
1.2.5 质量标志物的“可测性”内涵“可测性”是建立质量评价方法和质量标准的必要条件。即使满足了质量标志物的“有效”、“传递与溯源”的要求, 根据质量控制的目的, “可测性”还需要满足3个条件:即具有一定的含量和体内暴露量、具有定量测定的方法以及含量测定方法符合专属性要求。
中药成分复杂, 生物效应多样。“一物多性”, “一物多效”, “一物多用”现象普遍存在, 甚或像有三七止血与活血功效并存的情况。各成分在治疗疾病中发挥的作用亦不相同, 质量评价应体现其传统功效的“完整性”和其药用目的的“针对性”, 根据中药有效性多元表达方式, 有必要多元质量控制方法, 质量评价和质量控制方法的建立也要针对性的分主次、分层级、点-线-面-体结合等建立, 力求反映质量要素的完整性和质量控制的全面性。
2 中药质量标志物核心理论的建立中药质量标志物理论是以中医药理论为基础, 整合植物亲缘关系学、系统与进化植物学、植物化学分类学、植物区系地理学、中药资源生态学、分子生药学等相关学科的理论和方法, 形成面向基础与应用研究的理论体系。
2.1 中药质量标志物“有效性”的辨识和表达理论“有效”是质量标志物的核心要素, 是中药质量控制的主要依据和根本目的。传统中医药理论体系中对有效性的认识与西医药不同, 认为“药性”与“药效” (功效)均是中药传统功效的基本内涵, 是从不同侧面、不同角度对中药的生物效应表达的客观描述。“药味(性)”和“药效”体现中药的“物质基础”作用人体疾病主体的不同层面、不同方式的生物效应表达形式, 二者呈现复杂的离合关系, 均是临证治法、遣药组方的理论依据。因此, “药味(性)”和“药效”均应为中药有效性表达和质量标志物确定的依据。同时, 药物的体内过程及其动力学规律使其功效产生物质基础, PK/PD/T的时-效、量-效关系更是中药复杂体系生物效应表达规律的客观实质。因此, 中药质量标志物的有效性表达应体现在“药效”、药性和“体内过程”三个方面。
2.1.1 有效性的“药效”表达中药药效是中药治疗疾病的重要依据, 是中药有效性的核心内容。是在长期临床实践中总结的宝贵经验, 并经大量的实验研究证实的, 作为遣药组方、治疗疾病的重要依据。由于中药来源于动植物有机体, 化学成分复杂多样, 因此, 常存在“一物多性”、“一物多效”、“一物多用”的现象, “多元药效”是中药的一大特点。如当归兼甘、辛二性; 既能补血, 又能活血, 还可调经止痛, 润燥滑肠; 甚者如三七具有活血和止血“相反药效”。
中药的“多元药效”表达是由其复杂的化学物质基础决定的, 其化学生物学实质可能表现为: ①同一成分可作用于多靶点; ②同一成分体内可代谢为多个不同成分, 产生不同的生物效应; ③同一药材的多个不同成分, 表达多元的生物活性; ④同一药材不同组织部位的成分存在差异, 表现功效的差异; ⑤炮制产生化学成分变化, 改变药效。
中药质量是对中药有效性的客观反映, 基于中药“多元药效”、“相反药效”的特点和客观现实, 质量标志物的确定应力求反映质量属性的“完整性”和基于应用目的的“针对性”。
2.1.2 有效性的“药性”表达“药性”是中药的特有属性, 反映了中药的本质特征, 是药性理论的重要组成部分。其与归经、升降浮沉、十八反和十九畏等共同构成药性理论基本内容。而性味配伍则是遣药制方的关键环节, 是阐明中药作用机制的重要基础理论。“药性”与“药效” (功效)均是中医药理论的核心概念, 是从不同侧面、不同角度对中药的生物效应表达的客观描述。“药味(性)”和“药效”体现中药的“物质基础”作用人体疾病主体的不同层面、不同方式的生物效应表达形式, 二者呈现复杂的离合关系[35]。
药性的生物效应表达又可体现在药物作用的趋势(升降沉浮)、药物作用的靶点(归经)以及药效活性(功效)等不同的表达模式。功能相同的药物, 由于性味不同而表现在作用趋势、作用位置(途径、通路)和作用功效的差异, 并作为临证治法、遣药组方的重要依据。
药性理论是临证立法、配伍组方的重要依据。寒热理论贯穿于中医的理法方药全过程, 临床辨治中常依据寒热理论确立治疗大法, 成为指导组方的重要准则; 而“七情和合”更是“药对”、“方根”的关系及制方用药的基本原则。因此, 根据药物的气、味进行配伍组合, 是方剂组方的基本依据之一。
因此, 为了反映中药有效性的完整性, 凸显中医药理论体系特点, 特别是结合和指导临床用药实践, 质量标志物的确定应重视药性物质基础的发现和确定。
2.1.3 有效性的“体内过程”相关性中药化学成分的体内暴露及其动力学规律是中药有效性表达的物质基础和客观依据。在传统药性理论中, “药性走守”、“气味薄厚”、“升降浮沉”、“归经”、“引经报使”、“相须”等基本概念中均包含药物成分的药代动力学及体内过程(ADME/T)的科学内涵。因此, 药代动力学研究是揭示不同药性的药物传输特点、作用趋势、组织靶向及其不同药味之间的交互作用及其动力学规律的可行方法和必由路径。
原形成分仅是中药功效表达的先决条件, 而入血成分及其代谢产物才是产生生物效应的最终“效应物质”。药物成分的体内过程主要包括吸收、分布、代谢、消除的经时过程ADME/T及其动力学规律。
组织分布是药物体内过程的重要内容之一, 中药成分复杂, 各成分在体内的不同器官、组织中具有特异性的分布倾向和趋势, 组织分布特点作为不同疾病治疗和药物传输及释药技术设计的重要依据。因此, 药物成分的体内过程也是质量标志物确定的重要依据。
2.2 中药质量标志物“特有性”的理论依据中药种类繁多, 化学成分复杂, 同一化学成分来源于不同药材、不同药材含有相同成分十分多见。“专属性”是中药质量控制的基本要求, 而成分的“特有性”是质量控制方法“专属性”的基本条件, 其重要价值在于可对不同药材进行有效鉴别、评价。虽然中药成分复杂多样, 但每一种次生代谢产物都有其生物合成的依据。化学物质组的辨识和表征研究是成分“特有性”确定的前提, 但也不足作为“特有性”确定的全部条件, 还需进一步分析和探讨这些次生代谢产物在不同物种的遗传背景、生源途径以及生态地理条件下合成的理论依据。
植物次生代谢产物与物种及其亲缘关系、演化历程的地理和生态背景具有密切的关联规律, 我国植物化学家和药用植物学家根据中药资源特点, 提出“药用植物亲缘学”、“植物化学分类学”、“中药资源化学”、“分子生药学”、“中药资源生态学”等学科的理论和方法, 这些理论为中药质量标志物的“特有性”奠定了中药的理论基础。
2.2.1 化学成分特有性的亲缘学和生物合成途径理论依据药用植物有效成分种类多样、结构复杂, 其大多数生物合成的分子机制还不清楚, 药用成分往往是由多个酶促反应步骤并且在特定的分化细胞中完成的, 在植物体内形成复杂网络的调控模式。药用植物有效成分包括苯丙素类、醌类、黄酮类、萜类、甾体类、生物碱类以及鞣质等化学结构多样且复杂的化合物, 这些化合物在植物体内的生源途径主要包括:乙酸-丙二酸途径(acetate-melonate pathway), 生成各种聚酮类化合物, 醌类、脂肪酸类、酚类等化合物均来源于这一途径; 异戊二烯途径(isoprene pathway), 是萜类、甾体类化合物的主要生物合成途径; 莽草酸途径(shikimic acid pathway), 如苯丙素类、木脂素类、香豆素类均由这一途径衍化生成; 氨基酸途径(amino acid pathway), 大多数生物碱类成分由此途径生成; 以及复合途径:黄酮类和伪生物碱类的代谢合成都属于复合途径等产生。
2.2.2 化学成分特有性的地理分布理论依据按照系统与进化植物学理论, 药用植物次生代谢产物的形成不但与其个体发育过程密切相关, 其化学成分的类型和存在规律还可追溯到与其系统发育过程, 如种系发生、起源与演化、分布与散播途径、共祖近度、进化速率、地质历程、生态历程等。“系统与进化植物学”、“植物区系地理学”等理论是揭示植物次生代谢产物与其生存的地理环境关联规律的重要理论基础。
事实上, 植物的物种起源、演化及其时空分布是有特定的规律的。这一规律与地质历史和环境变迁密切相关, 并形成植物物种之间的亲缘和演化关系。也是植物次生代谢产物千差万别的重要成因, 因此, 分析植物次生代谢产物与地理分布的关联规律, 可为质量标志物的“特有性”提供重要的理论依据。
植物种属地理是植物区系地理学的重要内容, 而“多样化中心或演化中心, 分化中心”、“发生中心或起源中心”、“原始种保存地”、“分布区边缘”、“特有种和特有种分布区、古特有种、新特有种、生态特有种”等是其中的核心概念。
按照系统与进化植物学及植物区系地理学理论, 具有如下规律: ①单元发生的类群具有共同的祖先(祖种), 大多数属是一个自然的类群; ②属内各成员之间的差异无不打上地质历程和生态历程的烙印; ③与祖种亲缘关系近的类群含有该属的原始化学成分, 分布于属的起源中心或原始种保存地, 与祖种亲缘关系较远的类群含有该属的新生(进化)化学成分, 分布于属的进化中心或多样性中心或分布区边缘; ④近缘类群随地理梯度和生态梯度具有各种式样的替代现象。按照以上理论, 可以为寻找发现新的活性成分提供规律性的线索, 并为近源中药特有性成分的确定提供理论依据。
2.2.3 化学成分特有性的生态环境及化学性状环境饰变理论依据植物的遗传物质基础决定次生代谢产物的生物合成路径, 而环境因子决定次生代谢产物的合成效果。并且, 特殊的生态条件可以产生“环境饰变”, 形成特殊的“生态型”、“化学型”, 进而决定化学成分的“特有性”。成分的特有性反映在成分的种类与含量两个方面。
① 光照的影响:光照的强度、光照时间以及光质都对药用植物的目的活性物质代谢产生影响。如生于阳坡的金银花中绿原酸的含量高于阴坡:而对于阴生植物, 则须适当遮阴以减少光照强度, 以适合植物的生长和次生代谢产物的合成积累; 光质与次生代谢物的关系研究中紫外光B与酚醛类、萜烯类、黄酮类等的关系的研究比较多。一般认为, 紫外辐射的增强可诱导植物产生较多酚醛类等紫外吸收物质, 增强抗氧化能力, 减少紫外辐射对植物自身的伤害。研究表明:类黄酮合成的关键酶——查耳酮合酶受紫外光和蓝光调控, 在紫外辐射下类黄酮合成途径的苯丙氨酸裂解酶和查耳酮合酶以及其他分支点的酶活加强, 引起植物体内类黄酮及酚醛类化合物, 如丹宁、木质素等的增加。在温室中对烟草补加紫外光照射, 其绿原酸含量可增加到对照的5倍; 受红光照射时则产生较多的生物碱、较少的酚。不同光质对洋地黄组织培养中强心苷的形成与积累有影响, 蓝光照射下, 强心苷含量最高, 而黄光、红光、绿光及黑暗条件下则很低。
② 温度的影响:药用植物目的活性物质的合成也受到环境温度的影响, 温度可直接影响植物的生理功能, 进而影响其体内次生代谢产物的合成和积累。在高温干旱条件下, 颠茄、金鸡纳等植物体内生物碱的含量较高; 欧乌头在高温条件下含乌头碱, 在寒冷低温时则变为无毒。干旱胁迫通常会使药用植物体内的目的活性物质包括萜类、生物碱、有机酸等的含量升高, 例如, 干旱胁迫可对银杏叶片中槲皮素含量的提高有一定的促进作用, 而抑制了芦丁含量的增加; 干旱胁迫的薄荷叶中, 萜类物质含量升高, 水分较多时薄荷油的含量则下降。
③ 土壤的影响:土壤提供植物次生代谢产物合成的初始原料, 土壤中的无机营养元素在药用植物目的活性物质代谢过程中起着重要作用。通过对道地和非道地岷山当归栽培土壤成分进行主成分分析, 发现土壤元素钾、磷、锰、锌、镁和土壤有机质含量的差异是当归道地性形成的主要土壤生态因子。有研究表明额外追加氮肥将导致植物次生代谢物, 如萜烯的减少, 这是因为氮肥将会促进光合产物用于植物生长, 使非结构碳水化合物的含量下降, 但以氨基酸为前体的次生化合物水平随土壤含氮量的增加而升高。
2.2.4 化学成分特有性的入药部位及显微组织化学的特有性理论依据同一植物的不同器官作为不同药材也较为普遍, 如陈皮与橘红、郁金与姜黄等, 其成分与功效既有联系又存在差异, 对于这种情况, 分析成分的特有性及其理论依据就尤为重要。
事实上, 药用植物次生代谢产物生物合成具有组织和器官的特异性, 在细胞水平上, 植物在细胞不同区室中合成不同种类的次生代谢产物。植物中次生代谢相关的底物和酶的积累、储存及合成部位常常是分开的, 代谢途径中酶的亚细胞定位不同, 导致了次生代谢产物在细胞水平上的区室化。细胞中不同细胞器参与特异基因的表达和酶的活性调节, 进而调节次生代谢产物的合成和积累。喹诺里嗪啶(quinolizidine)和双稠吡咯烷衍生物(pyrraizidine)在羽扇豆(Lupinus albus)和天仙子(Hyoscyarnus niger)茎皮中的含量均比整个茎的含量高, 表明外表皮细胞是生物碱主要的分布区域。东莨菪碱生物合成途径的最后步骤天仙子胺的环氧化, 是发生在幼嫩根部的中柱鞘, 而后转运到地上部分被储存。
在特定的器官组织内合成或积累特异的化合物是次生代谢的一个特点。次生代谢途径中关键酶基因的表达, 也往往具有组织器官的特异性, 次生代谢产物的合成也相应地具有组织器官特异性。如红花、天竺葵、玫瑰等萜类药用成分在种类和总量上在花器官中合成较多, 如薄荷等一些药用草本植物的茎、叶、花等的腺毛是合成和储存特异的萜类代谢产物最主要的场所, 罂粟中的吗啡生物碱大量储存在蒴果的液泡中。
3 中药质量标志物研究方法按照中药质量标志物的有效、特有、传递与溯源、可测和处方配伍的所有要素要求, 基于中医药理论和临床用药方式以及中药材的生物学属性, 采用系统生物学、化学生物学以及化学物质组学等现代研究方法, 从物质与有效、特有、传递与溯源以及配伍等方面全面解析、表征和界定中药质量标志物, 建立基于质量属性完整表达的中药质量标志物研究模式。
3.1 化学物质组解析及中药形成全过程的质量属性传递变化规律研究基于质量标志物“传递与溯源”的要求, 首先要明确两个基本概念:即中药全产业链和药品整个生命周期。全产业链是指中药原料从药材种质、栽培、采收、加工、炮制、中成药的工业制备、储存、运输直至使用; 药品的整个生命周期是指中药药品的药效物质形成、获取、传输、体内过程直至最终生物效应表达。其次, 需要满足两个要求:最终效应成分阐明和全程质量控制体系的建立。
为满足上述要求, 需应用多学科知识系统解析中药有效物质在植物体内的“合成成分”、药材中的“原有成分”、饮片中的“转化成分”、制剂中获取的“原形成分”、吸收入血机体内代谢的“血中移行成分”直至发挥功效“效应成分”。质量标志物“传递与溯源”既厘清中药药效物质的传递、变化过程, 又着眼于全程质量控制体系建立的最终目的。本课题组在对元胡止痛滴丸的质量标志物研究中, 从元胡止痛滴丸中辨识出51个化学成分, 其中28个来源于延胡索药材, 主要为原小檗碱型、原阿片碱型和阿朴菲型生物碱, 21个来源于白芷药材, 主要为线型呋喃香豆素。从溯源和特有的角度, 分别对延胡索植物中原小檗碱型生物碱类成分生物合成途径以及线型呋喃香豆素类成分在白芷中的生物合成途径进行了分析; 从传递的角度, 对口服元胡止痛滴丸大鼠血中移行成分进行辨识, 检出24个原形成分和16个代谢产物, 进一步从脑组织中检出15个可透过血脑屏障成分, 最后对透过血脑屏障的转运机制进行了研究和探讨, 基本上阐释了该药化学质量属性的传递过程。
3.2 基于成分“特有性”质量标志物研究在明确中药的化学物质组的前提下, 以植物亲缘关系学、系统与进化植物学、植物化学分类学、植物区系地理学、中药资源生态学、分子生药学等理论, 分析各原料药材的植物学分类地位、系统位置和起源演化规律; 基于原料药材化学物质组和植物亲缘学分析结果, 提炼各药材的特有性成分和特征性成分, 对各成分进行次生代谢产物生源途径分析, 明确成分特有性的生源学依据; 结合化学成分的入药部位及显微组织特有性、采收期和生物生长时期的特有性以及生态环境及化学性状环境饰变特点, 分析不同基原、不同入药部位、不同炮制方法以及不同采收时间的化学成分差异性证据, 主要包括: ①同一类药材区别于其他药材的特征性成分; ②同一类药材中不同种药材间差异成分; ③同一药材不同基原之间的差异性成分; ④成分的生源途径及亲缘学依据。进一步明确成分的特有性及其生源学依据, 为聚焦质量标志物提供理论和研究证据。
3.3 基于成分与“有效性”相关的质量标志物研究基于对中药有效性的基本认识, 反映中医药理论特点和中药有效性表达的完整性, 应从成分与药效、药性及体内过程三方面的关联关系确定中药质量标志物。
3.3.1 成分与药效的关联研究基于中药复杂体系特点, 成分与药效的关联关系研究可采用系统生物学方法和谱-效相关分析方法, 从“系统-系统”的角度关联化学物质组与生物学效应, 分析提炼成分-靶点-通路-功效的关联关系; 亦可从“要素-要素”的角度, 采用离体器官、细胞、受体分子以及荧光分子探针、靶点垂钓捕获等化学生物学方法, 直接关联药物成分与靶点的对应关系。筛选药效物质基础, 确定质量标志物。本课题组对元胡止痛滴丸的质量标志物研究中, 采用腹腔注射缩宫素诱发大鼠痛经模型, 研究元胡止痛滴丸对痛经模型大鼠的镇痛作用及机制; 采用皮下注射硝酸甘油诱发大鼠偏头痛模型, 研究元胡止痛滴丸对偏头痛模型大鼠的镇痛作用及机制; 采用大鼠离体子宫收缩模型, 通过加入不同的激动剂和拮抗剂来观察元胡止痛滴丸对子宫收缩活动的影响, 进一步探寻其作用机制; 采用大鼠原代子宫平滑肌细胞钙内流影响探讨了对平滑肌的解痉机制; 采用大鼠痛经模型进行代谢组学研究, 探讨对内源性生物标志物的影响; 基于G蛋白偶联受体研究主要成分对相关受体的影响, 通过网络药理学实验分析了主要成分的靶点和通路。最后确定与有效性相关的质量标志物。在对疏风解毒胶囊的质量标志物研究中, 在应用5种整体动物模型研究的基础上, 进一步进行了基因组学、转录组等系统生物学研究, 并基于抗炎和解表作用, 进行谱-效筛选, 采用G-蛋白偶联受体筛选方法, 筛选主要成分的相关受体, 通过网络药理学实验分析了主要成分的靶点和通路。最后确定与有效性相关的质量标志物[36-40]。
3.3.2 成分与药性的关联研究药性(味)的内涵应包括酸、甘、苦、辛、咸温、热、寒、凉的原语义及其生物效应两个方面, 目前对于中药药性科学内涵的阐释仍在不断探索阶段, 本课题组针对五味药性的科学内涵, 从滋味、气味的“原语义”的角度, 采用电子舌、电子鼻等仿生模型研究和筛选了元胡止痛滴丸主要药味延胡索和白芷中辛、苦药味的物质基础, 进一步采用分子对接方法, 通过成分-嗅觉/味觉受体分子对接进行确证; 基于辛苦药味的“功效”分析, 选择相关的功能受体, 进行受体结合试验, 从成分与药性相关性的角度为质量标志物的确定提供理论和实验依据。
3.3.3 成分与体内过程及转运机制的关联研究中药的入血成分及其代谢产物的体内过程和动力学规律是中药发挥疗效的基础, 因此, 研究成分与体内过程及转运机制的关联关系也是质量标志物确定的必要途径。本课题组在对疏风解毒胶囊质量标志物的研究中, 首先对口服元胡止痛滴丸的入血成分及其代谢产物进行了辨识, 进一步研究了延胡索甲素、延胡索乙素、原阿片碱以及欧前胡素、异欧前胡素的药代动力学行为, 分析了延胡索甲素、延胡索乙素、原阿片碱、欧前胡素及异欧前胡素的脑组织分布规律, 最后, 研究和探讨了以上成分跨血脑屏障的转运机制。通过以上研究, 为质量标志物的确定提供理论和实验依据。
3.4 基于“配伍环境”的质量标志物研究中药多以复方的形式进行临床运用, 配伍理论是中医药理论的核心内容。同一药材在不同处方中可以发挥不同的作用, 因此, 针对性的质量标志物也不同。在质量标志物概念与核心理论中, 配伍环境占有非常重要的地位, 是质量研究回归到中医药理论的必要条件。基于配伍环境的中药质量标志物研究多以拆方的形式, 基于组方配伍原理, 以功效药对、减除药味以及谱-效分析和成分配伍等形式, 从整体动物、离体细胞、分子和网络分析等不同层次进行系统研究。本课题组在疏风解毒胶囊的质量标志物研究中, 首先将该方分成疏风解表和清热解毒两个药对, 以5种整体动物模型进行药效学评价, 进一步进行不同组的网络药理学分析、解表和抗炎的谱-效分析以及成分配伍的手提结合实验, 最后, 基于配伍环境确定质量标志物。
3.5 成分的“可测性”研究及多元质量控制方法的建立 3.5.1 指标成分(marker ingredient)含量测定的“指标成分”常被认为是质量评价的最重要的指标, 是评价质量优劣和合格限度的“金指标”。在“点-线-面-体”的质控模式中属于“点”的层次。指标成分应能反映所评价中药特有的、区别于它药的功效属性。大多数“有效成分”与中药的功效相关, 但专属性、特异性以及在方-证对应方面的功效针对性不强, 也达不到合理评价的要求。在“指标成分”层面, 应考虑到成分的结构类型、构-效关系、以及功效发挥的多靶点多途径的特点, 宜采用“多指标含量测定”的方法。
3.5.2 指示性成分(indicating ingredient)指示性成分一般是指在中药中含量较大、能代表同类结构、功效类似物质的代表性成分。在“点-线-面-体”的质控模式中属于“线”的层次。由于成分的结构类似, 具有相似的理化性质、溶解性和色谱、光谱特点, 常被用作新药研发中的工艺路线筛选和工艺参数优化评价指标, 起到指示性作用。也适合以“一测多评”的方法进行多指标成分的含量测定, 达到质量控制的目的。
3.5.3 类成分(class ingredient)类成分指结构相似的一类成分, 如总黄酮、总皂苷、总生物碱等。类成分反映一类活性的总体功效, 因此, 在质量评价中也非常重要, 常以总含量来表示, 在“点-线-面-体”的质控模式中属于“面”的层次。总含量测定关键应注意排除非测定成分的干扰, 保证方法的专属性和特异性。
3.5.4 全息成分(holographic ingredient)中药化学成分复杂, “有效成分”和“无效成分”尚不完全清楚, 临床功效表达方式复杂多样, 物质-功效之间呈现多元、非线性关系, 质量评价不但需要以某些成分的含量作为指标, 还需要对中药的整体“化学轮廓”及其相应的“生物学模式”进行相关性研究, 建立基于“全息成分”和“化学轮廓”的分析方法和质量评价方法, 在“点-线-面-体”的质控模式中属于“体”的层次。“全息成分”并不完全等于“全成分”。全息成分是在所用分析方法下能够显现的成分及其所呈现的理化及波谱学信息。基于全息成分的质量评价更适合使用模式识别的方法。指纹图谱技术是常用的基于全息成分的模式识别方法, 目前多用于评价质量的一致性, 但对于质量优劣差异的评价还存在许多技术瓶颈, 近些年来, 将中药指纹图谱与药效结合, 建立了中药活性指纹图谱技术, 为中药谱效关系研究提供研究手段, 也为从整体化学轮廓的角度评价中药质量提供新的思路和路径[15]。
4 结语长期以来, 我国中药科技工作者对中药质量评价模式和质量控制方法进行了大量研究和探索, 使中药质量研究得到了长足的进步, 但仍未能从根本上解决中药质量评价的共性问题。质量标志物的提出直接聚焦中药质量属性的本质内涵, 从有效性完整表达、特有性和专属性要求以及质量的传递与溯源角度统领中药质量研究, 实现从质量认识与质量评价的思路与模式的根本提升。
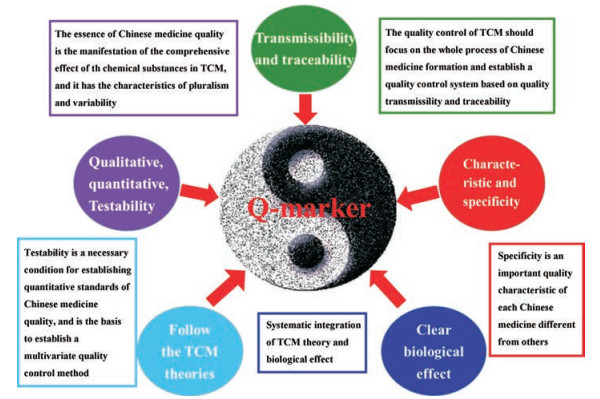
根据质量物质在药材、饮片、方药及其制剂中的“物质存在性”、“物质特有性”、“物质可测性”、中医药理论“物质功效关联性”和在产品生产过程中的“物质溯源性和传递性”的五大元素, 提出了复方中药质量标志物“五原则”, 为发现和确认质量标志物的基本思路、方法和研究路径(图 1)。
|
Figure 1 Five principles for determination of Q-marker of compound Chinese medicine preparations |
质量标志物的核心理论本质上是整合与应用的理论, 是以中医药理论和相关植物学科理论为基础, 以现代化学生物学技术为研究方法, 系统解析与有效性密切相关的中药内在化学质量属性, 提炼质量控制指标, 建立多元质量评价方法, 最终实现建立全程质量控制体系的目的。
质量标志物的概念与核心理论既是整合的理论, 又是开放的理论。需要利用多学科的理论和方法, 丰富和完善质量标志物的理论。不断完善中药质量评价方法, 提高中药质量控制水平。
| [1] | Liu CX, Chen SL, Xiao XH, et al. A new concept on quality marker of Chinese materia medica:quality control for Chinese medicinal products[J]. Chin Tradit Herb Drugs (中草药), 2016, 47: 1443–1457. |
| [2] | Zhang TJ, Bai G, Han YQ, et al. The method of quality marker research and quality evaluation of traditional Chinese medicine based on drug properties and effect characteristics[J]. Phytome-dicine, 2018, 44: 204–211. DOI:10.1016/j.phymed.2018.02.009 |
| [3] | Zhang HB, Wu X, Xu J, et al. The comparative pharmacokinetic study of Yuanhu Zhitong prescription based on five quality-markers[J]. Phytomedicine, 2018, 44: 148–154. DOI:10.1016/j.phymed.2018.02.005 |
| [4] | Zhang TJ, Bai G, Chen CQ, et al. Research approaches of quality marker (Q-marker) of Chinese materia medica formula based on "five principles"[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 1–13. |
| [5] | Zhang TJ, Wang J, Chen CQ, et al. Method of quality marker research and quality evaluation of Chinese materia medica based on drug properties and effect characteristics[J]. Chin Tradit Herb Drugs (中草药), 2017, 48: 1051–1060. |
| [6] | Zhang TJ, Xu J, Shen XP, et al. Relation of "property-response-component" and action mechanism of Yuanhu Zhitong Dropping Pills based on quality marker (Q-Marker)[J]. Chin Tradit Herb Drugs (中草药), 2016, 47: 2199–2211. |
| [7] | Liu CX. Determination of quality markers is basis for establishing quality standard and control of Chinese herbal medicines[J]. Chin Herb Med, 2017, 9: 299–300. DOI:10.1016/S1674-6384(17)60108-4 |
| [8] | Liu CX, Cheng YY, Guo DA, et al. A new concept on quality marker for quality assessment and process control of Chinese medicines[J]. Chin Herb Med, 2017, 9: 3–13. DOI:10.1016/S1674-6384(17)60070-4 |
| [9] | Liu CX, Guo DA, Liu L. Quality transitivity and traceability system of herbal medicine products based on quality markers[J]. Phytomedicine, 2018, 44: 247–257. DOI:10.1016/j.phymed.2018.03.006 |
| [10] | Li K, Li JF, Su J, et al. Identification of quality markers of Yuanhu Zhitong tablets based on integrative pharmacology and data mining[J]. Phytomedicine, 2018, 44: 212–219. DOI:10.1016/j.phymed.2018.03.002 |
| [11] | Li W, Polachi N, Wang XY, et al. A quality marker study on salvianolic acids for injection[J]. Phytomedicine, 2018, 44: 138–147. DOI:10.1016/j.phymed.2018.02.003 |
| [12] | Li YB, Zhang YN, Wang YM, et al. A strategy for the discovery and validation of toxicity quality marker of Chinese medicine based on network toxicology[J]. Phytomedicine, 2018. DOI:10.1016/j.phymed.2018.01.018 |
| [13] | Yang WZ, Zhang YB, Wu WY, et al. Approaches to establish Q-markers for the quality standards of traditional Chinese medicines[J]. Acta Pharm Sin B, 2017, 7: 439–446. DOI:10.1016/j.apsb.2017.04.012 |
| [14] | Bai G, Zhang TJ, Hou YY, et al. From quality markers to data mining and intelligence assessment:a smart quality-evaluation strategy for traditional Chinese medicine based on quality markers[J]. Phytomedicine, 2018, 44: 109–116. DOI:10.1016/j.phymed.2018.01.017 |
| [15] | Ding GY, Wang YS, Liu AN, et al. From chemical markers to quality markers:an integrated approach of UPLC/Q-TOF, NIRS, and chemometrics for the quality assessment of honeysuckle buds[J]. RSC Adv, 2017, 7: 22034–22044. DOI:10.1039/C6RA28152D |
| [16] | Zhou MG, Ma XY, Ding GY, et al. Comparison and evaluation of antimuscarinic and anti-inflammatory effects of five Bulbus Fritillariae, species based on UPLC-Q/TOF integrated dual-luciferase reporter assay, PCA and ANN analysis[J]. J Chromatogr B, 2017, 1041: 60–69. |
| [17] | Ding GY, Li BQ, Han YQ, et al. A rapid integrated bioactivity evaluation system based on near-infrared spectroscopy for quality control of Flos Chrysanthemi[J]. J Pharm Biomed Anal, 2016, 131: 391–399. DOI:10.1016/j.jpba.2016.09.008 |
| [18] | Ding GY, Nie Y, Hou YY, et al. An integrated strategy of marker ingredients searching and near infrared spectroscopy rapid evaluation for the quality control of Chinese eaglewood[J]. J Pharm Biomed Anal, 2015, 114: 462–470. DOI:10.1016/j.jpba.2015.06.029 |
| [19] | Li ZQ, Liu J, Zhang DQ, et al. Nuciferine and paeoniflorin can be quality markers of Tangzhiqing tablet, a Chinese traditional patent medicine, based on the qualitative, quantitative and dose-exposure-response analysis[J]. Phytomedicine, 2018, 44: 155–163. DOI:10.1016/j.phymed.2018.02.006 |
| [20] | Guo R, Zhang XX, Su J, et al. Identifying potential quality markers of Xin-Su-Ning capsules acting on arrhythmia by integrating UHPLC-LTQ-Orbitrap, ADME prediction and network target analysis[J]. Phytomedicine, 2018, 44: 117–128. DOI:10.1016/j.phymed.2018.01.019 |
| [21] | Wu X, Zhang HB, Fan SS, et al. Quality markers based on biological activity:a new strategy for the quality control of traditional Chinese medicine[J]. Phytomedicine, 2018, 44: 103–108. DOI:10.1016/j.phymed.2018.01.016 |
| [22] | Zhong Y, Zhu JQ, Yang ZZ, et al. Q-marker based strategy for CMC research of Chinese medicine:a case study of Panax notoginseng saponins[J]. Phytomedicine, 2018, 44: 129–137. DOI:10.1016/j.phymed.2018.01.023 |
| [23] | Jiang ZZ, Yang J, Wang YF. Discrimination and identification of Q-markers based on 'Spider-web' mode for quality control of traditional Chinese medicine[J]. Phytomedicine, 2018, 44: 98–102. DOI:10.1016/j.phymed.2017.12.034 |
| [24] | Wang XJ, Zhang AH, Kong L, et al. Rapid discovery of quality-markers from Kaixin San using chinmedomics analysis approach[J]. Phytomedicine, 2017. DOI:10.1016/j.phymed.2017.12.014 |
| [25] | He J, Feng XC, Wang K, et al. Discovery and identification of quality markers of Chinese medicine based on pharmacokinetic analysis[J]. Phytomedicine, 2018, 44: 182–186. DOI:10.1016/j.phymed.2018.02.008 |
| [26] | Chen TB, Zuo YH, Dong GT, et al. An integrated strategy for rapid discovery and identification of quality markers in Guanxin Kangtai preparation using UHPLC-TOF/MS and multivariate statistical analysis[J]. Phytomedicine, 2018, 44: 239–246. DOI:10.1016/j.phymed.2018.03.005 |
| [27] | Tang ZS, Liu YR, Lv Y, et al. Quality markers of animal medicinal materials:correlative analysis of musk reveals distinct metabolic changes induced by multiple factors[J]. Phytomedi-cine, 2018, 44: 258–269. DOI:10.1016/j.phymed.2018.03.008 |
| [28] | Xiong Y, Hu YP, Li F, et al. Promotion of quality standard of Chinese herbal medicine by the integrated and efficacy-oriented quality marker of effect-constituent index[J]. Phytomedicine, 2018, 45: 26–35. DOI:10.1016/j.phymed.2018.03.013 |
| [29] | Zhang YT, Xiao MF, Liao Q, et al. Application of TQSM polypharmacokinetics and its similarity approach to ascertain Q-marker by analyses of transitivity in vivo of five candidates in Buyanghuanwu injection[J]. Phytomedicine, 2018, 45: 18–25. DOI:10.1016/j.phymed.2018.03.012 |
| [30] | Huang BM, Zha QL, Chen TB, et al. Discovery of markers for discriminating the age of cultivated ginseng by using UHPLC-QTOF/MS coupled with OPLS-DA[J]. Phytomedicine, 2018, 45: 8–17. DOI:10.1016/j.phymed.2018.03.011 |
| [31] | Hou JJ, Cao CM, Xu YW, et al. Exploring lipid markers of the quality of coix seeds with different geographical origins using supercritical fluid chromatography mass spectrometry and chemometrics[J]. Phytomedicine, 2018, 45: 1–7. DOI:10.1016/j.phymed.2018.03.010 |
| [32] | Liu WL, Zhang XL, Fan SQ, et al. A novel concept of Q-Markers:molecular connectivity index[J]. Phytomedicine, 2018, 45: 36–40. DOI:10.1016/j.phymed.2018.03.015 |
| [33] | Wang ZQ, Shen J, Li P, et al. Research on quality markers of moutan cortex:quality evaluation and quality standards of Moutan Cortex[J]. Chin Herb Med, 2017, 9: 299–300. DOI:10.1016/S1674-6384(17)60108-4 |
| [34] | Guo DA. Quality marker concept inspires the quality research of traditional Chinese medicines[J]. Chin Herb Med, 2017, 9: 1–2. |
| [35] | Zhang TJ, Liu CX. Identification of Chinese materia medica and its chemical biology characterization path on five taste theory[J]. Chin Tradit Herb Drugs (中草药), 2015, 46: 1–6. |
| [36] | Feng Y, An MP, Hu JF, et al. Study on the effect of Yuanhu Zhitong dropping pills on contraction of uterus isolated from unpregnancy rats[J]. Asia-Pacitic Tradit Med (亚太传统医药), 2017, 13: 3–6. |
| [37] | Feng Y, Zhu ZN, Hu JF, et al. Study on compatibility rationality and comparative advantage of analgesic effect of Yuanhu Zhitong Dropping Pills on dysmenorrhea model[J]. Drug Eval Res (药物评价研究), 2017, 40: 917–921. |
| [38] | Feng Y, Hu JF, Di ZQ, et al. Analgesic effect of Yuanhu Zhitong Dropping Pills on experimental migraine in rats induced by nitroglycerin and its mechanism[J]. Drugs Clin (现代药物与临床), 2016, 31: 423–426. |
| [39] | Han YQ, Xu J, Gong SX, et al. Chemical constituents and mechanism of Corydalis Rhizoma based on HPLC-QTOF/MS and G protein-coupled receptor analysis[J]. Acta Pharm Sin (药学学报), 2016, 51: 1302–1308. |
| [40] | Han YQ, Xu J, Zhang XM, et al. Network pharmacology-based study on mechanism of Yuanhu Zhitong Dropping Pills in the treatment of primary dysmenorrhea[J]. Acta Pharm Sin (药学学报), 2016, 51: 380–387. |
 2019, Vol. 54
2019, Vol. 54


