2. 广东药科大学广东省药物新剂型重点实验室, 广东 广州 510006;
3. 广东药科大学广东省局部精准递药制剂工程技术研究中心, 广东 广州 510006
2. Guangdong Provincial Key Laboratory of Advanced Drug Delivery, Guangdong Pharmaceutical University, Guangzhou 510006, China;
3. Guangdong Provincial Engineering Center of Topical Precise Drug Delivery System, Guangdong Pharmaceutical University, Guangzhou 510006, China
中药为保障人类健康及繁衍生息做出了巨大的贡献, 其通常是在中医药理论指导下辩证施治, 按照“君、臣、佐、使”的配伍原则通过多成分、多靶点和多途径的特点发挥治疗或调理作用[1]。中药的这些功效归根结底都是由其药效物质组分来实现的, 针对疾病的表里虚实、轻重缓急, 以多种组分配伍的形式达到标本兼治的目的[2]。如何有效地递送中药复方多组分是防治疾病的关键。目前中药多组分的递送研究多强调释药的同步性, 但根据中医方剂配伍理论和中药药性理论, 中药的多组分递送模式不应是传统的单元型而应是多元化的, 每一个制剂单元应该根据各组分的理化性质、生物学特征及药理学作用对其递释行为进行相应的调控[2]。因此, 结合中药特点, 利用现代化制剂技术实现多组分有效的空间分布和多元化递释行为, 优化组分间的配伍效应, 充分发挥其协同作用, 是科学、合理的选择。
纳米递药系统已在小分子化学药物、多肽蛋白及基因药物等的递送上显示出优于传统制剂的巨大优势[3, 4], 将纳米技术引入中药剂型的研究开发可能是实现中药制剂现代化的一种有效途径[5]。当前采用纳米递药系统对中药单体的递释研究较多[6-8], 而少有对中药复方组分的报道, 究其原因主要在于中药复方组分繁多, 不同组分的理化性质差异较大, 难以实现多种亲、疏水性药物的共载[9]。而且, 即使有研究应用纳米递药系统实现了对多种中药组分的包载和缓释[10, 11], 也不能精确控制不同组分的释放次序及空间分布[12]。
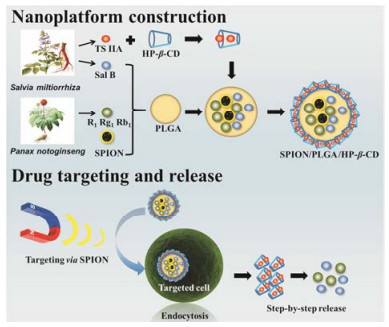
为此, 本研究构建了一种核壳型聚乳酸-羟基乙酸共聚物(PLGA)磁性纳米递药系统, 以克服目前中药复方多组分剂型设计的不足。以经典药对丹参-三七中理化性质差异较大的5种有效组分作为模型药物, 即三七中的水溶性组分三七总皂苷, 主要包括三七皂苷R1 (R1)、人参皂苷Rg1 (Rg1)和人参皂苷(Rb1);丹参中的水溶性组分丹酚酸B (Sal B)和脂溶性组分丹参酮IIA (TS IIA)。在该纳米递送系统的设计中(图 1), 利用羟丙基-β-环糊精(HP-β-CD)的疏水性内腔装载脂溶性组分TS IIA, 应用复乳法将其余4种水溶性组分及超顺磁性的四氧化三铁纳米粒(SPION)包载于PLGA纳米粒的内核里, 然后将HP-β-CD包合物与PLGA纳米粒共孵育, 形成具有核壳结构的复合磁性纳米体系。在外加磁场作用下, 该复合纳米粒可被细胞靶向摄取并迅速内吞, 外壳HP-β-CD包合物携带腔内脂溶性组分从载体脱落, 接着内核PLGA纳米粒中的药物伴随PLGA的降解而逐渐释放。
|
Figure 1 Schematic illustration of multiple components loading process and release properties of core-shell magnetic PLGA nanosystem. SPION: Super-paramagnetic iron oxide nanoparticles; PLGA: Poly-D, L-lactide-co-glycolide; HP-β-CD: Hydroxypropyl-β-cyclodextrin; TS IIA: Tanshinone IIA; Sal B: Salvianolic acid B; R1: Notoginsenoside R1; Rg1: Ginsenoside Rg1; Rb1: Ginsenoside Rb1 |
主要仪器 LSM710激光共聚焦显微平台(德国卡尔蔡司公司); T18型组织分散机(德国IKA公司); ZD-85A型气浴恒温振荡器(金坛市荣华仪器制造有限公司); TDL80-2B台式离心机(上海安亭科学仪器厂); JY92-IIA超声波细胞粉碎机(宁波新芝生物科技有限公司); DelsaTM Nano C激光粒度仪(美国Beckman Coulter公司); MPMS XL-7磁学性质测量系统(美国量子设计公司); RE-52A旋转蒸发仪(上海亚荣生化设备有限公司); LGJ-10型冻干机(北京松源华兴科技发展有限公司); NightOWLⅡ LB 983型小动物活体成像系统(德国伯托公司); LC-20AT液相泵、SIL-20A自动进样器、SPD-M20A二极管阵列检测器、CTO-10ASvp柱温箱、DGU-20Asr真空在线脱气机(日本岛津公司)。
药品和试剂 SPION (粒径约20 nm, 批号ZY151016, 上海克拉玛尔试剂公司); 丹参酮IIA (含量≥98.0%, 批号150106)、三七总皂苷(R1: 26.1%, Rg1: 36.5%, Rb1: 31.8%, 批号040902) (深圳美荷生物有限公司); 丹酚酸B (含量≥98.0%, 批号111562, 上海历鼎生物科技有限公司); 香豆素-6 (含量≥98%)、罗丹明B (含量≥95%) (美国Sigma-Aldrich公司); HP-β-CD (含量≥97%, 相对分子质量1 541.54, 批号C1505029, 阿拉丁试剂有限公司); PLGA (LA:GA = 50:50, 分子质量约10 kDa, 山东省医疗器械研究所); Span-80 (上海申宇医药化工厂); 油酸聚乙二醇甘油酯(LABRAFILM 1944 CS, 法国嘉法狮公司); 聚乙烯醇(PVA, 相对分子质量约31 000, 美国Sigma公司); DAPI (上海碧云天生物科技公司); a-MEM培养基(美国Hyclone公司); L929细胞(小鼠成纤维细胞, 购自中国科学院上海细胞库); 甲醇和乙腈(色谱纯, 迪马科技有限公司); 无水乙醇(分析纯, 天津市百世化工有限公司); 二氯甲烷和乙酸乙酯(分析纯, 天津富宇精细化工有限公司); 蒸馏水(屈臣氏集团有限公司)。
核壳型纳米体系的构建
羟丙基-β-环糊精包合物的制备 本文分别制备香豆素-6包合物及TS IIA包合物。具体方法:加入5 mg香豆素-6 (或50 mg TS IIA)和500 mg HP-β-CD于10 mL无水乙醇中, 超声10 min, 50 ℃搅拌4 h后常温搅拌4 h。接着将混悬液转移至旋转蒸发仪中, 至完全蒸干, 残渣用蒸馏水溶解后过0.22 μm微孔滤膜, 滤液冻干保存备用。
微球的制备 分别制备PLGA微球和HP-β-CD- PLGA微球。具体方法:称取PLGA 125 mg与罗丹明B 10 mg溶于1 mL二氯甲烷与乙酸乙酯的混合溶液中, 涡旋混匀作为油相, 取100 μL蒸馏水加入油相中涡旋混匀。在组织分散机下搅拌形成初乳, 再倾倒入2% PVA水溶液4 mL中并于组织分散机下再次搅拌形成复乳, 将制得的复乳转移至1% PVA水溶液25 mL中, 并于磁力搅拌器中搅拌4 h, 挥干有机溶剂, 低速离心, 取上清液, 即得罗丹明B-PLGA微球。接着, 取罗丹明B-PLGA微球溶液10 mL, 加入香豆素-6包合物水溶液1 mL, 磁力搅拌30 min后, 于100 r·min-1室温振荡6 h后低速离心, 取上清液, 即得香豆素-6-HP-β-CD-罗丹明B-PLGA微球。
纳米粒的制备 分别制备包载荧光物质纳米粒和共载丹参-三七复方多组分纳米粒。首先制备香豆素-6包合物及TS IIA包合物, 方法同上所述。然后, 制备罗丹明B-PLGA纳米粒和共载4种水溶性药物(Sal B、R1、Rg1和Rb1)的PLGA纳米粒, 具体方法:称取PLGA 125 mg和罗丹明B 10 mg (或Sal B 18 mg)溶于二氯甲烷与乙酸乙酯的混合溶液1 mL中, 涡旋混匀, 加入LABRAFILM 1944 CS和Span-80各50 mg, 混匀作为油相; 取蒸馏水(或三七总皂苷水溶液) 100 μL, 作为内水相加入油相中涡旋混匀, 于冰水浴中超声形成初乳, 再倾倒入2% PVA水溶液4 mL中, 于冰水浴中超声形成复乳, 将制得的复乳倾倒入1% PVA水溶液25 mL中并转移至旋转蒸发仪中, 于40 ℃下挥干有机溶剂, 低速离心, 取上清液, 冻干保存备用。最后, 将香豆素-6包合物与罗丹明B- PLGA纳米粒(或TS IIA包合物和共载4种水溶性药物的PLGA纳米粒)共孵育制备荧光纳米粒(或共载丹参-三七复方5种有效组分的纳米粒)。采用超滤管法测定共载丹参-三七复方多组分纳米粒的包封率(各组分的HPLC色谱条件参考前期实验所建立的方法[10]), R1、Rg1、Rb1、Sal B及TS IIA的包封率分别为78.97%、85.22%、85.64%、76.59%和94.70%。
磁性荧光纳米粒的制备 此方法同罗丹明B- PLGA纳米粒的制备所述, 区别仅在于油相的组成中需加入适量SPION。
微球和纳米粒的形貌表征
微球的激光共聚焦显微镜观察 将微球溶液稀释后于激光共聚焦显微镜下观察, 香豆素-6的激发波长为458 nm, 发射波长为505 nm; 罗丹明B的激发波长为540 nm, 发射波长为625 nm。
纳米粒的粒径测定及透射电镜观察 将PLGA纳米粒溶液和HP-β-CD-PLGA纳米粒溶液稀释后于激光粒度仪下测定粒径及粒度分布。分别取100 μL的PLGA纳米粒溶液和HP-β-CD-PLGA纳米粒溶液, 滴于铜网上, 吸附5 min后, 滴加2%磷钨酸染液负染3 min, 用滤纸吸去多余的染液, 晾干后, 于透射电镜下观察。
纳米粒的磁靶向行为考察
磁滞回线(VSM)测定 将冻干后的磁性PLGA纳米粒粉末置于2 K Oe的磁场中, 300 K下, 采用振动探针式磁强计对粉末样品的磁学性质进行测定, 根据结果绘制VSM曲线。
磁铁吸附实验 将磁性纳米粒溶液稀释后转移至2 mL带盖离心管中, 在离心管上方置永磁铁1枚, 吸附1 h后, 移去永磁铁后观察吸附情况。另取等量磁性纳米粒溶液同等操作, 但不放置永磁铁, 对比观察1 h后的吸附情况。
磁性荧光纳米粒的体外细胞摄取 取生长状态良好的对数生长期L929细胞悬液并调整细胞数为每毫升3.5×105个, 于细胞培养皿中细胞数为每毫升3.5×105个, 加入细胞悬液1 mL, 培养24 h, 待细胞贴壁后, 吸弃完全培养基, 磷酸盐缓冲液(PBS)洗涤2次, 再分别向每个皿中加入由基础培养基稀释500倍的磁性荧光纳米粒稀释液1 mL (荧光探针为罗丹明B)。设置对照组(无纳米粒)、无外加磁场组及有外加磁场组(永磁铁固定于细胞培养皿一侧), 培养1 h后, PBS洗涤3次, 10%福尔马林固定30 min, PBS洗涤3次, 加入DAPI染色10 min, PBS洗涤3次, 用锡箔纸包覆避光, 4 ℃下存放待检, 实验过程中避光操作。将细胞培养皿置于活体荧光成像系统下观察, 固定激发波长为540 nm再分别拍摄不同组荧光摄取情况, 对比得到不同组的荧光强度分布图。
纳米粒的程序性释放行为考察
荧光纳米粒的细胞内分布 取生长状态良好的对数生长期L929细胞悬液并调整细胞数为每毫升3.5×105个, 于共聚焦培养皿中加入细胞悬液1 mL, 培养24 h, 待细胞贴壁后, 吸弃完全培养基, PBS洗涤2次, 再分别向每个皿中加入由基础培养基稀释250倍的共载香豆素-6和罗丹明B的荧光纳米粒稀释液, 培养1、3、12、36和48 h后, PBS洗涤3次, 10%福尔马林固定30 min, PBS洗涤3次, 加入DAPI染色10 min, PBS洗涤3次, 用锡箔纸包覆避光, 4 ℃下存放待检, 实验过程中避光操作。将处理好的细胞样品置于激光共聚焦显微镜下观察, 激发波长和发射波长如下: DAPI激发波长340 nm、发射波长480 nm; 香豆素-6激发波长458 nm、发射波长505 nm; 罗丹明B激发波长540 nm、发射波长625 nm。
纳米粒的体外释放 取已除去游离药物的纳米粒冻干粉适量, 加适量蒸馏水复溶, 得到4 mL纳米粒胶体溶液并置于处理好的透析袋中, 扎紧透析袋两端, 将透析袋完全浸没于盛有26 mL蒸馏水的具塞锥形瓶中, 以100 r·min-1转速在37 ℃下恒温振荡, 分别于5、10、15、30 min和1、2、4、6、8、12、24、36、48和72 h, 取锥形瓶外释放介质1 mL, 同时补充等量同温新鲜释放介质。样品溶液加等量甲醇涡旋混匀, 过0.22 μm微孔滤膜后, 按复方组分测定HPLC色谱梯度洗脱条件[10]测定各组分含量, 计算累积释放度, 绘制纳米粒中各组分药物的累积释放曲线。另取共载丹参-三七复方5种组分药物的“非核壳型”PLGA纳米粒(制备参考前期工作[11])同法处理, 绘制其累积释放曲线。另外, 将5种组分配制成与纳米粒中各组分药物含量相当的游离药物组, 同法处理作为对照组。
统计学分析 释放实验结果以x± s表示, 应用Matlab软件对各组释放数据进行处理, 使用anova1命令进行方差分析, 以P < 0.01表示有显著性差异。
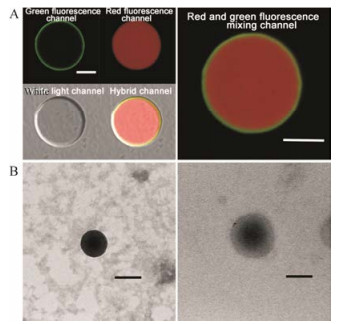
结果 1 微球和纳米粒的形貌通过共聚焦显微镜观察到, 在单一绿色通道下出现的绿色荧光条带位于微球的外部, 而在单一红色通道下出现的红色荧光位于微球的内部, 且红绿荧光出现的位置有清晰的界线; 在红绿混合通道下显示绿色荧光呈圆形条带状包裹于球形红色荧光外圈(图 2A)。两种荧光物质的分布说明, 罗丹明B-PLGA微球构成微球体系的内核, 香豆素-6-HP-β-CD包合物构成微球体系的外壳。
|
Figure 2 Nanocomposites characterization. A: Confocal microscopy image of a single microsphere demonstrated the core-shell compartmentalization of coumarin-6 (green) and rhodamine B (red). The scale bar represents 5 μm; B: Transmission electron microscope images of a single nanoparticle without HP-β-CD shell (left) and nanoparticle with HP-β-CD shell (right). The scale bar represents 100 nm |
经电镜观察到, PLGA纳米粒呈规则球形, 且边界清晰; 而HP-β-CD-PLGA纳米粒为不规则球形, 外层明显呈模糊状, 边界不清晰(图 2B), 提示可能存在核壳结构。
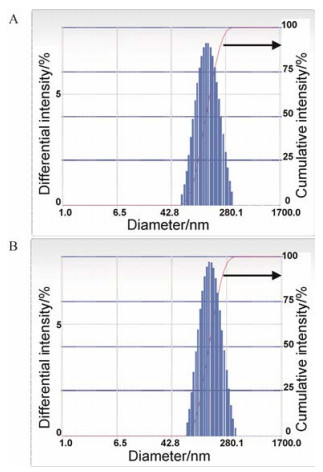
为了进一步说明PLGA纳米粒和HP-β-CD-PLGA纳米粒在粒子尺寸上是否有差异, 采用动态光散射法进行粒径测定(图 3)。结果显示, PLGA纳米粒平均粒径在145 ± 5 nm左右, HP-β-CD-PLGA纳米粒平均粒径在160 ± 4.5 nm左右, 修饰包合物后纳米粒的粒径略微增大, 进一步说明可能存在核壳结构, 与上述激光共聚焦及电镜的观察结果一致。
|
Figure 3 Particle size distribution of nanoparticle without HP-β-CD shell (A) and nanoparticle with HP-β-CD shell (B) |
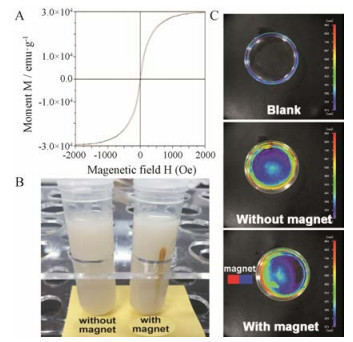
磁性纳米粒的VSM结果显示, 当外加磁场强度达到2 K Oe左右时, VSM曲线基本达到水平, 提示磁性PLGA纳米粒已达到饱和磁感应强度, 其饱和磁化强度约为3.0×10-4 emu·g-1 (图 4A)。
|
Figure 4 Characterization of site-specific drug delivery. A: VSM curve of the SPION loaded nanoparticles; B: In vitro aggregation of the SPION loaded nanoparticles under magnetic field; C: NIRF image of intracellular magnetic targeting. VSM: Vibrating sample magnetometer; NIRF: Near-infrared fluorescence |
磁铁吸附实验结果显示, 在未加磁场的情况下, 磁性PLGA纳米粒在1 h后未出现任何沉淀或吸附情况, 仍为稳定的胶体溶液; 当外加磁场1 h后, 离心管上部出现了明显的棕色聚集物, 表明纳米粒溶液中磁性纳米粒在磁场的作用下倾向聚集在离心管上部(即永磁铁的放置位置); 当移除永磁铁后, 轻轻振摇, 团聚消失(图 4B)。这表明, 该磁性纳米粒具有良好的磁响应性, 可在磁场作用下发生富集和团聚作用, 移除磁场后团聚消失, 可再次形成稳定的胶体溶液。
体外细胞摄取结果显示, 空白对照组中培养皿中间部分呈黑色, 无荧光信号; 无外加磁场组中, 培养皿中荧光分布较为均匀, 无明显的分布趋势, 培养皿中各位置细胞摄取荧光物质的量较为均一; 有外加磁场组中, 培养皿中荧光分布不均匀, 荧光有向外加磁场方向聚集的明显趋势(图 4C)。这表明, 在外加磁场位置细胞摄取荧光物质的量要高于其他位置, 可能是由于在外加磁场作用下磁性PLGA纳米粒向磁场方向聚集, 导致细胞摄取磁性荧光纳米粒的量发生不均衡, 即越靠近磁铁位置的细胞对纳米粒的摄取量就越多, 从而在活体荧光成像下显示出更强的荧光信号, 说明该磁性纳米粒具有物理靶向能力。
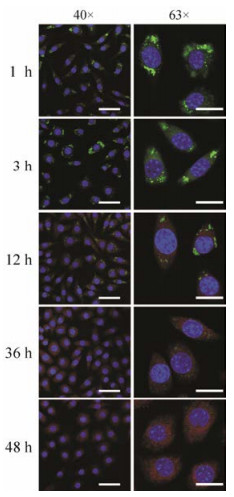
3 纳米粒的程序性释放在激光共聚焦显微镜视野下, 观察到L929细胞对荧光纳米粒在不同时间段的摄取结果显示, 1~3 h时细胞整体呈绿色荧光, 对单个细胞的放大观察也表明细胞内荧光基本为绿色, 几乎未见红色荧光出现; 12 h时, 细胞内开始出现红色荧光, 同时还可见黄色荧光(红绿荧光重叠而成), 间接反映此时绿色荧光仍然存在; 36 h时, 细胞内绿色荧光减弱, 而红色荧光呈弥散状, 分布于整个细胞中; 48 h时, 细胞内整体呈红色荧光, 几乎无绿色荧光存在(图 5)。通过上述结果推测, 当纳米粒被细胞摄取后, 其外壳的香豆素-6先释放, 导致在1~3 h时细胞内荧光基本为绿色, 之后内核的罗丹明B也慢慢释放, 导致细胞内红色荧光逐渐显现并越来越强, 这表明该核壳型纳米体系具有潜在的程序性释药能力, 即先释放外壳药物, 再释放内核药物。
|
Figure 5 Confocal microscopy images of intracellular drug release within L929 mouse fibroblast cells at predetermined timepoints. The scale bars in left column represent 50 μm and the scale bars in right column represent 20 μm |
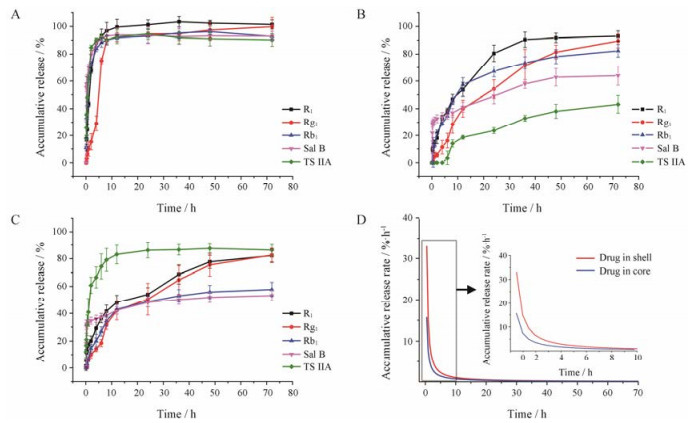
游离药物组、PLGA纳米粒组和HP-β-CD-PLGA纳米粒组的体外释放曲线图直观分析显示, 游离药物组中各药物释放曲线基本相似并在10 h基本释放完全(图 6A), PLGA纳米粒组在前6 h内的释放介质中检测不出TS IIA, 8 h后才能检测到TS IIA, 但72 h总累计释放率约为40% (图 6B); 而HP-β-CD-PLGA纳米粒在5 min时已经可以在释放介质中检测到TS IIA的存在, 且在8~12 h内基本释放完全, 累积释放率达80% (图 6C)。对比可知, TS IIA在HP-β-CD- PLGA纳米粒组中释放更加完全, 且释放速度明显快于PLGA纳米粒组, 统计学分析结果也表明, TS IIA在此两种纳米粒组中的累积释放度具有显著性差异(P < 0.001)。此外, 在HP-β-CD-PLGA纳米粒组中, 除TS IIA外, 其余4种药物则表现出明显的缓释性质, 在50 h才达到基本释放完全, 这表明HP-β-CD-PLGA纳米粒具有程序性释药行为特征, 即外壳HP-β-CD中的TS IIA释放较为迅速, 超过PLGA内核中其他4种成分的释放速度。
|
Figure 6 Release kinetics of TS IIA, Sal B and PNS from the nanoparticles. A: Accumulative release of free drugs; B: Accumulative release of TS IIA, Sal B and PNS from PLGA nanoparticles; C: Accumulative release of TS IIA, Sal B and PNS from HP-β-CD-PLGA nanoparticles; D: Accumulative release rate of drug in shell (red curve) and drug in core (blue curve). TS IIA: Tanshinone IIA; Sal B: Salvianolic acid b; PNS: Panax notoginseng saponins |
为了进一步说明内核药物和外壳药物的释放差异, 采用数学分析, 分别将TS IIA和其余4种药物各自的累积释放度之和视作外壳药物和内核药物的累积释放度, 并拟合累积释放度曲线的函数方程, 求导得到累积释放速率函数(图 6D)。结果显示, HP-β- CD-PLGA纳米粒外壳中药物的累积释放速率在12 h内均明显高于内核药物的累积释放速率。
讨论丹参、三七是经典的中药药对, 药味精简, 疗效确切, 有效组分理化性质各异, 其中TS IIA是一类脂溶性较强的成分, 溶出差, 生物利用度低, 通过将其制成环糊精包合物可提高其生物利用度。Sal B和三七总皂苷是一类水溶性较好的成分, 但容易发生突释, 因此采用PLGA将其包裹。而且, 本研究根据组分的药理效用特点将这5种成分分别载入“核”和“壳”, 以调控不同组分的释药顺序。
为了直观观察释药单元的空间结合方式是否为核壳型, 本研究在两种释药单元里分别载入脂溶性与水溶性荧光染料, 应用激光共聚焦显微镜观察不同荧光染料的分布情况以判断这两种释药单元的结合方式。但鉴于激光共聚焦显微镜分辨率有限, 无法观察到纳米尺寸的物质, 故又采用PLGA微球来代替PLGA纳米粒, 两者粒径不同, 但组成一致。因此, 由激光共聚焦显微镜直接观察到HP-β-CD和PLGA微球共孵育形成的核壳结构可以推测PLGA纳米粒与HP-β-CD也能形成类似结构, 与文献[13]方法一致。
借助纳米递药系统的设计方法实现对中药复方多组分的时空递释, 有助于充分发挥复方多组分的协同作用, 即可根据疾病病情发生发展的病理机制, 在特定的病灶部位渐次释放相应的药物[13, 14]。值得注意的是, 这种现代化的递送方式与中医药理论并不冲突, 在一定程度上契合了其配伍原则, 如利用磁场定位可使药物在特定疾病部位分布, 类似于“使药”即引经药的作用, 能引方中诸药以达病灶。此外, 所包载的磁性纳米粒还可作为磁共振成像(MRI)造影剂[15], 为疾病诊断提供重要参考。因此, 本文所构建的递药系统还具有潜在的诊疗一体化能力, 兼具传统中医药与现代医学特色。
| [1] | Cheng TF, Jin HZ, Liu CX, et al. LC-MS/MS-based molecular networking producing enlighten study of Chinese materia medica[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 265–273. |
| [2] | Jia XB. Cognition of material base of TCM based on the whole concept and development of innovative of TCM[J]. World Sci Technol-Mod Tradit Chin Med (世界科学技术-中医药现代化), 2017, 19: 1430–1434. |
| [3] | Gao HL, Jiang XG. The progress of novel drug delivery systems[J]. Acta Pharm Sin (药学学报), 2017, 52: 181–188. |
| [4] | Estrada LPH, Champion JA. Protein nanoparticles for therapeutic protein delivery[J]. Biomater Sci, 2015, 3: 787–799. DOI:10.1039/C5BM00052A |
| [5] | Alexander A, Ajazuddin, Patel RJ, et al. Recent expansion of pharmaceutical nanotechnologies and targeting strategies in the field of phytopharmaceuticals for the delivery of herbal extracts and bioactives[J]. J Control Release, 2016, 241: 110–124. DOI:10.1016/j.jconrel.2016.09.017 |
| [6] | Hu J, Fu S, Peng Q, et al. Paclitaxel-loaded polymeric nanoparticles combined with chronomodulated chemotherapy on lung cancer:in vitro and in vivo evaluation[J]. Int J Pharm, 2017, 516: 313–322. DOI:10.1016/j.ijpharm.2016.11.047 |
| [7] | Taebnia N, Morshedi D, Yaghmaei S, et al. Curcumin-loaded amine-functionalized mesoporous silica nanoparticles inhibit α-synuclein fibrillation and reduce its cytotoxicity-associated effects[J]. Langmuir, 2016, 32: 13394–13402. DOI:10.1021/acs.langmuir.6b02935 |
| [8] | Meli V, Caltagirone C, Falchi AM, et al. Docetaxel-loaded fluorescent liquid-crystalline nanoparticles for cancer theranostics[J]. Langmuir, 2015, 31: 9566–9575. DOI:10.1021/acs.langmuir.5b02101 |
| [9] | Liu Y, Feng N. Nanocarriers for the delivery of active ingredients and fractions extracted from natural products used in traditional Chinese medicine (TCM)[J]. Adv Colloid Interface Sci, 2015, 221: 60–76. DOI:10.1016/j.cis.2015.04.006 |
| [10] | Zhang X, Chen G, Wen L, et al. Novel multiple agents loaded PLGA nanoparticles for brain delivery via inner ear administration:in vitro and in vivo evaluation[J]. Eur J Pharm Sci, 2013, 48: 595–603. DOI:10.1016/j.ejps.2013.01.007 |
| [11] | Cai H, Wen X, Wen L, et al. Enhanced local bioavailability of single or compound drugs delivery to the inner ear through application of PLGA nanoparticles via round window administration[J]. Int J Nanomedicine, 2014, 9: 5591–5601. |
| [12] | Sun J, Luo C, Wang Y, et al. The holistic 3M modality of drug delivery nanosystems for cancer therapy[J]. Nanoscale, 2013, 5: 845–859. DOI:10.1039/c2nr32867d |
| [13] | Ruiz-Esparza GU, Wu S, Segura-Ibarra V, et al. Polymer nanoparticles encased in a cyclodextrin complex shell for potential site-and sequence-specific drug release[J]. Adv Funct Mater, 2014, 24: 4753–4761. DOI:10.1002/adfm.v24.30 |
| [14] | Wolfram J, Shen H, Ferrari M. Multistage vector (MSV) therapeutics[J]. J Control Release, 2015, 219: 406–415. DOI:10.1016/j.jconrel.2015.08.010 |
| [15] | Huang DH, Qi XY, Ge YR, et al. Application of magnetic iron oxide nanoparticles in magnetic resonance/photothermal dual-modal imaging[J]. Acta Pharm Sin (药学学报), 2017, 52: 481–487. |
 2018, Vol. 53
2018, Vol. 53


