2. 广东药科大学药学院广东省药物新剂型重点实验室, 广东 广州 510006;
3. 广东药科大学药学院广东省药物缓控释制剂工程技术研究中心, 广东 广州 510006
2. Guangdong Key Laboratory of New Drug Formulations, School of Pharmacy, Guangdong Provincial Pharmaceutical University, Guangzhou 510006, China;
3. Guangdong Drug Sustained/Controlled Release Preparation Engineering and Technology Research Center, School of Pharmacy, Guangdong Provincial Pharmaceutical University, Guangzhou 510006, China
文献[1]报道门诊处方中多达1/4的片剂属于分剂量使用, 住院药房成人片剂分剂量使用率为9.28%, 儿童、老年患者的片剂分剂量情况分别高达73.79%和32.37%。药品分剂量如此广泛且无可避免, 但我国一直以来沿用的片剂分剂量方法——徒手分劈或剪药器、磨粉分包和固体制剂液体化法, 存在药品易污染、剂量不准确、患者顺应性差和药品浪费等现象[2−4]。
3D打印技术是基于三维数字模型, 据离散、堆积成型原理, 用逐层制造方式将材料结合起来的工艺[5], 以其高度个性化、小批量和高重复性的特点契合个体化治疗的理念。2015年8月美国食品药品监督管理局(FDA)正式批准了Aprecia制药公司使用3D打印制造SPRITAM levetiracetem (左乙拉西坦)药片[6]。我国3D打印技术在制药领域中的研究, 主要集中在缓控释制剂等高端制剂方面[6−8], 尚未见研究报道将3D打印技术应用于医院药品分剂量。
华法林钠(warfrin sodium, WS)片剂为一线抗凝药物, 其疗效明确, 但治疗窗窄, 即使很小的剂量−反应变化也可能导致血栓或出血。其药理学作用比较复杂, 患者的种族、年龄、体重、生理状态和同时服用的药物、食物、环境等多种因素都能改变机体对抗凝血药物的反应性, 剂量必须个体化[9]。FDA批准的WS片剂有1~10 mg规格, 中间设有7个递增剂量规格供不同人群使用, 而国内上市的剂量规格仅有2.5和3 mg, 远不能满足治疗需求。氢氯噻嗪(hydrochlorothiazide, HCT)片剂作为利尿药[10]和抗高血压药, 小儿主要用于支气管、肺发育不良的预防和治疗, 每日按体重1~2 mg·kg−1或按体表面积30~60 mg·m−2, 分1~2次服用, 并按疗效调整剂量。医院常用4和5 mg剂量, 新生儿、早产儿剂量每次甚至只需要0.5或1 mg, 但市场仅有25 mg的成人剂量规格, 如此微小的分剂量, 无疑给药师带来极大挑战。
3D打印运用于医院药品分剂量较传统方法具有明显优势: ①剂量精准。3D打印分剂量片剂量误差可控制在± 10%以内(本课题组已实现), 其要求高于欧洲药典对分剂量要求(15%)。精准剂量保证了治疗效果, 也降低了窄治疗窗药物的毒副作用。②任意剂量。对于临床需用到的极微剂量(如1/50或1/100片西地那非治疗新生儿肺动脉高压), 3D打印可轻松制备; 对于某些需终身服用稳定剂量的药物, 3D打印也可打印出专属剂量供患者服用。③患者顺应性好。3D打印分剂量片, 整片美观, 易于吞服, 改善患者服药体验, 并且无需担心药物在运输、转移及服药过程中有效成分的损耗。④节省人力物力成本, 操作规范可回溯。3D打印技术的运用使分剂量更加自动化、规范化。机械的运用节省了大量的人力成本, 并且分剂量过程全程可监控、可回溯。大大规范了分剂量操作, 保障了用药安全。
本研究以市售WS和HCT为模型药品, 以医院常用剂量(WS 1 mg、WS 2 mg和HCT 5 mg)为目标剂量。将其研磨粉碎后加入适量填充剂及黏结剂, 以一定浓度乙醇配成浆状, 采用3D打印技术对其再成型, 制备分剂量片, 对成片按中国药典(2015版)项下检测, 并探讨3D打印分剂量可行性及可推广性。
材料与方法仪器与材料 桌面级食品打印机(螺杆挤出, 型号SHINNOVE-S1, 杭州时印科技公司); 生物3D打印机(压力挤出, 德国GeSim公司); YPD-200C型片剂硬度测试仪(上海黄海药检仪器有限公司); ZRS-8G智能溶出测定仪(天津大学无线电厂); 高效液相色谱仪1260 (安捷伦公司); UV-7750紫外分光光度计(日本岛津公司)。
WS (2.5 mg, 批号18170506 C, 上海信谊制药公司); HCT (25 mg, 批号20160720, 广东三才医药集团有限公司); 华法林钠标准品(92.3%, 101163-201001)、氢氯噻嗪标准品(99.7%, 100309-201404) (中国食品药品检定研究院); 稀释辅料选用药用级, 其他试剂为色谱纯或分析纯。
3D打印浆料的制备 取市售WS片、HCT片分别置于研钵研磨15 min, 按比例加入稀释剂混匀(表 1)并以75%乙醇配成糊状, 即得药品打印浆料。WS 1 mg和2 mg分剂量片选用同一处方、不同模型, 含药比例为2% (w/w); HCT含药比例为5%, 用倒装法装入一次性打印料筒中。
| Table 1 The proportion (w/w) of the raw materials in the printing paste. WS: Warfrin sodium; HCT: Hydrochlorothiazide; MCC: Microcrystalline cellulose; HPMC: Hydroxypropyl methylcellulose |
药片模型设计 3D打印分剂量片, 剂量与片剂质量直接相关。参照Skowyra和Pietrzak等[11, 12]报道, 打印一系列递增、高/直径相等的药片, 以其质量与模型体积拟合m-v (mass-volume)回归方程。确定理论体积后, 使高为实际层厚的整数倍, 再以此求得模型的直径值, 可降低切丝软件中的“半层误差”, 提高打印片质量的符合程度。以回归方程确定目标剂量的理论模型参数, 在此参数上进行微调直至打印平均片重质量符合目标质量(±1%以内), 最终确定打印模型。对于某些低剂量的分剂量片, 为避免药片过小, 同时也为了提高打印精度, 降低打印难度, 将其制备成网孔片以扩充体积。模型由Materialise Magics 21.0建模生成STL (stereolithography)格式, 随后由CURA软件进行切丝处理, 并对打印参数进行相应设置, 最后生成3D打印机识别的Gcode格式文件。
分剂量片的打印 将打印浆料装载至打印仓, 药片模型导入3D打印机。层层打印, 逐层叠加, 最终完成整个分剂量片的制备。出于对打印剂量准确性的考虑, 打印1 mg低剂量规格WS分剂量片采用更高精度的3D生物打印机(图 1a), 并打印成网孔结构使片型不致过小。出于对提高打印效率的考虑, 采用桌面级食品打印机(图 1b)来打印2 mg规格WS分剂量片, 并以此考察不同3D打印机、不同打印模式对打印片的性质影响。同时采用桌面级食品打印机制备另一种分剂量药物HCT 5 mg, 考察该分剂量技术在不同药品中的通用性与可推广性。打印参数见表 2。

|
Figure 1 3D bioprinter with high-precision (a); desktop-grade food printer with high print efficiency (b) |
| Table 2 The printing parameter of the divided-dose tablets |
物理机械性质 片重差异: 3组分剂量片分别随机选取20片, 精密称定单片重量, 计算平均片重, 评估质量波动程度。片厚、直径: 3组分剂量片分别随机选取10片, 用游标卡尺测量片厚与直径。硬度: 3组分剂量片分别随机选取6片, 采用硬度仪进行测定。脆碎度: 3组分剂量片分别随机选取数片(使其质量为6.5 g), 精密称定其重量后, 将其放入脆碎度仪中, 以25 r·min−1转动4 min, 拿出片剂, 吹去表面粉末, 再次称重, 计算丢失的重量百分比。
药物含量检测与含量均匀度 按照中国药典(2015年版), WS片剂含量测定方法:分别取WS 1 mg和2 mg片剂各20片, 研细, 精密称取50 mg (约相当于WS 1 mg), 置于50 mL量瓶中, 检测WS含量; HCT片含量测定方法:取HCT 5 mg片剂20片, 研细, 精密称取100.00 mg (约相当于HCT 5 mg), 置于10 mL量瓶中, 检测HCT含量。以上实验均重复3次。
按照中国药典(2015年版)含量均匀度检测法(通则0941), 分别随机选取3D打印WS 1 mg、WS 2 mg、HCT 5 mg各10片, 测定单一药片以标示量为100的相对含量xi, 测其均值(X)、标准差(S)以及标示量与均值之差的绝对值(A), A = |100 − X|, 计算A + 2.2 S, 若A + 2.2 S≤15, 则供试品的含量均匀度符合规定。另用10片中剂量/质量RSD评估市售品粉末在打印浆料中的混匀程度。
体外溶出释放 按照中国药典(2015年版)溶出度与释放度测定法(通则0931第一法)进行测定。WS 1 mg和2 mg分剂量片分别随机选取6片, 以磷酸盐缓冲液(pH 6.8) 500 mL作为溶出介质, 转速为50 r·min−1, 45 min时, 吸取溶液约10 mL, 滤过, 按含量测定项下方法计算每片的溶出量, 应大于标示量的70%; HCT 5 mg分剂量片分别随机选取6片, 以0.1 mol·L−1盐酸溶液900 mL为溶出介质, 转速100 r·min−1, 于30 min测定HCT溶出量, 应大于标示量的60%。
分剂量片的稳定性 对3组分剂量片取同一批次样品, 分别在第2、4、9、13和28天取样, 按上述方法测定药片含量及溶出限, 评估片剂放置30天的稳定性。
打印参数、打印处方对分剂量片的影响 对WS 1 mg网孔片采用不同填充率(10%、20%、40%、60%、80%和100%)探索孔隙率对崩解时间的影响; 对WS 2 mg片用不同孔径(0.26、0.42、0.62和0.84 mm)的喷嘴探索喷嘴孔径对分剂量片的影响; 同时选用不同药用填充剂(玉米淀粉、微晶纤维素、蔗糖和乳糖)、不同乙醇比例的黏结剂(25%、45%、55%、65%、75%、85%和95%)来考察处方对可打印性及打印片物理化学性质的影响。
统计学方法 用Excel对数据结果进行t检验, 以P < 0.05表示有显著差异, P < 0.01表示有非常显著性差异。
结果与讨论 1 分剂量片的性质测定 1.1 分剂量片物理机械性质3D分剂量片网孔分明、表面光洁(图 2)。对3种分剂量片厚、直径、片重差异、硬度与脆碎度进行评估, 见表 3。所有片剂符合药典规定。

|
Figure 2 From left to right are WS 1 mg tablets, WS 2 mg tablets, HCT 5 mg tablets |
| Table 3 Physical and mechanical properties of three divided-dose tablets. Diameter (d), height (h) (n = 10, x ± s), weight (n = 20, x ± s), hardness (n = 6, x ± s) |
片厚及直径: 3种分剂量片直径均小于预设模型直径(WS 1 mg分别为7.93和8.00 mm; WS 2 mg为8.23和8.40 mm, HCT 5 mg为7.84和8.00 mm)。网孔片片厚小于模型片厚(WS 1 mg分别为1.94和2.00 mm), 而实心片片厚却大于模型片厚(WS 2 mg分别为2.30和2.20 mm, HCT 5 mg为2.89和2.80 mm)。这可能是由打印片各部分固化速度不同导致, 实心片外圈部分水分交换速度快, 干燥皱缩更快, 而中心内在部分与空气接触程度低, 固化速度较慢, 内外圈固化速度不同从而拉伸整片, 半径略微减小。而网孔片由于内部孔隙, 干燥均匀, 没有这种现象发生。提示对于浆状、熔融状打印浆料, 适当的填充率和缓慢的打印速度(给予足够的固化时间)可使打印片的片型更为规整。
片重差异: WS 1 mg、WS 2 mg、HCT 5 mg的重量差异分别为49.70 ± 1.56、98.74 ± 3.62和99.20 ± 2.89 mg, 符合中国药典(2015年版)对低于0.3 g药物片重差异的要求(± 7.5%)。在打印材料混匀的前提下, 片重直接反映药片的剂量。3D打印药片过程中, 影响片重差异的主要因素: ①目标模型与实际打印模型间的体积差(半层误差)。②一次性喷嘴孔径的精密度。③打印材料的稳定性(均匀程度与黏度等随外界环境的变化)。④ 3D打印机的打印模式及精密度。通过合理设计模型, 优化处方, 采用同一批次、同一喷嘴, 控制室温、湿度及料管的填充体积, 可以使打印质量更准确(± 10%内), 优于欧洲药典对磨粉分包的质量偏差标准(15%)。
硬度与脆碎度: 3种分剂量片的平均硬度均在20 N以上, 能够满足保存运输要求。3种分剂量片的脆碎度均在1%内, 符合中国药典(2015年版)对片剂脆碎度的要求。测量中发现HCT 5 mg片剂硬度最大, 而脆碎度也大于硬度最小的WS 1 mg片, 这不符合硬度小、脆碎度大的一般性常识, 可能的原因: ①打印处方不同。本研究将市售品混以稀释剂配成浆料运用3D打印技术再成型, 市售片处方组成也影响着成片性质。②为了避免过筛导致有效成分损耗及含药率的变化, 本研究未对市售品粉末经过筛处理, 这可能导致打印浆料配制过程中少数大颗粒组分水润不均匀、干燥后掉粒, 从而产生整体不影响硬度, 而脆碎度降低的情况。
1.2 含量测定取WS 1 mg、WS 2 mg、HCT 5 mg分剂量片各20片研碎, 取单片质量粉末测定含量, 重复3次, 含量分别为1.02 ± 0.03、1.96 ± 0.01和5.19 ± 0.06 mg, 药物含量均在± 5%内, 符合中国药典(2015年版)对药物含量要求(95%~105%), 提示药物在辅料及3D打印工艺中几无降解损耗。
1.3 含量均匀度取WS 1 mg、WS 2 mg、HCT 5 mg分剂量片各10片, 称定每片质量并测量相应药物含量, 其含量均匀度分别为1.0、5.3和2.6, 符合中国药典(2015年版)对含量均匀度的要求。这证明3D打印分剂量高重复性的特点, 确保同一批次中药物含量在较小的范围内波动, 达到精准治疗。打印WS分剂量片, 3D生物打印机的含量均匀度优于食品打印机, 提示不同3D打印机型影响打印片的相关性质。计算3组药片含药比例(剂量/质量)分别为(1.96 ± 0.03) %、(2.01 ± 0.02) %和(5.12 ± 0.10) %, 符合预设含药比例。含量均匀度RSD为1.7%、1.2%和1.9%均在合理范围内, 这反映了药物在稀释辅料中的混匀程度, 提示3D打印分剂量工艺能确保药物在辅料中均匀分散。
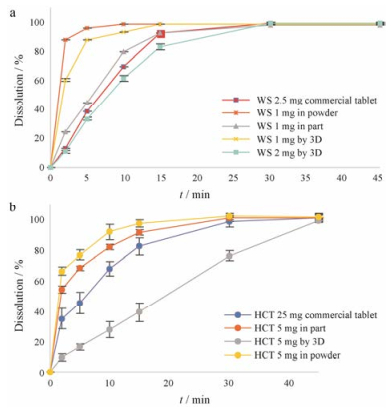
1.4 体外药物释放在45、45和30 min分别测定WS 1 mg、WS 2 mg和HCT 5 mg药物释放含量, 分别为(99.3 ± 1.2) %、(101.5 ± 0.3) %和(98.1 ± 0.8) %, 符合2015年版药典70%、70%和60%的溶出限规定。以临床常用分剂量片(药物磨粉、掰分片)及市售片体外溶出曲线与3D打印分剂量片进行对比(图 3a, b), 均能满足药典溶出要求, 但释放曲线有所差别。两种药物的磨粉释药速率最快, 2 min内药物释放分别达到88.1% (WS)和66.1% (HCT); 掰分片的释药速率与市售片最为接近; 3D分剂量片网孔结构的WS 1 mg片释药迅速, 5 min释药达87.7%, 实心片WS 2 mg释药仅33.4%, 提示网孔结构可加快药物溶出, WS 2 mg释放速率整体与市售片较为接近, 而HCT 5 mg释放速率较市售片明显偏慢(30 min释药76.1%, 市售片已完全释放), 两者均为实心片, 释药速率不同可能与市售粉末不同稀释倍数有关, HCT市售片较WS具有更高的含药比例, 打印低剂量分剂量片时需加入大量的稀释剂以满足体积、剂量准确性等要求。WS浆料中稀释辅料占比38.6%, 而HCT中占比86.8% (表 1)。大量的稀释剂及黏结剂使HCT各组分黏性加强, 因此崩解溶出偏慢。这提示运用3D打印技术制备低剂量分剂量片, 含药比例低的药品更适合制成实心片、含药比例高的药品制成网孔片以更接近市售品的释放性质, 并可通过网孔设置和处方配比来控制药物释放速率, 达到个体化治疗的效果。
|
Figure 3 In vitro dissolution profiles of various WS sub-doses, commercially available tablets (a) and HCT sub-doses and commercially available tablets (b). n = 6, x ± s |
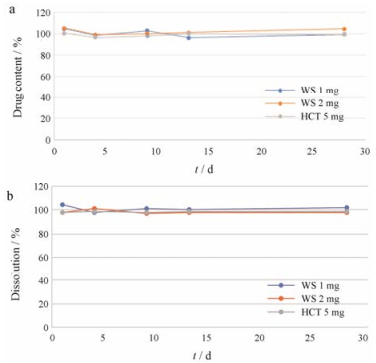
针对医院具体情况, 作者考察了30天内分剂量片的稳定性, 结果如图 4a, b。30天内3种3D打印片含量基本保持在95%~105%之间、溶出限均在95%以上, 符合国家药典规定。
|
Figure 4 The content stability (a) and dissolution limitation stability (b) of 3D-divided-dose tablet. n = 6 |
选用不同孔径喷嘴制备一定模型的WS分剂量片(表 4), 结果表明, 小孔径喷嘴能降低打印质量的波动程度。一方面由于小孔径喷嘴在机械误差中(如挤出压力波动)受影响较小; 另一方面由于小孔径喷嘴对应的打印速度低, 3D打印机在移动打印轴时更平缓, 移动震幅越小, 打印精度越高。同时打印速度低也能给予材料足够的固化时间, 提高打印精度, 但也增加打印所需时间。这提示小孔径喷嘴及低打印速度能在降低一定制备效率的前提下提高同一批次分剂量片的质量。0.84 mm喷嘴制备的片剂崩解时限较其他孔径喷嘴显著偏低(P < 0.01), 这可能与3D打印独特的丝状堆积结构有关。
| Table 4 Effect of nozzle size on tablet properties. n = 6, x ± s. **P < 0.01 vs 0.26 or 0.42 or 0.62 mm |
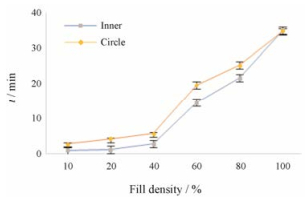
填充密度对WS 1 mg网孔片的崩解也有显著影响, 见图 5。在崩解实验中, 内圈很快崩解, 外圈则需要一段时间才能透过筛网。这是由于内外圈不同的堆积模式、不同的溶剂接触面积造成的。填充率在40%以下时, 孔隙率变化对崩解时长影响较小, WS 1 mg网孔片较快崩解(6 min内); 填充率大于60%时, 孔隙率变化对崩解时长有着更强的影响。这可能是填充率在40%以下片剂孔隙较大, 溶剂能充分浸润内圈, 整片崩解较快。当填充率加大到60%后, 溶剂无法迅速穿透孔隙浸润药片, 这与Sadia等[13]研究结果相吻合, 提示可通过填充密度来控制分剂量片的崩解释放性能。
|
Figure 5 Effect of fill density on the disintegration time. Radius 2.5 mm, height 2 mm, nozzle size 0.26 mm. n = 6, x ± s |
制备低剂量药片时, 为提高剂量精度, 同时为了增大药片体积, 3D打印分剂量片需加入适量填充剂稀释市售片含药比例。采用的稀释剂有玉米淀粉、微晶纤维素、乳糖、蔗糖和糊精。除玉米淀粉外, 其余4种稀释剂均对片剂硬度有明显改善。乳糖与蔗糖能提供矫味效果, 分剂量片表面美观、有光泽, 患者服药体验佳, 但易吸湿, 粒径偏大易堵喷嘴, 打印合格率低, 药品损耗大。玉米淀粉、微晶纤维素、糊精单加与市售片粉末混合打印成片易裂。通过正交试验, 以浆料可打印性、成片外观、硬度和稳定性等作为考察指标, 最终选择玉米淀粉/微晶纤维素= 7:6作为稀释剂, 此空白处方黏性适中, 出丝均匀细腻, 挤出后能快速固化; 成片洁白有光泽, 硬度合格, 放置不裂片。玉米淀粉具有如下特点:一定黏性、粒径小、成浆后均匀包覆黏结其他组分和出丝滑腻, 适合3D打印糊状浆料需求; 具有一定的崩解效果, 加快药物崩解溶出; 天然高分子材料, 服用安全, 价格经济实惠。为达到适宜黏度, 加入适量羟丙基甲基纤维素(hydroxypropyl methylcellulose, HPMC)作为黏合剂。HPMC中的羟基与醚键和水缔合形成氢键, 发生水化作用, 达到保水匀质的效果。HPMC颗粒均匀有效分散, 包裹所有固态微粒, 在表面形成润湿膜。一方面在不断的搅拌过程中使物料具有黏性, 并使各组分均匀细致; 另一方面覆盖在浆料表面, 使浆料顺滑, 减少堵喷嘴情况发生。选用的HPMC型号为E30, 在药剂学上一般用作黏结剂。
打印浆料的黏性对可打印性、成片性质有关, 但由于黏性太强、测量过程中极快固化, 鲜有打印浆料黏性的测定研究报道。本实验在一定挤出压力下, 以10 s内挤出浆料质量来评估浆料的黏性。图 6所示为不同含水比例乙醇在不同压力下10 s挤出质量。随着乙醇中水比例增加, 10 s内相同压力挤出的浆料质量减小。25%乙醇在相同压力下挤出浆料质量最低, 这是由于水分增加, 水化作用加强, 黏性增强, 导致浆料难以挤出。85%乙醇黏性最低, 一定压力下挤出质量最大。95%乙醇中水成分太少, 难以形成足够的HPMC水凝胶将各组分包裹匀质, 导致无法成浆, 不能均匀挤出, 故未能采集有效数据。因此选择75%乙醇作为润湿剂。乙醇−水比例适中, 较高的乙醇比例加快打印片固化速度, 一定的含水量与HPMC形成水凝胶成浆。作者也试过用糊精等辅料作为黏结剂, 但黏度无法满足要求。煮浆法将糊精糊化形成淀粉浆, 黏性可满足要求, 但所成片烘干后有裂片现象。这是由于糊精糊化后体积膨胀数倍, 干燥老化后丢失太多水分导致片型皱缩裂片。对打印浆料黏度的控制应以装入料筒后手推可挤出、直立浆料不见明显滴落为准, 这样既能保证挤出参数具有足够的调试空间, 又能避免打印中因为重力引起的滴落误差。

|
Figure 6 The mass of filaments extruded at different concentrations of ethanol at different pressures. n = 6 |
本课题组运用3D打印技术对市售品华法林钠片、氢氯噻嗪片进行分剂量操作, 3种分剂量片含药量、溶出限及物理机械性质均符合药典规定, 两种不同的打印器械均可满足分剂量片的要求。在儿童专用药如此缺乏、传统分剂量方法有待改进的情况下, 3D打印技术不失为一种优良的分剂量方法。
| [1] | Arnet I, Hersberger KE. Misleading score-lines on tablets:facilitated intake or fractional dosing?[J]. Swiss Med Weekly, 2010, 140: 105–110. |
| [2] | Liu YJ, Liao JW, Chen JY, et al. Reasons, problems and countermeasures of tablet dosages[J]. Chin J Hosp Pharm (中国医院药学杂志), 2011, 31: 692–695. |
| [3] | Lin Y. Investigation on the Accuracy of Tablet Dosage and Its Influence on Children's Medication Safety (药片分剂量准确性考察及对儿童用药安全的影响)[D]. Hangzhou: Zhejiang University, 2014. |
| [4] | Huang SY, Shi F, Li H, et al. Investigation of the use of high-risk tablets for oral administration in hospitals in a children's hospital in Shanghai[J]. China Pharm (中国药师), 2018, 21: 257–260. |
| [5] | Zhang HX, You J. 3D printing of aspirin immediate-release dual-layer tablets[J]. Chin Pharm J (中国药学杂志), 2017, 52: 298–302. |
| [6] | Li QJ, Wen HY, Jia DY, et al. Preparation and investigation of controlled-release glipizide noveloral device with three-dimensional printing[J]. Int J Pharm, 2017, 525: 5–11. DOI:10.1016/j.ijpharm.2017.03.066 |
| [7] | Li QJ, Guan XY, Cui MS, et al. Preparation and investigation of novel gastro-floating tablets with 3D extrusion-based printing[J]. Int J Pharm, 2018, 535: 325–332. DOI:10.1016/j.ijpharm.2017.10.037 |
| [8] | Chen XY, Peng Q, Hu DQ, et al. Correlation of CYP2C9 and VKORCl polymorphisms with warfarin steady stable dose and computer model-predicted dose[J]. Acta Med Univ Sci Technol Huazhong (华中科技大学学报医学版), 2015, 44: 92–95. |
| [9] | Hu J, Zhu JR, Yu F. Meta-analysis of safety and efficacy of warfarin dose prediction formulae for clinical use[J]. Chin J Clin Pharm Ther (中国临床药理学与治疗学), 2015, 20: 296–303. |
| [10] | Wei Y, Sun YY, Wang KS, et al. Pharmacokinetics of the combined preparation of lisinopril and hydrochlorothiazide on Chinese healthy volunteers[J]. Acta Pharm Sin (药学学报), 2011, 46: 955–961. |
| [11] | Skowyra J, Pietrzak K, Alhnan MA. Fabrication of extended-release patient-tailored prednisolone tablets via fused deposition modelling (FDM) 3D printing[J]. Eur J Pharm Sci, 2015, 68: 11–17. DOI:10.1016/j.ejps.2014.11.009 |
| [12] | Pietrzak K, Isreb A, Alhnan MA. A flexible-dose dispenser for immediate and extended release 3D printed tablets[J]. Eur J Pharm Biopharm, 2015, 96: 380–387. DOI:10.1016/j.ejpb.2015.07.027 |
| [13] | Sadia M, Arafat B, Ahmed W, et al. Channelled tablets:an innovative approach to accelerating drug release from 3D printed tablets[J]. J Control Release, 2018, 269: 355–363. DOI:10.1016/j.jconrel.2017.11.022 |
 2018, Vol. 53
2018, Vol. 53


