2. 天津药物研究院中药现代研究部, 天津 300193
2. Department of Modern Chinese Medicine, Tianjin Pharmaceutical Research Institute, Tianjin 300193, China
连翘为“疮家圣药”, 归心经, 肺经, 具有清热解毒、疏散风热、消肿散结等多种功效, 在临床上运用广泛。中医本着“寒者热之, 热者寒之”的治则, 选用味苦性寒凉之品来治疗热证, 连翘作为清热解毒的中药常被使用。而现代药理学研究发现, 连翘主要的临床作用与其抗炎药理活性有一定的相关性[1]。炎症是指具有血管系统的活体组织对损伤因子所做出的防御反应, 对应至中医上则为阳证、热证、火证。目前连翘的研究多集中在单一化学成分及其药理作用的解析, 中医理论指导下的清热解毒功效的物质基础及分子作用机制方面的研究相对匮乏[2-4]。
中药是多成分组合体, 其分子机制相对复杂, 难以深入研究。网络药理学是基于系统生物学的理论, 对生物系统的网络分析, 广泛运用于从分子网络角度阐明中药的分子机制[2]。本课题组长期运用网络药理学研究方法尝试解析中药及其复方的分子作用机制[5-8], 积累了一定的研究技术和方法。本研究以连翘清热解毒功效为切入点, 通过对连翘化学成分、靶点、对应疾病的数据挖掘, 进而构建成分-靶点-疾病网络图、并运用分子对接进行初步验证, 以期从分子层面系统阐明连翘发挥清热解毒功效的分子机制。本文在中医理论指导下, 结合现代分子生物学理论, 尝试从新的角度阐释中药功效的科学内涵, 为阐明中药功效提供思路和方法。
材料与方法小分子数据库的构建 搜集TCMSP[9]、TCMID[8]数据库中连翘化学成分, 结合CNKI、GCBI数据库中已报道的连翘相关文献, 构建连翘成分数据库。其次, 按照OB≥30%、DL≥0.18[9]为条件进行初步筛选, 通过PubChem数据库下载上述化学成分的结构, 数据库中未收录结构的成分, 利用ChemBioDraw Ultra 14.0软件进行绘制, 构建小分子数据库。
靶点预测及靶点富集分析 将上述小分子以mol2的格式导入Pharmmapper[8]在线分析平台, 参数设置如下: Select Targets Set选择Human Protein Targets Only (v2010, 2241), 其余参数均为默认设置。将所有靶点分别导入mas3.0、DAVID数据库进行靶点富集分析。并将筛选所得的疾病依次输入MeSH数据库, 点击Search, 记录Tree Number(s), 再点击Tree View, 对照Tree Number, 记录每个疾病的每一级名称, 将其进行分类。
网络图构建 将上述步骤构建的小分子数据库中的化合物与对应靶点、疾病之间的对应关系, 保存为xlsx格式文件, 导入Cytoscape 3.4.0软件中进行网络构建, 分别用不同颜色、不同形状的节点来区分成分、所对应的靶点和疾病。
器官定位 通过BioGps数据库对靶点进行器官定位分析, 将所有靶点输入至搜索框, 点击Search, 然后对各靶点的信息进行统计, 得出不同器官所对应的靶点种类及数目, 最后对结果进行整理, 并绘图表示。
分子对接 为验证炎症靶点蛋白与其所对应活性成分之间的结合活性, 运用SYBYL-X 2.0软件将上述得到的靶点蛋白与其相关成分进行对接, 再对其对接结果进行分析。
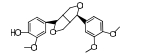
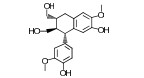
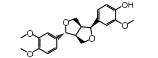
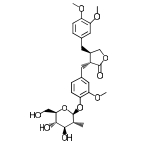
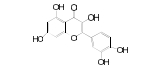
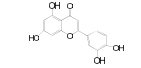
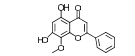
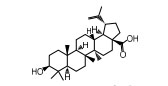
结果与讨论 1 揭示连翘中主要活性成分及作用靶点本研究共收集连翘中化学成分1, 以OB≥30%、DL≥0.18为条件进行筛选, 得到化合物15个(表 1)[10-21]。所得连翘活性成分共含有5种化合物类型, 分别为木脂素及其苷类(5个)、黄酮类(4个)、三萜类(4个)、C6~C2天然醇及其苷类(1个)、甾体类(1个), 其中黄酮类、三萜类、木脂素及其苷类为3种主要的类型。
| Table 1 Detail information of 15 compounds |
再将筛选得到的15个化学成分通过PharmMapper数据库对靶点进行预测分析, 得到相关靶点26个(表 2)。
| Table 2 Information of related targets |
对数据进行分析可以发现:每个成分均对应3个及以上靶点, 其中, 最少的为β-谷甾醇(β-sitosterol), 只对应3个靶点, 最多的为汉黄芩素(wogonin), 对应14个靶点。同时, 靶点CYP2C9对应于化合物C2、C3、C5、C6、C7、C8、C9、C10、C11、C12、C13、C14多个成分; 靶点NOS3对应于化合物C3、C5、C6、C8、C10、C11、C13、C14、C15多个成分。由此可知, 连翘的活性成分与其所对应的靶点之间存在一个成分对应多个靶点、一个靶点对应多个成分的关系, 即“多成分-多靶点”协同发挥作用。
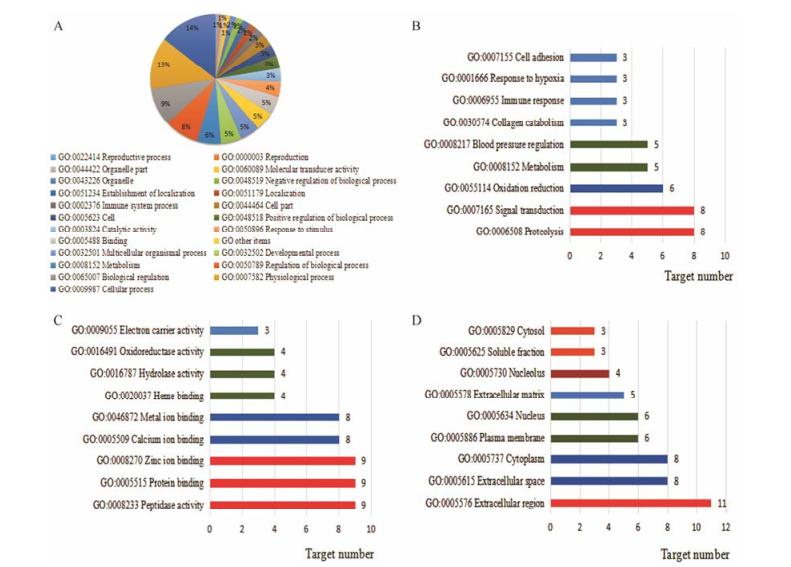
2 靶点富集分析及疾病分类为阐明所得靶点的生物学活性, 将靶点导入MAS 3.0数据库进行GO分析[22], 结果如图 1所示。
|
Figure 1 GO analysis results. A: GO mapping; B: Biological process; C: Molecular function; D: Cellular component |
由图 1A可知, 13%靶点参与了细胞过程和生理过程, 9%靶点参与生物调节过程, 8%靶点参与生物过程调控; 由图 1B得知, 靶点参与蛋白质水解、信号转导、氧化还原作用等生物进程; 由图 1C可知, 靶点涉及肽酶活性、蛋白质结合、锌离子结合、钙离子结合和重金属离子结合等分子功能; 由图 1D可知, 靶点在胞外区、细胞外间隙、细胞核和细胞质中均有分布。由此, 可以得出连翘行使其清热解毒功效参与了多种生物学进程。为了更加明确连翘清热解毒功效发挥的分子机制及其所对应的药理作用, 本研究将所得的26个靶点导入DAVID数据库, 其结果见图 2。

|
Figure 2 Target enrichment analysis results. Each spoke represents the name of the disease enriched by the target, and the length of the spoke is proportional to the number of targets corresponding to the disease |
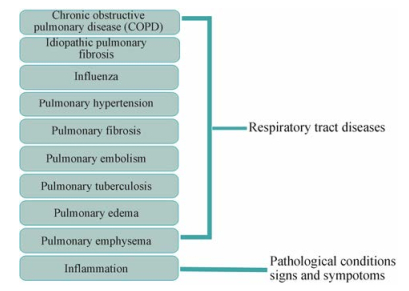
图中橙黄色部分表示为靶点数目, 雷达图最外侧部分为靶点富集所得的不同类型的疾病。筛选所得26个靶点中, 13个与慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)有关, 8个与炎症有关, 7个与肺结核、肺纤维化有关, 6个与肺动脉高压有关, 3个与特发性肺纤维化、肺气肿有关, 2个与肺栓塞有关, 1个与流感、肺水肿有关。将所对应的疾病依次输入MeSH数据库, 共得到10个二级分类, 2个一级分类:呼吸道疾病和病理状况两种(图 3)。
|
Figure 3 Disease classification results |
26个靶点所对应的疾病中, 有9种疾病属于呼吸道疾病, 包括: COPD、特发性肺纤维化(idiopathic pulmonary fibrosis)、流感(influenza)、肺动脉高压(pulmonary hypertension)、肺纤维化(pulmonary fibrosis)、肺栓塞(pulmonary embolism)、肺结核(pulmonary tuberculosis)、肺水肿(pulmonary edema)、肺气肿(pulmonary emphysema); 1种属于病理状况、体征和症状为:炎症(inflammation)。
呼吸道疾病与炎症反应之间有着不可分割的联系[23]。慢性气道炎症是COPD的发病机制, COPD为多种炎症因子参与介导的系统性炎症性疾病; 而且COPD形成过程中可能伴随着肺气肿, 可能进一步发展为肺动脉高压, 在肺动脉高压的形成过程中, 气道炎症和肺血管炎症起着很重要的作用[24]; 肺纤维化病理早期以下呼吸道急性炎症反应为主; 肺栓塞的发生发展期间往往伴随着氧化应激、血管内皮细胞损伤等炎症反应的发生[25]; 特发性肺纤维化、肺结核、肺水肿的发生也离不开炎症反应[26]; 流感发生时, 伴随着产生大量的趋化因子和促炎细胞因子, 这些因子往往聚集于某些部位, 从而导致该部位发生病变、感染和损伤[27, 28]。综上所述, 呼吸道疾病的发生往往伴随着炎症, 而且长期炎症反应也会导致呼吸系统疾病。本研究从靶点与疾病相关性角度验证了连翘发挥其清热解毒的功效是通过抗炎的药理作用, 而其治疗的主要疾病为呼吸道系统疾病, 这一研究结果与连翘的临床功效和使用相符。
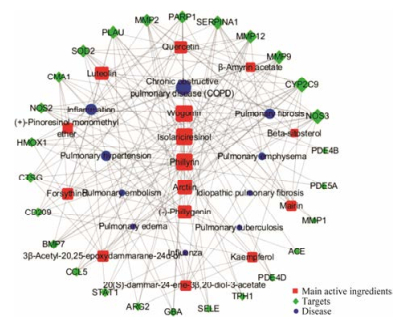
3 成分-靶点-疾病网络图利用Cytoscape软件构建了连翘成分-靶点-疾病网络图(图 4), 图中最外一圈绿色的菱形表示这些活性成分所对应的26个靶点, 中间橙色的方框为连翘所含的15个活性成分, 蓝色的圆圈表示这些成分所治疗的10种疾病。
|
Figure 4 Components-targets-disease network of Forsythia suspensa |
利用Network Aalyzer插件对网络的拓扑结构进行分析:有8个靶点与炎症相关, 分别为NOS2、NOS3、MMP2、MMP9、CMA1、STAT1、PARP1、HMOX1。其中, NOS为NO合成酶, 连翘通过下调iNOS蛋白表达, 即抑制NOS2或者NOS3抑制炎症介质NO而发挥抗炎作用[29]; MMPs在涉及炎症的生理情况和病理状况中表达, MMP2参与各种生理和病理过程, 包括血管生成、组织修复和炎症, MMP9的增加与炎症细胞对坏死组织的侵袭相关, 而且, 其表达活性的增加在数量上和质量上与炎症的不同阶段相关[30-32]; CMA1与STAT1均与炎症相关; PARP1与炎症抑制有关, 在诱导炎性应激时, PARP1在介导NF-κB依赖性基因转录中发挥重要作用[33]; HMOX1在组织中的表达升高通常与增加炎症或氧化应激相关[34]。
这些靶点所对应的活性成分中汉黄芩素在整个网络模型中重要程度最高, 研究表明, 汉黄芩素的抗炎活性显著, 同时有文献[35]报道其具有抗病毒、抗肿瘤、抗氧化以及神经保护等药理作用; 连翘苷具有抗菌、保肝、抗病毒、抗炎等药理作用[36]。从靶点与成分对应关系分析说明连翘发挥清热解毒的功效是建立在其抗炎的药理作用基础之上。
4 器官定位分析与归经理论的相关性分析中医理论认为人体是一个整体, 心、肝、脾、肺、肾五脏协同作用, 共同维持机体正常运行。治病的方式为调节多个器官达到一种平和的状态, 为明确连翘发挥功效与器官之间的关系, 本研究将所有靶点导入BioGPS数据库中进行器官定位, 结果见图 5。由图可见, 不同的颜色表示不同的器官, 各器官类型见中心部分小图标指示, 分别为心、肝、肺、肾及其他器官, 不同颜色的小方框表示对应不同的器官; 有21个靶点作用于肺, 7个靶点作用于心, 5个靶点作用于肝, 3个作用于肾, 4个作用于其他器官。此外, 对应至心上的7个靶点在肺上均有分布。这印证了中医理论中的整体观, 即人体为一个统一的、互相关联的整体, 内部之间各个脏器互相联系, 互相影响。其中, 肺与心表现为气与血之间相互依存和互根互用的关系, 靶点间互相联系, 互相作用。

|
Figure 5 Organ positioning results. The small central icon of each figure is represented by the type of each organ, and the small squares are represented as different targets corresponding to the organs, and the different colors represent different organs |
结合上图器官定位的结果, 定位至肺的数量最多(81%), 心次之(27%)。从中医角度讲, 连翘归肺、心、小肠经。其中, 肺与心表现为气与血之间相互依存和互根互用的关系。气为血之帅, 血为气之母。肺主气, 肺气的推动作用能够促进、辅助心脏推动血液运行, 从而保证心血正常运行。心主血脉, 心气的推动作用, 运载清浊之气, 肺才能有效呼吸从而主气[37]。该研究结果与中医理论相符, 初步阐明了中药的归经理论。
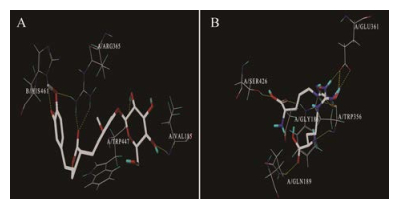
5 分子对接验证为明确炎症靶点蛋白与所对应的成分之间的结合活性, 本研究选取常见炎症因子与部分活性化合物进行分子对接分析。利用SYBYL-X 2.0软件[38]通过分子对接和阳性对照过程进行验证, 对接过程中部分示意图见图 6, 对接得分结果见表 3、表 4。
|
Figure 6 Molecular docking schematic. A: Docking results of C13 and NOS3; B: Docking results of NOS3 and ligand HAR |
| Table 3 Docking results of the partial active compound with inflammation targets |
| Table 4 Target protein docking results with ligands |
图 6所示分子对接的结果, 由于C13化合物与NOS3有4个结合位点, 故对接所得分数最高。表 3的小分子与靶点蛋白的对接得分, 表 4的靶点蛋白与相应的配体对接得分(阳性对照)显示, 炎症靶点蛋白与相应的活性成分具有一定的结合活性, 根据Li等[39]的研究发现, 对接得分在4.25以上认为分子与靶点有一定的结合活性, 大于5.0说明有较好结合活性, 大于7.0说明具有强烈的结合活性。而且, 阳性对照的对接得分均低于小分子与靶点蛋白的对接得分。由此可以推测, 连翘是通过特定的活性成分作用于炎症靶点蛋白发挥其抗炎的药理作用, 从而发挥清热解毒的功效。
具有清热解毒功效的中药众多, 临床应用广泛。连翘作为清热解毒的常用中药, 其药理研究虽多, 但是针对其中药功效的研究并不多见。本研究使用网络药理学的方法, 运用化合物分子的筛选、靶点的预测、靶点富集分析、疾病分类、构建C-T-D网络图和器官定位来探究连翘清热解毒的物质基础及分子机制。研究得到连翘15个活性成分中, 5个木脂素及其苷类化合物、4个黄酮类化合物、4个三萜类化合物、C6~C2天然醇及其苷类、甾体类化合物各1个; 预测共得到26个靶点, 每一个活性成分均对应于多个靶点(3个以上)。其中, 最少的为1个成分对应3个靶点, 最多的为1个成分对应14个靶点, 进一步证实了连翘通过“多成分-多靶点”的机制发挥其清热解毒的功效; 靶点富集分析发现, 所得靶点中有13个与慢性阻塞性肺病有关, 8个与炎症有关, 7个与肺结核、肺纤维化有关, 6个与肺动脉高压有关; 疾病归类结果显示其中呼吸道相关的疾病最多, 而呼吸道疾病的发生往往与炎症有一定联系; 器官定位得到, 连翘有21个靶点作用于肺, 7个靶点作用于心, 从分子角度初步证明连翘的归心、肺经的物质基础; 并进一步用分子对接验证了炎症靶点蛋白与连翘相关活性成分的结合能力。综上所述, 本研究通过网络药理学的研究方法, 将中医理论与现代学研究紧密结合初步阐明了连翘清热解毒功效的科学内涵, 为连翘的临床合理用药提供理论基础。
通过网络图的构建发现, 连翘可能通过作用于靶点NOS2和NOS3, 从而抑制一氧化氮(NO)的影响。Miao等[40]同样阐明了连翘等清热解毒类中药的抗炎机制涉及到对NO的调节。连翘还可能调控MMPs (包括MMP2和MMP9)在涉及炎症的生理情况和病理状况中的表达等多种途径来发挥清热解毒功效的抗炎机制, 这与Robert等[31]的研究相一致。本文只采用了网络药理学的方法对连翘进行了相关研究, 但并未进一步深入探讨生物学实验, 需要进一步的研究, 更深层次阐明连翘清热解毒的治疗机制。
| [1] | Guo Y, Lin L, Wang Y. Chemistry and pharmacology of the herb pair Flos Lonicerae japonicae-Forsythiae fructus[J]. Chin Med, 2015, 10: 16. DOI:10.1186/s13020-015-0044-y |
| [2] | Yan XJ, Wen J, Xiang Z, et al. Chemical constituents from fruits of Forsythia suspense[J]. Chin Tradit Herbal Drugs (中草药), 2017, 48: 644–647. |
| [3] | Quan YY, Yuan A, Gong XH, et al. Basic screening study on anti-inflammatory pharmacodynamics of Forsythia[J]. Nat Prod Res Dev (天然产物研究与开发), 2017, 29: 435–438, 471. |
| [4] | Luo L, Yuan A, Dang J, et al. Study on antipyretic and anti-inflammatory effects of volatile oil of Forsythia suspensa L. by different rat models[J]. Nat Prod Res Dev (天然产物研究与开发), 2018, 30: 207–211, 256. |
| [5] | Shen X, Zhao Z, Luo X, et al. Systems pharmacology based study of the molecular mechanism of SiNiSan formula for application in nervous and mental diseases[J]. Evid Based Complement Alternat Med, 2016, 2016: 9146378. |
| [6] | Shen X, Zhao Z, Wang H, et al. Elucidation of the anti- inflammatory mechanisms of Bupleuri and Scutellariae Radix using system pharmacological analyses[J]. Mediators Inflamm, 2017, 2017: 3709874. |
| [7] | Wang H, Zhao ZY, Ma H, et al. Material basis of Acori Tatarinowii Rhizoma for Alzheimer's disease[J]. Center South Pharm (中南药学), 2017, 15: 933–936. |
| [8] | Wang H, Zhao ZY, Shen X, et al. Systemic pharmacology- based study on mechanism of Polygala Radix in the treatment of Alzheimer's disease[J]. Acta Pharm Sin (药学学报), 2017, 52: 1554–1561. |
| [9] | Ru JL. Construction and Utilization of Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform (中药系统药理学数据库和分析平台的构建和应用)[D]. Yangling: Northwest A & F University (西北农林科技大学), 2015. http://cdmd.cnki.com.cn/Article/CDMD-10712-1015332723.htm |
| [10] | Xia YG, Yang BY, Liang J, et al. Optimization of simultaneous ultrasonic-assisted extraction of water-soluble and fat-soluble characteristic constituents from Forsythiae Fructus using response surface methodology and high-performance liquid chromatography[J]. Pharmacogn Mag, 2014, 10: 292–303. DOI:10.4103/0973-1296.137370 |
| [11] | Xiao HB, Sui GG, Lu XY. Phillyrin lowers body weight in obese mice via the modulation of PPAR/-ANGPTL 4 pathway[J]. Obes Res Clin Pract, 2018, 12: 71–79. DOI:10.1016/j.orcp.2017.02.002 |
| [12] | Liang J, Gong FQ, Sun HM. Simultaneous separation of eight lignans in Forsythia suspensa by β-cyclodextrin-modified capillary zone electrophoresis[J]. Molecules, 2018, 23: 514. DOI:10.3390/molecules23030514 |
| [13] | Yan XJ. Chemical constituents and pharmacological activities of Forsythia Suspensa (Thunb.) Vahl[C] // The 5th National Commodity Commodity Academic Conference of China Commodity Society (中国商品学会第五届全国中药商品学术大会论文集). Harbin: Chinese Commodity Society (中国商品学会), 2017: 23. |
| [14] | Qin K, Liu Q, Cai H, et al. Chemical analysis of raw and processed Fructus arctii by high-performance liquid chromatography/diode array detection-electrospray ionization-mass spectrometry[J]. Pharmacogn Mag, 2014, 10: 541. DOI:10.4103/0973-1296.141806 |
| [15] | Ventura SP, Fa ES, Quental MV, et al. Ionic-liquid-mediated extraction and separation processes for bioactive compounds: past, present, and future trends[J]. Chem Rev, 2017, 117: 6984. DOI:10.1021/acs.chemrev.6b00550 |
| [16] | Powers CN, Setzer WN. A molecular docking study of phytochemical estrogen mimics from dietary herbal supplements[J]. Silico Pharmacol, 2015, 3: 4. DOI:10.1186/s40203-015-0008-z |
| [17] | Kim HP, Lim H, Yong SK. Therapeutic potential of medicinal plants and their constituents on lung inflammatory disorders[J]. Bio Ther, 2017, 25: 91–104. DOI:10.4062/biomolther.2016.187 |
| [18] | Wu X, Liu P, Zhang H, et al. Wogonin as a targeted therapeutic agent for EBV+ lymphoma cells involved in LMP1/ NF-κB/miR-155/PU[J]. BMC Cancer, 2017, 17: 147. DOI:10.1186/s12885-017-3145-4 |
| [19] | Shih-Hsiang L, Cheng KC, Li YX, et al. Development of betulinic acid as an agonist of TGR5 receptor using a new in vitro assay[J]. Drug Des Dev Ther, 2016, 10: 2669–2676. DOI:10.2147/DDDT |
| [20] | Kuo PC, Chen GF, Yang ML, et al. Chemical constituents from the fruits of Forsythia suspensa and their antimicrobial activity[J]. Biomed Res Int, 2014, 2014: 304830. |
| [21] | Xing SH. The Study on Effective Substances of Scutelariae Radix and Forsythia Fructus Based on Gastrointestinal Metabolism (基于胃肠道代谢的黄芩、连翘药效物质基础研究)[D]. Shanghai: Shanghai Jiaotong University (上海交通大学), 2015. http://cdmd.cnki.com.cn/Article/CDMD-10248-1016787612.htm |
| [22] | Wu D, Gao Y, Xiang H, et al. Exploration into mechanism of antidepressant of Bupleuri radix based on network pharmacology[J]. Acta Pharm Sin (药学学报), 2018, 53: 210–219. |
| [23] | Wu BF, Su HM, Shang JH, et al. A summary review of the establishment of animal models of emphysema and the relevant research progress[J]. J Yunnan Univ Nat (Nat Sci)[云南民族大学学报(自然科学版)], 2018, 27: 108–112. |
| [24] | Li XY. Chronic obstructive pulmonary disease related pulmonary hypertension and inflammatory response[J]. J Clin Pulm Med (临床肺科杂志), 2014, 19: 900–902. |
| [25] | Zhou HH. The Relationship between Inflammation Biomarkers and CT Pulmonary Artery Obstruction Index in Patients with Pulmonary Embolism (肺栓塞患者炎症指标与CT肺动脉阻塞指数的关系)[D]. Nanning: Guangxi Medical University (广西医科大学), 2017. http://cdmd.cnki.com.cn/Article/CDMD-10598-1017205435.htm |
| [26] | Arora VK, Chopra KK. Inflammation plays a central role in respiratory diseases, including tuberculosis[J]. Indian J Tuberc, 2018, 65: 103–105. DOI:10.1016/j.ijtb.2018.03.001 |
| [27] | Wang XB, Jiang S, Wang S, et al. Progress in animal models of pulmonary edema[J]. Pharm J Chin PLA (解放军药学学报), 2013, 29: 69–71, 74. |
| [28] | Zeng LJ. The Study of Lian Hua Qing Wen Capsule Components against Influenza Virus on Pharmacological Characteristics (连花清瘟胶囊拆方抗流感病毒药理机制研究)[D]. Guangzhou: Guangzhou University of Chinese Medicine (广州中医药大学), 2016. http://cdmd.cnki.com.cn/Article/CDMD-10572-1016276968.htm |
| [29] | Saleh A, Stathopoulou MG, Dadé S, et al. Angiogenesis related genes NOS3, CD14, MMP3 and IL4R are associated to VEGF gene expression and circulating levels in healthy adults[J]. BMC Med Genet, 2015, 16: 90. |
| [30] | Kapoor C, Vaidya S, Wadhwan V, et al. Seesaw of matrix metalloproteinases (MMPs)[J]. J Cancer Res Ther, 2016, 12: 28. DOI:10.4103/0973-1482.157337 |
| [31] | Robert S, Gicquel T, Victoni T, et al. Involvement of matrix metalloproteinases (MMPs) and inflammasome pathway in molecular mechanisms of fibrosis[J]. Biosci Rep, 2016, 36: e00360. DOI:10.1042/BSR20160107 |
| [32] | Ning C, Min H, Khalil RA. Biochemical and biological attributes of matrix metalloproteinases[J]. Prog Mol Biol Transl Sci, 2017, 147: 1. DOI:10.1016/bs.pmbts.2017.02.005 |
| [33] | Feng FY, de Bono JS, Rubin MA, et al. Chromatin to clinic: the molecular rationale for PARP1 inhibitor function[J]. Mol Cell, 2015, 58: 925–934. DOI:10.1016/j.molcel.2015.04.016 |
| [34] | Ryter SW, Choi AMK. Targeting heme oxygenase-1/carbon monoxide for therapeutic modulation of inflammation[J]. Transl Res, 2016, 167: 7–34. DOI:10.1016/j.trsl.2015.06.011 |
| [35] | Khan NM, Ahmad I, Ansari MY, et al. Wogonin, a natural flavonoid, intercalates with genomic DNA and exhibits protective effects in IL-1β stimulated osteoarthritis chondrocytes[J]. Chem Biol Interact, 2017, 274: 13–23. DOI:10.1016/j.cbi.2017.06.025 |
| [36] | Wei JB, Yang GY, Chen H, et al. Recent advances in extraction methods, pharmacology, toxicology and pharmacokinetics studies of phillyrin[J]. China Pharm (中国药师), 2015, 18: 2144–2148. |
| [37] | Peng B, Wang L, Wang ZX, et al. Pulmonary heart treated with chronic obstructive pulmonary disease with pulmonary hypertension[J]. Hebei J Tradit Chin Med (河北中医), 2018, 40: 453–455. |
| [38] | Lin ZF, Huang XA, Xu PP, et al. Study on the inhibitor of Reduning Injection on the HRV 3C protease based on virtual screening[J]. Pharmacol Clin Chin Med (中药药理与临床), 2017, 33: 142–146. |
| [39] | Li J, Gao L, Gao Y, et al. Exploration in targets action of antitussive and expectorant bioactive components from Farfarae Flos based on network pharmacology[J]. Chin Tradit Herbal Drugs (中草药), 2018, 49: 179–187. |
| [40] | Miao YL, Zhang WX, Wang YE, et al. Anti-inflammatory mechanism of antipyretic and detoxifying traditional Chinese medicine[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2018, 24: 228–234. |
 2018, Vol. 53
2018, Vol. 53