瓜蒌皮(Pericarpium Trichosanthis)为葫芦科栝楼属植物栝楼(Trichosanthes kirilowii Maxim)或双边栝楼(Trichosanthes rosthorinii Harms)的干燥成熟果皮[1]。瓜蒌皮注射液是以瓜蒌皮(来源为栝楼)为原料, 经水提醇沉, 用离子交换树脂对药效成分富集制得, 临床上用于冠心病、稳定型心绞痛的治疗[2-6]。瓜蒌皮注射液临床应用广泛, 但其化学与药效物质基础尚不明确, 质量标准仅测定精氨酸含量[7], 难以有效地反映注射液的真实质量。文献[8]报道采用UPLC/ESI-QTOF-MS方法鉴定了瓜蒌皮注射液中19个成分, 包括7个氨基酸、4个核苷酸、5个黄酮、1个多肽、1个唾液酸和1个含氮化合物, 对阐明注射液的药效物质基础具有重要意义。但是, 在本研究中发现, 该注射液中除氨基酸和核苷类成分外, 还含有丰富的生物碱类成分, 这些成分在反相色谱柱上保留弱, 难以得到有效的分离, 因此本研究中采用了亲水作用色谱柱(hydrophilic interaction chro matography, HILIC), 使这类成分得到了较好的分离。
近年来, 超高效液相色谱-高分辨质谱联用技术在天然产物及代谢物的鉴定中得到了广泛的应用[9-12], 高效的分离能力和稳定的质量精度, 大大提高了化合物鉴定的数量和准确度, 结合化合物鉴定软件以及日益完善的数据库, 有效提高了中药复杂体系中化学成分鉴定的速度和准确性。本研究采用四极杆-静电场轨道阱-线性离子阱三合一组合式高分辨质谱仪(UHPLC-Orbitrap Fusion Lumos HRMS), 静电场轨道阱质量分析器分辨率高达50万, 对区分质量数相近的成分具有极高的鉴定率, 同时采用“Top Speed”算法进行数据依赖的二级扫描, 最大限度地对一级质谱图中满足动态排除条件的离子进行碎裂, 鉴定更多的成分。采用Compound Discoverer软件, 将质谱数据与在线数据库ChemSpider、mzCloud中的化合物信息进行比对来智能化鉴定各成分, 同时应用Mass Frontier中小分子碎裂机理库Fragmentation LibraryTM, 对碎片离子进行结构归属, 共鉴定了48个成分, 基本阐明了该注射液的化学物质基础。
材料与方法仪器 美国Thermo-Fisher UltiMate 3000 series高效液相色谱仪(配有二元液相泵、自动进样器、在线脱气机、柱温箱); 美国Thermo-Fisher四极杆-静电场轨道阱-线性离子阱三合一组合式高分辨质谱仪(UHPLC-Orbitrap Fusion Lumos HRMS); 电子分析天平:赛多利斯科学仪器有限公司产品。
试剂 氨基酸对照品包括丝氨酸、甘氨酸、苏氨酸、瓜氨酸、精氨酸、丙氨酸、γ-氨基丁酸、酪氨酸、缬氨酸、苯丙氨酸、异亮氨酸、亮氨酸、脯氨酸、谷氨酰胺、天冬酰胺、甲基组氨酸、鸟氨酸、2-氨基丁酸、蛋氨酸、组氨酸、色氨酸、半胱氨酸、天冬氨酸、谷氨酸、赖氨酸、高脯氨酸、乙酰精氨酸, 核苷及其碱基对照品包括胞苷、胞嘧啶、肌苷、次黄嘌呤、腺苷、腺嘌呤、尿苷、尿嘧啶、鸟苷、胸苷、胸腺嘧啶、黄嘌呤, 生物碱类对照品包括葫芦巴碱、水苏碱、甜菜碱、氯化胆碱、盐酸肉碱和烟酸均购自中国食品药品检定研究院。21批瓜蒌皮注射液由上海第一生化药业有限公司提供, 批号分别为1410402 (S1)、1410403 (S2)、1410404 (S3)、1607401 (S4)、1607403 (S5)、1607404 (S6)、1607405 (S7)、1607406 (S8)、1607407 (S9)、1609402 (S10)、1609403 (S11)、1609404 (S12)、1609405 (S13)、1501401 (S14)、1501403 (S15)、1503401 (S16)、1503402 (S17)、1503403 (S18)、1503405 (S19)、1503406 (S20)、1503407 (S21), 其中, 注射液S1~S3、S4~S9、S10~S13、S14~S21的原料药材分别来源于R1 (批号131226)、R2 (批号160401)、R3 (批号160708)和R4 (批号150302), 这些药材经鉴定为葫芦科植物栝楼Trichosanthes kirilowii Maxim.的干燥成熟果皮(鉴定人:上海中医药大学, 崔亚君教授); 乙腈、甲醇均为色谱纯, 购自德国Merck公司; 甲酸、甲酸铵、乙酸铵均为色谱纯, 购自阿拉丁试剂有限公司; 实验用水为超纯水, 由美国Milli-Q超纯水系统制得。
色谱条件 采用ACQUITY XBridge Amide (100 mm × 2.1 mm, 3.5 μm)色谱柱; 流动相: A为0.1%甲酸乙腈溶液, B为0.1%甲酸水溶液(含5 mmol·L-1甲酸铵和5 mmol·L-1乙酸铵), 梯度洗脱, 程序为0~8 min, 8%~15% B; 8~14 min, 15%~50% B; 14~15 min, 50% B。柱温35 ℃, 流速0.4 mL·min-1, 进样量2 μL。
质谱条件 电喷雾离子源(ESI)正离子模式检测, 喷雾电压3.8 kV, 离子源温度350 ℃, 鞘气流速35 Arb, 辅助气流速10 Arb, 毛细管温度350 ℃。采用FT采集一级质谱数据, 质量范围m/z 70~700, 分辨率120 K, AGC (auto gain control)为100 000, 采用高能诱导裂解(HCD)方式裂解, 归一化碰撞能量30%, 采用FT采集二级质谱数据, 分辨率30 K, 采用“Top Speed”算法进行数据依赖扫描, 离子强度高于2.5e4一级离子进行二级碎裂, 动态排除时间为6 s。数据采集和处理使用Xcalibur 4.0软件。
供试品溶液的制备 取瓜蒌皮注射液1 mL, 加水稀释至50 mL, 混匀, 用乙腈稀释1倍, 即得。
对照品溶液的制备 称取各对照品适量, 精密称定, 加水制成质量浓度为1 mg·mL-1的储备液, 分别精密吸取氨基酸类对照品储备液适量于同一量瓶中, 加水稀释定容至刻度, 得浓度为1 μg·mL-1的混合溶液, 用乙腈稀释1倍即得氨基酸混合对照品溶液, 对于分子式相同的化合物, 分开制备。同法制备其他类别化合物的混合对照品溶液。
分析流程 整体分析和鉴定的流程图如图 1所示, 将原始数据导入Compound Discoverer 2.2软件, 根据仪器采集的精确分子量(< 5 ppm), 拟合出可能的元素组成, 与在线数据库ChemSpider和mzCloud中数据进行比对, 其中mzCloud数据库中含有化合物多级碎片质谱数据, 从而初步对各化合物进行鉴定, 进一步通过与对照品对比保留时间和碎片离子进行准确鉴定。

|
Figure 1 Workflow for compound identification |
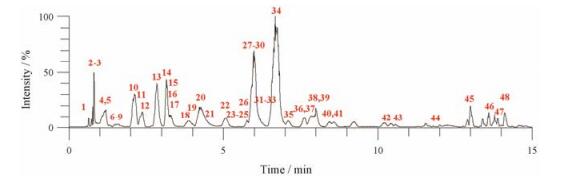
对色谱和质谱条件进行了系统的考察和优化, 包括色谱柱种类、梯度洗脱条件、质谱离子化模式等, 最终确定实验条件, 典型的总离子流色谱图如图 2所示, 主要色谱峰得到了良好的分离。
|
The peak numbers are in accordance with the compound numbers in Figure 3 and Table 1 Figure 2 Typical TIC chromatogram. |
结构鉴定结果显示, 一级离子流色谱中共有618个离子进行了二级质谱碎裂, 对其中峰强度高于35 000的151个离子进行结构鉴定, 通过与ChemSpider和mzCloud数据库检索, 共鉴定了45个成分, 其中25个通过与对照品比对进行了准确鉴定, 包括葫芦巴碱、水苏碱、胆碱、甜菜碱、肉碱、苏氨酸、瓜氨酸、精氨酸、γ-氨基丁酸、缬氨酸、苯丙氨酸、亮氨酸、异亮氨酸、脯氨酸、高脯氨酸、色氨酸、乙酰精氨酸、脯氨酰胺、腺苷、腺嘌呤、鸟苷、鸟嘌呤、烟酸、次黄嘌呤和4-guanidinobutyric acid, 其余各成分结合Compound Discoverer软件中结构解析功能进行了碎片结构归属, 对结果进行确证, 此外, 通过与对照品对比还鉴定了3个成分, 由于一级质谱扫描中丰度相对较低, 没有进行二级质谱裂解, 包括酪氨酸、胞苷和胞嘧啶。综上所述, 共鉴定了48个成分(表 1), 化合物结构见图 3。
| Table 1 Compound identification results. *Identified by comparing the retention time and MS information with those of reference standards |

|
Figure 3 Chemical structures |
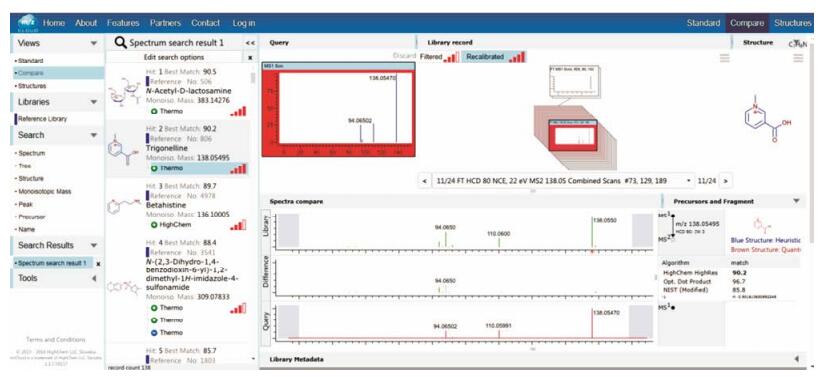
在瓜蒌皮注射液中共鉴定了生物碱类成分24个, 结构类型较多, 包括噻唑、哌啶、吡啶、吡咯、季铵碱等, 含量较高的有葫芦巴碱、水苏碱、甜菜碱等。正离子模式下, 芳香族类生物碱的质谱裂解主要发生在侧链上, 包括丢失CO (27.994 9)、CO2 (43.989 8)、H2O (18.010 6)或者HCOOH (46.005 3)等。以丰度最高的葫芦巴碱为例对结构鉴定过程和化合物的裂解行为进行解析。mzCloud数据库检索结果如图 4所示, 二级质谱图中主要碎片离子m/z 110.059 91和m/z 94.065 02与数据库中相应离子匹配较好, 分别为母离子[M+H]+丢失1分子CO和CO2得到。通过与葫芦巴碱对照品进行比较, 对该化合物进行了准确鉴定。脂肪族类季铵碱(包括化合物12、13、27、29、30、38和47)的二级质谱碎裂主要是丢失N(CH3)3 (59.073 6)或者电荷保留在氮原子上得到m/z 60.080 7的碎片离子。Compound Discoverer 2.2软件含有Fragmentation LibraryTM裂解谱图库, 具有预测碎裂工具以及自动谱图注释功能, 对二级谱图中碎片离子进行结构归属, 大大简化了结构鉴定过程, 例如化合物47各碎片离子的归属见图 5。
|
Figure 4 Identification of trigonelline by searching the mzCloud database |

|
Figure 5 Attribution of the fragments for compound 47 |
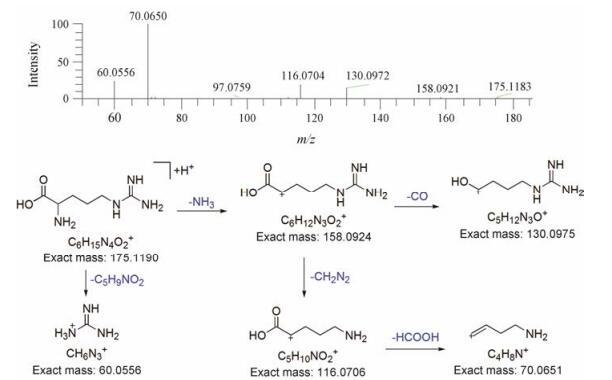
在注射液中共鉴定了17个氨基酸, 其中15个氨基酸通过与对照品的保留时间和质谱数据比较, 进行了准确鉴定, 其中包括6种人体必需氨基酸, 分别为亮氨酸、苯丙氨酸、异亮氨酸、色氨酸、脯氨酸和缬氨酸。氨基酸在亲水作用色谱柱上的保留行为呈现典型的正相色谱性质, 即非极性氨基酸保留弱, 出峰快, 极性氨基酸尤其是带有电荷的氨基酸保留强, 出峰较晚, 例如带正电荷的精氨酸最晚出峰。在正离子模式下, 氨基酸二级质谱碎裂主要是丢失HCOOH (46.005 3)和NH3 (17.026 6)。以精氨酸为例, 对质谱裂解过程进行解析, 如图 6所示, 一级质谱图中呈现[M+H]+峰(m/z 175.118 9), 根据高分辨数据推测元素组成为C6H14N4O2 (ppm -0.527), 二级质谱图上主要的碎片离子包括m/z 158.092 1、m/z 130.097 2、m/z 116.070 4、m/z 70.065 0和m/z 60.055 6, 其中, 离子m/z 158.092 1为母离子丢失1分子NH3后的产物, 该离子进一步丢失CO和CH2N2 (42.021 8)后得到离子m/z 130.097 2和m/z 116.070 4, 进一步反应丢失HCOOH (46.005 3)后得到m/z 70.065 0, 而离子m/z 60.055 6为母离子碎裂后正电荷保留在胍基上得到的产物。通过与精氨酸对照品比较, 对该化合物进行了准确鉴定。
|
Figure 6 Proposed fragmentation of arginine |
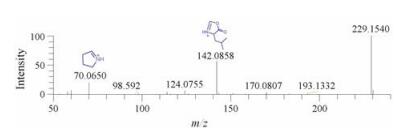
另外, 本文鉴定到两个二肽成分prolylleucine和prolylisoleucine (化合物24和39), 通过与mzCloud数据库比较进行初步鉴定, 化合物24的二级质谱图如图 7所示, 对主要的碎片离子进行了归属, 化合物39与24具有相同的二级质谱图, 根据亮氨酸和异亮氨酸的出峰顺序, 推测保留时间短的(化合物24)为prolylleucine, 保留时间长的(化合物39)为proly lisoleucine。
|
Figure 7 Attribution of the fragments for compound 24 |
在注射液中共鉴定核苷类成分3个, 核苷碱基类4个, 通过与对照品比较进行了准确鉴定包括次黄嘌呤、腺嘌呤、腺苷、胞嘧啶、胞苷、鸟嘌呤和鸟苷。核苷的二级质谱裂解主要是丢失1分子核糖(130.042 2), 碱基的裂解主要是丢失1分子NH3 (17.026 6)。
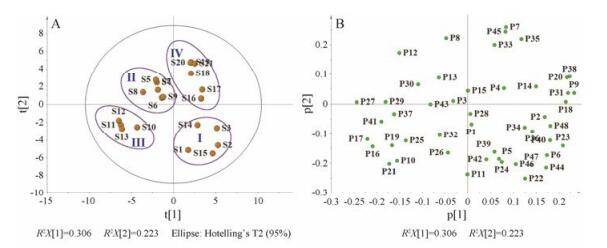
3 统计分析为了对不同批次制剂稳定性进行考察, 本文采用SIMCA-P 13.0软件对21批样品进行了主成分分析(principal component analysis, PCA), 以色谱峰峰号(即相应化合物)为变量, 以相应化合物精确分子量的提取离子色谱峰峰面积为观察值, 采用UV Scaling方式对21批样品的归一化数据进行预处理后展开主成分分析, 结果如图 8所示, 前两个主成分的累积方差贡献率为52.9%, 从得分图(scatter plot, 图 8A)中可以看出样品分散在4个象限, 大致分为4组, 其中Ⅱ、Ⅲ和Ⅳ组中注射液原料药材分别为R2、R3和R4, Ⅰ组中S1~S3原料来源为R1, 可见对于同一原料生产的注射液重现性相对良好, 说明制备工艺相对稳定, 但是S14和S15原料来源为R4, 远远偏离Ⅳ组, 与Ⅰ组中注射液的成分分布更相似, 因此, 除原料药材外, 制备工艺也是影响制剂批间稳定性的重要因素。
|
A: Scatter plot; B: Loading plot Figure 8 PCA results. |
瓜蒌皮注射液疗效明确, 临床应用广泛, 但是药效物质基础研究薄弱, 本研究首次采用HILIC/Orbitrap Fusion Lumos对瓜蒌皮注射液的化学成分进行了全面分析, 得到其所含成分的高分辨精确分子量和碎片离子信息, 采用Compound Discoverer软件结合mzCloud和ChemSpider在线数据库, 快速智能化的鉴定了48个化合物, 其中25个通过与对照品对照进行了准确鉴定, 基本阐明了该注射液的化学物质基础。
考察了反相C18色谱柱和HILIC色谱柱的分离效果, 结果显示在反相C18色谱柱上大部分成分保留较差, 出峰快, 瓜蒌皮注射液中化学成分包括生物碱、氨基酸、核苷及其碱基等, 化合物极性大, 在反相色谱柱上保留弱, 本研究尝试采用亲水作用色谱柱(HILIC)进行分离, 它是以强极性填料为固定相(如未衍生化的硅胶、二醇基键合硅胶、酰胺键合硅胶等), 高比例有机相(如乙腈)为流动相, 通过复杂的机制可以实现强极性化合物的有效分离, 结果显示瓜蒌皮注射液中各成分分离度大大提高, 同时HILIC色谱柱与质谱联用, 高比例的有机相可明显增加化合物的质谱响应, 提高灵敏度。
考察了质谱条件正离子和负离子两种采集模式, 发现正离子模式下化合物的响应明显高于负离子模式, 预实验中发现瓜蒌皮注射液中含有丰富的含氮类成分, 这些成分在正离子模式下具有更好的响应, 因此选择了正离子模式检测。
文献[7]报道瓜蒌皮注射液中还含有黄酮、N-乙酰神经氨酸和S-乳酰谷胱甘肽, 本研究从瓜蒌皮注射液总离子流色谱图中提取相应化合物的精确分子量, 结果显示一级质谱图中未检索到芦丁、N-乙酰神经氨酸和S-乳酰谷胱甘肽, 检索到了其余4个黄酮(木犀草素、香叶木素-7-O-葡萄糖苷、芹菜素-7-O-β-D-葡萄糖苷、木犀草素-7-O-β-D-葡萄糖苷), 但是这些化合物含量很低, 均未进行二级质谱碎裂, 因此本文没有鉴定这些成分。由于该类化合物极性相对小, 更适合用反相色谱柱进行分离和分析。
本研究采集了21批注射液的质谱数据, 采用主成分分析法进行统计分析, 结果显示样品分散在4个象限, 与注射液的原料药材具有相关性, 制剂制备工艺相对稳定, 因此, 为了保证注射液的批间稳定性, 需要对原料药材的质量进行严格控制。
| [1] | Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[M]. Part 1. Beijing: China Medical Science Press, 2015: 114. |
| [2] | Zhao RZ, Shi B, Wang DM, et al. Efficacy of Pericarpium Trichosanthis injection on stable angina in patients complicated with type 2 diabetes mellitus[J]. Chin J New Drugs (中国新药杂志), 2010, 19: 1871–1874. |
| [3] | Wang LC. Clinical observation of Pericarpium Trichosanthis injection on patients with coronary heart disease[J]. Cardiovasc Dis J Integr Tradit Chin West Med (中西医结合心血管病杂志), 2016, 4: 65–66. |
| [4] | Liu L, Niu XP. Effect of Pericarpium Trichosanthis injection on vascular endothelium function in stable angina pectoris with phlegm-stasis syndrome[J]. Chin J Integr Med Cardio-/Cerebrovas Dis (中西医结合心脑血管病杂志), 2014, 12: 3–5. |
| [5] | Huang ZW, Huang JS, Huang JW. Study on clinical effect of snakegourd fruit injection of wind-phlegm obstructing collateral type stroke[J]. World Chin Med (世界中医药), 2016, 11: 2661–2664. |
| [6] | Lu C, Huang ZH. Liquid chromatography fingerprinting test method of Pericarpium Trichosanthis or Pericarpium Trichosanthis injection: China, CN200610118771.6[P]. 2007-10-24. |
| [7] | Hong YL, Du SY, Yang G, et al. Quantification of the total amino acids in Pericarpium Trichosanthis and Pericarpium Trichosanthis injection[J]. Chin J Exp Tradit Med Formulae (中国实验方剂学杂志), 2004, 10: 10–11. |
| [8] | Wang HJ, Ke Y, Ye G. UPLC/ESI-QTOF-MS analysis of chemical constituents in Gualoupi injection[J]. Shanghai Med Pharm J (上海医药), 2017: 60–65. |
| [9] | Wang N, Ahmad H, Jia YM, et al. Identification of polygala oligosaccharide esters and their metabolites in rat plasma after oral administration of ethanol extract of Kai Xin San by UHPLC-MS[J]. Acta Pharm Sin (药学学报), 2017, 52: 1592–1598. |
| [10] | Yang ZL, Zhao J. Qualitative and quantitative analysis of icariin analogues in Epimedium koreanum by UPLC-Q-TOF MS[J]. J Chin Mass Spectrom Soc (质谱学报), 2017, 38: 19–29. |
| [11] | Hu YH, Xu WQ, Qin X, et al. Rapid identification of chemical constituents in Huangqi Jianzhong Tang by UHPLC coupled with hybrid quadrupole-orbitrap MS[J]. Acta Pharm Sin (药学学报), 2017, 52: 964–970. |
| [12] | Zhang JX, Yang WZ, Li SR, et al. An intelligentized strategy for endogenous small molecules characterization and quality evaluation of earthworm from two geographic origins by ultra-high performance HILIC/QTOFMSE and progenesis QI[J]. Anal Bioanal Chem, 2016, 408: 3881–3890. DOI:10.1007/s00216-016-9482-3 |
 2018, Vol. 53
2018, Vol. 53


