2. 北京中医药大学 北京中医药研究院, 北京 100029
2. Institute of Traditional Chinese Medicine, Beijing University of Chinese Medicine, Beijing 100029, China
糖尿病视网膜病(diabetic retinopathy, DR), 是糖尿病患者在后期最严重的微血管并发症, 也是工作人群失明的首要原因[1]。中医药在治疗DR方面的优势不断凸显, 已成为防治DR的重要组成部分[2]。复方血栓通作为国家二级中药保护品种, 是眼底病用药的第一品牌。它是由三七、黄芪、丹参和玄参组成的中药复方, 功能为活血化瘀、益气养阴, 具有扩张血管、增加血流量、改善血液循环和微循环的药理作用, 能有效减轻黄斑水肿, 改善视力[3]。复方血栓通的药理学机制包括扩张血管、提高抗缺氧能力、抑制氧化应激、减少凋亡、抑制血管内皮生长因子(vascular endothelial growth factor, VEGF)表达、调控Hippo信号通路等[4]。但是DR发病机制复杂, 因此复方血栓通的药理机制仍未完全阐明。
网络药理学是在高通量组学数据分析、计算机虚拟计算及网络数据库检索基础上, 从分子生物网络角度, 系统地揭示药物药理作用及其作用机制[5]。中药复方多成分、多靶点、多途径的特征正是网络药理学研究的重点[6]。
Cheng等[7]利用网络药理学的思路与方法, 建立了“药物-靶点-通路-网络”的研究模式, 预测清肺消炎丸的潜在靶标及作用途径, 初步揭示了其抗炎作用的多维调控网络。Liu等[8]首先收集了四君子汤的化学成分信息, 构建化合物-靶点和靶点-疾病网络, 然后采用网络药理学方法预测了四君子汤潜在的作用靶点与可能作用的疾病。但是在上述利用网络药理学研究中药复方药理机制的范例中, 靶点是由化学成分推导而来, 并没有考虑到靶点是否与特定疾病的核心发病机制密切相关, 这样将导致药物靶点广泛并且复杂。本文拟把中药复方的成分靶点与疾病靶点取交集进行分析, 这样取得的结果将对疾病更加有针对性, 更加明确可靠。
材料与方法化学成分信息 从TCMSP (http://lsp.nwu.edu.cn/tcmsp.php)中分别检索三七、黄芪、丹参和玄参的化学成分, 收集化学成分-靶点信息。
DR相关靶点的获得 从OMIM (http://www.omim.org/)、TTD (http://systemsdock.unit.Oist.jp/iddp/home/index)、pharmGkb (https://www.pharmgkb.org/)、DiGSeE (http://210.107.182.61/geneSearch/)、GAD (http://geneticassociationdb.nih.gov/) 5个疾病相关靶点的数据库检索DR相关靶点, DiGSe (http://210.107. 182.61/geneSearch)为在线文本挖掘工具, 可以挖掘疾病相关基因。
靶点名称矫正 利用Uniprot (http://www.uniprot.org/)数据库, 输入从TCMSP和5个数据库得到的靶点名称, 得到对应的基因名称, 对蛋白质名称进行矫正。优先选择Swiss-prot收录并且匹配程度高的基因名称。将复方血栓通和DR矫正后的基因取交集。
靶点通路注释分析 利用DAVID (http://david.nifcrf.gov/)数据库对得到的交集基因进行GO注释分析(Gene-Ontology)和KEGG通路分析(Kyoto Encyclopedia of Genes and Genomes)。交集基因可以直接映射到通路上。
化学成分-交集基因-通路网络构建 根据上述复方血栓通化学成分的靶点预测结果, 采用Cytoscape 3.6.1软件构建化学成分-交集靶点-通路网络模型。网络中, 节点(node)表示化学成分、交集基因和通路。若某一靶点为某化合物的潜在作用靶点, 则以边(edge)相连, 该靶点参与某一通路时, 将靶点与作用通路也以边相连。通过构建网络揭示复方血栓通治疗DR多成分、多靶点、多通路的特点[9]。
分子对接 利用UniProt检索, 选择合适的目标靶点的PDB ID, 利用RSCB PBD (http://www.rcsb.org/pdb/home/home.do)下载对接蛋白和对照配体的3D结构文件, 对照配体由RSCB PBD系统自动匹配。利用PubChem下载化合物的3D结构文件。使用SystemsDock在线分子对接工具进行在线分子对接。
结果 1 化学成分和靶点基因的收集检索得到复方血栓通中三七的化学成分有119种, 丹参202种, 黄芪87种, 玄参47种。删除重复项共427种化学成分, 包括黄酮、萜类、苷类、糖类、脂肪酸和氨基酸等化合物, 如木犀草素(luteolin)、芹菜素(apigenin)、丹参酮ⅡA (dehydrotanshinone Ⅱ A)、丹酚酸B (salvianolic acid b)、熊果酸(ursolic acid)、L-赖氨酸(L-lysin) (编号分别为6、8、2651、7074、511、55)等。Sun等[10]通过UPLC-MS/MS法对复方血栓通胶囊中的主要化学成分进行了含量测定, 发现其中丹参酮ⅡA、丹酚酸B和熊果酸等的含量分别为1.135、2.343和0.560 mg·g-1。复方血栓通的化学成分对应376个基因, 例如VEGF、丝裂原活化蛋白激酶8 (mitogen-activated protein kinase 8, MAPK8)、白细胞介素-1β (interleukin 1β, IL-1β)等(图 1)。

|
Figure 1 The part of compositions-genes network for potential targets from Compound Xueshuantong. The purple round means the number of chemical compound, and the yellow round means drug target |
从5个数据库得到DR相关基因共247个, 包括血管内皮生长因子A (vascular endothelial growth factor A, VEGFA)、MAPK1、MAPK8等, DAVID分析得到有Toll样受体信号通路(Toll-like receptor signaling pathway, TLR)、MAPK受体信号通路(MAPK signaling pathway)、VEGF信号通路(VEGF signaling pathway)等通路信息(表 1)。
| Table 1 The part of pathways and genes of diabetic retinopathy (DR) |
将复方血栓通靶点基因和DR的相关基因取交集, 共有37个相同基因, 包括VEGF、基质金属蛋白酶(matrix metalloproteinases, MMP)、IL-1β、PTGS2 (别名环氧酶-2, cyclooxygenase 2, COX-2)和MAPK8等。
将37个交集基因通过DAVID系统进行生物分子功能注释。对获取靶点信息进行GO注释分析和KEGG通路分析。其中GO注释分析分为三部分, 分别为生物过程分子功能(molecular function, MF)、细胞组分(cellular component, CC)和生物过程(biological process, BP) (图 2~4)。
|
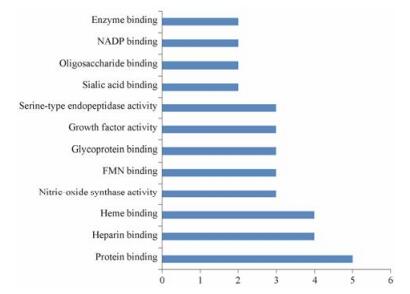
图 2 The count of genes and molecular function |
|
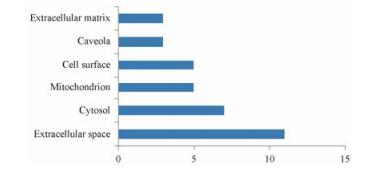
图 3 The count of genes and cellular component |
|
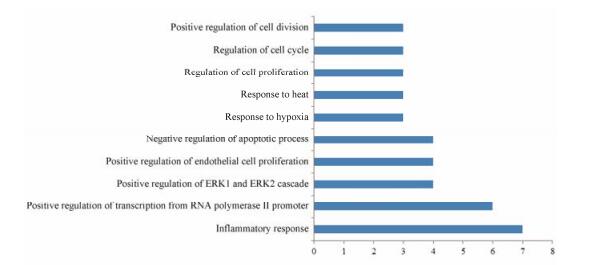
图 4 The count of genes and biological process (just show the top 10 of biological process) |
交集基因在分子功能中对蛋白结合(protein binding)和肝素结合(heparin binding)功能参与最多, 相关基因包括转录因子AP-1 (transcription factor AP-1, JUN)、原癌基因酪氨酸蛋白激酶(proto- oncogene tyrosin e-protein kinase Src, SRC)、VEGFA等(图 2)。
交集基因在细胞外间隙(extracellular space)、细胞溶质(cytosol)、细胞表面(cell surface) 3个部位分布最多。超氧化物歧化酶[Cu-Zn] (superoxide dismutase [Cu-Zn], SOD1)、IL-6和IL-1β等基因参与其中(图 3)。
交集基因参与炎症应答、RNA聚合酶Ⅱ启动子转录的正调控、内皮细胞增殖的正调控作用等生物过程最多。一氧化氮合酶1 (nitric-oxide synthase 1, NOS1)、IL-6、IL-1β和VEGFA等基因参与其中(图 4)。
4 化学成分-交集基因-通路网络的构建由KEGG分析, 共得到18条通路, 包括24个交集基因, 以P≤0.05为标准筛选通路, 最终得到14条通路(FoxO信号通路、甘油脂代谢、黏附连接和孕酮介导的卵母细胞成熟, P > 0.05剔除)及22个基因(LPL和AKR1B1剔除)。
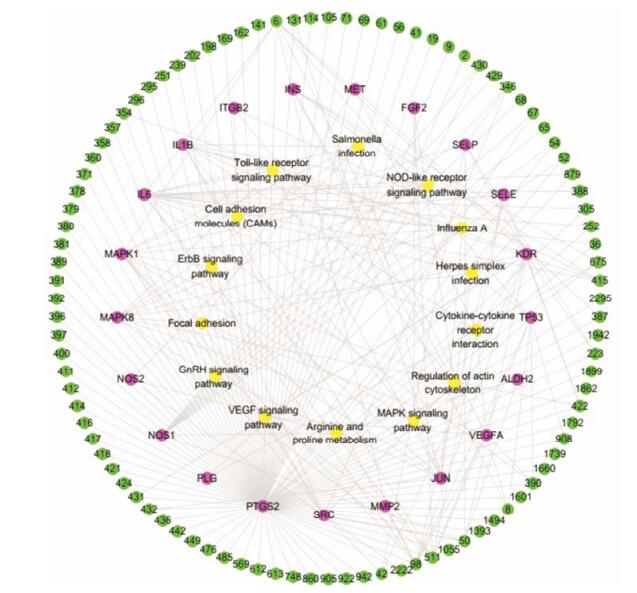
采用Cytoscape软件构建化学成分-基因-通路网络模型(图 5)。共169个节点, 458个边。作用于MAPK8、IL-6、IL-1β、COX-2的有效化学成分较多, 这些靶点涉及较多的通路有TLR信号通路、MAPK信号通路和VEGF信号通路。作用于上述靶点和通路的化学成分有木犀草素、芹菜素、熊果酸、L-赖氨酸等。复方血栓通主要活性成分的作用靶点分布在不同的信号通路上, 相互协调, 共同发挥作用。并且文献[4]报道复方血栓通治疗DR的机制主要有扩张血管、提高抗缺氧能力、抑制氧化应激、减少凋亡、抑制VEGF等, 也与本文网络预测结果符合。本研究可以从多角度揭示复方血栓通治疗DR的药理机制。
|
Figure 5 ingredients-targets-pathways network of Compound Xueshuantong, active ingredients (green), targets (purple), pathways (yellow) |
选择COX-2和VEGFR2两个靶点, 木犀草素、芹菜素、槲皮素、山奈酚和熊果酸(编号6、8、98、422、511) 5个化合物及4个靶点的对照配体进行分子对接(表 2)。
| Table 2 The result (docking score) of molecular docking |
分子对接的结果与本文利用网络药理学预测的结果一致, 编号6、8、98、422、511这5个化合物的对接打分均明显高于对照配体, 说明5个化合物与COX-2和VEGFR2作用良好。
讨论复方血栓通治疗DR已经在临床上得到证实[4]。但是目前对复方血栓通治疗DR的药理机制尚不明确。2008年, Hopkins[11]明确提出“网络药理学”的概念, 本文利用网络药理学的研究思路, 探讨了复方血栓通治疗DR潜在的作用靶点和机制, 预测复方血栓通治疗DR的可能作用靶点和通路。
炎症反应是视网膜血管被高糖刺激后出现的初始反应, 表现为白细胞聚集, 炎症因子分泌大量增加; 新生血管形成则是DR的标志性病理特征。本文在对DR相关性基因进行分析后发现, 在炎症反应及血管增生过程中, VEGF信号通路[12]、TLR信号通路[13]及MAPK信号通路[14]扮演了核心角色, 涉及到MAPK1、COX-2、VEGFA、IL-1β、IL-6和成纤维细胞生长因子2 (fibroblast growth factor 2, FGF2)等基因。COX-2是炎症过程中的一个重要的诱导酶, COX-2促血管生成可能与其诱导组织生成VEGF有关, VEGF特异性地直接作用于内皮细胞表面受体, 促进血管生成[15]。VEGF-A是VEGF家族的重要成员, 可促进新生血管形成和血管通透性增加。
VEGF信号通路、TLR通路和MAPK通路三者相互协调, 相互影响。例如, COX-2与TLRs均能通过诱导组织生成VEGFA, 后者与其受体KDR结合后, 激活MAPK1/8或c-Jun氨基末端激酶(c-Jun N-terminal kinase, JNK)等, 从而影响MAPK信号通路; MAPK是FGF2诱导血管生成的调节因子[16], FGF2对内皮细胞有趋化和促进有丝分裂作用, 促进血管形成, 导致血管增生的发生。同时, Seghezzi等[17]研究发现外源和内源FGFs都能诱导VEGF产生, 影响血管形成。
在本文的研究中, 结合TCMSP和DAVID的数据结果分析发现, 木犀草素、熊果酸、槲皮素、山奈酚和芹菜素等在内共92个化合物, 可能通过21个靶点对上述的3条通路有作用。文献报道[18]熊果酸对人脐静脉血管内皮细胞的增殖具有抑制作用, 而且显著减少MAPK信号通路中ERK1、c-Jun等相关基因的转录和翻译。Chen等[19]用DR大鼠模型, 研究了槲皮素治疗DR的作用机制, 发现槲皮素可以改善DR大鼠视网膜组织水肿和空泡化, 并且显著降低MMP-9和VEGF的转录和表达。槲皮素也抑制COX-2的表达[20]。山奈酚抑制IL-1β诱导的MAPK途径, 阻碍MMP1、MMP3和COX-2的表达[21]。与本文网络药理学预测熊果酸、槲皮素和山奈酚的作用靶点有IL-1β、IL-6、MAPK8等结果一致。文献及网络药理学结果共同提示, 复方血栓通可能具有多种抗炎或抗血管增生机制防治DR。
本文数据分析还发现, 在复方血栓通的化学成分中, 一种化学成分可以对应多个靶点, 参与多个信号通路。如玄参中的熊果酸对应的靶点有IL-1β、MAPK8、JUN和MMP2等, 调控VEGF信号通路、TLR信号通路和局部黏连等。而且, 在DR的发病过程中, 复方血栓通的多个化学成分也可以对应一个共同靶点, 如木犀草素、芹菜素、和熊果酸等共同作用于VEGFA。
总之, 本课题对复方血栓通进行成分和靶点分析, 收集DR的相关基因, 运用网络药理学的方法, 得到二者交集基因的相关通路, 预测复方血栓通通过熊果酸、槲皮素和山奈酚等多个化学成分作用于VEGF、TLR及MAPK等多个信号通路。此研究表明复方血栓通作为中药复方, 其化学成分可能直接作用于DR关键的通路靶点, 通过抑制炎症、血管增生等治疗DR。本研究为进一步深入揭示复方血栓通治疗DR的药理机制奠定了基础。
| [1] | Jin Y. Effect of traditional Chinese medicine of Qi and dissipating blood stasis on non-proliferative diabetic retinopathy and its effect on VEGF, Ang and ANGPT[J]. Mod J Integr Trad Chin West Med (现代中西医结合杂志), 2017, 35: 3923–3926. |
| [2] | Xiang PP, Xu W. Research progress on traditional Chinese medicine treatment of diabetic retinopathy[J]. China J Trad Chin Med Pharm (中华中医药杂志), 2014, 29: 813–815. |
| [3] | Huang CX, Qiang Y, Xiao C, et al. Study on prevention and treatment of Fufang Xueshitong capsule on retinal microvascular changes in diabetic rats[J]. Chin J Ocul Fundus Dis (中华眼底病杂志), 2008, 24: 272–275. |
| [4] | Jing C, Du JH, Sun ZH. Progress of Compound Xueshuantong in treating diabetic retinopathy[J]. Chin J Clin (Electron Edit) (中华临床医师杂志, 电子版), 2012, 22: 7373–7375. |
| [5] | Xu JJ, Mei BY, Nan Z. Clinical observation on early diabetic retinopathy with Compound Xueshuantong Capsule[J]. China J Tradit Chin Med Pharm (中华中医药杂志), 2012, 27: 3247–3249. |
| [6] | Li S, Zhang B, Jiang D, et al. Herb network construction and co-module analysis for uncovering the combination rule of traditional Chinese herbal formulae[J]. BMC Bioinformatics, 2011, 11: S6. |
| [7] | Cheng BF, Hou YY, Min J, et al. Anti-inflammatory mechanism of Qingfei Xiaoyan Wan studied with network pharmacology[J]. Acta Pharm Sin (药学学报), 2013, 4: 686–693. |
| [8] | Liu XK, Wu JR, Lin MJ, et al. Mechanism of Si Junzitang based on network pharmacology[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2017, 23: 194–202. |
| [9] | Yao G, Li G, Gao XX, et al. An exploration in the action targets for antidepressant bioactive components of Xiaoyaosan based on network pharmacology[J]. Acta Pharm Sin (药学学报), 2015, 50: 1589–1595. |
| [10] | Sun Z, Hu YR, Zuo LH, et al. Simultaneous determination of 9 components in Compound Xueshuantong capsules by UPLC-MS/MS[J]. China Pharm (中国药房), 2017, 28: 2959–2963. |
| [11] | Hopkins AL. Network pharmacology: the next paradigm in drug discovery[J]. Nat Chem Biol, 2008, 4: 682–690. DOI:10.1038/nchembio.118 |
| [12] | Song E, Xu Q, Wang XR, et al. Expression of vascular endothelial growth factor in the retina of diabetic rats[J]. J Jilin Univ (Med Edit) (吉林大学学报, 医学版), 2003, 29: 38–40, 44. |
| [13] | Zhao M, Li CH, Liu YL. Toll-like receptor (TLR)-2/4 expression in retinal ganglion cells in a high-glucose environment and its implications[J]. Genet Mol Res, 2016. DOI:10.4238/gmr.15026998 |
| [14] | Du Y, Tang J, Li G, et al. Effects of p38 MAPK inhibition on early stages of diabetic retinopathy and sensory nerve function[J]. Invest Ophthalmol Vis Sci, 2010, 51: 2158–2164. DOI:10.1167/iovs.09-3674 |
| [15] | Dong Y, Zhang MC. Effect of COX-2 and its inhibitor celcoxib on corneal neovascularization[J]. Chin Ophthal Res (眼科研究), 2007, 25: 424–427. |
| [16] | Matsumoto T, Turesson I, Book M, et al. p38 MAP kinase negatively regulates endothelial cell survival, proliferation, and differentiation in FGF-2–stimulated angiogenesis[J]. J Cell Biol, 2002, 156: 149–160. DOI:10.1083/jcb.200103096 |
| [17] | Seghezzi G, Patel S, Ren CJ, et al. Fib roblast growth factor-2 (FGF-2) induces vascular endothelial growth factor (VEGF) expression in the endothelial cells of forming capillaries: an autocrine mechanism contributing to angiogenesis[J]. J Cell Biol, 1998, 141: 1659–1673. DOI:10.1083/jcb.141.7.1659 |
| [18] | Li W, Liu Q, He L, et al. Effect of ursolic acid on proliferation of vascular endothelial cells and relevant mechanism[J]. Chin J Biol (中国生物制品学杂志), 2011, 24: 157–162, 168. |
| [19] | Chen B, He T, Xing YQ, et al. Effects of quercetin on the expression of MCP-1, MMP-9 and VEGF in rats with diabetic retinopathy[J]. Exp Ther Med, 2017, 14: 6022–6026. |
| [20] | Zhang Li, Zhu QY, Wei YF, et al. Effect of quercetin on the expression of VEGF and COX-2 in prostate cancer PC3 cells[J]. J New Chin Med (新中医), 2012, 44: 125–127. |
| [21] | Yoon HY, Lee EG, Lee H, et al. Kaempferol inhibits IL-1β-induced proliferation of rheumatoid arthritis synovial fibroblasts and the production of COX-2, PGE2 and MMPs[J]. Int J Mol Med, 2013, 32: 971–977. DOI:10.3892/ijmm.2013.1468 |
 2018, Vol. 53
2018, Vol. 53


