2. 安徽省第二人民医院药学部, 安徽 合肥 230041
2. Pharmacy Department of Anhui No.2 Provincial People's Hospital, Hefei 230041, China
瓜蒌为葫芦科植物栝楼(Trichosanthes kirilowii Maxim.)或双边栝楼(Trichosanthes rosthornii Harms.)的成熟果实[1], 主产于河南、河北、山东、安徽等地, 具宽胸散结之功效, 用于胸痹心痛等。薤白为百合科植物小根蒜(Allium macrostemon Bge.)或薤(Allium chinense G. Don)的干燥鳞茎[1], 具利水渗湿, 除痹之功效, 用于水肿、癌肿等。
瓜蒌薤白配伍使用源自于张仲景的《金匮要略·胸痹心痛短气病脉证治》篇, 用于胸痹心痛等。课题组前期对瓜蒌薤白配伍抗大鼠心肌缺血-再灌注损伤(myocardial ischemia reperfusion injury, MIRI)的药效学进行了研究, 发现瓜蒌薤白配伍可有效抑制MIRI大鼠心电图ST段的抬高, 降低大鼠肌酸激酶MB同工酶、肌红蛋白、心肌肌钙蛋白-T值(P < 0.05或P < 0.01), 改善心肌组织状况, 降低心肌梗死百分率(P < 0.01)[2]。研究表明心肌细胞凋亡对MIRI起主导作用, PI3K/Akt信号通路可能是调控细胞凋亡最重要的途径之一[3]。
因此, 本课题采用网络药理学方法[4, 5], 构建瓜蒌薤白配伍的化学成分-靶点蛋白-信号通路, 探讨瓜蒌薤白配伍的作用机制。在此基础上, 观察瓜蒌薤白滴丸预处理对急性心肌缺血-再灌注损伤大鼠心肌细胞凋亡及凋亡相关信号通路PI3K/Akt中蛋白表达的影响, 采用原位末端脱氧核苷酸转移酶标记(TdT-mediated dUTP nick-end labeling, TUNEL)法测定心肌细胞凋亡百分率, 蛋白质免疫印迹法测定Akt、p-Akt和caspase-3蛋白的表达。检测心肌缺血-再灌注损伤对大鼠心肌细胞凋亡及PI3K/Akt通路中蛋白表达的影响, 探讨PI3K信号通路特异性阻断剂渥曼青霉素(wortmannin)对瓜蒌薤白滴丸调控心肌细胞凋亡及蛋白表达的作用, 明确瓜蒌薤白配伍抗心力衰竭的作用机制。
材料与方法实验动物 SPF级Sprague Dawley (SD)大鼠, 雄性, 体重180~250 g, 由浙江省实验动物中心提供, 合格证号: SCXK (浙) 2008-0033。
药品与试剂 瓜蒌薤白滴丸(批号: 20140101, 皖南医学院药学院药物制剂及质量控制课题组提供); 凯基TUNEL细胞凋亡原位检测试剂盒(南京凯基生物科技发展有限公司, KGA7032);二喹啉甲酸 (bicinchoninic acid, BCA)蛋白测定试剂盒(武汉博士德生物工程有限公司, AR0146);超敏电化学发光(electro-chemiluminesence, ECL)试剂盒BeyoECL Plus (P0018)、caspase-3抗体(AC033)、phospho-Akt (Ser473)抗体(AA329-1)、Akt抗体(AA326)、tubulin抗体(AT819)、辣根过氧化物酶(horseradish peroxidase, HRP)标记山羊抗兔IgG (H+L) (A0208)、HRP标记山羊抗小鼠IgG (H+L) (A0216)、wortmannin (S1952) (碧云天生物技术研究所)。
仪器 HX-300小动物呼吸机、BL-420生物机能采集系统(成都泰盟软件有限公司); TE70X型半干转膜仪(美国Hoefer); Chemi Scope 3400化学发光成像系统(Clinx Science Instruments Co., Ltd); DYY-2C型电泳仪(北京六一仪器厂)。
数据库及分析软件 数据库主要包括TCM Database@Taiwan (http://tcm.cmu.edu.tw/)、TCMSP (http://lsp.nwsuaf.edu.cn/tcmsp.php)、DRAR-CPI (http://cpi.bio-x.cn/drar)、UniProt (http://www.uniprot.org/)、CooLGeN (http://ci.smu.edu.cn/CooLGeN/Home.php)、DAVID数据库(https://david.ncifcrf.gov/tools.jsp); 分析软件主要有ChemBioDrawUltta 14.0、Gephi0.9.2软件。
化学成分的筛选 通过检索TCM Database@ Taiwan、TCMSP数据库(检索日期为2018年3月18日), 筛选出符合口服生物利用度(oral bioavailability, OB)≥30%、类药性(drug like, DL)≥0. 18的化合物21个。腺苷(adenosine)的OB为15.98%, DL为0.18, 该化合物为已知瓜蒌薤白中的药效成分[6], 因此共获得22个化合物, 见表 1。所有化合物分子结构式采用ChemBioDrawUltta 14.0软件进行绘制, 结果保存为MDL SDfile (*.sdf)文件格式备用。
| Table 1 Information on main compounds in Gualou and Xiebai. (Z)-3-Acrylamide: (Z)-3-(4-Hydroxy-3-methoxy-phenyl)-N-[2-(4-hydroxyphenyl)ethyl]acrylamide |
潜在靶点的预测 登陆DRAR-CPI数据库分别上传表 1中各成分sdf格式文件(数据上传日期为2018年3月18日, 完成日期为2018年4月2日), 选择Z'-score < -1筛选蛋白靶点并将PDB ID导入UniProt数据库, 获得瓜蒌薤白中各成分的基因靶点(检索日期为2018年4月3日)。
心力衰竭相关的靶标蛋白质的收集 通过CooLGeN数据库, 以“heart failure”为关键词, 捜索Medline及GeneRIF数据库, 收集与心力衰竭相关的靶点蛋白(检索日期为2018年4月5日)。
生物功能及靶点通路注释分析 将靶点蛋白复制至DAVID数据库的列表中, 选择标示符为official_gene_symbol, 物种注释为homo sapiens, 进行GOTERM_BP_DIRECT富集分析和Kyoto Ency_clopedia of Genes and Genomes (KEGG)_PATHWAY通路注释分析(检索日期为2018年4月6日)。
成分-蛋白靶点-信号通路网络分析和构建 根据预测结果, 使用Gephi软件将筛选出来的活性成分、靶点蛋白和作用通路构建成分-靶点蛋白-信号通路网络。
动物分组及给药 SPF级SD大鼠随机分为6组, 每组6只, 假手术组、模型组、wortmannin组分别给予生理盐水, 瓜蒌薤白滴丸组22.5 g·kg-1, 瓜蒌薤白滴丸22.5 g·kg-1和wortmannin合用组, 复方丹参滴丸组85.05 mg·kg-1, 每天1次, 灌胃, 灌胃体积3 mL·kg-1。造模前15 min, wortmannin组及wortmannin合用组腹腔注射wortmannin 15 μg·kg-1, 其余各组腹腔注射生理盐水, 注射体积5 mL·kg-1。
MIRI动物模型制备 将大鼠腹腔注射10%水合氯醛(3 mL·kg-1)麻醉, 气管插管, 监测心电图变化, 左冠状动脉结扎30 min后解结扎再灌注120 min。再灌注结束后, 于左心室取血并置于含乙二胺四乙酸二钠抗凝剂的取血管中, 制备血浆置于-80 ℃冰箱, 备用; 同时取心脏并于心尖处分两部分, 分别置于-80 ℃冷冻和用4%多聚甲醛溶液固定24~48 h, 备用。
心肌细胞凋亡测定 取出4%多聚甲醛固定心脏, 采用TUNEL法检测大鼠心肌细胞的凋亡指数。凋亡指数(apoptosis index, AI), 即心肌细胞凋亡率= (凋亡心肌细胞数/心肌细胞总数)×100%[7]。
心肌组织蛋白提取及Western blot法分析 取-80 ℃保存的心脏, 称重并匀浆。按心脏重量(g) :裂解液(mL) = 1:10加入RIPA裂解液, 混匀, 冰上孵育至完全裂解, 13 000 ×g离心5 min, 取上清液即为蛋白样品。用BCA蛋白定量试剂盒计算各样品蛋白浓度。用聚丙烯酰胺凝胶电泳分离蛋白样品, 半干式转膜法转膜, 将转好的PVDF膜用BSA封闭后进行抗体孵育, 一抗、二抗分别为小鼠抗兔单克隆抗体、HRP标记的羊抗兔IgG; ECL自显影; 凝胶成像系统拍照观察Akt、p-Akt、caspase-3蛋白的表达情况[5]。
统计学分析 应用SPSS 13.0软件进行统计分析, 各统计指标以均数±标准差(x±s)表示, 两组间比较用t检验。P < 0.05为差异有统计学意义, P < 0.01为差异有显著统计学意义。
结果 1 靶点的预测通过DRAR-CPI数据库共得到324个靶点蛋白, 其中与Medline及GeneRIF数据库中心力衰竭相匹配的靶点蛋白有56个, 将56个靶点蛋白复制至DAVID数据库的列表中, 获得KEGG_PATHWAY通路注释分析结果, 与P < 0.05的注释通路相对应的靶点蛋白有28个, 见表 2。
| Table 2 Main potential target information related to heart failure in Gualou and Xiebai |
Gene ontology (GO)生物功能分析是指从生物功能上对基因产物进行标准化描述, 对基因产物进行注释, 通过GO富集分析可以了解差异基因富集的生物学功能。将28个靶点蛋白复制至DAVID数据库的列表中, 获得GOTERM_BP_DIRECT富集分析结果, 按P值大小排序, 前20个GO生物功能结果见表 3。生物学过程与激素刺激反应(response to hormone stimulus)、磷酸化(phosphorylation)和细胞凋亡调控(regulation of apoptosis)等相关性大。
| Table 3 GO biological process enrichment analysis of potential targets of active ingredients in Gualou and Xiebai |
为进一步明确28个靶点蛋白的生物学功能, 通过对信号通路进行富集分析, 可知与心力衰竭相关的通路, 包括胰岛素信号通路(insulin signaling pathway)、MAPK信号通路(MAPK signaling pathway)、细胞凋亡(apoptosis)等, P < 0.05的信号通路富集结果, 见表 4。
| Table 4 KEGG signaling pathway enrichment analysis of potential anti-heart failure targets in Gualou and Xiebai |
使用Gephi软件将筛选出来的22个瓜蒌薤白中的活性成分、28个靶点蛋白和22条信号通路构建活性成分-靶点蛋白-信号通路网络(图 1)。瓜蒌薤白中的活性成分和靶点蛋白、作用通路间存在复杂的网络关系, 瓜蒌薤白中活性成分可作用于不同的靶点蛋白, 借助不同的信号通路发挥作用。
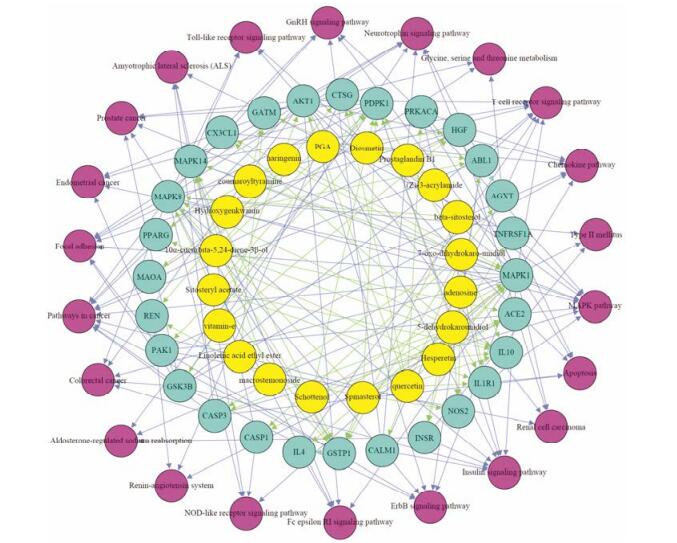
|
Figure 1 Compounds (   |
在各信号途径中, PI3K/Akt信号通路参与多个信号途径, 如细胞凋亡、趋化因子信号通路、结肠直肠癌、子宫内膜癌、ErbB信号通路、Fc-ε受体RI信号通路、黏着斑、胶质瘤、胰岛素信号通路、黑色素瘤、mTOR信号通路、神经营养素信号通路、非小细胞肺癌、癌症通路、孕酮介导的卵母细胞成熟、前列腺癌、T细胞受体信号通路、Toll样受体信号通路等。为此, 选择细胞凋亡途径中的PI3K/Akt信号通路进行生物学验证, 考察瓜蒌薤白滴丸预处理对心肌缺血-再灌注损伤大鼠心肌细胞凋亡及凋亡相关信号通路PI3K/Akt中蛋白表达的影响。
5 瓜蒌薤白滴丸对大鼠心肌缺血再灌注心肌组织细胞凋亡的影响按心肌细胞凋亡测定方法处理, 检测大鼠心肌细胞的凋亡指数。结果见图 2。统计各组凋亡指数, 结果见表 5。
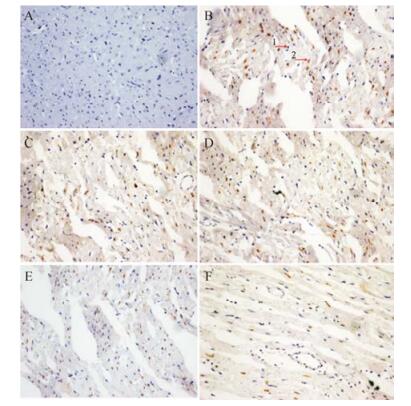
|
A: Sham operation group; B: Model group; C: Gualou-Xiebai dropping pills group; D: Wortmannin group; E: Gualou-Xiebai dropping pills + wortmannin group; F: Compound Danshen dropping pills group; 1: Normal cells; 2: Apoptotic cells Figure 2 Stained sections of Gualou Xiebai dropping pills against myocardial apoptosis induced by ischemia and reperfusion injury in rats (×200). |
| Table 5 Compare of each group myocardial apoptotic index. n = 6, x±s. *P < 0.05 vs model group; #P < 0.05 vs Gualou Xiebai dropping pills group |
与模型组比较, wortmannin组心肌细胞凋亡指数差异无统计学意义, 瓜蒌薤白滴丸心肌细胞凋亡指数显著减少(P < 0.01);与瓜蒌薤白滴丸组比较, 瓜蒌薤白滴丸与wortmannin合用组心肌细胞凋亡指数增加(P < 0.01)。
6 瓜蒌薤白滴丸对大鼠缺血再灌注心肌PI3K/Akt信号通路影响观察各组大鼠心肌缺血再灌注后caspase-3、Akt、p-Akt表达(图 3), 与假手术组比较, 模型组caspase-3的活性明显升高(P < 0.05), 提示造模成功; 与模型组比较, wortmannin组caspase-3和p-Akt/Akt表达无明显差异, 说明wortmannin对caspase-3、Akt、p-Akt表达的影响可忽略; 与模型组比较, 瓜蒌薤白滴丸组能显著抑制caspase-3的活性(P < 0.01), 激活PI3K/Akt磷酸化过程, 上调p-Akt蛋白表达水平; 与瓜蒌薤白滴丸组比较, 瓜蒌薤白滴丸与wortmannin合用组p-Akt/Akt值显著减小(P < 0.01), 提示wortmannin能阻断Akt蛋白的磷酸化过程, 抑制PI3K/Akt信号通路的激活, 促进细胞凋亡。
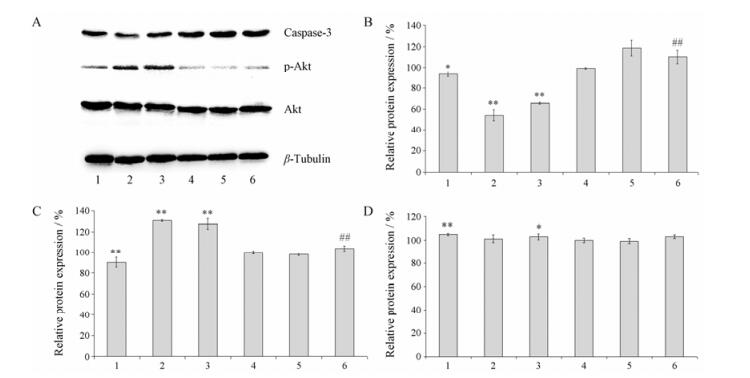
|
The protein expression of caspase-3 (B), p-Akt (C) and Akt (D) relative to β-tubulin. 1: Sham operation group; 2: Gualou-Xiebai dropping pills group; 3: Compound Danshen dropping pills group; 4: Model group; 5: Wortmannin group; 6: Gualou-Xiebai dropping pills + wortmannin group. n = 6, x±s. *P < 0.05, **P < 0.01 vs model group; ##P < 0.01 vs Gualou Xiebai dropping pills group Figure 3 The protein expressions of caspase-3, p-Akt and Akt were determined by Western blot analysis (A). |
本研究借助DRAR-CPI及DAVID等数据库, 对瓜蒌薤白中22个化合物进行网络药理学分析, 发现10α-cucurbita-5, 24-diene-3β-ol和macrostemonoside等22个化合物通过多靶点、多生物途径及多通路方式协同抗心力衰竭, 涉及激素刺激反应、磷酸化、细胞凋亡调控等生物学途径和胰岛素、MAPK、细胞凋亡等信号通路, 部分功能已有文献报道, 如瓜蒌薤白通过3种MAPKs信号通路参与抗大鼠急性心肌缺血所致的心肌损伤[8];瓜蒌薤白煎液通过抑制大鼠被激活的p38、c-Jun氨基末端激酶信号通路, 降低心肌损伤, 磷酸化过程有着重要的作用[9];此外, 瓜蒌薤白汤通过下调Fas/Fas-L的表达对抗异丙肾上腺素诱导的心肌细胞凋亡[10];通过小鼠离体MIRI模型实验证明, 瓜蒌薤白白酒汤可通过促进Akt/糖原合成酶激酶-3β磷酸化、增加Bcl-2/Bax比值、下调cleaved-caspase-3表达而抑制心肌细胞凋亡等[11]。
细胞凋亡是心肌缺血再灌注损伤的主要细胞死亡形式, 有多种基因参与。通过本文网络药理学研究可知, 瓜蒌薤白中5-dehydrokarounidiol、7-oxo- dihydrokaro-unidiol、quercetin (来自瓜蒌)及sitosteryl acetate (来自薤白) 4种成分通过调控Akt1、TNFRSF1A、IL1R1、CASP3和PRKACA等基因参与细胞凋亡过程。其中caspase-3 (CASP3)是半胱氨酸天冬氨酸蛋白酶家族中最重要的成员之一, 是细胞凋亡及级联反应的必经之路[12]。PI3K/Akt信号通路是抑制细胞凋亡的重要信号通路[13], Akt的磷酸化程度非常关键[14], 活化的Akt可激活下游靶点, 抑制CASP3导致的细胞凋亡[15]。特异性信号通路阻断剂wortmannin可抑制PI3K/Akt的磷酸化过程。
本实验结果显示, 与模型组相比, wortmannin对心肌细胞凋亡水平的影响无统计学意义, 瓜蒌薤白滴丸组可降低心肌细胞凋亡指数(P < 0.01)。与瓜蒌薤白滴丸组相比, 瓜蒌薤白滴丸与wortmannin合用组凋亡指数增加(P < 0.01), 说明wortmannin能抑制瓜蒌薤白滴丸抗心肌细胞凋亡作用。瓜蒌薤白滴丸能有效抑制大鼠急性心肌缺血-再灌注损伤时心肌中CASP3蛋白的表达, 促进Akt蛋白的磷酸化。综上, 瓜蒌薤白配伍可通过细胞凋亡调控和磷酸化等生物学途径发挥抗心力衰竭作用, 进一步验证了网络药理学的预测结果, 对于下一步深入研究瓜蒌薤白配伍抗心力衰竭的作用机制具有重要意义。
| [1] | China Pharmacopoeia Committee. Chinese Pharmacopoeia Vol Ⅰ (中国药典.一部)[S]. Beijing: China Medical Science Press, 2015: 112, 376. |
| [2] | Zou CC, Wei ML, Yan HY, et al. Effects of Gualou Xiebai dropping pills against myocardial ischemia reperfusion injury[J]. J Int Pharm Res (国际药学研究杂志), 2016, 43: 926–930. |
| [3] | Li XD, Yang YJ, Geng YJ, et al. Phosphorylation of endothelial NOS contributes to simvastatin protection against myocardial no-reflow and infarction in reperfused swine hearts: partially via the PKA signaling pathway[J]. Acta Pharmacol Sin, 2012, 33: 879–887. DOI:10.1038/aps.2012.27 |
| [4] | Wu D, Gao Y, Xiang H, et al. Exploration into mechanism of antidepressant of Bupleuri radix based on network pharmacology[J]. Acta Pharm Sin (药学学报), 2018, 53: 210–219. |
| [5] | Sun LM, Liu LF, Zhu HX, et al. Network pharmacology- based study on intervention mechanism of Huanglian Jiedu decoction in the treatment of Alzheimer's disease[J]. Acta Pharm Sin (药学学报), 2017, 52: 1268–1275. |
| [6] | Liu DL, Qu GX, Wang NL, et al. Anti-platelet aggregation constituents from Trichosanthes kirilowii[J]. Chin Tradit Herb Drugs (中草药), 2004, 35: 1334–1336. |
| [7] | Wei ML. Effects and Mechanism of Gualou Xiebai Dropping Pills on Myocardial Ischemia Reperfusion Injury Rats (瓜蒌薤白滴丸抗心肌缺血-再灌注损伤的作用及相关机制研究)[D]. Wuhu: Wannan Medical College: 2016. http://cdmd.cnki.com.cn/Article/CDMD-10368-1016152815.htm |
| [8] | Yan BW. Protective Effects of Trichosanthes Kirilowii Maxim and Allium Macrostemon Bge on Chronic Myocardial Ischemia ("瓜蒌-薤白"对慢性心肌缺血保护作用的研究)[D]. Wuhan: Hubei University of Chinese Medicine: 2013. |
| [9] | Lei Y. Study on Protective Effect of Trichosanthes Kirilowii Maxim and Allium Macrostemon Bge on Myocardial Ischemia- Reperfusion Injury in Rat ("瓜蒌-薤白"药对对大鼠抗急性心肌缺血的保护作用的研究)[D]. Wuhan: Hubei University of Chinese Medicine: 2013. |
| [10] | Ding YF, Peng YR, Shen MQ, et al. Effects of Gua Lou Xie Bai Decoction on cardiomyocyte apoptosis and apoptosis regulation gene expression[J]. J Med Mater (中药材), 2011, 34: 1922–1925. |
| [11] | Cheng J, Huang L, Kong CC, et al. Gualou Xiebai Baijiu Decoction alleviates myocardial ischemia reperfusion injury via Akt/GSK-3β signaling pathway[J]. J Shanghai Univ Trandit Chin Med (上海中医药大学学报), 2018, 32: 82–85. |
| [12] | Fan Y, Bergmann A. The cleaved-caspase-3 antibody is a marker of caspase-9-like DRONC activity in Drosophila[J]. Cell Death Differ, 2010, 17: 534–539. DOI:10.1038/cdd.2009.185 |
| [13] | Hausenloy DJ, Yellon DM. New directions for protecting the heart against ischaemia-reperfusion injury: targeting the reperfusion injury salvage kinase (RISK)-pathway[J]. Cardiovasc Res, 2004, 61: 448–460. DOI:10.1016/j.cardiores.2003.09.024 |
| [14] | McGuire VA, Gray A, Monk CE, et al. Cross talk between the Akt and p38α pathways in macrophages downstream of toll-like receptor signaling[J]. Mol Cell Biol, 2013, 33: 4152–4165. DOI:10.1128/MCB.01691-12 |
| [15] | Sussman MA, Völkers M, Fischer K, et al. Myocardial Akt: the omnipresent nexus[J]. Physiol Rev, 2011, 91: 1023–1070. DOI:10.1152/physrev.00024.2010 |
 2018, Vol. 53
2018, Vol. 53


