2. 漳州卫生职业学院, 福建 漳州 363000;
3. 西南医科大学附属中医医院, 四川 泸州 646000;
4. 四川厚德医药科技有限公司, 四川 成都 610041;
5. 江西中医药大学, 江西 南昌 330004
2. Zhangzhou Health Vocational College, Zhangzhou 363000, China;
3. Affiliated Traditional Chinese Medicine Hospital of Southwest Medical University, Luzhou 646000, China;
4. Sichuan Houde Medical Technology Co., Ltd., Chengdu 610041, China;
5. Jiangxi University of Traditional Chinese Medicine, Nanchang 330004, China
混合是固体制剂制备的关键环节。中药传统丸剂大多全粉末入药, 粉体来源复杂, 物性差异大, 属典型的复杂体系; 突出表现为粒径分布宽, 形态各异, 密度悬殊, 黏弹性不同, 树脂、多糖类药物粉碎后黏附性、凝聚性强, 油脂类粉末粉碎后油脂外溢、产生团聚, 严重影响粉体混合的均匀性。同时, 混合工艺与设备也存在一定的不适宜。与液体混合不同, 粉末由于单元间分隔度与分隔界面的存在, 无法实现分子层面的完全扩散混合, 始终存在混合与脱混两个相反的过程, 工序转换与扰动易造成相对均匀的粉末脱混离析。而混合普遍采用单一的V型、双圆锥形、二维或三维运动型设备, 以对流混合为主, 剪切为辅, 不能满足高黏性、高油性物料的混合要求。
为了解决复杂中药粉体混合均匀性难题, 提升传统丸剂的品质内涵, 课题组充分考虑原料粉体性质、粉碎混合工艺与装备作用原理, 提出以粉体微观结构设计为核心的中药粒子设计技术, 着力解决原料分散与粉层稳定2个核心问题。其工艺特征是将处方药物根据不同的粉体性质进行分类(如易粉碎原料、难粉碎原料), 在不外加物质的条件下, 控制不同类别粉体的加入顺序、振动磨工作参数等, 在微观层面构建分散均匀、结构稳定的核-壳粒子[1-3], 前期已在口腔溃疡散[4]和感咳双清分散片[5]等小复方中成功运用, 有必要验证其在大复方复杂体系中的适宜性。
小金丸出自清代王洪绪《外科证治全生集》, 是由人工麝香、当归、乳香、没药、五灵脂、制草乌、地龙、香墨、枫香脂和木鳖子10味药组成的糊丸, 为妇科临床治疗乳腺增生的首选中成药[6]。小金丸组方药味复杂而特殊, 包含贵细药、树脂树胶类药物、动物药、粪便类药物、植物药和矿物药。方中乳香、没药、枫香脂黏性强, 占处方总量29.5%;木鳖子、当归含大量油性成分, 占处方量22.1%, 导致粉体发黏结块、泛油成团; 五灵脂、地龙、制草乌、香墨等质地不同, 密度差异较大; 人工麝香用量仅占处方总量的2.94%, 又属易挥发性成分。生产实践表明, 传统工艺生产的小金丸普遍存在色泽不均, 气味差异明显, 批间差异大等问题; 甚至影响其临床疗效, 引起不良反应[7]。
为此, 本文以小金丸为载体, 以粉体色差值、黏附性、接触角和麝香酮含量均匀度为评价指标, 采用正交实验设计研究振动磨粉碎温度、壳粒子粉碎时间与复合粒子复合时间对核壳粒子成型性的影响, 筛选最优成型工艺; 另制备核壳粒子人工混合粉体及药典法制备粉体为对照, 借助粒径、色差值[8]与11个成分的含量均匀度[9-11]对制备效果进行综合评价, 以期解决小金丸混合均一性难题, 丰富中药粒子设计技术的适宜性, 形成改善复杂中药粉体均一性的共性思路、方法与技术。
材料与方法仪器 振动式药物超微粉碎机(济南倍力粉技术工程有限公司); 高速多功能粉碎机(上海冰都电器有限公司); Mastersizer 2000激光粒度仪(英国马尔文公司); DZF-6050型真空干燥箱(上海新苗医疗器械制造有限公司); ZJ型(三速)应变控制直剪仪(南京土壤仪器厂有限公司); ADCI-60-C通用型全自动测色色差计(北京辰泰克仪器技术有限公司); JY-PHb接触角测定仪(承德金和仪器制造有限公司); BT-1000粉体综合特性测试仪(丹东百特仪器有限公司); Agilent6460C三重串联四极杆液质联用仪, 配有ESI离子源, Agilent7690气相色谱仪(美国Agilent公司)。
材料 小金丸物料:酒当归饮片、醋灵脂饮片、地龙(段)饮片、制草乌饮片、香墨饮片、木鳖子、枫香脂、制乳香和制没药均购于四川科伦天然药物有限公司, 批号分别为130301、130302、130307、130301、130301、130301、130301、130305、130305。人工麝香(2013YR314) 购于北京联馨药业有限公司。麝香酮(muscone)、新乌头碱(mesaconitine, MA)、乌头碱(aconitine, AC)、次乌头碱(hypaconitine, HA)、苯甲酰新乌头原碱(benzoylmesaconitine, BMA)、苯甲酰乌头原碱(benzoylaconitine, BAC)和苯甲酰次乌头原碱(benzoylhypaconitine, BHA)购于中国食品药品检定研究院, 批号分别为110719-201014、111795-200901、111794-200901、111796-201303、110799-201106、110720-201111和110798-201106。肌苷(creatinine, Cr)购于成都植标化纯生物技术有限公司, 批号为151014。齐墩果酸(oleanolic acid, OA)、原儿茶酸(protocatechuic acid, PA)和藁本内酯(ligustilide, Lig)购于成都普瑞法科技开发有限公司, 批号分别为1506230302、15121808和15092501。以上对照品纯度均大于等于98%。淀粉:药用级, 批号20110407, 曲阜市药用辅料有限公司; 乙腈为色谱纯, 批号155758, 购于Fisher Scientific公司; 甲醇为色谱纯, 批号16051118, 购于Tedia Company; 甲酸为色谱纯, 批号2016062901, 购于成都市科隆化工试剂厂。水为蒸馏水, 购于屈臣氏集团, 批号为20160725C。
粒径测定方法 取样品3 g左右, 真空干燥4 h, 采用Mastersize 2000激光粒径测定仪测定各组样品的粒径d0.9。样品测定时间12 s, 背景时间8 s, 普通模式, 采样信号强度0.5~0.6;分散进样控制:空气压力200 kPa, 进样速度50%。
色差值测定方法 将粉体置样品盒内, 采用恒压粉体制样器将粉体制成均匀平整的平面, 将全自动色差计测量探头放在压制平整的粉体上进行测量。依CIE 1976 (L*a*b*)色度空间对颜色进行表达, 公式为dE*= [(dL*)2+(da*)2+(db*)2]1/2。其中dL*为明度差异, da*为红/绿差异, db*为黄/蓝差异, 以仪器设定公式计算色差, dE*为综合色差值[12]。
黏附性测定方法[13] 经典的表达式为库伦定律τf = σ·tanφ + c, 其中φ为内摩擦角, c为内聚力, τf为剪应力。按土工试验要求, 放入粉体样品、透水石, 同时调整量力环百分表对零, 以12 r·min-1转速依法进行剪切试验, 记录数据。
接触角测定方法[14] 测定前利用单冲压片机将粉体压制成直径13 mm, 压力为7 MPa的片子。采用视频光学接触角测定仪测定。测定时, 选择片剂的下表面作测试面, 测试液分别为蒸馏水, 每次测试液体积为50 μL, 速率为0.5 μL·s-1。固定针尖下端与片子顶端的距离约为1.5 cm, 每种粉体测5次, 待水滴在片子表面形成较固定的接触角时, 每次固定时间1 min。记录平衡接触角。
气相色谱法测定方法[15]
色谱条件 色谱柱: Rtx-1型石英毛细管柱(30 mm × 0.32 mm, 0.25 μm); 柱温采用程序升温:起始130 ℃, 10 ℃·min-1升至190 ℃, 保持14 min; 气化温度250 ℃; FID检测器温度: 280 ℃; 以氮气为载气, 流速15.0 mL·min-1; 进样量1 μL; 分流比为30:1。
对照品溶液的制备 精密称取麝香酮对照品适量, 加无水乙醇溶解得到质量浓度为19 mg·mL-1的对照品溶液。
供试品溶液的制备 取小金丸各粉体样品0.5 g, 精密称定, 精密加入无水乙醇2 mL, 称定重量, 密塞, 超声15 min, 再称定重量, 用无水乙醇补足丢失的重量, 摇匀, 静置, 取上清液滤过, 取续滤液, 即得。
粒子制备方法 将小金丸处方中的10味药材进行分类, 其中壳粒子物料为:五灵脂、地龙、制草乌、酒当归、香墨与辅料, 此类药材为易粉碎药材, 粉碎粒度对包覆效果有重要影响, 宜保证此类药材的细度, 拟作为复合粒子的壳粒子; 核粒子物料为:乳香、没药、枫香脂、木鳖子和人工麝香, 此类药材中部分药材量大, 易发黏, 是影响粉碎的重要因素, 人工麝香为处方君药, 且为小组分、具一定挥发性的贵细中药, 粉碎后的分散均匀性非常重要, 宜选为核粒子。经处方分析, 拟定出小金丸核壳结构复合粒子的粒子设计工艺路线如图 1所示。取拟设为壳粒子的易粉碎性物料:五灵脂、地龙、酒当归、制草乌、香墨与辅料; 拟作为核粒子的难粉碎性物料:乳香、没药、枫香脂、木鳖子及人工麝香, 分别置振动磨中, 混合粉碎, 定时取样, 检测粉末粒径。

|
Figure 1 The design process of composite particles of Xiaojin Pill |
粒子设计粉体制备优化实验 以色差值、黏附性、接触角(色散力与极性力)、含量均匀性(麝香酮)等评价指标, 对复合粒子制备进行优化考察。借助粉体学评价手段, 以壳粒子物料的颜色为标准对照, 测定各粉体样品的色差值, 以判断其与壳粒子的相似程度, 进而判断核/壳型粒子设计粉体是否成型; 抗剪强度是粉体黏附性的重要指标, 与物料表面性质直接相关, 考察黏附性可直接反映粉体表面壳粒子的包覆情况; 接触角不仅是液体与固体间润湿性能的表征, 而且与固体的表面自由能有关, 除物料表面粗糙情况、环境温度与湿度等条件外, 接触角的大小主要是与物料表面元素的组成与分布、杂质分布等相关, 是反映物料表面性能的重要指标, 本实验以作为表面壳粒子的易粉碎性物料为对照, 考察粒子设计后粉体表面与其相近程度。麝香为君药, 且用量极少, 以麝香酮为指标, 进行含量均一性评价, 可直观反映小金丸粉体混合均匀程度。
将物料(人工麝香除外) 置鼓风干燥箱中低温干燥至含水率达到3%以下, 将五灵脂、地龙、制草乌、香墨粉碎过3号筛, 乳香、没药、枫香脂、木鳖子、当归粉碎过1号筛, 备用。按处方比例称取五灵脂、地龙、制草乌、香墨、当归及淀粉, 置振动磨中粉碎一定时间, 采样; 然后加入乳香、没药、枫香脂、木鳖子和人工麝香, 粉碎复合一定时间, 取出, 采样。依法检测各样本的色差值、黏附性、接触角和麝香酮含量均一性。
评分分值的计算 采用综合评分法进行评价分值的计算。根据各指标对复合粒子成型及质量均一性相关程度, 拟定色差值的权重系数为0.2, 黏附性的权重系数为0.2, 接触角的权重系数为0.2, 含量均匀性(麝香酮)的权重系数为0.4。在评分前, 将各评价指标数据结果进行无量纲化处理, 以避免因各指标之间单位不同而影响对综合评分结果的贡献值, 处理方法如下。① 色差值: dEx* / dE*×100%, 其中dE*为易粉碎物料(壳粒子)量, dEx*为各样品量; ② 黏附性: φx / φs × 100%, 其中φx为各样品内摩擦角, φs为难粉碎物料(核粒子)内摩擦角; ③ 接触角: CAx / CAmin × 100%, 其中CAmin为易粉碎物料(壳粒子)接触角, CAx为各样品接触角; ④ 含量均匀性: RSDx / RSDmin × 100%, 其中RSDx为各样品RSD值, RSDmin为麝香酮含量RSD最小值。综合评分计算公式: Y = dEx* / dE × 20% + φx / φs × 20% + CAx / CAmin × 20% + RSDx / RSDmin× 40%。以综合评分分值为指标, 采用正交试验设计L9(34), 对振动磨粉碎温度、易粉碎物料粉碎时间、复合时间等3个主要影响因素进行重点考察。
小金丸复合粒子质量均一性评价 为定量描述不同小金丸粉体混合均一性, 以《中国药典》2015版一部项下制法所制备的混合粉体(药典法制备粉体)及小金丸核壳粒子人工混合粉体为对照, 对小金丸粒子设计符合粉体的质量均一性进行评价。
不同小金丸粉体的制备
小金丸药典法制备粉体 (powder prepared by Pharmacopia, PPP)的制备 按照2015版《中国药典》记载的小金丸制备方法进行制备, 即除人工麝香外, 其余9味粉碎成细粉, 将人工麝香研细, 与上述粉末配研, 过筛, 即得对照粉体。
小金丸核壳粒子人工混合粉体 (manmade mixed powder, MMP) 的制备按处方比例称取制草乌、五灵脂、地龙、当归、香墨及辅料, 置鼓风干燥箱中干燥至含水率达3%以下, 过3号筛, 置振动磨中, 在-15 ± 5 ℃下粉碎50 min, 取出细粉, 备用。按处方比例称取乳香、没药、枫香脂、木鳖子、人工麝香, 过1号筛, 置振动磨中, 粉碎3 min, 取出, 采用人工混合方式与上述细粉混合均匀, 即得。
小金丸粒子设计复合粉体 (particle designed powder, PDP)的制备 将物料(人工麝香除外)置鼓风干燥箱中干燥至含水率达到3%以下, 将五灵脂、地龙、制草乌、香墨粉碎过3号筛, 乳香、没药、枫香脂、木鳖子、当归粉碎过1号筛, 备用。按处方比例称取五灵脂、地龙、制草乌、香墨、当归及辅料等, 置振动式超微粉碎机(-15 ℃)中粉碎50 min, 然后加入乳香、没药、枫香脂、木鳖子和人工麝香等, 粉碎复合3 min, 取出, 即得。
取样方法 结合国家食品药品监督管理局颁布的《药品抽样指导原则》[16], 采用多点单次采样与同点多次采样相结合。将粉体堆成圆锥状, 分别从圆锥的上、中、下、前、后、左、右等不同部位取样, 共7个点, 再选择3个固定点取样, 共计10个取样点。
粉体学评价
粒径检查 以粉体d0.9为指标, 对3种不同小金丸粉体粒径进行检查。
色差检查 采用ADCI系列全自动色差计测定其颜色, 依CIE 1976 (L*a*b*)色度空间对颜色进行表达。以dE*为指标, 各自粉体混合物颜色的平均值为标准, 检测样品的颜色差异。
含量均匀度评价
GC法测定麝香酮含量 分别对3种小金丸粉体的麝香酮含量进行测定。
LC-MS/MS法同时测定10种化学成分含量[17] 建立HPLC-MS/MS法, 对小金丸组方活血药当归所含藁本内酯, 活血化瘀药五灵脂中原儿茶酸, 通络药地龙中肌酐, 散结消肿药木鳖子所含的齐墩果酸, 制草乌中毒性成分新乌头碱、次乌头碱、乌头碱及其解毒产物苯甲酰新乌头原碱、苯甲酰次乌头原碱和苯甲酰乌头原碱等10种成分同时进行快速分析, 比较3种小金丸粉体不同化学成分含量的均一性。按取样方法项下所述, 分别取3种小金丸粉体每份约0.3 g, 精密称定, 每种粉体取10个样。制备供试品溶液, 进行HPLC-MS/MS分析, 建立LC-MS/MS法同时测定10种成分的回归方程、相关系数、线性范围、检测线(LOD)和定量限(LOQ)。
聚类分析和主成分分析 由于11种化学成分在不同种类小金丸粉体中含量不同, 趋势也不一致, 因此采用基于欧氏距离的聚类分析和主成分分析法, 对数据进行降维处理, 观察小金丸粉体样品的分布趋势。将小金丸粉体的麝香酮气相含量测定数据和其他10种化学成分的液质含量测定数据标准化后导入MetaboAnalyst 3.0数据分析软件中, 采用Heatmap与PCA数据处理方法对3种小金丸粉体中11种化学成分含量进行系统聚类分析与主成分分析, 同时建立双标图模型对3种小金丸粉体中11种化学成分含量进行分析, 寻找差异性成分。
结果 1 分类物料的混合粉碎 1.1 易粉碎性物料根据物料入磨初始粒度研究结果, 拟设粉碎时间60 min, 结果见图 2A。由图可知, 随着粉碎时间的延长, 药材粉末粒径逐渐减小, 且粉碎时间-粒径回归方程表明, 粉碎时间与易粉碎性物料粒径呈良好的相关性。根据回归方程, 可推测物料在47.50 min时粒径可达到最小值为29.07 μm。

|
Figure 2 The time and particle size (d0.9) of the crushed material (A) and the hard to crush material (B) |
根据物料入磨初始粒度研究结果, 拟设粉碎时间为30 min, 结果见图 2B。由图可知, 粉碎时间与难粉碎性物料粒径呈良好的相关性。根据回归方程, 可推测难粉碎性物料在22.28 min时粒径可达到最小值为52.32 μm。粉碎4 min时粉碎物料的混合粉体粒径为117.85 μm。
基于机械粉碎法的核/壳型复合粒子成型原理, 核/壳型物料粒径比可保持在5:1以上, 壳粒子粒径越小可能越有利于核/壳成型。因此, 易粉碎性物料适宜粉碎时间为50 min左右, 难粉碎性物料适宜粉碎时间为4 min左右。
2 粒子设计粉体制备条件优化优化正交试验因素水平见表 1。正交试验设计结果见表 2。方差分析结果见表 3。通过直观分析, 各因素对指标的影响大小为粉碎温度(A)>粉碎时间(B)>复合时间(C)。方差分析表明, 因素A对结果具有极其显著性影响(P<0.01), 因素B具显著性影响(P<0.05), 因素C无影响。经试验优化条件为A3B2C2, 即粉碎温度-15 ℃、粉碎时间50 min和复合时间3 min。
| Table 1 The levels and factors of orthogonal test |
| Table 2 Design and results of orthogonal test. CHV: Chromatic value; ADH: Adhesiveness; COA: Contact angle; COU: Content uniformity; COS: Comprehensive score |
| Table 3 Analysis of variance |
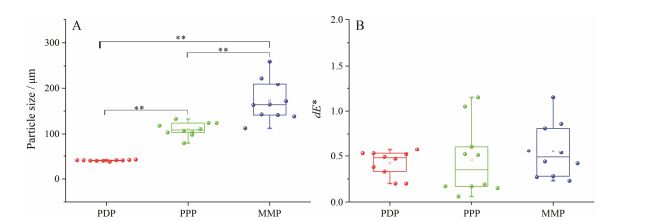
以粉体d0.9为指标, 对3种不同小金丸粉体粒径进行检查, 结果如图 3A所示。结果表明, 核壳粒子人工混合粉体粒径变化范围最大, 粒径差超过150 μm, RSD值达26.07%, 表明其粒子大小相差悬殊, 混合均匀性差。对照粉体粒径超过50 μm, RSD近15%, 其粒子大小相差明显。复合粒子粉体粒径变化范围仅为4 μm左右, RSD值3.18%, 表明其粒子大小具良好均一性。由平均粒径来看, 核壳粒子人工混合粉体远大于粒子设计复合粉体, 且明显大于药典法制备粉体。
|
Figure 3 The result of 3 different kinds of Xiaojin powder's particle diameter (A) and chroma check (B). n = 10, x± s. **P < 0.01. PDP: Particle designed powder; PPP: Powder prepared by Pharmacopia; MMP: Manmade mixed powder |
采用ADCI系列全自动色差计测定其颜色, 依CIE 1976 (L*a*b*)色度空间对颜色进行表达。以dE*为指标, 各自粉体混合物颜色的平均值为标准, 检测样品的颜色差异。结果见图 3B。由图可知, 药典法制备粉体dE*值变化范围最大, 色差差值达1.09, RSD值达84.56%, 表明其颜色波动大, 混合均匀性差。核壳粒子人工混合粉体dE*值变化范围较大, 色差差值达0.92, RSD值达53.83%, 表明其颜色波动较大, 混合均匀性较差。粒子设计粉体dE*值变化范围最小, 仅为0.38, RSD值为32.83%。由平均色差来看, 核壳粒子人工混合粉体大于药典法制备粉体, 粒子设计粉体平均色差最小。颜色的波动可反映粉体中粒子分布混合的均匀性。粒子设计复合粉体色差小, 表明其混合均匀性好。
3.3 GC法测定麝香酮含量3种小金丸粉体的麝香酮含量测定结果见图 4A。麝香酮在小金丸处方中属贵细药, 其混合均匀性对药品质量有直接影响。由图 4A可知, 以麝香酮为指标, 核壳粒子人工混合粉体RSD值最大, 为12.27%, 麝香酮含量均匀性较差。药典法制备粉体RSD值为11.29%, 略小于核壳粒子人工混合粉体。粒子设计粉体麝香酮含量RSD值最小, 为6.52%, 提示人工麝香在复合粒子粉体中的分布状态较均匀, 明显优于核壳粒子人工混合粉体与药典法制备粉体。

|
Figure 4 The differences of 11 compounds in the powder of three kinds of Xiaojin powder. A: Muscone; B: Ligustilide; C: Protocatechuic acid; D: Creatinine; E: Oleanolic acid; F: Benzoylmesaconitine; G: Benzoylhypaconitine; H: Benzoylaconitine; I: Mesaconitine; J: Hypaconitine; K: Aconitine |
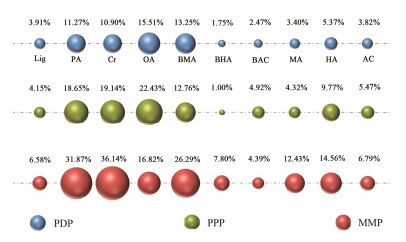
建立LC-MS/MS法同时测定10种成分的回归方程、相关系数、线性范围、LOD和LOQ如表 4所示。3种小金丸粉体中10种化合物含量的差异如图 4B~K、图 5所示。结果表明, 10种化学成分中, 粒子设计粉体有8种成分RSD值低于药典法制备粉体, 10种化学成分含量均一性均明显高于核壳粒子人工混合粉体。提示当归、五灵脂、地龙、木鳖子和制草乌5种药物在粒子设计粉体中分布状态较均匀, 而其在核壳粒子人工混合粉体中分布极不均匀, 在药典法制备粉体中分布均一性低于粒子设计粉体。表明中药粒子设计技术可以有效改善中药粉体混合均一性。
| Table 4 Regression equations, correlation coefficients, linear ranges, LOD, and LOQ of ten compounds. Lig: Ligustillide; PA: Protocatechuic acid; Cr: Creatinine; OA: Oleanolic acid; BMA: Benzoylmesaconitine; BHA: Benzoylhypaconitine; BAC: Benzoylaconitine; MA: Mesaconitine; HA: Hypaconitine; AC: Aconitine |
|
Figure 5 Comparison of RSD% among three different kinds of Xiaojin powder |
聚类分析和主成分分析对不同种类小金丸粉体中11种成分的含量测定结果进行基于欧式距离的系统聚类分析, 结果如图 6A所示。由图可见, 粒子设计粉体中有10个样本差异较小, 药典法制备粉体和核壳粒子人工混合粉体样本组间差异较大。进行PCA建模, 成分1和成分2特征值占总方差的百分比为91.8%, 表明模型可靠。图 6B为3种小金丸粉体中11种成分含量经PCA后, 主成分PC1和PC2得分图。为了使用尽量少的指标反映更多的信息, 选取前2个因子作为主成分, 代表主要的小金丸质量指标。由图 6B可见, 粒子设计粉体在主成分空间中的分布相对集中, 药典法制备粉体和核壳粒子人工混合粉体在主成分空间中的分布较为分散。由此可以解释不同种类小金丸粉体之间均一性存在差异, 进一步验证了粒子设计技术可以有效改善小金丸粉体质量均一性。双标图模型如图 6C所示, 从PCA得分图与双标图的对应关系来看, 3种小金丸粉体中粒子设计粉体麝香酮含量较高, 说明粒子设计技术可以减少挥发性组分的散失, 提高小金丸粉体的质量稳定性, 同时粒子设计粉体空间分布集中, 表明其质量均匀性较好。肌苷和齐墩果酸在部分药典法制备粉体和部分核壳粒子人工混合粉体中含量较高, 且两种小金丸粉体空间分布较分散, 表明这两种粉体质量均一性较差。

|
Figure 6 The results of 3 different kinds of Xiaojin powder's cluster analysis chart (A), PCA score plots (B) and biplots (C) |
中药粒子设计技术秉承“药辅合一”的理念[18, 19], 结合“化繁为简”的处理思路, 根据药物质地、理化性质等因素, 对药物进行分类处理, 将复杂的中药粉体体系简化为“壳粒子”物料(易粉碎物料)和“核粒子”物料(难粉碎物料)。通过控制两类物料的加入顺序、投料粒径与振动磨机械参数, 按照核壳模型, 在微观层面进行精密分散与重组, 构建分散均匀、性质稳定的重组粒子, 能有效解决复杂粉体混合均匀性差等问题。
原料分散的本质是在混合机内靠随机的相对运动进行混合, 机制包括对流混合、剪切混合和扩散混合。在混合开始阶段, 一般以对流与剪切混合为主导, 随后扩散作用逐渐增加[20]。在混合机内混合多种物料时往往伴随脱混现象, 降低混合均匀度的影响因素主要包括物料因素和设备因素:原料药性质差异是导致中药制剂成型困难的主要因素。中药原料药来源复杂, 包括植物药、动物药、矿物药和动植物的油脂及提取物(含单体成分)。且理化性质复杂多变, 质地差异较大, 呈现出粉性、油性、纤维性、黏性和脆性等质地特征。理化性质的差异导致粉碎后粒径分布范围不同、密度差异较大, 油性及黏性物料导致粉体发黏结块、泛油成团, 严重影响了中药复杂粉体混合均一性, 通过一般机械混合难以改善其粉体均一性。选用振动磨, 将粉碎与混合两个过程同时进行。振动磨是利用介质自身运动产生高强度、高频率振动, 使被粉碎物料在磨筒内受到高强度挤压、撞击和切磋能在较短时间内达到比较理想的粉碎效果。磨介之间的物料在筒体高频振动时受到正向压力与切向剪切力的作用, 同频振动使粉体的高速自转被激发, 各种粉体的运动频率趋于同步, 为复杂中药粉体的均匀复合提供了可能。
颜色是评价中药丸剂质量均一性的重要指标, 传统丸剂的制备以颜色与纹理一致性作为判断标准, 《本草蒙筌》: “其丸药中, 有各研磨者, 虽已筛细, 和诸药末, 又必重复筛过, 庶色理和同为佳”。本文采用CIE1976 (L*a*b*)色彩模式快速评价3种粉体色差, 发现粒子设计粉体dE*值小于1, 色泽基本一致; 而药典法制备粉体与人工混合粉体dE*值均在1.5以内, 有一定差异, 提示粒子设计粉体混合均匀性好。粒径分布范围的大小可直观反映粉体粒子大小均一性, 药材质地差异较大, 粉碎程度不等, 混合不均必然导致粉体粒径变化范围变大。以d0.9为指标, 对不同粉体粒径分布进行检查, 快速评价粉体混合均一性, 发现粒子设计粉体粒径分布范围与另两种粉体相比有显著性差异, 表明粒子设计能显著改善复杂中药粉体混合均一性。
本文建立GC含量测定方法对组方贵细药人工麝香中的麝香酮进行含量测定, 建立HPLC-MS/MS方法对活血药当归中的藁本内酯, 活血化瘀药五灵脂中原儿茶酸, 通络药地龙中的肌苷, 散结消肿药中的齐墩果酸, 制草乌中毒性药效成分苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱、新乌头碱、次乌头碱和乌头碱等10种成分同时进行含量测定。建立不同方法, 多角度、全方位对小金丸粉体均一性进行综合研究。
粒子设计技术通过调控粉体物性、加入顺序和工艺参数等, 使得复杂粉体实现了精密分散与稳定, 实现了质量均一化。该技术将粉碎与混合合二为一, 区别于传统混合方法, 操作简单, 生产适宜性强, 应用前景广阔, 为传统中药固体制剂精准制造提供了技术示范, 对于推动中药制剂的传承创新具有十分重要的意义。
| [1] | Han L, Zhang DK, Lin JZ, et al. Study on powder modifica-tion technology for Chinese materia characteristics[J]. Chin Tradit Herb Drugs (中草药), 2013, 44: 3253–3259. |
| [2] | Guo LW, Fu YM, Li LJ, et al. Optimal design and method of inhaled composite for complex system of Chinese materia medica[J]. Chin Tradit Herb Drugs (中草药), 2011, 42: 2165–2172. |
| [3] | Motokawa T, Makino M, Enomoto-Rogers Y, et al. Novel method of the surface modification of the microcrystalline cellulose powder with poly (isobutyl vinyl ether) using mechanochemical polymerization[J]. Adv Powder Technol, 2015, 26: 1383–1390. DOI:10.1016/j.apt.2015.07.012 |
| [4] | Zhang DK, Qin CF, Han L, et al. Effect of particle design on micromeritic property of dental ulcer powder[J]. Chin J Chin Mater Med (中国中药杂志), 2013, 38: 334–340. |
| [5] | Zhang F, Han L, Zhang DK, et al. Using mixture design to optimize preparation technology of gankeshuangqing dispersible tablets[J]. Chin Med Mat (中药材), 2014, 37: 499–503. |
| [6] | Shen HL, Zhou J. Cost-effectiveness analysis of 3 kinds of Chinese patent medicine therapeutic regimen for breast hyper-plasia[J]. Chin Pharm (中国药房), 2010, 21: 3818–3819. |
| [7] | Cai W, Chen XL, Chen XP, et al. Safety evaluation and rational use of xiaojin pills[J]. Chin Hosp Pharm (中国医院药学杂志), 2013, 33: 819–820. |
| [8] | Newkirk JW, Kriewall CS. On the current state of powder characterization[J]. Microsc Microanal, 2016, 22: 1956–1957. DOI:10.1017/S143192761601062X |
| [9] | Han L, Zhang F, Zhang DK, et al. Determination methods of content uniformity in preparations of Chinese materia medica[J]. Chin Tradit Herb Drugs (中草药), 2014, 45: 2125–2331. |
| [10] | Zhu GX, Wu CW, Liang SW, et al. Advance research of digitalization in quality of Chinese medicine[J]. Chin J Exp Tradit Med Formulae (中国实验方剂学杂志), 2016, 22: 225–229. |
| [11] | Cai B, Dong LY, Wang J, et al. Simultaneous determination of seven components in Xiaojin Pills by UPLC-MS[J]. Chin Pharm J (中国药学杂志), 2015, 50: 718–721. |
| [12] | Wu D, Sun DW. Colour measurements by computer vision for food quality control-a review[J]. Trends Food Sci Technol, 2013, 29: 5–20. DOI:10.1016/j.tifs.2012.08.004 |
| [13] | Gao Y, Hong YL, Xian JC, et al. Evaluating method of the characteristic physical properties of the wetting mass using texture analyser[J]. Acta Pharm Sin (药学学报), 2012, 47: 1049–1054. |
| [14] | Zhang DK, Lin JZ, Liu JY, et al. Powder modification tech-nology used for the preparation of the hydrophilic decoction pieces of indigo naturalis and the modification principle[J]. Acta Pharm Sin (药学学报), 2013, 48: 1148–1155. |
| [15] | He Y, Lu J, Zhang Y, et al. Quality control of valuable medicines in Dahuoluo pills[J]. Chin J Pharm Ana (药物分析杂志), 2016, 36: 1287–1292. |
| [16] | Geng DS. Discussion on definition of the sample size in the drug sampling[J]. Chin Pharm Aff (中国药事), 2011, 25: 1104–1105. |
| [17] | Xiong X, Pan Y, Zhang T, et al. Consistency evaluation for commercially Xiaojin pills using determination of multi-component contents by HPLC-MS/MS method coupled with chemometrics[J]. Chin Tradit Herb Drugs (中草药), 2017, 48: 2189–2196. |
| [18] | Yang M, Han L, Yang S, et al. Particles design technology for Chinese materia medica based on characteristics of tradi-tional pill and powder[J]. Chin Tradit Herb Drugs (中草药), 2012, 43: 9–14. |
| [19] | Zhang DK, Fu CM, Lin JZ, et al. Study on theory and application value of "unification of medicines and excipients" in Chinese materia medica preparations[J]. Chin Tradit Herb Drugs (中草药), 2017, 48: 1921–1929. |
| [20] | Cai GX. Chinese Medicine Powder Engineering (中药粉体学工程)[M]. Beijing: People's House, 2008: 1-3. |
 2017, Vol. 52
2017, Vol. 52


