中药原料的吸湿性严重影响中药固体制剂生产研发的各个环节, 如中药固体制剂的处方筛选[1]、工艺优化[2]、产品的包装和储藏[3]等。中药原料在生产过程中如制粒、压片和储存等, 中药原料或中药制剂均可能和水分接触后吸湿并影响其物理化学属性如流动性、压缩成形性甚至有效成分的溶出等。
中药原料的吸湿过程主要取决于中药原料的表面性质、蒸汽压及环境的温湿度等因素。当中药原料暴露于外界环境中, 水分通过氢键的作用和中药原料表面的亲水性基团结合, 随着吸湿量的逐渐增大, 水分逐渐在中药原料的表面形成单分子饱和吸附[4], 并逐步形成多分子层吸附向中药原料的内部扩散, 直至达到吸湿平衡。因此, 在中药原料中的水分可以分为以下3类:自由水、结合水和非结合水。
吸湿等温线是研究中药原料吸湿性的常用工具之一。描述了在恒定温度条件下, 平衡吸湿量与环境相对湿度或水分活度之间的关系, 通过吸湿等温线可以预测物料在某温湿度下的吸湿量。吸湿等温线通常可以应用数学模型模拟, 常用的数学模型主要有3类:动力学模型(BET模型、GAB模型)、半经验模型(Halsey模型、Ferro-Fontan模型)、经验模型(Oswin模型)[5]。
动态水蒸气吸附法是测定固体物料吸湿等温线的常用方法, 通过程序改变测定环境的相对湿度, 测定物料在每个相对湿度的平衡吸湿量绘制其吸湿等温线。本文以葛根提取物为研究对象, 通过动态水分吸附的方法研究中药原料的吸湿性并分析吸湿性对压缩成形性的影响。
材料与方法材料与仪器 葛根提取物(PLR, 批号: 20150903, 华润三九药业股份有限公司惠赠), 微晶纤维素(Avicel PH102, FMC公司惠赠)。样品动态水分吸附仪(SPS23-100n, 德国ProUmid公司)、感应式压片机(XP1, 德国Korsch AG公司), 片剂硬度仪HT 10 (瑞士SOTAX公司)。
吸湿等温线测定 利用DVS Advantage 1动态水蒸气吸附仪测定单个样品的吸湿等温线, 测定过程中通过混合不同比例含湿氮气与干燥氮气控制湿度的环境。待测样品首先置于相对湿度为0的环境中脱湿, 并作为参比质量, 随后样品以5%的湿度梯度程序变化湿度进行吸湿和解吸, 并设定平衡条件为在10 min内质量随时间的变化率(dm/dt)不大于0.002 mg·min-1。
吸湿等温线的数学模拟 中药提取物在298、308和318 K的吸湿等温数据分别用表 1中的数学模型通过Origin Pro 9.0 (OriginLab Corporation)进行非线性回归, 模型的拟合优度分别用校正决定系数(Radj2)和模型的均方根误差(RMSE)表示, 校正决定系数越大, 均方根误差越小, 模型的拟合效果越好。
| Table 1 The models applied to describe moisture adsorption experimental data |
吸湿热力学参数的计算 通过对物料吸湿等温线的模拟与分析得到其吸湿热力学参数如吸湿焓、吸湿熵和吉布斯自由能, 可以用于优化其浓缩干燥条件及预测其吸湿行为。其中, 焓主要表征在吸湿过程中水分子和物料之间相互作用引起的能量变化; 熵作为衡量体系混乱程度的一个热力学参数, 主要与水分子和物料分子之间的相互作用力的强弱有关; 而吉布斯自由能主要表征物料对水分子的亲和力并判断吸湿过程是否为自发过程。
吸附焓(ΔH)是表征表面非均匀性的一个重要参数, 是指吸附热和纯水的汽化热的差值, 其数值通常为一个常数, 不随吸附量增加而变化[6]。当达到吸湿平衡时, 物料的含水量不随时间变化, 假设吸附热不随温度的变化而变化, 则该物料的吸附焓可以通过克-克方程(5) 计算得到。
| $ \frac{\partial \rm{ln}\left( {{\mathit{a}}_{\mathit{w}}} \right)}{\partial \rm{ln}\left( 1/\mathit{T} \right)}=-\frac{\Delta \mathit{H}}{\rm{R}} $ | (5) |
其中, aw为相对湿度, T(K)为绝对温度, R为气体常数(8.314 KJ·mol-1·K-1)。通过吸湿等温模型计算得到物料在不同温度、不同平衡吸湿量(EMC)时的水分活度, 并对ln(aw)和1/T进行线性回归, 则直线的斜率为
吸附熵(ΔS)与物料的表面覆盖率相关, 随着吸湿量的变化而变化。在物理化学上, 熵代表吸湿体系内部的混乱程度。吸附熵与吸附热之间满足吉布斯-赫姆霍兹方程如式(6)。
| $ \Delta G=\Delta H-T\Delta S $ | (6) |
其中, ΔG为体系的吉布斯自由能, 对于吸湿平衡体系而言, 温度是恒定不变的。则式(6) 可以变形为式(7) 即,
| $ \Delta G=-\rm{R}\mathit{T}\rm{ln}\left( {{\mathit{a}}_{\mathit{w}}} \right) $ | (7) |
则ln(aw) = -ΔH/T +ΔS/R, 因此, 对ln(aw)和1/T进行线性回归, 则直线的截距为
焓熵补偿现象[7]本质上是指一组相关实验的焓变和熵变之间存在明显的线性相关关系, 即
| $ \Delta H=a+b\Delta S $ | (8) |
其中, a, b为常数, b通常称为等速温度(TB)。调和温度(Thm)为研究温度的调和平均值, 即
| $ {{\mathit{T}}_{\mathit{hm}}}=\frac{N}{\sum\nolimits_{i=1}^{N}{\left( 1/\mathit{T} \right)}} $ | (9) |
其中, N为研究所使用的吸湿等温线的数量, T为绝对温度(K)。
片剂的制备 取吸湿后的葛根提取物与微晶纤维素(PH102) 按3: 1的比例混合均匀后, 取粉末约0.3 g, 精密称定重量, 填充于压片机的冲模内, 压制成直径为8.5 mm的平片。
压缩成形性的评价 压缩成形性是指被压制成形的可能性和被压缩物的坚实紧密程度。目前衡量压缩成形性的常用方法是在一定的压力下测定压缩粉体所形成的片剂的硬度。但是, 片剂的硬度并不能反映成形过程中粉体形变的压缩特性。因此, 评价粉体的压缩成形性时, 还要考虑其抗张强度、弹性复原、黏弹性斜率和屈服压力等参数, 用以表征在压缩过程中的形变过程。
抗张强度 片剂的抗张强度是直接反映粉体结合性及片剂结合力的最终参数, 不仅可以评价片剂质量, 而且广泛应用于片剂处方设计中。由于抗张强度的计算公式(10) 包含了片剂的直径及厚度, 因而克服了不同片剂差异产生的偏差。
| $ \rm{TS=}\frac{2{{\mathit{f}}_{\mathit{c}}}}{2\pi \mathit{dh}} $ | (10) |
其中, TS为抗张强度(MPa), fc为硬度(N), d为片径(mm), h为片厚(mm)。
一般认为, 如果用较小的压力能获得较大的片剂硬度时, 表明该粉体的压缩成形性较好。
弹性复原率 在压缩过程中, 当解除压力并将片剂推出模孔后, 由于内应力作用, 使片剂发生弹性膨胀, 称为弹性后效。通常用弹性复原率(E)表示, 即片剂从模孔中推出后引起的体积增加值和片剂在最大压力下的体积之比, 可用下式表示:
| $ E=\frac{{{H}_{0}}-H}{{{H}_{0}}}\times 100\% $ | (11) |
其中, H为片剂推出后放置24 h的厚度(mm), H0为最大压力下片剂的厚度(mm)。
由于粉体的塑性反映了片剂成型过程中保持一定形状的能力, 但不能确切表明粉体一定能结合成致密和破碎力较高的压实体, 而弹性复原率则可说明粉体克服其弹性彼此结合成型的能力, 因此粉体弹性复原率越大, 片剂的结合力越弱, 硬度降低, 甚至易于裂片。
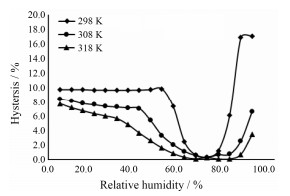
结果与讨论 1 吸湿等温线葛根提取物在298、308和318 K时的吸湿等温线测定结果见图 1。葛根提取物的吸湿等温线均存在不同程度的迟滞现象, 而且在298 K时的迟滞显著大于其他两个温度, 见图 2。迟滞现象说明, 葛根提取物吸湿过程并不是一个完全可逆的过程[8]。对于物料在吸附过程中的迟滞现象形成的主要原因可以分别从物料的化学组成和微观结构两个方面解释。在化学组成方面, 由于在吸湿的过程中存在水溶性或亲水性的高分子物质, 其分子链段在溶胀作用下不断延展, 因此有更多的吸湿位点暴露在湿空气中, 而在解吸附阶段, 由于高分子的失水, 其分子链段蜷缩部分水分被包裹在其中, 不能发生脱附[9]。此外, 也有研究认为由于大分子物质在吸湿后发生耦合扩散-弛豫[10]及玻璃化转变温度降低[11]均可能造成吸湿等温线迟滞现象; 在微观结构分析方面, 在干燥过程中, 形成了很多的空隙, 其中有大孔、介孔和微孔, 因此形成了“墨水瓶”效应[12]。在吸湿过程中, 由于环境湿度不断增大, 在毛细管作用下水分通过微孔进入大孔和介孔中; 而在解吸附的过程中, 环境的湿度不断降低, 被吸附进入“墨水瓶”内部的水分很难通过瓶颈(微孔)发生脱附, 则表现为在吸湿等温线上脱附曲线位于吸附曲线的上方。

|
Figure 1 The sorption-desorption profiles of extracts of Puerariae Lobatae Radix (PLR) at 298 K (a), 308 K (b) and 318 K (c) |
|
Figure 2 The hysteresis of PLR at 298 K, 308 K and 318 K |
将葛根提取物在3个温度条件下的吸湿数据分别应用GAB、Ferro-Fontan、Halsey和Oswin模型拟合, 拟合结果见表 2。结果表明, 4个模型对于葛根提取物吸湿行为的模拟效果依次为GAB、Ferro-Fontan、Oswin和Halsey, 其中GAB模型和Ferro-Fontan模型对其吸湿行为的拟合效果相当。因为在不同环境湿度条件下物料和水分之间作用关系的复杂性, 目前还没有一个吸湿等温模型能够对所有湿度条件的吸湿量和环境湿度的关系进行模拟。同时, 文献[13]研究表明, 物料的吸湿等温线可以同时应用多个模型进行模拟。
| Table 2 Calculated values of model parameters obtained from analysis of moisture sorption isotherms |
通过Ferro-Fontan模型计算葛根提取物在298、308和318 K不同含水量下的水分活度, 并将ln(aw)对1/T进行线性回归, 通过回归方程的斜率和截距计算吸湿过程的焓变和熵变, 结果见图 3。从图中可以看出, 随着吸湿过程中含水量的增加, 吸附焓和熵呈现减小的趋势。由于葛根提取物其化学组成复杂, 造成这种现象的原因可能是在吸湿开始时, 存在大量的高能级活性位点可供水分子吸附, 随着吸湿时间的延长, 这些位点被逐渐占据, 水分子开始被低能级活性位点吸附, 因而吸附热逐渐减少[14]。

|
Figure 3 Enthalpy (a) and entropy (b) as a function of moisture content |
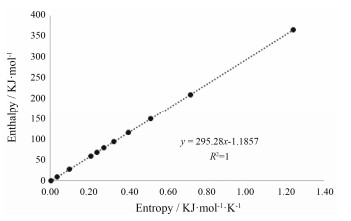
从图 4可以看出, 在所研究的湿度范围内, 样品的焓变和熵变呈现良好的线性关系, 并且在吸湿过程中存在明显的焓熵补偿, 其等速温度小于研究的调和温度307.78 K[15], 表明吸湿过程主要来自熵驱动, 即相对于其复杂的化学组成而言, 粉末的微观结构是影响其吸湿性的主要因素[16]; 对于多孔性不定型物料的吸湿过程而言, 影响其吸湿行为的因素主要有① 水分沿孔径方向的扩散; ② 水分向孔洞(微孔)内部的扩散[17], 当水分向孔洞内部扩散成为整个吸湿过程的限速步骤时, 大量的水分在孔洞的入口处累积, 进而由于毛细管效应或表面吸附被吸附进入孔洞, 则整个吸湿过程表现为熵驱动过程[18]。
|
Figure 4 Enthalpy-entropy relationship for water adsorption in PLR |
样品的吉布斯自由能变随吸湿过程的进展含水量增加而减少, 如图 5, 说明其吸湿是一个自发过程, 在吸湿的初始阶段, 物料的含水量较低, 存在较多的吸附位点可供水分子吸附, 其吉布斯自由能较高。因此, 随着吸湿温度的降低, 含水量的增加, 其吉布斯自由能减少。

|
Figure 5 Gibbs free energy of adsorption at 298 K (a), 308 K (b) and 318 K (c) as a function of moisture content |
吸湿后分别取不同含水量的粉末按“片剂的制备”项下方法于不同压力和转速下压片, 其抗张强度随含水量、压片力和压片速度的变化, 见图 6。

|
Figure 6 Three-dimensional plots of compress pressure (a) and compress speed (b) on the compaction of PLR of different moisture content |
从结果可知, 随提取物的吸湿、含水量增加, 其抗张强度增加, 弹性复原率下降。而且随压片力的增加, 压片速度的减少, 其成型能力增强。但是, 当含水量不断增加, 其成型能力对压力和压片速度的敏感性逐渐减小, 直至最终由于含水量过大发生粘冲不能成型。说明当中药原料的吸湿控制在一定程度时, 其吸收的水分在一定程度上有助于成型, 主要原因在于适量的水分可以在中药原料的颗粒中间发挥润滑剂的作用, 有助于颗粒之间的自由流动。同时, 当外力作用于颗粒时, 颗粒间的水分可以发挥液体桥的作用, 有助于颗粒之间的黏结成型。
结论本文通过动态水蒸气吸附的方法测定了葛根提取物的吸湿等温线, 分析了其吸湿行为及吸湿对压缩成形性的影响。结果表明, 中药原料的吸湿过程可以应用GAB模型或Ferro-Fontan模型模拟, 其吸湿过程是一个放热过程, 在研究的温度范围内(298~318 K)属于熵驱动过程。当吸湿量较小时, 由于吸湿而引入的水分有利于其压缩成形, 但过量水分的存在, 将会对其压片过程造成困扰。
| [1] | Jiang YR, Zhang ZH, Jia XB. Preparation and application on compound excipient of sodium stearyl fumarate and plasdone S-630[J]. Acta Pharm Sin (药学学报), 2013, 48: 125–130. |
| [2] | Zeng RG, Jiang QY, Liao ZG, et al. Improvement of powder flowability and hygroscopicity of traditional Chinese medicine extract by surface coating modification technology[J]. China J Chin Mater Med (中国中药杂志), 2016, 41: 2245–2249. |
| [3] | Mubalake YJ, He B, Dilinuer A. Investigation on the stability of Xuanfeiqingre granules in different packaging materials[J]. J Xinjiang Med Univ (新疆医科大学学报), 2009, 32: 1240–1243. |
| [4] | Hancock BC, Shamblin SL. Water vapour sorption by pharmaceutical sugars[J]. Pharm Sci Technol Today, 1998, 1: 345–351. DOI:10.1016/S1461-5347(98)00088-1 |
| [5] | Al-Muhtaseb AH, Hararah MA, Megahey EK, et al. Moisture adsorption isotherms of microwave-baked madeira cake[J]. LWT-Food Sci Technol, 2010, 43: 1042–1049. DOI:10.1016/j.lwt.2010.01.003 |
| [6] | Tsami E. Net isosteric heat of sorption in dried fruits[J]. J Food Eng, 1991, 14: 327–335. DOI:10.1016/0260-8774(91)90022-K |
| [7] | Polachini TC, Betiol LFL, Lopes-Filho JF, et al. Water adsorption isotherms and thermodynamic properties of cassava bagasse[J]. Thermochim Acta, 2016, 632: 79–85. DOI:10.1016/j.tca.2016.03.032 |
| [8] | Al-Muhtaseb AH, Mcminn WAM, Magee TRA. Water sorption isotherms of starch powders. Part 1:mathematical description of experimental data[J]. J Food Engineer, 2004, 61: 297–307. DOI:10.1016/S0260-8774(03)00133-X |
| [9] | Shah U, Augsburger L. Evaluation of the functional equivalence of crospovidone NF from different sources. Ⅰ. Physical characterization[J]. Pharm Dev Technol, 2001, 6: 39–51. DOI:10.1081/PDT-100000012 |
| [10] | Watt IC. Adsorption-desorption hysteresis in polymers[J]. J Macromol Sci Chem, 1980, 14: 245–255. DOI:10.1080/00222338008066635 |
| [11] | Saripella KK, Mallipeddi R, Neau SH. Crospovidone Interactions with Water. Ⅰ. Calorimetric study of the effect of polyplasdone particle size on its uptake and distribution of water[J]. J Pharm Sci, 2014, 103: 669–675. DOI:10.1002/jps.23846 |
| [12] | Miguel YD, Rohr T, Sherrington DC. Structure, morphology, physical formats and characterization of polymer supports[M]//Buchmeister, MR (Ed.). Polymeric Materials in Organic Synthesis and Catalysis. Weinheim:Wiley-VCH. Verlag GmbH & Co. KGaA, 2003:1-52. |
| [13] | Lomauro CJ, Bakshi AS, Labuza TP. Evaluation of food moisture sorption isotherm equations. Part Ⅱ:milk, coffee, tea, nuts, oilseeds, spices and starchy foods[J]. LWT-Food Sci Technol, 1985, 18: 118–124. |
| [14] | Kumar AJ, Singh RRB, Patil GR, et al. Effect of temperature on moisture desorption isotherms of kheer[J]. LWT-Food Sci Technol, 2005, 38: 303–310. DOI:10.1016/j.lwt.2003.10.009 |
| [15] | Telis-Romero J, Kohayakawa MN, Silveira V Jr, et al. Enthalpy-entropy compensation based on isotherms of mango[J]. Ciênc Tecnol Aliment, 2005, 25: 297–303. DOI:10.1590/S0101-20612005000200020 |
| [16] | ViganÓ J, Azuara E, Telis VRN, et al. Role of enthalpy and entropy in moisture sorption behavior of pineapple pulp powder produced by different drying methods[J]. Thermochim Acta, 2012, 528: 63–71. DOI:10.1016/j.tca.2011.11.011 |
| [17] | Rao MB, Jenkins RG, Steele WA. Potential functions for diffusive motion in carbon molecular sieves[J]. Langmuir, 1985, 1: 137–141. DOI:10.1021/la00061a024 |
| [18] | Fletcher AJ, Thomas KM. Compensation effect for the kinetics of adsorption/desorption of gases/vapors on microporous carbon materials[J]. Langmuir, 2000, 16: 6253–6266. DOI:10.1021/la9916528 |
 2017, Vol. 52
2017, Vol. 52


