2. 福建医科大学药学院, 福建 福州 350108;
3. 厦门大学医学院, 福建 厦门 360000
2. College of Pharmacy, Fujian Medical University, Fuzhou 350108, China;
3. Medical College, Xiamen University, Xiamen 360000, China
西罗莫司(sirolimus, SRL), 又名雷帕霉素, 是一种新型的免疫抑制剂, 在抗排斥作用和延长移植物存活的能力方面有较强作用, 临床上可用于器官移植抗排异作用和治疗类风湿性关节炎、红斑狼疮和牛皮癣等自身免疫性疾病[1, 2]。但由于SRL在水中的溶解度较小, 属于BCSⅡ类药物, 口服生物利用度只有14%~31%, 在很大程度上影响了其疗效的发挥。因此改善其溶解度及溶出性能, 是提高生物利用度的关键。
自微乳化给药系统(self-microemulsifying drug delivery system, SMEDDS)是一种提高水难溶性药物溶解度的有效方法[3, 4]。自微乳化给药系统通常由油相、乳化剂和助乳化剂组成, 遇水自发形成粒径小于300 nm的纳米乳。市售产品如Sandimmun Neoral、Norvir和Fortovase都是由自微乳化给药系统构成的。由于自微乳是黏稠的液体, 不易运输、贮存和使用, 且几乎所有的SMEDDS制剂均以浓缩液的形式灌封于软胶囊中。软胶囊胶壳处方中含有一定量的水分, 而SMEDDS中含有大量表面活性剂, 这些成分在贮存过程中不断夺取胶壳水分, 最终导致胶壳变硬, 影响其崩解和自微乳化效果[5, 6]。因而, 将自微乳固化就显得尤为重要。
介孔二氧化硅纳米粒(mesoporous silica nanoparticles, MSN), 由于其较高的孔隙率、良好的生物相容性、可调节的孔径、较大的比表面积及较好的稳定性, 可以通过多种不同的载药方法将难溶性药物通过一定的方式吸附在材料的表面及材料孔道内部, 使药物分子以无定形或非晶体形态存在, 从而在一定程度上有效地提高药物的溶解度或溶出度, 近几年来已逐渐成为药物载体的研究热点[7-9]。SBA-15是一种最为常见的MSN。SBA-15较一般的MSN具有更大的可调节孔径(5~30 nm)和更厚的孔壁, 拥有连续的孔道、更强的物理稳定性, 且孔道之间有微孔相连接[10]。通过查阅相关国内外文献, 发现利用SBA-15作为SMEDDS的吸附剂的研究还鲜有报道。因此, 本文拟采用搅拌法, 使用SBA-15对自微乳进行固化, 并考察不同孔径的SBA-15对药物释放的影响。
材料与方法试剂 西罗莫司对照品(批号060425, 含量99.9%)、西罗莫司原料药(批号060702, 含量99.5%) (福建科瑞药业有限公司); 油酸聚乙二醇甘油酯(Labrafil M1944CS)、二乙二醇单乙基醚(Transcutol HP) (法国Gattefosse公司); 聚氧乙烯-35-蓖麻油(Cremophor EL, 德国BASF公司); 聚环氧乙烷-聚环氧丙烷-聚环氧乙烷三嵌段共聚物(P123, 美国Sigma-Aldrich公司); 硅酸四乙酯(TEOS, 上海阿拉丁试剂公司); 盐酸、乙腈、甲醇、乙醇(天津化工有限公司), 所用试剂均为色谱纯。
主要仪器 Agilent 1200型高效液相色谱仪(UV检测器, 美国Agilent公司); Nicomp 380粒径测定仪(美国PSS公司); Nova NanoSEM 230型扫描电子显微镜(荷兰飞利浦公司); JEOL 2010透射电子显微镜(日本电子株式会社); Rigaku Dmax-3CX射线粉末衍射仪(日本Rigaku公司); Tristar Ⅱ 3020吸附仪(美国Micromeritics公司); TA-Q20差示扫描量热仪(美国TA公司); 药物溶出度仪RCZ-6B2 (上海黄海药检仪器有限公司)。
色谱条件 色谱柱: Eclipse XDB-C18 (150 mm × 4.6 mm, 5 μm, 美国Agilent公司)。流动相:乙腈-甲醇-水(45:34:21), 流速: 1 mL·min-1, 检测波长: 278 nm; 柱温: 50 ℃; 进样量: 20 μL。理论塔板数为1998, 分离度为2.11。该方法具专属性、灵敏和简便, 可满足SRL制剂质量控制的需要。
检测波长的确定 精密称取SRL对照品适量, 按紫外分光光度法在200~400 nm内进行扫描。
方法专属性考察 称取SRL原料药适量, 置100 mL量瓶中, 加流动相适量至刻度, 摇匀, 精密量取1.0 mL至10 mL量瓶中加流动相稀释, 摇匀, 即得供试品溶液。同法配制对照品溶液。
线性关系考察 精密称取SRL对照品适量, 配制成2、4、8、12、16和20 μg·mL-1对照品溶液。0.45 μm微孔滤膜滤过, 续滤液进样。以浓度(C, µg·mL-1)为横坐标, 峰面积(A)为纵坐标, 进行回归方程。
方法精密度考察 称取SRL适量, 分别配制质量浓度为8、10和12 μg·mL-1溶液, 每个浓度连续进样5次, 得日内精密度; 再连续5日进样测定, 得日间精密度。
西罗莫司自微乳(SRL-SMEDDS)的制备与表征 SRL-SMEDDS的制备基于前期课题组的处方及实验步骤[11], 并进行了少许改动, 具体操作如下:精密称取SRL粉末1 g, 加入助乳化剂Transcutol HP 19 g中, 不断搅拌直至溶解, 再加入油相Labrafil M1944CS 22 g及乳化剂Cremophor EL 38 g, 不断搅拌至淡黄色澄清溶液, 即得SRL-SMEDDS。
取SRL-SMEDDS 0.5 mL加入50 mL超纯水中, 室温下以50 r·min-1的速度搅拌。将完全形成自微乳的时间记作自微乳化时间, 并使用Nicomp 380粒径测定仪测定其粒径及多分散指数(polydispersity index, PDI)。
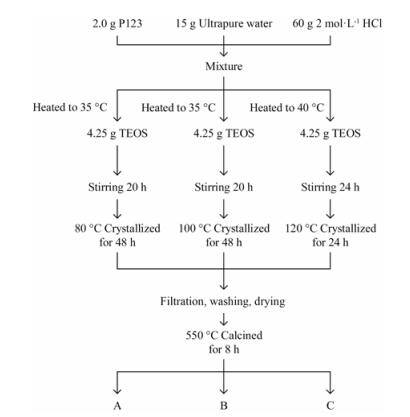
不同孔径大小的SBA-15的制备与表征 SBA-15的合成采用Zhao等[10]的方法:首先称取P123 (2.0 g)溶于15 g超纯水及60 g的2 mol·L-1 HCl中。搅拌均匀后, 将反应体系加热至35 ℃, 并加入TEOS 4.25 g, 随后搅拌20 h。反应结束后在80 ℃下晶化48 h。待样品冷却至室温后, 过滤、洗涤, 45 ℃干燥12 h。再将新合成的样品置于马弗炉中, 550 ℃煅烧8 h, 即得孔径为6.3 nm的SBA-15, 命名为SBA-15 (6.3);调节反应温度为35 ℃反应20 h, 随后升温至100 ℃晶化48 h, 反应步骤及其他反应条件相同, 得孔径为8.1 nm的SBA-15, 命名为SBA-15 (8.1);调节反应温度为40 ℃反应24 h, 随后升温至120 ℃晶化24 h, 反应步骤及其他反应条件相同, 得孔径为10.8 nm的SBA-15, 命名为SBA-15 (10.8)。制备流程图如图 1所示。
|
Figure 1 Preparation of different pore size of mesoporous silica nanoparticles (SBA-15). A: SBA-15 (6.3); B: SBA-15 (8.1); C: SBA-15 (10.8) |
扫描电子显微镜(scanning electron microscope, SEM)和透射电子显微镜(transmission electron microscope, TEM)分别使用Nova NanoSEM 230型扫描电镜及JEOL 2010型透射电镜拍摄; 小角度X-射线衍射(small angle X-ray diffraction, SAXD)测定使用Rigaku Dmax-3CX射线粉末衍射仪测定; 氮气吸附-脱附等温曲线采用Tristar Ⅱ 3020吸附仪在77 K条件下测得, 采用BET法方法计算样品的比表面积, 采用BJH模型计算孔容和孔径。
载西罗莫司自微乳SBA-15 (SRL-SMEDDS-SBA-15) 的制备与表征 采用搅拌法:称取SBA-15 (1 g), 将不同比例的SRL-SMEDDS逐滴加入其中, 边加边搅拌。待加入完毕后, 于干燥器中放置过夜, 确保吸附完全, 即得SRL-SMEDDS-SBA-15。
将一定量的SRL-SMEDDS-SBA-15分散于0.4%SDS中, 持续超声30 min, 所得溶液于10 000 r·min-1离心10 min, 取上清液, 过0.22 μm微孔滤膜后, 按上述“色谱条件”进样分析, 计算SRL-SMEDDS-SBA-15载药量。

|
通过测定SBA-15与SRL-SMEDDS-SBA-15的休止角(angle of repose)、压缩度(compressibility index)及豪斯纳比(Hausner ratio), 考察粉末的流动性。使用差示扫描量热法(differential scanning calorimetry, DSC), 对SRL、SBA-15、物理混合物及SRL-SMEDDS-SBA-15进行表征。
重分散实验 称取含有0.75 g SRL-SMEDDS的SRL-SMEDDS-SBA-15 (6.3)、SRL-SMEDDS-SBA-15 (8.1) 和SRL-SMEDDS-SBA-15 (10.8), 分别加到50 mL超纯水中, 于50 r·min-1的速度搅拌。待溶液基本均匀时, 于干燥器中室温放置24 h, 上清液使用Nicomp 380粒径测定仪测定粒径。
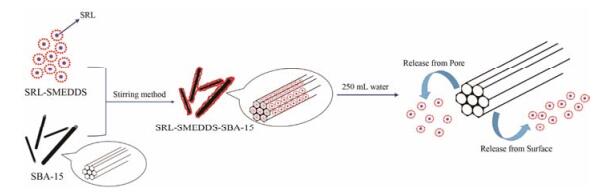
体外释放度的测定 SRL-SMEDDS-SBA-15的体外溶出方法采用2015年中国药典(第四部)小杯法。称取SRL原料药1 mg及含1 mg SRL的市售片剂雷帕鸣以SRL-SMEDDS-SBA-15 (6.3)、SRL-SMEDDS-SBA-15 (8.1) 和SRL-SMEDDS-SBA-15 (10.8) 填充胶囊, 以250 mL水为溶出介质, 反应条件为37 ℃, 75 r·min-1。于5、10、15、20、30、45、60、90和120 min取样1 mL, 并补充等量释放介质。样品经10 000 r·min-1离心10 min后过0.22 μm微孔滤膜, 使用上述“色谱条件”进样分析。SRL-SMEDDS-SBA-15的制备及溶出机制见图 2。
|
Figure 2 Mechanism of the preparation and release of SRL-SMEDDS-SBA-15. SRL: Sirolimus; SMEDDS: Self-microemulsifying drug delivery system |
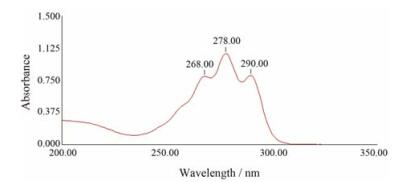
SRL在278 nm处有最大紫外吸收, 结果如图 3。因此, 选择278 nm作为检测波长。
|
Figure 3 The ultraviolet spectrum of SRL |
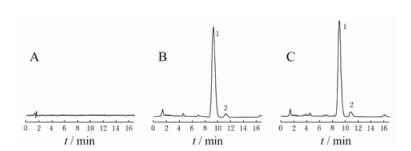
所得色谱图见图 4。结果表明, 空白溶剂对SRL的测定无干扰, 方法专属性较好。
|
Figure 4 High performance liquid chromatogram of SRL. A: Blank; B: Standard; C: Sample; 1: SRL; 2: SRL isomer |
在本色谱条件下, SRL在2~20 µg·mL-1内峰面积与测定浓度线性关系良好。回归方程为:
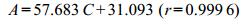
|
低、中、高浓度的日内精密度分别为0.70%、0.55%、0.47%, 低、中、高浓度的日间精密度分别为0.65%、0.55%、0.36%, 所有值均小于2 %, 说明精密度良好。
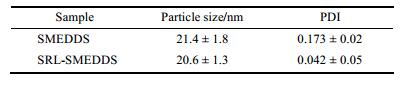
2 SRL-SMEDDS的表征空白自微乳及载SRL自微乳的粒径及PDI见表 1。药物的加入对自微乳化效果影响不大, 甚至在一定程度上更有利于自微乳的形成。
| Table 1 The particle sizing distribution and polydispersity index (PDI) of SMEDDS and SRL-SMEDDS. n = 3, x± s |
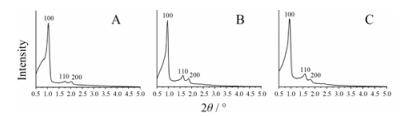
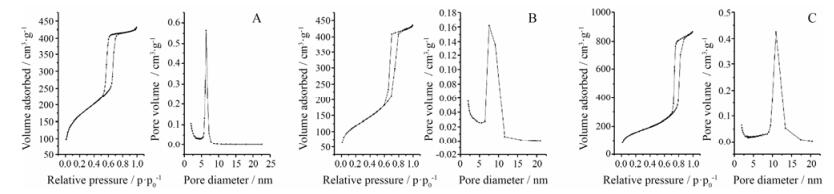
制备的SBA-15的扫描电镜及透射电镜如图 5所示。从扫描电镜和透射电镜中可以看到SBA-15均呈柱状, 且内部孔道为有序结构。从图 6中可见, 100、110、200的3个峰再次说明SBA-15为有序介孔孔道结构。在图 7中, SBA-15 (6.3)、SBA-15 (8.1) 和SBA-15 (10.8) 均呈现Ⅳ型等温线和H1型迟滞回线。由国际纯粹与应用化学联合会(IUPAC)提出, Ⅳ型等温线和H1型迟滞回线由介孔材料产生。因此, 可以进一步佐证所制备的材料为介孔材料。通过氮气吸脱附实验测得SBA-15 (6.3)、SBA-15 (8.1) 和SBA-15 (10.8) 的比表面积分别为578.5、410.2和554.6 m2·g-1, 孔径分别为6.3、8.1和10.8 nm。

|
Figure 5 Scanning electron microscope (SEM) of SBA-15 (6.3) (A), SBA-15 (8.1) (B), SBA-15 (10.8) (C) and transmission electron microscope (TEM) of SBA-15 (6.3) (D), SBA-15 (8.1) (E), SBA-15 (10.8) (F) |
|
Figure 6 Small angle X-ray diffraction (SAXD) of SBA-15 (6.3) (A), SBA-15 (8.1) (B), SBA-15 (10.8) (C) |
|
Figure 7 N2Adsorption-desorption isotherm and pore size distribution of SBA-15 (6.3) (A), SBA-15 (8.1) (B), SBA-15 (10.8) (C) |
按m (SRL-SMEDDS):m (SBA-15) = 1:1、2:1、3:1比例制备SRL-SMEDDS-SBA-15, 并测其载药量, 结果见表 2。孔径大小对载药量几乎没有影响。随着SRL-SMEDDS的增加, 载药量逐渐增加。
| Table 2 Drug loading rate of SRL-SMEDDS-SBA-15 with different ratio of SRL-SMEDDS to SBA-15. n = 3, x± s |
粉末的流动性结果如表 3所示。当比例增至3:1时, SRL-SMEDDS-SBA-15外观上已经过于黏稠, 流动性差, 因此未进行流动性考察; 当比例为1:1及2:1时, SRL-SMEDDS-SBA-15与SBA-15的流动性数据差异不大, 且休止角均小于40°, 压缩度小于20%, 豪斯纳比小于1.25, 说明SRL-SMEDDS-SBA-15粉末流动性良好。故将最终比例确定为2:1, 用于后续实验。
| Table 3 Flow properties of SRL-SMEDDS-SBA-15 (6.3), SRL-SMEDDS-SBA-15 (8.1), SRL-SMEDDS-SBA-15 (10.8) |
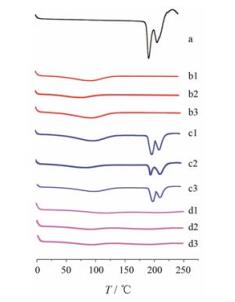
SRL、SBA-15、物理混合物及SRL-SMEDDS-SBA-15的DSC结果如图 8所示。从图中可知, SRL在190 ℃和210 ℃有两个特征衍射峰, 在物理混合物中依然清晰可见。但在SRL-SMEDDS-SBA-15中SRL的特征衍射峰消失, 表明SRL以无定形装载在载体材料中。
|
Figure 8 DSC of SRL-SMEDDS-SBA-15. a: SRL; b1, b2, b3: SBA-15 (6.3), SBA-15 (8.1), SBA-15 (10.8); c1, c2, c3: physical mixture of SRL and SBA-15 (6.3), physical mixture of SRL and SBA-15 (8.1), physical mixture of SRL and SBA-15 (10.8); d1, d2, d3: SRL-SMEDDS-SBA-15 (6.3), SRL-SMEDDS-SBA-15 (8.1), SRL-SMEDDS-SBA-15 (10.8) |
使用SBA-15固化后的SRL-SMEDDS在粒径上较SRL-SMEDDS并无太大改变, 见表 4。结果表明, 使用SBA-15对SRL-SMEDDS进行吸附及释放, 此过程并未对SRL-SMEDDS的粒径造成很大影响。
| Table 4 Particle sizing distribution of SRL-SMEDDS-SBA-15. n = 3, x± s |
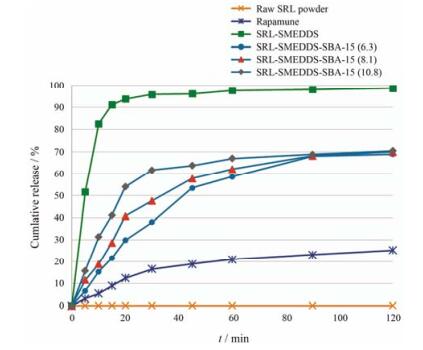
SRL粉末在2 h内基本无释放; 市售片剂雷帕鸣释放度只达25%左右; SRL-SMEDDS释放最快, 在30 min时释放达到95%以上, 并且其体外释放终点接近100%。从SRL-SMEDDS-SBA-15 (6.3), SRL-SMEDDS-SBA-15 (8.1) 和SRL-SMEDDS-SBA-15 (10.8) 三者的体外溶出度数据可见, 孔径大小对于释放终点无显著影响, 但对1 h内的体外释放有较大影响。孔径越大, 突释现象越明显。结果见图 9。
|
Figure 9 Cumulative release rate of different formulation of SRL |
研究选用HPLC法对SRL体外含量进行测定, 该方法专属性好、灵敏和简便, 可满足SRL质量控制*的需要。在成功制备SRL-SMEDDS后, SRL在水中的溶解度有了极大的提高[11]。自微乳因其具有不易贮存运输、较为黏稠等特点, 选择适宜的物质对其进行固化就显得尤为必要。在制备了3种不同孔径大小的SBA-15后, 通过SEM、TEM、SAXD和BET对其进行表征, 发现所制备的3种不同孔径的SBA-15各项表征结果良好, 与现有文献报道相一致[12]。使用搅拌法制备了SRL-SMEDSS-SBA-15, 并考察了SRL-SMEDDS与SBA-15比例分别为1:1、2:1和3:1时对SRL-SMEDDS-SBA-15外观及粉体学性质的影响。当SRL-SMEDDS与SBA-15比例为2:1时, 采用SBA-15 (6.3), SBA-15 (8.1) 和SBA-15 (10.8) 所制备SRL-SMEDDS-SBA-15在外观上不黏连, 流动性较好。通过重分散实验, 发现固化过程对液态自微乳及SBA-15粒径影响不大, 重分散结果良好。载药量实验表明, 使用3种不同孔径SBA-15吸附的SRL-SMEDDS载药量与孔径大小无关, 且与理论值差异不大。
SRL-SMEDDS-SBA-15的体外溶出结果表明, 在水中2 h时三者释放终点无显著差异, 但在释放开始后1 h三者溶出度有较大差异。SBA-15 (6.3)、SBA-15 (8.1) 和SBA-15 (10.8) 三者的孔径不同, 在一定程度上也造成了比表面积的不同。一般来说, 比表面积的大小会影响吸附在外表面的SRL-SMEDDS的量[13]及SRL的释放。但从体外溶出实验结果可以发现, 孔径越大突释现象越明显, 因此孔径是影响突释的主要因素。造成此现象的原因可能是因为SBA-15孔径内表面相对外表面吸附了更多的SRL-SMEDDS, 导致孔径大小在一定程度上成为控制体外溶出的主要因素。最终的累积释放度只达到70%左右, 可能是由于SBA-15的孔道很深, 且其纳米级别的孔径很小, 导致有一定量的自微乳残留在孔道深处接触不到释放介质, 在一定程度上降低了SRL体外溶出释放终点。有文献[14-16]报道, 可将介孔二氧化硅纳米粒制成片剂, 也有良好的释药效果。因此, 后续研究可能会基于此固体自微乳粉末进行剂型方面的考察。
综上所述, 通过搅拌法成功使用不同孔径的SBA-15对SRL-SMEDDS进行固化, 制得的3种不同SRL-SMEDDS-SB1-15的粉体学性质与重分散效果良好, 在水中的2 h体外溶出度与SRL粉末及市售片剂相比有明显提高。该制备方法操作简便, 可行性高, 为后续液态自微乳制剂的固化研究提供新的思路和方法。
| [1] | Chatel MA, Larkin DFB. Sirolimus and mycophenolate as combination prophylaxis in corneal transplant recipients at high rejection risk[J]. Am J Ophthalmol, 2010, 150: 179–184. DOI:10.1016/j.ajo.2010.03.010 |
| [2] | Sousa JE, Costa MA, Abizaid A, et al. Four-year angiographic and intravascular ultrasound follow-up of patients treated with sirolimus-eluting stents[J]. Circulation, 2005, 111: 2326–2329. DOI:10.1161/01.CIR.0000164271.01172.1A |
| [3] | Lü FQ, Li H, Xu W, et al. Preparation of self-microemulsion drug delivery system of the mixture of paeonol and borneol based on Xingbi Fang[J]. Acta Pharm Sin (药学学报), 2013, 48: 1602–1610. |
| [4] | Chen HX, Xu XG, Yan XS. Plasma concentration and phar macokinetics of ursolic acid carried in self-microemulsifying drug delivery system in rats studied by UPLC-MS/MS[J]. Acta Pharm Sin (药学学报), 2014, 49: 938–941. |
| [5] | Franceschinis E, Voinovich D, Grassi M, et al. Self-emulsi fying pellets prepared by wet granulation in high-shear mixer: influence of formulation variables and preliminary study on the in vitro absorption[J]. Int J Pharm, 2005, 291: 87–97. DOI:10.1016/j.ijpharm.2004.07.046 |
| [6] | Balakrishnan P, Lee BJ, Oh DH, et al. Enhanced oral bioavailability of dexibuprofen by a novel solid self-emulsi fying drug delivery system (SEDDS)[J]. Eur J Pharm Biopharm, 2009, 72: 539–545. DOI:10.1016/j.ejpb.2009.03.001 |
| [7] | Quan GL, Chen B, Wang ZH, et al. Improving the dissolu tion rate of poorly water-soluble resveratrol by the ordered mesoporous silica[J]. Acta Pharm Sin (药学学报), 2012, 47: 239–243. |
| [8] | Slowing II, Trewyn BG, Giri S, et al. Mesoporous silica nanoparticles for drug delivery and biosensing applications[J]. Adv Funct Mater, 2007, 17: 1225–1236. DOI:10.1002/(ISSN)1616-3028 |
| [9] | Slowing II, Vivero-Escoto JL, Wu CW, et al. Mesoporous silica nanoparticles as controlled release drug delivery and gene transfection carriers[J]. Adv Drug Deliv Rev, 2008, 60: 1278–1288. DOI:10.1016/j.addr.2008.03.012 |
| [10] | Zhao D, Feng J, Huo Q, et al. Triblock copolymer syntheses of mesoporous silica with periodic 50 to 300 angstrom pores[J]. Science, 1998, 279: 548–552. DOI:10.1126/science.279.5350.548 |
| [11] | Liu ZH, Hu XW, Tao C, et al. Studies on sirolimus self-microemulsifying drug delivery system and its solidification[J]. J Pharm Pract (药学实践杂志), 2016, 34: 142–147. |
| [12] | Sevimli F, Yılmaz A. Surface functionalization of SBA-15 particles for amoxicillin delivery[J]. Micropor Mesopor Mat, 2012, 158: 281–291. DOI:10.1016/j.micromeso.2012.02.037 |
| [13] | Kallakunta VR, Bandari S, Jukanti R, et al. Oral self-emul sifying powder of lercanidipine hydrochloride: formulation and evaluation[J]. Powder Technol, 2012, 221: 375–382. DOI:10.1016/j.powtec.2012.01.032 |
| [14] | Wu QL, Quan GL, Hong Y, et al. Preparation and release behaviour of mesoporous silica/ethylcellulose sustained-release mini-matrix[J]. Acta Pharm Sin (药学学报), 2015, 50: 492–499. |
| [15] | Li CX, Tu JS, Zhang PH, et al. Preparation and dissolution characteristics of mesoporous silica-based risperidone sustained-release tablets[J]. Chin J New Drug (中国新药杂志), 2015, 24: 79–84. |
| [16] | Li H, Gu J, Shah LA, et al. Bone cement based on vancomycin loaded mesoporous silica nanoparticle and calcium sulfate composites[J]. Mater Sci Eng C Mater, 2015, 49: 210–216. DOI:10.1016/j.msec.2014.12.082 |
 2017, Vol. 52
2017, Vol. 52