白血病 (leukemia) 也称作“血癌”, 是一类造血干细胞的恶性克隆性疾病。病因是由于细胞内DNA变异形成的骨髓中造血组织生成大量不成熟、无法正常工作的白细胞, 妨碍骨髓的其他功能, 使正常白细胞、红细胞、血小板减少进而导致其他生理功能失调。2016年, 美国约有60 140人被诊断为白血病患者, 死于这种恶性肿瘤的有24 400人[1]。在所有白血病患者中, 成年人约占90%[2]。白血病在儿科恶性肿瘤的发病率中占居首位, 其死亡率在导致儿童及20岁以下成年人死亡的恶性肿瘤中高居首位[3]。
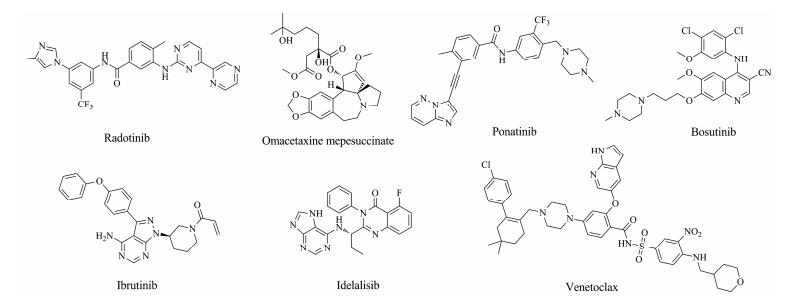
白血病按照病程进展的速度分为急性和慢性, 主要有慢性骨髓性白血病 (CML)、慢性淋巴性白血病 (CLL)、急性骨髓性白血病 (AML) 和急性淋巴性白血病 (ALL) 4种类型。Radotinib是第二代Bcr-Abl融合蛋白酪氨酸激酶和血小板衍生生长因子受体 (PDGFR) 抑制剂[4], 2012年由韩国食品药品管理局批准上市, 用于imatinib难治的“费城染色体阳性 (Ph+)” CML的二线治疗。Omacetaxine mepesuccinate[5]是从粗榧 (Cephalotaxus harringtonia) 中提取的一种生物碱, 也可由三尖杉碱半合成制得, 2012年获FDA批准用于治疗对2种以上酪氨酸激酶抑制剂 (TKI) 耐药或不可耐受的CML患者。Bosutinib[6]是一种TKI, 2012年获FDA批准上市, 主要用于治疗CML。Ponatinib是一种多靶点TKI, 用于治疗成人CML、Ph+型ALL, 2012年获FDA批准上市, 2013年10月FDA警示其具有致死性血凝块和严重血管狭窄风险, 随后要求暂停其销售[7]。2013年FDA批准ibrutinib用于治疗套细胞淋巴瘤 (MCL), 2014年批准用于治疗CLL[8], 是第一种布鲁顿酪氨酸激酶 (Bruton’s tyrosine kinase, BTK) 抑制剂。Idelalisib是2014年FDA批准上市的首个口服、选择性的磷酸肌醇3-激酶δ (PI3Kδ) 抑制剂, 和rituximab联合治疗复发的CLL[9], 但其常伴有肝脏毒性、严重腹泻或肠炎、以及肺炎和肠穿孔等不良反应。2016年4月FDA批准venetoclax上市, 用于治疗CLL[10], 成为第一个特异性针对Bcl-2蛋白的新型口服靶向药物。这些上市药物的化学结构见图 1。
|
Figure 1 Structures of the marketed anti-leukemia drugs |

|
Scheme1 Synthesis of the target compounds |
虽然近年来陆续上市的新药使得白血病在全球范围内的病情得到一定程度的遏制, 但是白血病治疗的最大威胁是由于疾病本身的进化和诱导化疗引起的骨髓抑制以及疾病的耐药及复发, 所以临床上依旧迫切需要具有全新化学结构的白血病治疗新药。
Mannich碱是很多合成药物及天然产物的关键中间体, 同时还存在于许多生物碱、核苷酸、甾族化合物、肽、抗生素和维生素等化合物中。Mannich碱具有非甾体雄激素受体调节[11]、抗糖尿病[12]、抗结核[13]、抗真菌[14]、抗疟[15]、抗炎[16]等生物活性, 但是未见Mannich碱具有抗白血病活性的文章报道。为了寻找新型抗白血病药物, 期望在具有广泛生物活性的Mannich碱中有所发现。作为一种尝试, 设计了含有对甲苯乙酮的Mannich碱; 借助高原子经济性的Mannich反应, 以对甲基苯乙酮、芳香醛和芳香胺为原料, 一锅法制备了所设计的曼尼希碱 (合成路线1)。生物活性测试发现, 该类结构中某些分子具有很强的抗白血病活性, 为新型白血病药物的研发提供了新的结构类型。
结果与讨论 1 化合物的合成及鉴定Mannich反应是有机化学中构筑C-C键的重要反应[17]。β-氨基酮型Mannich碱的合成, 既有直接合成法也有间接合成法。间接合成法有查尔酮与胺的Michael加成、胺交换法、胺盐酸盐法、酮交换法、Schiff碱与酮的缩合等方法[18]。直接Mannich反应有“可烯醇化的酮和预合成的纯净Schiff碱缩合的二步法”以及“醛酮胺三组分一锅煮”两种比较常见的方法[17]。借鉴本研究室以往的经验[19, 20], 本研究以对甲基苯乙酮、芳香醛和芳香胺为原料, 借助Mannich反应, 按照合成路线1, 一锅法合成了33个Mannich碱 (表 1), 所有合成的化合物的结构经1H NMR、IR、MS确证 (表 2, 其中, TM17~TM33的表征信息见文献21)。IR结果显示, 所有化合物中含有的特征吸收峰在3 410~3 300 cm-1和1 710~ 1 650 cm-1, 分别是N-H和C=O的伸缩振动。
| Table 1 Experimental results of target compounds |
| Table 2 1H NMR, MS and IR data of compounds TM1-TM16 |
测试了TM1-TM33对P338肿瘤细胞生长的体外抑制活性 (表 3)。在1×10-4 mol·L-1测试浓度下, 所有化合物对P338肿瘤细胞生长显示抑制作用; 在测试浓度为1×10-8 mol·L-1时, 多数化合物表现出较弱的抑制作用, 但TM33的抑制作用依然很强, 高达60.3%。
| Table 3 Inhibition of compounds TM1-TM33 against P388 cancer cell line |
从目标化合物的结构来看, 分子之间的差别主要是取代基R1和R2的位置、电性和空间体积, 目标化合物对P338肿瘤细胞生长的抑制活性强弱应该是既取决于分子的整体性质, 也取决于取代基R1和R2。按照IC50 < 6 μmol·L-1的标准, R1为H、NO2及Cl的化合物, 其生物活性总体比R1为CH3的好, 但TM33是例外。
R1=NO2 (TM1~TM8) 时, R2在对位比在间位生物活性好, 如TM4 (p-Cl) > TM3 (m-Cl); R2为H (TM2) 或者CH3 (TM1) 的生物活性好于R2为CO2C2H5 (TM6) 及NO2 (TM8) 的化合物, 而R2 = p-COOH (TM7) 时生物活性居中, IC50 = 5.18 μmol·L-1。
R1=Cl (TM9~TM16) 时, R2在对位与在间位的生物活性相当, 如TM11 (m-Cl) 和TM12 (p-Cl) 的IC50分别为5.84和5.86 μmol·L-1; R2为H或者为强吸电子基团 (p-COOH, p-NO2) 对生物活性总体有利, 虽然R2=p-CO2C2H5 (TM14) 的生物活性较低。
R1=H (TM17~TM25) 时, R2在间位比在对位的生物活性好, 如TM19 (m-Cl) > TM20 (p-Cl), TM25 (m-NO2) > TM24 (p-NO2); R2在对位, 取代基不同, 其生物活性也不同, 如TM22 (p-CO2C2H5) > TM21 (p-Br) > TM18 (H) > TM24 (p-NO2) > TM20 (p-Cl) > TM17 (p-CH3) > TM23 (p-CO2H)。
R1=CH3 (TM26~TM33) 时, 生物活性普遍较弱, 但是TM33 (R2=m-NO2) 是例外, 不仅生物活性好, 而且是33个化合物中生物活性最好的, 测试浓度为1×10-8 mol·L-1时, 其抑制率高达60.3%, IC50低至0.45 nmol·L-1。
3 化合物理化性质和毒性的计算药物的化学结构决定药物的理化性质, 药物的理化性质与药物活性密切相关, 是药物类药性的具体体现。因此, 对IC50值小于5 μmol·L-1的高活性化合物, 使用Eli Lilly and Company提供的计算平台Plexus进行了理化性质的计算, 结果见表 4。clogP是化合物疏水性的重要指标, clogP值越大, 化合物的疏水性越好; 高活性化合物的clogP在5~6, 说明这些化合物脂溶性较强。tPSA是化合物内极性原子的总表面积, 通常可用于作为药物透膜性的评价指标, 目前认为tPSA值≤140较好[22]; 本研究合成的高活性化合物的tPSA都小于80, 都有较好的透膜性。
| Table 4 Physicochemical properties and toxicity prediction data. *OM: Omacetaxine mepesuccinate |
此外, 使用凡默谷公司 (PharmoGo) 的毒性预测软件ADMET Predictor 7.0预测了高活性化合物的毒性 (表 4)。TOX-hERG定量预测化合物的心脏毒性, 规定TOX-hERG≤6 mol·L-1才是正常值; 根据表 4中的预测结果可知, 高活性化合物的TOX-hERG < 6 mol·L-1。TOX-RAT预测化合物的急性毒性, 以半数致死浓度LC50 (大鼠动物模型) 表示, 要求大多数药物分子的LC50预测值都应该≥300 mg·kg-1; 高活性化合物LC50 > 300 mg·kg-1, 除TM15的LC50 = 394 mg·kg-1外, 其他化合物的LC50 > 1 500 mg·kg-1, TM33的LC50高达2 069 mg·kg-1。TOX-BRM-Rat (大鼠动物模型) 和TOX-BRM-Mouse (小鼠动物模型) 预测化合物的致癌性, 大多数药物分子半数致癌浓度TD50的预测值应该≥4 mg·kg-1·d-1和≥25 mg·kg-1·d-1, 而高活性化合物TOX-BRM-Rat的TD50 > 20 mg·kg-1·d-1, TOX-BRM-Mouse的TD50 > 70 mg·kg-1·d-1, 可能没有相关毒性或者毒性较小。TOX-MUT-Risk是对化合物致突变性预测结果进行综合打分, 对于大多数药物分子, TOX-MUT-Risk ≤2;预测结果显示, 高活性化合物TOX-MUT-Risk符合规定范围, 致突变性较低。对于大多数药物, TOX-Risk ≤3, 高活性化合物也是符合要求的。值得高兴的是, 相较于表 4中的上市药物分子, 本研究的高活性化合物的毒性可能更小。
4 结论本研究设计合成了33个对甲基苯乙酮、芳香醛和芳香胺的Mannich碱; 生物活性测试发现, TM33活性最好, IC50低至0.45 nmol·L-1; 毒性预测显示, TM33比多数上市药物的毒性低。因此, TM33可作为新型抗白血病先导化合物进一步研究。
实验部分所有实验材料除另外说明外, 均为市售AR或CP。PK-60000FT-IR仪 (美国Mattson公司产品, KBr压片); ACE-200核磁共振仪 (Bruker, USA; TMS为内标); ESI质谱仪 (1946B, Agilent); 电热熔点测定仪 (英国生产, 未经校正)。
1 目标化合物TM1~TM33的合成通法于圆底烧瓶中加入芳香胺 (0.1 mol)、芳香醛 (0.1 mol)、无水乙醇150 mL, 室温搅拌10 min后, 加入对甲基苯乙酮 (0.1 mol) 和催化量的浓HCl, 然后于环境温度搅拌反应。TLC监测反应结束后, 将反应液冷却过夜, 抽滤析出的固体, 并用无水乙醇洗涤。所得固体悬浮于180 mL 95%乙醇中, 室温搅拌1.5 h, 用饱和NaHCO3中和溶液至碱性, 抽滤, 用少量无水乙醇洗涤滤饼, 粗品经乙醇/水混合溶剂 (体积比1:1) 重结晶, 得到纯品。
2 生物活性测试——四氮唑盐 (MTT) 还原法取对数生长期细胞, 调整适当浓度接种于96孔培养板, 每孔100 μL, 悬浮生长细胞 (P338) 接种后即加入待测化合物。每孔加入10 μL (被测化合物母液用RPMI1640培养液稀释至所需浓度), 每个浓度设3个平行孔, 并设一组不加药而加等体积培养液的癌细胞悬液为阴性对照组, 同时以阳性对照药物设立一组阳性对照。加药后细胞置37 ℃、5% CO2培养箱中孵育24~48 h后, 加入MTT 20 μL, 继续培养4 h, 离心倾去上清液, 加入150 μL DMSO, 振荡10 min, 用酶标仪测定570/630 nm双波长吸光度 (A) 值, 以Excel Forecast函数计算IC50值。
致谢: 感谢本学院老师在红外、质谱、核磁共振测试中提供支持和帮助, 上海国家新药筛选中心在活性测试方面提供帮助。| [1] | The Leukemia & Lymphoma Society. Leukemia [EB/OL]. http://www.lls.org/http%3A/llsorg.prod.acquia-sites.com/facts-and-statistics/facts-and-statistics-overview/facts-and-statistics#Leukemia. 2016/2016-12-17. |
| [2] | National Cancer Institute. A Snapshot of Leukemia [EB/OL]. http://www.cancer.gov/researchandfunding/snapshots/leukemia. 2014-06-18/2016-12-17. |
| [3] | The Leukemia & Lymphoma Society. Blood cancer facts 2015-2016 [EB/OL]. http://www.lls.org/sites/default/files/file_assets/PS13%20-%20FactsCard2015_2016_english.pdf. 2016-06-01/2016-12-17. |
| [4] | Bronson J, Black A, Murali Dhar TG, et al. "Radotinib (Anti-cancer)"[J]. Annu Rep Med Chem, 2013, 48: 523–524. |
| [5] | Wu L, Li X, Su J, et al. Effect of low-dose cytarabine, homoharringtonine and granulocyte colony-stimulating factor priming regimen on patients with advanced myelodysplastic syndrome or acute myeloid leukemia transformed from myelodysplastic syndrome[J]. Leuk Lymphoma, 2009, 50: 1461–1467. DOI:10.1080/10428190903096719 |
| [6] | Cortes JE, Kim DW, Kantarjian HM, et al. Bosutinib versus imatinib in newly diagnosed chronic-phase chronic myeloid leukemia: results from the BELA trial[J]. J Clin Oncol, 2012, 30: 3486–3492. DOI:10.1200/JCO.2011.38.7522 |
| [7] | The U.S. Food and Drug Administration (FDA). FDA Drug Safety Communication: FDA. asks manufacturer of the leukemia drug Iclusig (ponatinib) to suspend marketing and sales [EB/OL]. http://www.fda.gov/Drugs/DrugSafety/ucm373040.htm. 2013-10-31/2016-12-17. |
| [8] | Azvolinsky A. FDA Approves Ibrutinib for Chronic Lym-phocytic Leukemia [EB/OL]. http://www.cancernetwork.com/news/fda-approves-ibrutinib-chronic-lymphocytic-leukemia. 2014-02-13. |
| [9] | Furman RR, Sharman JP, Coutre SE, et al. Idelalisib and rituximab in relapsed chronic lymphocytic leukemia[J]. N Engl J Med, 2014, 370: 997–1007. DOI:10.1056/NEJMoa1315226 |
| [10] | The U.S. Food and Drug Administration (FDA). FDA approves new drug for chronic lymphocytic leukemia in patients with a specific chromosomal abnormality [EB/OL]. http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm495253.htm. 2016-04-11/2016-12-17. |
| [11] | Zhou C, Wu G, Feng Y, et al. Discovery and biological characterization of a novel series of androgen receptor modulators[J]. Br J Pharmacol, 2008, 154: 440–450. |
| [12] | Zhou ZW, Yan JF, Tang XM, et al. Synthesis and preliminary evaluation of antidiabetic activity for β-amino ketone contain-ing isoxazole moiety[J]. Chin J Org Chem (有机化学), 2010, 30: 582–589. |
| [13] | Ji L, Long QX, Yang DC, et al. Identification of Mannich base as a novel inhibitor of mycobacterium tuberculosis isocitrate by high-throughput screening[J]. Int Biol Sci, 2011, 7: 376–382. DOI:10.7150/ijbs.7.376 |
| [14] | Karthikeyan MS, Prasadrasad DJ, Poojar YB. Synthesis and biological activity of Schiff and Mannich bases bearing 2, 4-dichloro-5-fluorophenyl moiety[J]. Bioorg Med Chem, 2006, 14: 7482–7489. DOI:10.1016/j.bmc.2006.07.015 |
| [15] | Lopes F, Capela R, Goncaves JO, et al. Amidomethylation of amodiaquine: antimalarial N-Mannich base derivatives[J]. Tetrahedron Lett, 2004, 45: 7663–7666. DOI:10.1016/j.tetlet.2004.08.093 |
| [16] | Liu D, Yu W, Li J, et al. Novel 2-(E)-substituted ben-zylidene-6-(N-substituted aminomethyl) cyclohexanones and cyclohexanols as analgesic and anti-inflammatory agents[J]. Med Chem Res, 2013, 22: 3779–3786. DOI:10.1007/s00044-012-0362-x |
| [17] | Yu ZM, Liao XL, Wei JY, et al. Advances in the Mannich reaction of aromatic aldehydes, aromatic ketones with aromatic amines[J]. J Org Chem Res (有机化学研究), 2016, 4: 61–68. DOI:10.12677/JOCR.2016.43009 |
| [18] | Tang GX, Yan JF, Fan L, et al. Synthesis of novel β-amino ketones containing a p-aminobenzoic acid moiety and evalua-tion of their antidiabetic activities[J]. Sci China Chem, 2013, 56: 490–504. DOI:10.1007/s11426-012-4816-2 |
| [19] | Yang DC, Fan L. The Mannich reaction of 4-aminobenzoic acid and acetophenone with aromatic aldehydes[J]. J South-west China Norm Univ (Nat Sci) (西南师范大学学报 (自然科学版)), 1996, 21: 585–589. |
| [20] | Yang DC, Yan JF, Xu J, et al. Synthesis and investigation on antidiabetic activity of 4-(1-aryl-3-oxo-5-phenylpentylamino) benzenesulfonamide[J]. Acta Pharm Sin (药学学报), 2010, 45: 66–71. |
| [21] | Yang DC, Zhang GL, Yang Y, et al. The Mannich reaction of 4-methylacetophenone with aromatic aldehydes and aromatic amines[J]. Chem Res Chin Univ (高等学校化学学报), 2000, 21: 1694–1696. |
| [22] | Lu SY, Jessen B, Strock C, et al. The contribution of physicochemical properties to multiple in vitro cytotoxicity endpoints[J]. Toxicol In Vitro, 2012, 26: 613–620. DOI:10.1016/j.tiv.2012.01.025 |
 2017, Vol. 52
2017, Vol. 52


