2. 中国医学科学院、北京协和医学院医药生物技术研究所, 北京 100050
2. Institute of Medicinal Biotechnology, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100050, China
近年来, 我国乃至全世界肿瘤的发生率每年都呈增长趋势, 死于恶性肿瘤的患者越来越多。继心脑血管疾病, 肿瘤已成为威胁人类健康的又一大杀手, 肿瘤的预防和治疗已成为重要的工作之一。现今许多抗肿瘤药物仍以细胞毒作用为主, 有很强的毒副作用, 降低了患者的生存质量, 而且极易产生耐药性。靶向抗肿瘤药物有其他抗肿瘤药物所不具备的优点, 专一性强、低毒性, 从而解决了这一问题, 因此筛选靶向抗肿瘤药物的任务迫在眉睫。
自20世纪80年代开始, 随着对酵母及果蝇分子遗传学研究的深入, 调控有丝分裂的一些重要激酶被先后发现, 其中包括保罗样激酶 (polo样激酶)[1]。Polo样激酶属polo-like kinase (Plks) 家族成员, 是一类存在于真核生物中的丝/苏氨酸蛋白激酶。其结构特征是在氨基端 (N端) 包括1个高度保守的丝/苏氨酸蛋白激酶区域, 羧基端 (C端) 具有3个相似的、被称为polo-box序列的非催化区域[2]。羧基端包含的特征性结构域 (polo-box domain, PBD) 是多种丝/苏氨酸磷酸化蛋白质的结合位点, 与调节PLK1的激酶活性有关[3]。Plks家族不同成员的PBD对同一底物的亲和力不同, 4种Plks的PBD分别为PBD1、PBD2、PBD3、PBD4, 其中前3者显示高度同源性, 由特性的两个polo-box (PB1和PB2) 组成。PB1由78个氨基酸组成, PB2序列也相差不大; PBD4为两个PLK4聚合后的变异体, C端序列存在很大的特异性, 且仅存在一个polo-box[4]。
PLK1在有丝分裂中起重要作用, 参与细胞周期的调控, 包括促进中心体成熟、纺锤体形成、染色体的分离及胞质分裂等。临床前结果表明, PLK1的异常表达与多种人类肿瘤相关, 是肿瘤细胞生长与增殖所必需[5]。阻断PLK1的通路, 能有效抑制肿瘤细胞的增殖, 并诱导肿瘤细胞的凋亡, PLK1是一个颇具吸引力的治疗靶点[6, 7], 因此PLK1 PBD成为了近年来寻找高选择性PLK1抑制剂的新靶点[8-15]。
荧光偏振方法由Perrin[16]于1926年提出, 是一种通过检测固有荧光分子或者荧光标记分子的荧光强弱变化来研究分子间相互作用的有力工具。荧光偏振值 (fluorescence polarization, FP) 的大小由分子大小决定, 若荧光分子很小, 当有偏振光照射到每个快速转动的分子时, 小分子各自发射出荧光, 方向随机, FP值低; 反之当荧光分子大时, FP值高。
本研究对中国医学科学院医药生物技术研究所新药 (微生物) 筛选实验室化合物库中筛选的阳性化合物F083-0063进行体外活性研究, 包括MTT检测细胞毒性、流式细胞仪检测周期及凋亡、Western blotting分析细胞周期相关蛋白的表达、划痕实验检测对细胞的迁移作用、虚拟分子对接检测化合物F083-0063与PLK1 PBD可能的结合方式, 探讨其抗肿瘤的可能性。
材料与方法细胞株 人前列腺癌细胞PC3用含10%胎牛血清 (fetal bovine serum, FBS) 的F12K培养基进行培养; 人宫颈癌细胞HeLa、人结直肠癌细胞HCT-116、人正常肝细胞LO2和小鼠巨噬细胞Raw264.7均用含10% FBS的DMEM培养基培养; 人成骨肉瘤细胞MG-63用含10% FBS的1640培养基培养; 人肝癌细胞HepG2用含10% FBS的MEM培养基培养; 人直肠腺癌细胞HT-29用DMEM/F12+5% FBS+NEAA (1:100) 培养基培养; 以上细胞株均由中国医学科学院医药生物技术研究所新药 (微生物) 筛选实验室提供。
试剂 40 000个化合物均购自北京百灵威科技有限公司; 重组蛋白PLK1 PBD由中国医学科学院医药生物技术研究所重点实验室陈云雨博士提供; Annexin V-FITC/PI双染试剂盒购自北京四正柏生物科技有限公司; DMEM高糖培养基、MEM、F12K购自美国Sigma公司; NaCl、Tris-HCl、EDTA、RNase A、碘化丙啶 (PI)、噻唑蓝 (MTT)、DMSO、30%丙烯酰胺、4×浓缩胶缓冲液、4×分离胶缓冲液、考马斯亮蓝染色均购自北京普利莱基因技术有限公司。
主要仪器 Envision 2014 Multilabel Reader酶标仪购自美国PerkinElmer公司产品; FACS Caliur流式细胞仪购自美国Beckman Coulter公司; DFC450C型活细胞显微观察及图像采集仪为德国Leica公司产品; powerPacTM HC稳压稳流电泳仪购自美国Bio-Rad公司。
荧光偏振法初筛 将化合物库中40 000个化合物的初始质量浓度10 mg·mL-1稀释至1 mg·mL-1于96孔板中方便后续使用, 溶剂为DMSO。利用荧光偏振模型对1 mg·mL-1的化合物进行初步筛选。于384孔板中依次加入经纯化的PLK1 PBD蛋白30 μL (400 nmol·L-1)、经稀释的化合物0.3 μL, 并设立阳性阴性对照, 其中加入DMSO 0.3 μL为阴性对照, 不加PLK1 PBD为阳性对照, 25 ℃、140 r·min-1振荡条件下培养60 min; 最后分别加入FITC (60 nmol·L-1) 30 μL, 继续避光振荡培养15 min, 酶标仪检测40 000个样品的偏振值并进行数据分析。通过偏振值寻找与PLK1 PBD结合率高的活性化合物。抑制率 (%)=(FP阴性-FP化合物) / (FP阴性-FP阳性) × 100%。将所有可与PLK1 PBD蛋白结合的化合物稀释至终质量浓度为10、5、2.5、2、1、0.5、0.25、0.1、0.05、0.02、0.01 μg·mL-1, 检测偏振值, GraphPad Prism 5计算化合物的半数抑制浓度 (IC50) 值。
MTT比色法 取对数生长的细胞, PBS清洗一次, 胰酶消化, 调整每孔细胞数为3×103~6×103个。周边用灭菌的PBS或不加血清的培养基封闭, 避免边缘效应。将化合物稀释8个浓度梯度, 每个浓度设立3个复孔, 并设立对照组 (不加化合物), 继续培养48 h, 每孔加入适当浓度的MTT使其终质量浓度为0.5 mg·mL-1, 孵育4 h后弃掉培养基, 加入DMSO 150 μL避光振荡15 min, 酶标仪570 nm处检测吸光度值。抑制率计算方式如下:抑制率 (%)=(1-OD受试药组/OD空白组平均值) × 100%, 并计算IC50值。
流式细胞仪检测细胞周期 取对数生长的细胞接种于6孔板中, 待细胞贴壁每孔加入胸腺嘧啶 (0.1 mol·L-1) 40 μL, 使其终浓度为2 mmol·L-1, 此过程为第一次阻断, 细胞于细胞培养箱培养8~12 h, PBS洗3次, 加含10% FBS的DMEM培养基继续培养12 h, 进行第二次阻断, 方法同第一次, 经过两次胸腺嘧啶阻断和培养后加入浓度为5、10、15、20 μmol·L-1的化合物, 并设立空白组。将加药12 h的实验组细胞用胰酶消化, 900 r·min-1离心4 min。倒掉培养基, 加入PBS 1 mL, 轻轻吹打使细胞分散, 离心, 洗涤一次。倾去PBS加入70%冰乙醇1 mL固定至少1 h, 上机检测前去除冰乙醇, PBS洗2次, RNase A (100 μg·mL-1) 孵育30 min, PI (50 μg·mL-1) 室温避光孵育30 min, 以200目的尼龙膜过滤, 用流式细胞仪检测并做数据分析。
Annexin V-FITC/PI双染色法检测细胞凋亡 将每孔接种105个细胞于6孔板中培养8~12 h使其贴壁, 化合物作用24 h后的细胞, 以4 ℃ PBS洗涤2次, 加入Annexin V-FITC后避光孵育30 min, 上机前加入PI孵育5~15 min, FACS进行检测并分析数据。
Western blotting 收集化合物作用16 h后的细胞加RIPA细胞裂解液, 冰浴, 离心。BCA法测收集的蛋白上清液总蛋白浓度, 将样品蛋白质量浓度调整为2 mg·mL-1, 每孔上样量为20 μL。电泳后, Bio-Rad半干法转膜仪上转膜, 封闭2 h, TBST漂洗3次, 孵一抗、二抗, 曝光成像。
化合物与PLK1蛋白PBD结构域的分子对接 Discovery Studio 4.0软件调出PLK1 PBD结构并进行修饰, 去水、加氢, 将化合物F083-0063与蛋白活性区域对接。
化合物对细胞迁移作用 (划痕) 的影响 将每孔接种1×105个细胞于6孔板中, 培养24 h后用灭菌的枪头划痕致伤, PBS清洗3次去掉悬浮的细胞, 加入5、15、20 μmol·L-1的化合物, 培养48 h后拍照。20 μmol·L-1浓度的化合物作用于细胞, 分别在12、24、36、48 h拍照。
数据处理 每组实验重复3次, 组间比较采用t检验, P < 0.05具有显著性差异。
结果 1 化合物初筛结果利用荧光偏振模型对化合物库里40 000多的化合物进行初步筛选, 最终得到一个对PLK1 PBD抑制率较高的化合物F083-0063 (图 1), 筛选到的化合物属于噻唑类。F083-0063在10 μg·mL-1时抑制率为 (99.7±0.4) %, 较筛选得到的、可与PLK1 PBD结合的化合物, F083-0063的抑制率最高, 说明化合物F083-0063与PLK1 PBD结构域有很好的亲和性。

|
Figure 1 The structure of compound F083-0063 |
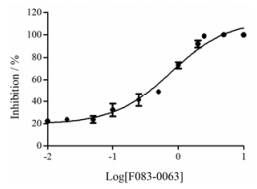
将F083-0063梯度稀释, 使终质量浓度分别为10、5、2.5、2、1、0.5、0.25、0.1、0.05、0.02、0.01 μg·mL-1, 荧光偏振模型测定其对PLK1 PBD的抑制活性, 利用软件Graphpad Prism 5计算IC50值为1.9±0.1 μmol·L-1 (图 2), 较筛选得到的、可与PLK1 PBD结合的化合物, IC50值最低, 说明PLK1 PBD结构域与底物结合具有较好的抑制作用。
|
Figure 2 F083-0063 inhibition curve for PLK1 PBD |
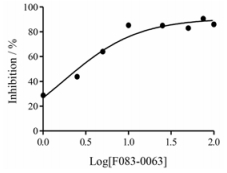
利用MTT法测定F083-0063对不同细胞系增殖的影响, 发现在PC3、HCT-116和MG-63细胞上化合物作用并不明显, 而在HeLa细胞上作用敏感, IC50值为5.8±0.6 μmol·L-1(图 3、表 1)。故后续研究均采用HeLa细胞为实验对象。
|
Figure 3 The inhibition ratio of F083-0063 for HeLa cells |
| Table 1 Cytotoxicity of F083-0063 to different cells |
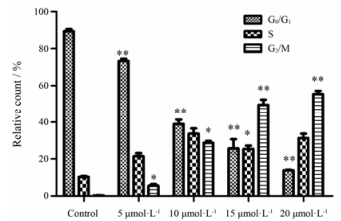
通过双胸腺嘧啶阻断HeLa细胞, F083-0063作用12 h, 流式细胞仪检测发现, 整个细胞周期的G2/M比例随着化合物浓度的增加有所增加。尤其是在20 μmol·L-1时由对照组的 (0.3±0.1) %增加到 (56.4±2.3) % (图 4)。结果表明F083-0063具有G2/M期阻滞作用, 并且有明显的浓度依赖性。
|
Figure 4 F083-0063 induced G2/M phase arrest in HeLa cells treated with 5, 10, 15 and 20 μmol·L-1for 12 h. n=3, x±s. *P < 0.05, **P < 0.01 vs control |
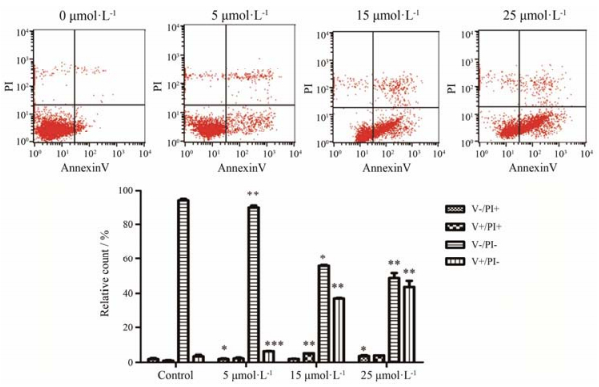
通过流式细胞仪的检测发现, 与空白组对比, F083-0063能够促进HeLa细胞凋亡, 尤其是早期凋亡。如 (图 5) 所示, F083-0063作用24 h后, 早期凋亡比例由 (6.2±0.1) %增加到 (37.1±0.4) %。当浓度达到25 μmol·L-1时, 早期凋亡比例增加到 (43.6±3.5) %。早期凋亡的细胞数量随着剂量的增加而增加, 呈现浓度依赖性。
|
Figure 5 Quantitative analysis of massive apoptosis caused by compound F083-0063. The lower left quadrant shows live cells for Annexin V-/PI-; The upper left quadrant shows the detection error within the allowable range Annexin V-/PI+; The lower right quadrant showed early apoptotic cells for Annexin V+/PI-; The upper right quadrant shows non-living cells, apoptotic cells and necrotic cells for Annexin V+/PI+. n=3, x±s. *P < 0.05, **P < 0.01, ***P < 0.001 vs control |
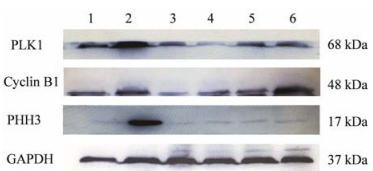
Western blotting检测发现, 5、10和15 μmol·L-1 F083-0063在HeLa细胞中作用16 h, PLK1、cyclin B1和PHH-3随着药物浓度的增加逐渐积累, 这与F083-0063可以引发HeLa细胞在G2/M期阻滞的结果相一致 (图 6)。
|
Figure 6 Analysis of the increase of PLK1, cyclin B1, PHH3 caused by F083-0063 using Western blotting assay. 1: Thymidine; 2: Nocodazole; 3: DMSO; 4: 5 μmol·L-1 F083-0063; 5: 10 μmol·L-1 F083-0063; 6: 15 μmol·L-1 F083-0063 |
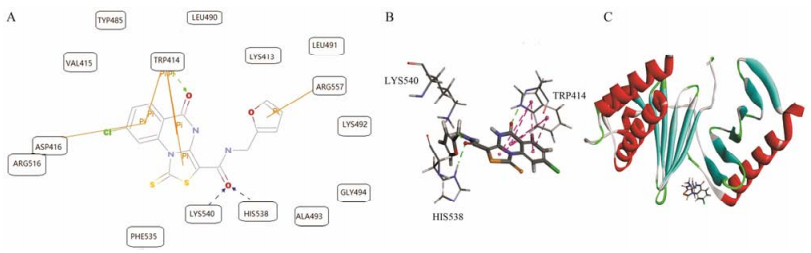
PLK1 PBD结构域是由His538、Lys540、TRP414、Lys540和Asp416等多个氨基酸组成, 通过对接结果显示 (图 7), F083-0063与PLK1 PBD的结构域呈现出较高的亲和性, 其中小分子抑制剂苯环上的羰基能与His538、Lys540、TRP414形成牢固的氢键, 同时与TRP414、ASP416、ARG516以及ARG557形成叠加的π键。此外, F083-0063与PLK1 PBD还存在非共价键的竞争结合方式, 进而使得小分子抑制剂与PBD结构域结合得更加紧密。
|
Figure 7 Virtual docking of F083-0063 with PBD1 domain. A: 2D floor plan of the interaction of the protein and small molecule; B: Interaction diagrams of the protein and small molecule; C: Spatial location schematic diagram of the protein and small molecule. The carbonyl group on the benzene ring can form a strong hydrogen bond with His538, Lys540, TRP414 and form a superposition of π bonds with TRP414, ASP416, ARG516 and ARG557. In addition, F083-0063 and PLK1 PBD also exist the non-covalent bond combination of competition |
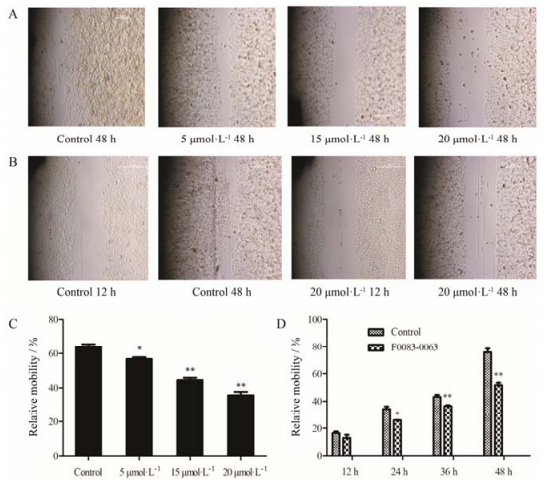
细胞迁移结果如 (图 8A、C) 所示, 与对照组相比, 加药组的细胞迁移能力明显减弱, 尤其是在20 μmol·L-1时, 由最开始的 (58.8±0.5) %变为 (39.6±0.7) %。随着剂量的逐渐增加, 迁移率明显受抑制, 存在剂量依赖性。
8.2 F083-0063作用不同时间对HeLa细胞迁移的影响F083-0063在20 μmol·L-1的作用下, HeLa细胞在不同时间表现出不同的迁移状态, 与对照组相比加药组的迁移抑制明显, 呈现出一定的时间依赖趋势 (图 8B、D)。
|
Figure 8 Effect of F083-0063 on migration ability of HeLa cells at different concentration (5, 15 and 20 μmol·L-1) (A, C) and different time (12, 24, 36, 48 h) (B, D). n=3, x±s. *P < 0.05, **P < 0.01 vs control |
据美国癌症协会 (American Cancer Society, ACS) 的一份统计报告称, 2012年约有1 640 000例新发癌症病例, 因癌症而离世的美国人达577 000例, 平均每天就有1 500例[17]。为寻找疗效好、毒副作用小的抗肿瘤药, 研究人员一直在不懈努力。抗肿瘤药数量虽多, 但理想的药物数量有限。分子靶向治疗代表了肿瘤生物治疗最新的发展方向, 如治疗淋巴瘤的小分子抑制剂BI2536、治疗鼻咽癌的小分子抑制剂Ro5203280。PLK1 PBD结构域作为抗肿瘤药物研究的新靶点可以满足高选择性、低毒性的要求。
PLK1是许多细胞周期相关事件的重要调节因子, 包括纺锤体两极的形成、染色体分离、G2晚期/DNA合成早前期中心体的成熟、Cdc2的激活、APC/C的调节及胞质分裂的完成[18-20]。在大多数人类肿瘤细胞中, PLK1呈现过表达状态, 且这种过表达往往伴随着不良预后, PLK1结构域PBD是位于PLK1 C端的特征结构域, 具有调节酶的催化活性和亚细胞动态定位的重要功能。因此PLK1被公认为是一个潜在的治疗癌症的有效靶点[21, 22]。基于对PLK1在肿瘤发生中作用的认识, 抑制PLK1的活性可以抑制肿瘤的发生发展。
Reindl等[23]以荧光偏振技术从22 461个分子化合物库中筛选出一个可以结合于PBD1的小分子化合物, 从而开创了以小分子干扰PLK1与底物间相互作用从而发挥生物调控作用的先河。近年来, 以“荧光偏振”这种物理学现象为基础的技术正在生命科学研究的多个领域中扮演着越来越重要的角色[24]。该方法不仅快速灵敏而且操作简单, 节约原料, 价格低廉。
目前, 报道的PLK1 PBD抑制剂主要包括小分子抑制剂和多肽类抑制剂, 小分子抑制剂主要包括百里香醌 (thymoquinone, TQ) 及其结构类似物[25]、红倍酚 (purpurogallin, PPG)、马兜铃内酰胺 (aristilactam, AIIIa) 以及绿茶儿茶素类等。但是这些小分子抑制剂多属天然产物, 极大地限制了靶向PLK1 PBD小分子抑制剂的筛选。所以本研究采用了荧光偏振法对本实验室的化合物库进行了高通量筛选, 得到的化合物F083-0063是一类结构新型的抗肿瘤化合物, MTT结果显示F083-0063在HeLa细胞中的抑制作用最为明显; 流式细胞仪结果表明, F083-0063可导致肿瘤细胞的G2/M期阻滞; F083-0063促进HeLa细胞凋亡明显, 量效关系突出; 分子对接也证实了F083-0063与PBD结构域有较强的亲和性; Western blotting证明F083-0063可以引发周期相关蛋白表达量的增加。
综上所述, 由荧光偏振模型筛选出小分子抑制剂F083-0063有较好的抗肿瘤活性和开发使用前景, 随着研究的不断深入, PLK1 PBD为靶点的抗肿瘤药物研究必将进入一个新阶段。
| [1] | Sunkel CE, Glover DM. Polo, a mitotic mutant of Drosophila displaying abnormal spindle poles[J]. J Cell Sic, 1988, 89: 25–38. |
| [2] | Li B, Ouyang B, Pan H, et al. Prk, a cytokine-inducible human protein serine/threonine kinase whose expression appears to be down regulated in lung carcinomas[J]. J Biol Chem, 1996, 271: 19402–19408. DOI:10.1074/jbc.271.32.19402 |
| [3] | Jang YJ, Ma S, Terada Y, et al. Phosphorylation of threonine 210 and the role of serine 137 in the regulation of mammalian polo-like kinase[J]. J Biol Chem, 2002, 277: 44115–44120. DOI:10.1074/jbc.M202172200 |
| [4] | Zhang L, Cao YH, Lu S, et al. Targeting the substrate binding domain of polo-like kinase 1:advances in the study of PBD1 inhibitors[J]. Acta Pharm Sin (药学学报), 2013, 48: 315–324. |
| [5] | Craig SN, Wyatt MD, McInnes C. Current assessment of polo-like kinase as anti-tumor drug targets[J]. Expert Opin Drug Discov, 2014, 9: 773–789. DOI:10.1517/17460441.2014.918100 |
| [6] | Han DP, Zhu QL, Cui JT, et al. Polo-like kinase 1 is over-expressed in colorectal cancer and participates in the migration and invasion of colorectal cells[J]. Med Sci Monit, 2012, 18: BR237–BR246. |
| [7] | Gorlick R, Kolb EA, Keir ST, et al. Initial testing (stage 1) of the polo-like kinase inhibitor volasertib (BI 6727), by the Pediatric Preclinical Testing Program[J]. Pediatr Blood Cancer, 2014, 61: 158–164. DOI:10.1002/pbc.v61.1 |
| [8] | Lee KS, Idle JR. Pinning down the polo-box domain[J]. Chem Biol, 2008, 15: 415–416. DOI:10.1016/j.chembiol.2008.04.009 |
| [9] | Strebhardt K. Multifaceted polo-like kinases:drug targets and antitargets for cancer therapy[J]. Nat Rev Drug Discov, 2010, 9: 643–660. DOI:10.1038/nrd3184 |
| [10] | Yun SM, Moulaei T, Lim D, et al. Structural and functional analyses of minimal phosphopeptides targeting the polo-box domain of polo-like kinase 1[J]. Nat Struct Mol Biol, 2009, 16: 876–882. DOI:10.1038/nsmb.1628 |
| [11] | Liu F, Park JE, Qian WJ, et al. Serendipitous alkylation of a Plk1 ligand uncovers a new binding channel[J]. Nat Chem Biol, 2011, 7: 595–601. DOI:10.1038/nchembio.614 |
| [12] | Richter S, Neundorf I, Loebner K, et al. Phosphopeptides with improved cellular uptake properties as ligands for the polo-box domain of polo-like kinase 1[J]. Med Chem Lett, 2011, 21: 4686–4689. DOI:10.1016/j.bmcl.2011.06.103 |
| [13] | Śledź P, Stubbs CJ, Lang S, et al. From crystal packing to molecular recognition:prediction and discovery of a binding site on the surface of polo-like kinase 1[J]. Angew Chem Int Ed Engl, 2011, 50: 4003–4006. DOI:10.1002/anie.201008019 |
| [14] | Śledź P, Lang S, Stubbs CJ, et al. High-throughput interrogation of ligand binding mode using a fluorescence-based assay[J]. Angew Chem Int Ed Engl, 2012, 51: 7680–7683. DOI:10.1002/anie.201202660 |
| [15] | Qian WJ, Park JE, Lim D, et al. Peptide-based inhibitors of Plk1 polo-box domain containing mono-anionic phos-phothreonine esters and their pivaloyloxymethyl prodrugs[J]. Chem Biol, 2013, 20: 1255–1264. DOI:10.1016/j.chembiol.2013.09.005 |
| [16] | Perrin F. Polarization of light of fluorescence, average life of molecules in the excited state[J]. J Phys Radium, 1926, 7: 390–401. DOI:10.1051/jphysrad:01926007012039000 |
| [17] | Siegel R, Naishadham D, Jemal A. Cancer statistics, 2013[J]. CA Cancer J Clin, 2013, 63: 11–30. DOI:10.3322/caac.v63.1 |
| [18] | Lane HA, Nigg EA. Antibody microinjection reveals an essential role for human polo-like kinase 1 Plk1 in the functional maturation of mitotic centrosomes[J]. J Cell Biol, 1996, 135: 1701–1713. DOI:10.1083/jcb.135.6.1701 |
| [19] | Jiang PD, Zhao YL, Shi W, et al. Cell growth inhibition, G2/M cell cycle arrest, and apoptosis induced by chloroquine in human breast cancer cell line Brap-37[J]. Cell Physiol Biochem, 2008, 22: 431–440. DOI:10.1159/000185488 |
| [20] | Degenhardt Y, Lampkin T. Targeting polo-like kinase in cancer therapy[J]. Clin Cancer Res, 2010, 16: 384–389. DOI:10.1158/1078-0432.CCR-09-1380 |
| [21] | Lowery DM, Mohammad DH, Elia AE, et al. The polo-box domain:a molecular integrator of mitotic kinase cascades and polo-like function[J]. Cell Cycle, 2004, 3: 128–131. |
| [22] | Rudolph D, Steegmaier M, Hoffmann M, et al. BI 6727, a polo-like kinase inhibitor with improved pharmacokinetic profile and broad antitumour activity[J]. Clin Cancer Res, 2009, 15: 3094–3102. DOI:10.1158/1078-0432.CCR-08-2445 |
| [23] | Reindl W, Yuan J, Krämer A, et al. Inhibition of polo-like kinase 1 by blocking polo-box domain-dependent protein-protein interactions[J]. Chem Biol, 2008, 15: 459–466. DOI:10.1016/j.chembiol.2008.03.013 |
| [24] | Chen XN, Leanna L, Kwok PY. Fluorescence polarization in homogeneous nuleic acid analysis[J]. Genome Res, 1999, 9: 492–498. |
| [25] | Yin Z, Song Y, Rehse PH. Thymoquinone blocks pSer/pThr recognition by Plk1 polo-box domain as a phosphate mimic[J]. ACS Chem Biol, 2013, 8: 303–308. DOI:10.1021/cb3004379 |
 2017, Vol. 52
2017, Vol. 52


