近年来,眼用凝胶剂具有使用方便、亲和力强、舒适性好、滞留时间长等优点,受到越来越多的重视[1]。其售价一般也高于同品种滴眼液、眼膏剂等剂型。但国内外药典收载的眼用凝胶剂质量标准中几乎均未收载特定的方法来区分眼用凝胶剂与其他眼用制剂。《中国药典》2015年版已收载了流变仪测定药物黏度的方法,这为研究眼用制剂的流变学性质,提高此类制剂的质量控制水平,促进眼用制剂质量标准的进步起到了极大的作用。本文采用流变仪对4种眼用凝胶剂的流变学指标和参数进行研究,建立眼用凝胶剂流变学性质的质量控制方法,并与3种非凝胶型眼用制剂进行对比,验证了方法的专属性、可靠性与准确性。
材料与方法仪器 Malvern Kinexus流变仪; 锥平板模具; CP4/40转子 (直径40 mm,锥角4°)。
眼用凝胶剂 卡波姆眼用凝胶 (批号: 344,德国博士伦制药有限公司); 维生素A棕榈酸酯眼用凝胶 (批号: 418889,瑞士诺华制药有限公司); 重组牛碱性成纤维细胞生长因子眼用凝胶 (批号: 20150606,珠海亿胜生物制药有限公司); 小牛血去氧蛋白提取物眼用凝胶。
溶液型滴眼液 溴莫尼定噻吗洛尔滴眼液 (批号: E75964,爱尔兰爱尔建制药有限公司)。
混悬型滴眼液 夫西地酸滴眼液 (混悬型,批号: EL1258,爱尔兰利奥制药有限公司)。
眼膏剂 盐酸金霉素眼膏 (批号: 130310,上海通用药业股份有限公司)。
性状观察 取上述7种眼用制剂各约1 mL,置于玻璃载玻片上,观察各自的扩散情况。
非稳态流变学研究
应变扫描 取上述7种眼用制剂各约2 mL置流变仪锥板式模具上,用CP4/40转子,在温度为25.0 ℃,扫描频率为1 Hz,应变范围为0.1%~150%进行应变扫描,记录弹性/黏性模量-应变曲线。
频率扫描 取上述7种眼用制剂各约2 mL置流变仪锥板式模具上,用CP4/40转子,在温度为25.0 ℃,应变为0.5%,扫描频率为0.1~10 Hz进行频率扫描,记录弹性/黏性模量-频率曲线。
稳态流变学研究
流变曲线 取上述7种眼用制剂各约2 mL置于流变仪的锥板式模具上,用CP4/40转子,测量温度设定为25.0 ℃,剪切速率为0.1~200 s-1内测定样品的动力黏度,记录动力黏度-剪切速率曲线。
屈服应力测定 取上述7种眼用制剂各约2 mL置于流变仪的锥板式模具上,用CP4/40转子,在温度为25.0 ℃,逐渐增加施加于样品的剪切应力值,测定7种眼用制剂动力黏度的变化情况。根据测定结果,仪器自动计算各屈服应力值。
触变性 取上述7种眼用制剂各约2 mL置流变仪锥板式模具上,温度为25.0 ℃,在1 s-1连续剪切50 s后,立即将剪切速率增大至100 s-1连续剪切50 s; 再将剪切速率恢复至1 s-1,继续剪切50 s。记录7种眼用制剂的动力黏度变化情况。
动力黏度 取上述7种眼用制剂各约2 mL置流变仪锥板式模具上,在温度为25.0 ℃,剪切速率为10、25、50、100和150 s-1条件下,记录样品的动力黏度。
结果 1 性状观察小牛血去氧蛋白提取物眼用凝胶、溴莫尼定噻吗洛尔滴眼液和夫西地酸滴眼液 (混悬型) 均能在玻璃载玻片表面上自由扩散,呈溶液状态; 其他3种眼用凝胶剂与盐酸金霉素眼膏均呈堆积状态,不易扩散。
2 非稳态流变学研究 2.1 应变扫描应变扫描是固定扫描频率,观察弹性/黏性模量在不同应变条件下的变化情况,其意义在于确定样品的线性黏弹区范围,因为只有在线性黏弹区范围内测量才能获得样品的特性流变学常数[2, 3]。
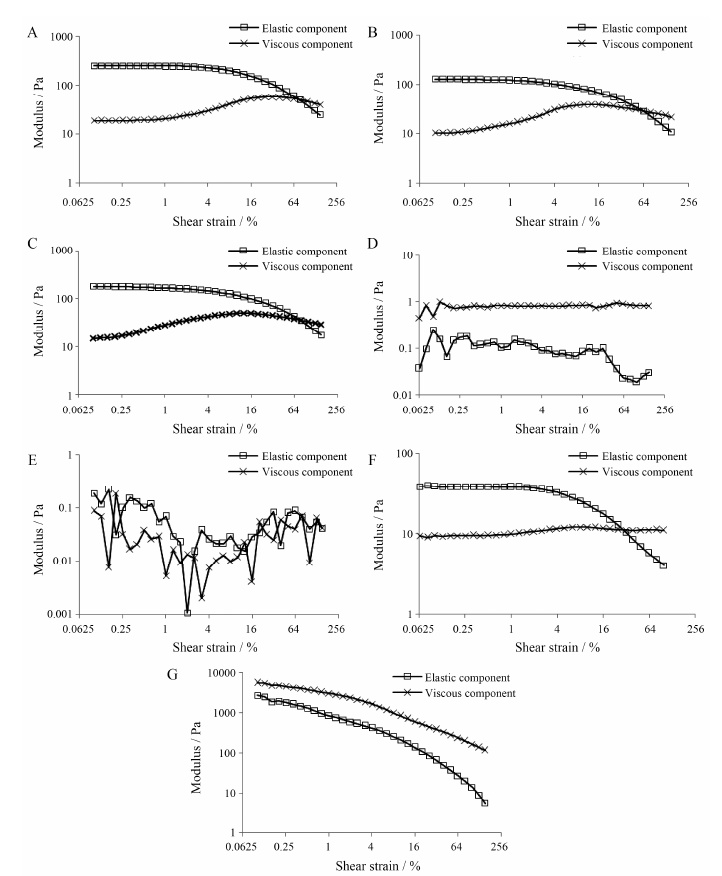
7种眼用制剂在温度为25.0 ℃,扫描频率为1 Hz,应变范围为0.1%~150% 的弹性/黏性模量-应变曲线见图 1。由图 1可知,7种眼用制剂中卡波姆眼用凝胶、维生素A棕榈酸酯眼用凝胶、重组牛碱性成纤维细胞生长因子眼用凝胶3种凝胶剂和夫西地酸滴眼液 (混悬型) 的线性黏弹区[4, 5]均为0.1%~1%。在该范围内弹性模量基本不变,且均大于黏性模量[6]; 而小牛血去氧蛋白提取物眼用凝胶和盐酸金霉素眼膏在该应变范围内,弹性模量始终小于黏性模量; 溴莫尼定噻吗洛尔滴眼液无明显的线性黏弹区,呈溶液状态; 小牛血去氧蛋白提取物眼用凝胶与溴莫尼定噻吗洛尔滴眼液的弹性模量和黏性模量均远远小于其他5种眼用制剂,均不呈显著的凝胶特性。
|
Figure 1 Elastic/viscous component curves of seven ophthalmic preparations with differentshear strain at 25 ℃ and 1 Hz. A: Carbomer eye gel (sample A); B: Vitamin A palmitate eye gel (sample B); C: Recombinant bovine basic fibroblast growth factor eye gel (sample C); D: Deproteinized calf blood extract eye gel (sample D); E: Brimonidine tartrate and timolol maleate eye drops (sample E); F: Fusidic acid eye drops (sample F); G: Chlortetracycline hydrochloride eye ointment (sample G) |
频率扫描是选择线性黏弹区范围内的某个应变条件,扫描不同频率,观察弹性/黏性模量的变化情况,其意义在于比较线性黏弹区范围内弹性模量和黏性模量的大小。
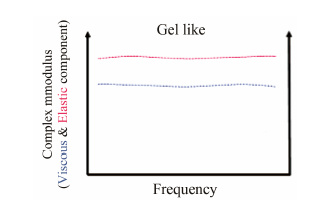
在温度为25.0 ℃,剪切应变为0.5% 的条件下,7种眼用制剂在0.1~10 Hz内的弹性/黏性模量-频率曲线见图 2。马尔文流变仪对应工作站给出的凝胶剂典型频率扫描图谱见图 3。由图 3可知,凝胶剂在线性黏弹区范围内,弹性模量应大于黏性模量。由上述结果可知,7种眼用制剂中小牛血去氧蛋白提取物眼用凝胶、溴莫尼定噻吗洛尔滴眼液和盐酸金霉素眼膏的曲线与凝胶剂典型频率扫描图谱不一致; 而其他3种眼用凝胶剂及夫西地酸滴眼液 (混悬型) 的曲线图均与凝胶剂典型扫描图谱一致。

|
Figure 2 Elastic/viscous component curves of seven ophthalmic preparations with different frequency at 25 ℃ and 0.5% shear strain. A: Sample A; B: Sample B; C: Sample C; D: Sample D; E: Sample E; F: Sample F; G: Sample G |
|
Figure 3 The classic elastic/viscous component curve with different frequency of gels |
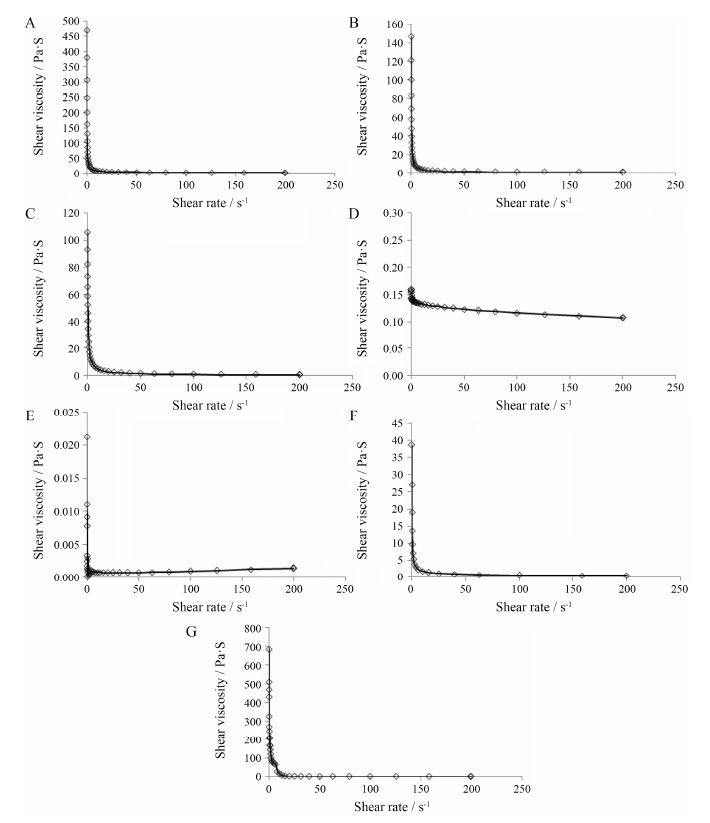
7种眼用制剂在温度25.0 ℃,剪切速率为0.1~200 s-1的动力黏度-剪切速率曲线见图 4。
|
Figure 4 Shear viscosity curves of seven ophthalmic preparations with different shear rate at 25 ℃. A: Sample A; B:Sample B; C: Sample C; D: Sample D; E: Sample E; F: Sample F; G: Sample G |
采用幂律方程: τ = K·γn (式中τ为剪切应力,K为流体的稠度系数,γ为剪切速率,n为流动指数) 对上述样品的流变曲线进行拟合,结果见表 1。幂律方程中,当n = 1时,为牛顿流体; n < 1时,为剪切变稀的非牛顿流体,也即假塑性流体; 当n >1时,为剪切变稠的非牛顿流体,又叫涨塑性流体[7, 8]。
| Table 1 The regression results of seven ophthalmic prepara tions with power-law equation at 25 ℃. K: Consistency index; n: Flow index |
由图 4和表 1可知,7种眼用制剂中,除小牛血去氧蛋白提取物眼用凝胶的动力黏度随剪切速率的增大变化不明显外,其余5种眼用制剂的动力黏度均随着剪切速率的增大而显著减小。另从表 1可见,只有小牛血去氧蛋白提取物眼用凝胶的流动指数接近于1,且其黏度系数远远小于其余3种眼用凝胶剂,这说明小牛血去氧蛋白提取物眼用凝胶近似为牛顿流体,而其余6种眼用制剂均为剪切变稀的假塑性非牛顿流体[9]。
3.2 屈服应力的研究屈服应力是指流体在剪切应力的作用下发生形变的阈值[10, 11]。7种眼用制剂的屈服应力值见表 2。实验结果表明,小牛血去氧蛋白提取物眼用凝胶与溴莫尼定噻吗洛尔滴眼液的屈服应力值相似,均远远低于其他5种眼用制剂。这表明二者不需要施加太大的剪切应力即可发生流动。而卡波姆眼用凝胶与盐酸金霉素眼膏的屈服应力均较大,这表明它们较难发生形变或流动[12]。
| Table 2 Yield stress of seven ophthalmic preparations at 25 ℃ |
眼用凝胶剂应具有触变性,即一触即变的性质,在低剪切时有较高黏度; 在高剪切时有较低黏度; 再恢复低剪切时,黏度也快速恢复。
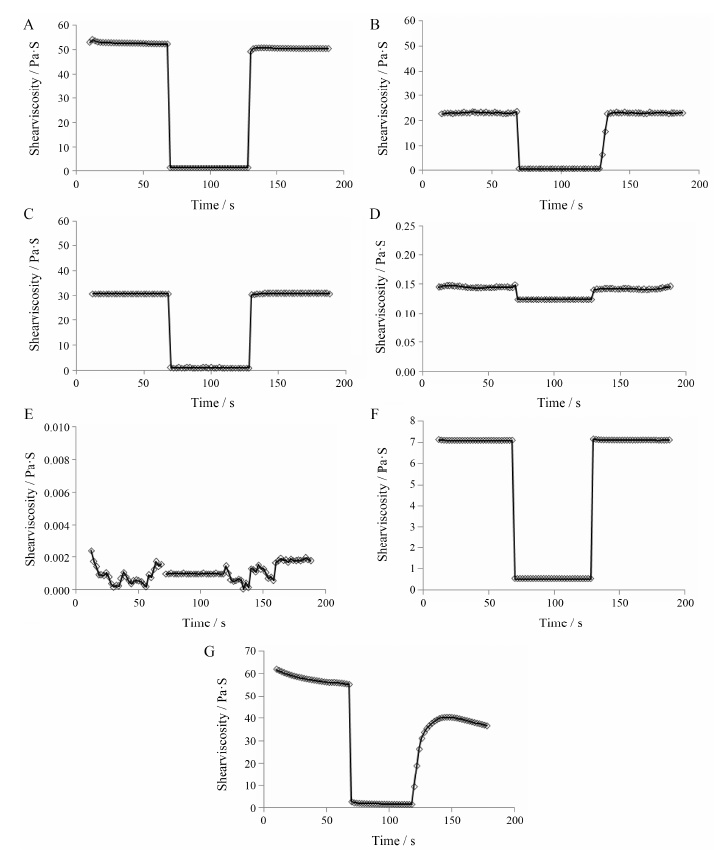
本文采用了三阶段法分析样品的触变性[13]。7种眼用制剂的动力黏度变化情况见图 5。实验表明,7种眼用制剂中,小牛血去氧蛋白提取物眼用凝胶、溴莫尼定噻吗洛尔滴眼液和盐酸金霉素眼膏的触变性较小,其他4种眼用制剂均为触变性较大的流体。
|
Figure 5 Shear viscosity curves of seven ophthalmic preparations with high and low shear rate at 25 ℃. A: Sample A; B: Sample B; C: Sample C; D: Sample D; E: Sample E; F: Sample F; G: Sample G |
在温度为25 ℃,剪切速率为10、25、50、100和150 s-1的条件下,测定7种眼用制剂的动力黏度。在上述各剪切速率条件下,均连续剪切1 min,每隔2 s记录1次动力黏度值,取28个测定点 (舍弃前两个点) 计算动力黏度的平均值,结果见表 3。实验结果表明,在5个不同的剪切速率下,小牛血去氧蛋白提取物眼用凝胶的动力黏度测定值远远小于其他3种眼用凝胶剂。而这3种眼用凝胶剂的动力黏度值比较近似。故判断小牛血去氧蛋白提取物眼用凝胶可能并非是凝胶型制剂。
| Table 3 Shear viscosity of seven ophthalmic preparations with different shear rate at 25 ℃ |
文献[14]表明国外大部分眼用制剂在处方设计阶段都依据释药特性进行过流变学性质的研究,而国内的研究机构在眼用制剂流变学研究方面仅局限在测定样品在单个剪切速率时动力黏度的大小,从未涉及到对黏弹性相对大小的控制。而眼用凝胶剂具有不同于滴眼液的流变学特征[4]。本文通过研究,认为眼用凝胶剂的流变学特征指标有5个 (表 4)。通过这5个指标可以全面合理地对眼用凝胶剂进行质量控制,为眼用凝胶剂的处方研究、生产工艺和质量标准的改进提供流变学方面的参考依据。
| Table 4 The comparison of rheological parameters between ophthalmic gels and non-ophthalmic gels. √: Means match the parameters; ×: Means doesn’t match the parameters |
非稳态流变学研究表明,眼用凝胶剂在低剪切时,即静态状态下,弹性模量较大,不易流动,制剂性质较为稳定; 在高剪切时,黏性模量较大,流动性增强。在线性黏弹区范围内,弹性模量和黏性模量均比较稳定,且弹性模量应大于黏性模量。稳态流变学研究表明,眼用凝胶剂为剪切变稀的假塑性非牛顿流体,其优点为在低剪切时高黏度利于制剂在贮藏时的稳定性和均匀性; 在高剪切时,即在使用时,黏度快速降低有利于凝胶剂在眼部的涂布,提高患者的使用舒适性[8]。屈服应力是指流体发生流动时所需的最小剪切应力值。眼用凝胶剂均具有一定大小的屈服应力值,这样可以保证凝胶剂在挤出涂布时,不会像滴眼液一样极易流出眼外而降低生物利用度[9]。眼用凝胶剂为触变性流体,其触变性体现在,当滴入眼睛后,随着眼睑眨动带来的快速剪切,凝胶剂黏度迅速降低,有利于制剂在眼球表面的涂布; 当眼睑停止眨动后,剪切停止,凝胶剂黏度迅速恢复。这个特性可以延长药物在眼球表面的停留时间,增加载药在眼部的释放,提高生物利用度[15]。
通过对7种眼用制剂非稳态与稳态流变学性质的研究,发现4种眼用凝胶剂中,小牛血去氧蛋白提取物眼用凝胶与其余3种凝胶剂的流变学性质有显著差异,而与滴眼液相似。故判断其不是凝胶型眼用制剂,而是溶液型眼用制剂。经实验发现,本研究中夫西地酸滴眼液 (混悬型) 的流变学性质呈显著的凝胶特性。故判断该滴眼液实为眼用凝胶剂,而非溶液型滴眼液。
结论综上所述,眼用凝胶剂的特征流变学指标为: ①在线性黏弹区范围内弹性模量应大于黏性模量; ② 应为剪切变稀型非牛顿流体; ③ 应具有一定大小的屈服应力; ④ 应为触变性凝胶。参考性指标为: 在25 ℃、剪切速率为50 s-1时,动力黏度应大于0.5 Pa·S。
| [1] | Wang ZG. The recent research and development of ophthalmic gels[J]. China Licens Pharm (中国执业药师), 2012, 9: 33–36. |
| [2] | Liu YL, Zhang XL, Wang YP, et al. Evaluation on rheological properties of dange ophthalmic in-situ gel and its common gel[J]. Chin Trad Herb Drugs (中草药), 2014, 45: 1388–1392. |
| [3] | Jens C, Annick L. Optimisation of carbomer viscous eye drops:an in vitro experimental design approach using rheological techniques[J]. Eur J Pharm Biopharm, 2002, 54: 41–50. DOI:10.1016/S0939-6411(02)00036-X |
| [4] | Lu XG, Zhang GZ, Liu G, et al. Steady state vs dynamic rheology measurement of gel crude oil[J]. Oil Gas Stor Trans (油气储运), 2013, 32: 27–30. |
| [5] | Luo ML, Jia Zl, Sun HT, et al. Rheological properties of environment-friendly MES viscoelastic micelle solutions[J]. Appl Chem Ind (应用化学), 2012, 41: 8–15. |
| [6] | Wu XL, Ma JF, Nie L, et al. Rheological property and dynamic viscosity determination method of fusidic acid eye drop[J]. Chin J Pharm Aff (中国药事), 2016, 30: 401–405. |
| [7] | Chen YP, Wang LB, Shao H, et al. Study on determination method of dynamic viscosity of hydroxypropylcellulose[J]. Chin J Pharm Anal (药物分析杂志), 2011, 31: 2252–2255. |
| [8] | Wang LB, Liu W, Chen ZK, et al. Research on method for measurement of the dynamic viscosity of vitamin A palmitate gel[J]. Chin J Pharm Anal (药物分析杂志), 2009, 29: 2040–2043. |
| [9] | Mattias P, Helene H, Katarina E. Rheological studies of the gelation of deacetylated gellan gum (Gelrite) in physiological conditions[J]. Eur J Pharm Sci, 1999, 9: 99–105. DOI:10.1016/S0928-0987(99)00051-2 |
| [10] | Chen YP, Wang LB, Shao H, et al. Determination method of dynamic viscosity of methylcellulose[J]. Chin Pharm J (中国药学杂志), 2013, 48: 385–388. |
| [11] | Giulia B, Sante M, Giovanni F, et al. Rheological, mucoadhesive and release properties of Carbopol gels in hydrophilic cosolvents[J]. Int J pharm, 2004, 282: 115–130. DOI:10.1016/j.ijpharm.2004.06.012 |
| [12] | Yoon WB, Kim BY, Park JW. Rheological characteristics of fibrinogen-thrombin solution and its effects on Surimi gels[J]. J Food Sci, 1999, 64: 291–294. DOI:10.1111/jfds.1999.64.issue-2 |
| [13] | Hu J, Chen DW, Quan DQ. Rheological properties of poloxamer 407 aqueous solutions[J]. Acta Pharm Sin (药学学报), 2011, 46: 227–231. |
| [14] | Katarina E, Johan C, Roger P. Rheological evaluation of poloxamer as an in situ gel for ophthalmic use[J]. Eur J Pharm Sci, 1998, 6: 105–112. DOI:10.1016/S0928-0987(97)00075-4 |
| [15] | Li Y, Tang Z, Wang Q. Recent advances of in situ gel for ocular drug delivery[J]. Chin Pharm J (中国药学杂志), 2015, 50: 1174–1179. |
 2017, Vol. 52
2017, Vol. 52


