2. 呼吸疾病诊疗与新药研发河南省协同创新中心, 河南 郑州 450046;
3. 河南中医药大学药学院, 河南 郑州 450046
2. Collaborative Innovation Center for Respiratory Disease Diagnosis and Treatment and Chinese Medicine Development of Henan Province, Zhengzhou 450046, China;
3. College of Pharmacy, Henan University of Chinese Medicine, Zhengzhou 450046, China
葶苈子为常用中药材, 始载于《神农本草经》, 列为草部下品, 该药味辛、苦, 性大寒, 归肺与膀胱经, 具有宣泄平喘、行水消肿的功效。2015版《中国药典》收录的“葶苈子”有南北之分, 其中十字花科植物独行菜Lepidium apetalum Willd.的干燥成熟种子习称“北葶苈子”, 而播娘蒿Descurainia sophia (L.) Webbex Prantl.的干燥成熟种子习称“南葶苈子”[1]。虽然南北葶苈子都做正品葶苈子用, 但其植物来源、外观性状和药理活性均有所差异[2, 3]。然而, 目前对南葶苈子各方面的研究较为全面, 而北葶苈子的相关研究较少。现代药理学表明, 北葶苈子主要具有强心作用, 而其化学成分主要是黄酮类。本文采用多种色谱技术从北葶苈子中分离得到3个化合物, 其中化合物1是一个新的苯乙酰胺类化合物, 命名为N-[(7'-胺基)苯次甲基]苯乙酰胺, 通过波谱和理化性质鉴定其结构, 命名为葶苈胺A。化合物2、3为硫苷类化合物, 是首次从该植物中分离得到, 并首次对化合物desulfoglucotropaeolin的构型进行确定。结构见图 1。
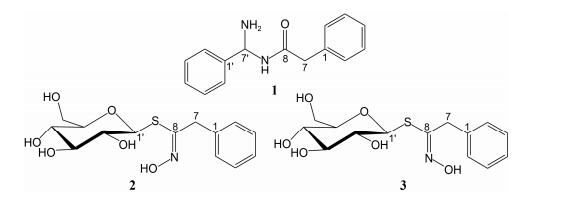 | Figure 1 Structures of compounds 1-3 |
化合物1为黄色结晶粉末(CH3OH)。HR-TOF-MS给出分子离子峰m/z: 241.133 6 [M]+ (计算值为241.133 5), 提示化合物的分子式为C15H16N2O。在1H NMR (CD3OD, 500 MHz)中, 在低场区共有10个氢信号, 分别为δ7.52 (2H, m, H-2, 6)、7.42 (3H, m, H-3, 4, 5)、7.31 (2H, m, H-2', 6')和7.26 (3H, m, H-3', 4', 5'), 说明结构中有两个单取代苯环; δ 6.01 (1H, s, H-7')提示结构中有一个-CH, δ 4.54 (2H, s, H-7)提示结构中有一个-CH2。在13C NMR (CD3OD, 125 MHz)中, 共给出11个碳信号, 其中136.3 (C-1)、127.9 (C-2, 6)、130.0 (C-3, 5)、130.7 (C-4)和135.6 (C-1')、128.5 (C-2', 6')、129.9 (C-3', 5')、129.2 (C-4')为两个单取代苯环的特征信号[4]; 168.2是C=O的特征信号; 76.9是CH的特征信号; 46.8是CH2的特征信号, 在HSQC谱中, δH6.01 (H-7')与δC 76.9 (C-7')相关、δH 4.54 (H-7)与δC 46.8 (C-7)相关。在HMBC谱中(图 2), δH6.01和4.54均与δC 168.2相关、δH 6.01与δC 127.9和130.7有远程相关、δH 4.54与δC 128.5和129.2有远程相关[5]。综上所述, 化合物1的结构确定为N-氨苄基苯乙酰胺[N-(amino benzyl)-2-phenylacetamide], 为新化合物, 命名为葶苈胺A (lepidiumamide A)。其1H NMR和13C NMR数据见表 1。
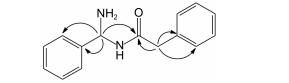 | Figure 2 Key HMBC correlations of compound 1 |
| Table 1 1H NMR (500 MHz in CD3OD) and 13C NMR (125 MHz in CD3OD) spectral data of compound 1 |
化合物2为白色粉末(MeOD), HR-TOF-MS给出准分子离子峰m/z 330.101 3 [M+H]+(计算值为330.101 1), 提示化合物的分子式为C14H19NO6S。在1H NMR (DMSO-d6, 500 MHz)中, 在低场区δ 7.25 (4H, m)、δ7.20 (1H, m), 说明结构中有一个单取代苯环; δ 3.82 (2H, s)提示结构中有一个-CH2。在13C NMR (DMSO-d6, 125 MHz)中, 共给出12个碳信号, 其中136.1 (C-1)、129.0 (C-2, 6)、128.3 (C-3, 5)、126.4 (C-4)为单取代苯环的特征信号; 153.1是-C=N-基团的特征信号; 83.0 (C-1')、72.4 (C-2')、78.3 (C-3')、69.4 (C-4')、81.0 (C-5')、60.6 (C-6')是葡萄糖硫苷的特征信号[6], 结合1H NMR中4.84 (1H, d, J=10.0 Hz), 说明该葡萄糖为β-构型。在HSQC谱中, δH3.82 (H-7)与δC 36.8 (C-7)相关、δH 4.84 (H-1')与δC 83.0 (C-1')相关。在HMBC谱中, δH3.82与δC 136.1和153.1相关、δH 4.84和11.25与δC 153.1有远程相关, 说明该结构为desulfoglucotropaeolin[7, 8]。而根据NOE谱中, δH 11.25与3.82无相关信号, 说明该化合物中-C=N-的构型为cis-构型。综上所述, 化合物2的结构确定为cis-desulfoglucotropaeolin, 其结构和主要远程相关见图 1和图 3。其1H NMR、13C NMR数据见表 2。
 | Figure 3 Key HMBC and NOE correlations of compound 2and3 |
| Table 2 1H NMR (500 MHz in DMSO-d6) and 13C NMR (125 MHz in DMSO-d6) spectral data of compound 2 and3 |
化合物3为无色结晶粉末(MeOD), HR-TOF-MS给出准分子离子峰m/z 330.101 4 [M+H]+ (计算值为330.101 1), 提示化合物的分子式为C14H19NO6S。在1H NMR (DMSO-d6, 500 MHz)中, 在低场区δ 7.27 (5H, m), 说明结构中有一个单取代苯环。在13C NMR (DMSO-d6, 125 MHz)中, 共给出11个碳信号, 其中137.4 (C-1)、128.4 (C-2, 3, 5, 6)、126.4 (C-4)为单取代苯环的特征信号; 150.9是-C=N-基团的特征信号; 81.2 (C-1')、73.0 (C-2')、78.1 (C-3')、69.9 (C-4')、81.0 (C-5')、61.1 (C-6')是葡萄糖硫苷的特征信号[6], 37.7是-CH2-的碳信号。其碳信号的个数与结构片段与化合物2类似。在HSQC谱中, δH4.02 (1H, d, J=16.0 Hz)和3.85 (1H, d, J=16.0 Hz)与δC 37.7相关、δH 4.41 (H-1')与δC 81.2 (C-1')相关。在HMBC谱中, δH4.02和3.85均与δC 137.4和150.9相关、δH 4.41和11.15与δC 150.9有远程相关, 说明该结构也为desulfoglucotropaeolin[7, 8]。而在NOE谱中, δH 11.15与4.02有相关信号, 说明该化合物中-C=N-的构型为trans-构型。综上所述, 化合物3的结构确定为trans-desulfoglucotropaeolin, 其结构和主要远程相关见图 1和3。其1H NMR、13C NMR数据见表 2。
虽然化合物desulfoglucotropaeolin已有报道, 但在文献[7, 8]中提出的是cis-desulfoglucotropaeolin构型, 而其碳谱和氢谱数据与trans-desulfoglucotropaeolin是一致的。因此, 本文对这两种构型进行结构分析, 并对其波谱数据进行归属。
实验部分Bruker AVANCE Ⅲ 500核磁共振仪, TMS为内标; Bruker maxis HD型飞行时间质谱仪(德国); LC50型高压制备液相色谱仪由赛谱锐思(北京)科技有限公司生产, 紫外检测器为(UV200), 色谱柱为(YMC-Pack ODS-A, 250 mm × 10 mm. D. S-5 μm, 12 μm); 柱色谱填充剂所用Diaion HP-20、MCI Gel CHP-20、Toyopearl HW-40为日本三菱化学公司生产, Sephadex LH-20为Parmacia Biotech公司生产, 柱色谱所用硅胶H (160~200目)为青岛海洋化工厂生产, 所用分析纯和色谱纯试剂为北京化工厂和天津第三化学试剂厂生产。
本课题所选的北葶苈子, 采自河南南阳, 经河南中医药大学陈随清教授和董诚明教授鉴定为十字花科植物独行菜(Lepidium apetalum Willd.)的干燥成熟种子。
1 提取与分离北葶苈子首先采用清炒法, 于240 ℃下炒制5.5 min对其进行炮制。称取炮制后的北葶苈子8 kg, 加10倍量水提取3次, 每次1.5 h, 提取液减压浓缩, 浓缩液以80%乙醇沉淀, 上清液离心过滤, 浓缩至无醇味, 用Dianion HP-20柱进行色谱分离, 依次用水、20%乙醇、40%乙醇、60%乙醇和95%乙醇洗脱, 将各部位减压浓缩干燥, 分别得到361、71、89、67和28 g。其中20%乙醇洗脱组分(71 g)通过Toyopearl HW-40柱色谱, 甲醇−水(0%→100%)洗脱, 得组分A1~A5。组分A2 (15 g)经ODS-18反相柱色谱, 甲醇−水(0%→100%)洗脱, 得到B1~B7。组分B4经Sephadex LH-20柱色谱, 70%甲醇−水洗脱, 得到组分C1~C3。组分C2再经半制备HPLC分离, 流动相为甲醇−水(32:68)得到化合物2 (32 mg, tR=40.6 min)和化合物3 (13 mg, tR=86.6 min)。组分B5经Toyopearl HW-40柱色谱, 70%甲醇−水洗脱, 得到组分D1~D3。组分D3再经半制备HPLC分离, 流动相为甲醇−水(42:58), 得到化合物1 (12 mg, tR=51.1 min)。
2 结构鉴定化合物1黄色粉末。[α]20 D −3.88 (c 0.12, MeOD); UV λmax (MeOH)/nm (logε): 206 (1.94); IR νmax/cm−1:3 371, 2 926, 2 845, 2 518, 1 653, 1 454, 1 237, 1 116, 1 020, 804, 698; HR-TOF-MS m/z 241.133 6 [M]+ (calcd. C15H17N2O, 241.133 5); 1H NMR (500 MHz, MeOD)和13C NMR (125 MHz, MeOD)数据见表 1。
化合物2白色粉末。[α]20 D −33.9 (c 0.10, MeOD); UV λmax (MeOH)/nm (logε): 207 (1.37), 228 (0.63); IR νmax/cm−1: 3 325, 2 942, 2 834, 1 656, 1 593, 1 493, 1 451, 1 376, 1 227, 1 187, 1 091, 1 029, 976, 883, 706; HR-TOF-MS m/z 330.101 3 [M+H]+(calcd. C14H19NO6S, 330.101 1); 1H NMR (500 MHz, DMSO-d6)和13C NMR (125 MHz, DMSO-d6)数据见表 2。
化合物3无色结晶性粉末。[α]20 D −14.8 (c 0.10, MeOD); UV λmax (MeOH)/nm (logε): 209 (2.92), 230 (1.19); IR νmax/cm−1: 3 284, 2 923, 1 666, 1 583, 1 453, 1 370, 1 228, 1 187, 1 102, 976, 880, 810, 706; HR-TOF-MS m/z 330.101 4 [M+H]+(calcd. C14H19NO6S, 330.101 1); 1H NMR (500 MHz, DMSO-d6)和13C NMR (125 MHz, DMSO-d6)数据见表 2。
| [1] | Chinese Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[M].Part 1. Beijing: China Medical Science Press, 2015 : 313 -314. |
| [2] | Zhou XD, Tang LY, Zhou GH, et al. Advances on Lepidii semen and Descurainiae semen[J]. China J Chin Mater Med (中国中药杂志), 2014, 39 :4699–4708. |
| [3] | Shi PP, Chao LP, Wang TT, et al. New bioactive flavonoid glycosides isolated from the seeds of Lepidium apetalum Willd[J]. Fitoterapia, 2015, 103 :197–205. DOI:10.1016/j.fitote.2015.04.007 |
| [4] | Fan QL, Huang WH, Guo BL. Chemical constituents of Semen lepidii Sativi[J]. J Anhui Agric Sci (安徽农业科学), 2014, 42 :3533–3534. |
| [5] | Khalil AT. Benzylamides from Salvadora persica[J]. Arch Pharm Res, 2006, 29 :952–956. DOI:10.1007/BF02969277 |
| [6] | Feng WS, Li CG, Zheng XK, et al. Three new sulphur glycosides from the seeds of Descurainia sophia[J]. Nat Prod Res, 2016, 30 :1675–1681. DOI:10.1080/14786419.2015.1135141 |
| [7] | Kiddle G, Bennett RN, Botting NP, et al. High-performance liquid chromatographic separation of natural and synthetic desulphoglucosinolates and their chemical validation by UV, NMR and chemical ionisation-MS methods[J]. Phytochem Anal, 2001, 12 :226–242. DOI:10.1002/(ISSN)1099-1565 |
| [8] | Bai N, He K, Roller M, et al. Flavonolignans and other constituents from Lepidium meyenii with activities in antiinflammation and human cancer cell lines[J]. J Agric Food Chem, 2015, 63 :2458–2463. DOI:10.1021/acs.jafc.5b00219 |
 2016, Vol. 51
2016, Vol. 51


