2. 广东省中医药工程技术研究院, 广东省中医药研究开发重点实验室, 广东 广州 510095;
3. 中国医学科学院、北京协和医学院药用植物研究所, 中药(天然产物)创新药物研发北京市重点实验室, 北京 100193
2. Guangdong Province Engineering Technology Research Institute of Traditional Chinese Medicine, Guangdong Provincial Key Laboratory of Research and Development in Traditional Chinese Medicine, Guangzhou 510095, China;
3. Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing Key Laboratory of Research and Development in Traditional Chinese Medicine(Natural Products), Beijing 100193, China
帕金森病 (Parkinson’s disease,PD) 是临床上较为常见的中枢神经系统退行性病变,以运动功能缺陷,包括静止性震颤、肌强直、运动迟缓和姿势步态异常为特征。帕金森病的病理改变主要为黑质多巴胺能神经元的选择性丢失以及纹状体中多巴胺水平的降低[1]。
虽然目前PD的发病机制尚未明确,但已有研究表明氧化应激是导致帕金森病的多巴胺能神经元死亡的关键机制[2]。氧化应激是一种活性氧产生压倒了内源性抗氧化酶系统的不平衡状态,过量产生的活性氧促进了帕金森病的发生。活性氧能够引起线粒体功能失调并激活凋亡信号通路,导致神经细胞功能失调和凋亡。所以,抗氧化应激成为神经保护并防治帕金森病的重要策略。
目前PD的治疗仍以左旋多巴的替代治疗为主,但是存在严重的不良反应,临床也缺乏理想的治疗药物。三七总皂苷是三七的主要活性成分,在帕金森病体内实验中表现出神经保护作用。另外,三七总皂苷中单体成分如Rg1和Re同样在帕金森病体内实验中表现出神经保护作用[3,4]。但是,三七总皂苷是否通过抑制氧化应激发挥神经保护作用,目前还不清楚。深入研究三七总皂苷抗PD的作用靶点和分子机制,对PD的药物研发具有重要意义。
血红素加氧酶 (HO-1)、超氧化物歧化酶 (SOD)、过氧化氢酶 (CAT) 和谷胱甘肽过氧化物酶 (GSH-Px) 等抗氧化酶在神经氧化损伤的保护过程中发挥关键的作用。很多药物能够通过激活Nrf2信号通路上调抗氧化酶,增强神经细胞对氧化应激的抵抗能力[5]。Nrf2的激活是抗氧化酶转录表达的关键起始步骤。静息状态下,Nrf2在胞浆中与Keap1结合形成无活性的复合体。药物干预后,Nrf2从Nrf2-Keap1复合物中释放出来,转位至细胞核内与抗氧化反应元件 (ARE) 序列相互作用,促进抗氧化酶的表达[6]。三七总皂苷是否通过激活Nrf2信号通路上调抗氧化酶,从而发挥神经保护作用,目前还不清楚。因此,本研究采用6-OHDA致SH-SY5Y细胞凋亡的PD体外模型,探讨三七总皂苷的细胞保护作用,并通过检测Nrf2/HO-1信号通路的变化,对其作用机制进行初步探讨。
材料与方法 药物与试剂三七总皂苷购自上海融禾医药科技发展有限公司; SH-SY5Y细胞由中国医学科学院北京协和医学院细胞库提供; DMEM培养基、胎牛血清、青霉素−链霉素购自美国Gibco公司; 胰蛋白酶购自Amersco公司; 6-OHDA购自美国Sigma-Aldrich公司; TUNEL检测试剂盒购自美国Roche公司; 乳酸脱氢酶 (LDH)、MDA、SOD、CAT和GSH-Px检测试剂盒购自南京建成生物工程研究所; 活性氧自由基 (ROS) 检测试剂盒和JC-1购自美国Enzolife Sciences公司; caspase-3荧光检测试剂盒购自美国BioVision; RIPA蛋白裂解液、蛋白酶抑制剂和BCA蛋白定量 试剂盒购自Pierce Biotechnology公司; Nrf2和HO-1抗体购自美国Santa Cruz Biotechnology公司。原人 参二醇类皂苷、原人参三醇类皂苷购自上海融禾医 药科技发展有限公司; 4',6-二脒基-2-苯基吲哚 (4'-6- diamidino-2-phenylindole,DAPI) 购自碧云天生物技术公司; SDS-聚丙烯酰胺凝胶电泳配胶试剂盒购自康为世纪生物科技有限公司。
主要仪器超净工作台购自上海智成分析仪器制造有限公司; 二氧化碳培养箱购自美国Thermo Scientific公司; 倒置相差显微镜购自日本Olympus公司; 离心机购自中国Anke公司; 酶标仪购自美国Bio- Tek公司; 荧光显微镜购自德国Leica公司; PYY-7C型电泳仪购自北京市六一仪器厂; Chemi DOCTM型凝胶成像系统购自美国Bio-Rad公司。
细胞培养和药物配制SH-SY5Y细胞接种于含10% 胎牛血清、100 u·mL−1青霉素和100 μg·mL−1链霉素的DMEM高糖培养基中,37 ℃、5% CO2条件 下培养,培养液每2天更换1次。待单层细胞80% 融合后,用0.25% 胰蛋白酶消化,传代培养,取对数生长期细胞进行实验。三七总皂苷溶于DMSO,配制 成储备溶液 (100 g·L−1),然后稀释成所需浓度使用。6-OHDA溶解于含0.1% 抗坏血酸的无菌蒸馏水中,配制储备溶液 (1 mol·L−1),置于4 ℃贮存备用,实验时用无血清高糖稀释至终浓度为25、50、100和200 μmol·L−1的工作液。原人参二醇类皂苷、原人参三醇类皂苷溶于DMSO,配制成储备溶液 (100 g·L−1),然后稀释成所需浓度使用。实验分为以下4组: 空白对照组 (DMEM中添加等量DMSO,浓度不高于0.1%)、模型组 (在培养液中加入终浓度为100 μmol·L−1 6-OHDA培养24 h)、三七总皂苷干预组 (加入终质量浓度为25 μg·mL−1三七总皂苷作用24 h后,加入100 μmol·L−1 6-OHDA继续培养24 h)、单加药组 (加入终质量浓度为25 μg·mL−1三七总皂苷作用24 h)。
MTT 法检测细胞存活率SH-SY5Y细胞以每毫升1×105个接种于96孔板,培养24 h后进行药 物干预,每组设6个复孔。终止培养前吸掉培养液,每孔加入MTT溶液 (终质量浓度为1 g·L−1),37 ℃继续培养4 h。吸去孔内MTT溶液,每孔加入DMSO 100 μL溶解甲臜结晶,置振荡器中振荡约10 min,用酶标仪在570 nm波长处检测OD值。按如下公式计算细胞存活率,细胞存活率 (%) = (实验组吸光度值−空白组吸光度值均值)/正常对照组吸光度×100%。实验重复3次。
LDH 漏出率检测收集细胞培养液,测定培养液中LDH活力。胰酶消化收集细胞,反复冻融破碎细胞,测定细胞中LDH活力。LDH漏出率 = 培养液中LDH活力/(培养液中LDH活力+细胞中LDH活力)。
TUNEL 法检测细胞凋亡SH-SY5Y细胞 (每孔1×105) 种植于细胞玻片上,继续培养24 h。SH-SY5Y细胞经4% 多聚甲醛室温固定30 min,滴加0.3% H2O2孵育30 min,并滴加0.1% Triton X-100溶液孵育30 min。滴加N末端脱氧核苷酸转移酶后,置于湿盒中37 ℃孵育1 h,然后滴加抗地高辛结合物孵育30 min。DAPI (0.1 g·mL−1) 染细胞核,置荧光显微镜观察并拍照。
线粒体膜电位检测SH-SY5Y细胞加入JC-1溶液 (终浓度为2 μmol·L−1),37 ℃避光孵育30 min,PBS洗2遍,荧光显微镜进行观察拍照。线粒体膜电位的变化由红绿荧光相对比例表示。
Caspase-3 活力检测胰酶消化收集细胞,用预冷细胞裂解液50 μL重悬细胞,冰浴裂解15 min。50 μg细胞裂解物加入2×反应缓冲液 (含10 mmol·L−1DTT) 50 μL,然后加入DEVD-7-amino-4-trifluoromethylcoumarin (终浓度为50 μmol·L−1) 5 μL,混匀后37 ℃孵育2 h。采用酶标仪读取样品荧光值 (Ex = 400 nm,Em = 505 nm)。
细胞内总 ROS 检测胰酶消化并收集细胞,洗涤剂洗一遍,加入carboxy-H2DCFDA (终浓度25 μmol·L−1) 溶液,37 ℃避光孵育30 min,用高内涵仪器检测荧光值。
氧化应激水平检测收集SH-SY5Y细胞培养上清液,使用MDA试剂盒检测SH-SY5Y细胞MDA含量。胰酶消化收集SH-SY5Y细胞,反复冻融裂解细胞。4 ℃、3 000 r·min−1离心10 min,取上清,使用试剂盒测定抗氧化酶SOD、CAT和GSH-Px活力。
Western blot 检测蛋白表达胰酶消化收集SH- SY5Y细胞,加入含蛋白酶抑制剂、磷酸酶抑制剂和PMSF的细胞蛋白抽提试剂,冰上裂解30 min。4 ℃、12 000 r·min−1离心15 min,取上清。BCA试剂盒定量样品蛋白浓度。将5×SDS-PAGE上样缓冲液与蛋白样品按1∶4混匀,煮沸5 min。吸取等量蛋白样品,加入10% SDS-PAGE胶,电压80 V电泳至溴酚蓝到达分离胶底部,然后将蛋白转至NC膜。取NC膜置于5% 脱脂牛奶 (TBST配制) 摇床封闭2 h。一抗4 ℃孵育过夜。TBST洗膜3次,每次15 min,HRP标记的二抗孵育2 h。TBST洗膜3次,每次15 min,用增强型ECL显色液避光孵育5 min,采用凝胶成像系统进行显影拍照。
检测三七总皂苷中主要单体成分对 SH-SY5Y 细胞活力的影响将SH-SY5Y细胞 (每毫升5×104个) 种植于96孔板中。不同浓度的三七总皂苷各单体成分 (6.25、12.5、25、50和100 μg·mL−1) 孵育SH-SY5Y细胞24 h,MTT法检测细胞活力。
比较单体成分对 6-OHDA 诱导 SH-SY5Y 细胞损伤的保护作用将SH-SY5Y细胞 (每毫升5×104个) 种植于96孔板中。原人参二醇类皂苷 (25 μg·mL−1) 和原人参三醇类皂苷 (100 μg·mL−1) 各预孵育细胞24 h,然后用100 μmol·L−1 6-OHDA处理细胞24 h,再用MTT法检测细胞活力。
统计学分析 数据采用均数±标准差 (Mean ± SD) 表示,组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验,使用统计软件SPSS19.0进行统计分析,以P < 0.05为具有统计学显著性差异。
结果 1 三七总皂苷能够抑制6-OHDA神经毒性不同浓度三七总皂苷单药 (6.25、12.5、25、50和100 μg·mL−1) 对SH-SY5Y细胞预孵育4、8、12、24、48和72 h,与空白对照组相比,不同浓度三七总皂苷 (6.25、12.5和25 μg·mL−1) 预孵育4、8、12、24、48和72 h对正常SH-SY5Y细胞的活力无显著性差异 (图 1A,P > 0.05); 三七总皂苷 (50 μg·mL−1) 对SH-SY5Y细胞预孵育24 h细胞活力下降,48和 72 h呈现活力抑制作用; 三七总皂苷 (100 μg·mL−1) 对SH-SY5Y细胞预孵育呈剂量和时间依赖的抑制作用 (图 1A)。
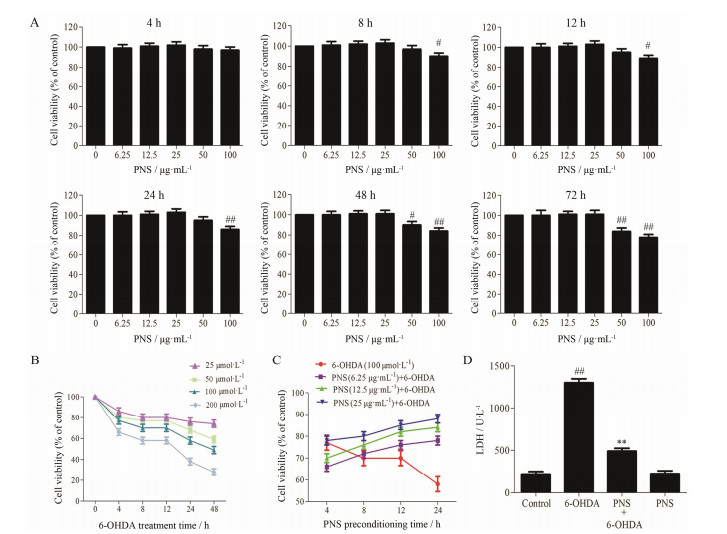 | Figure 1 Effects of Panax notoginseng saponins (PNS) on cell viability of SH-SY5Y cells. A: The survival rate of SH-SY5Y treated with PNS for the indicated time point respectively; B: The survival rate of SH-SY5Y induced by 6-hydroxydopamine (6-OHDA); C: The survival rate of SH-SY5Y pretreated with PNS for 4,8,12 and 24 h,respectively; D: The levels of lactate dehydrogenase (LDH). #P < 0.05,##P < 0.01 vs control group; **P < 0.01 vs 6-OHDA group |
为选择6-OHDA损伤的最佳浓度,SH-SY5Y细胞给予不同浓度的6-OHDA (25、50、100和200 μmol·L−1) 作用4、8、12、24和48 h。6-OHDA对SH-SY5Y细胞活力呈剂量和时间依赖的抑制作用 (图 1B)。在100 μmol·L−1 6-OHDA作用24 h下,SH-SY5Y细胞存活率为58%左右,因此选择100 μmol·L−1 6-OHDA作用24 h为最佳模型条件。不同浓度的三七总皂苷 (6.25、12.5和25 μg·mL−1) 预孵育4、8、12和24 h,与模型组相比,三七总皂苷各剂量组的细胞活力显著提高 (图 1C),且呈浓度和时间依赖性。在25 μg·mL−1三七总皂苷作用24 h下,SH-SY5Y细胞活力为88% 左右,因此选择25 μg·mL−1三七总皂苷作用24 h为最佳给药条件。与空白组相比,模型 组细胞中LDH含量显著升高 (P < 0.01); 与模型组 相比,三七总皂苷 (25 μg·mL−1) 能显著降低细胞中LDH含量 (图 1D,P < 0.01)。以上结果表明三七总皂苷在一定浓度范围内孵育能够显著抑制6-OHDA神经毒性。
2 三七总皂苷能够显著抑制6-OHDA诱导SH-SY5Y细胞的凋亡与对照组比较,6-OHDA (100 μmol·L−1) 能够显著增加TUNEL阳性细胞数 (图 2A和2B,P < 0.01);与模型组相比,三七总皂苷 (25 μg·mL−1) 预孵育能够显著减少TUNEL阳性细胞数,提示三七总皂苷能够抑制6-OHDA诱导SH-SY5Y细胞的DNA断裂。进一步考察6-OHDA对SH-SY5Y细胞线粒体膜电位的影响,发现6-OHDA能够显著降低线粒体膜电位 (图 2C和2D,P < 0.01),同时,6-OHDA能够明显增强caspase-3活性 (图 2E,P < 0.01)。提示6-OHDA可使SH-SY5Y细胞线粒体膜电位去极化和caspase-3活化。三七总皂苷预孵育能够显著抑制6-OHDA诱导线粒体膜电位去极化和caspase-3的活化 (图 2C~2E,P < 0.01)。表明三七总皂苷对6-OHDA诱导SH-SY5Y细胞凋亡具有明显的抑制作用。
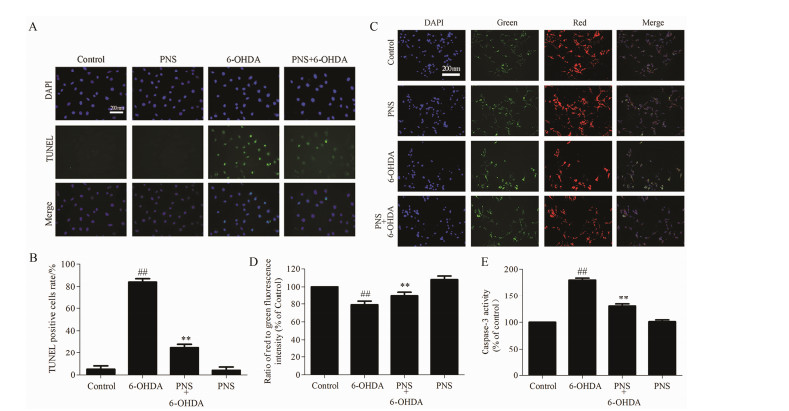 | Figure 2 Effects of PNS on 6-OHDA-induced apoptosis in SH-SY5Y cells. A,B: PNS pretreat can inhibit 6-OHDA induced DNA fragmentation in SH-SY5Y cells. C,D: Effects of PNS on 6-OHDA-induced mitochondrial transmembrane permeability transition in SH-SY5Y cells. E: PNS pretreat can inhibit 6-OHDA induced the activation of caspase-3. PNS: 25 μg·mL−1,6-OHDA: 100 μmol·L−1. ##P < 0.01 vs control group; **P < 0.01 vs 6-OHDA group |
与对照组比较,6-OHDA导致SH-SY5Y细胞ROS水平显著增加 (图 3A和3B,P < 0.01)。MDA含量明显升高 (图 3C,P < 0.01)。而且,细胞内抗氧化酶SOD、CAT和GSH-Px活力显著下降 (图 3D~3F,P < 0.01),提示6-OHDA可使SH-SY5Y细胞处于氧化应激状态。然而,三七总皂苷预孵育显著降低ROS水平,减少MDA含量,显著增强SOD、CAT和GSH-Px活力,提示三七总皂苷显著改善6-OHDA诱导SH-SY5Y细胞氧化应激。
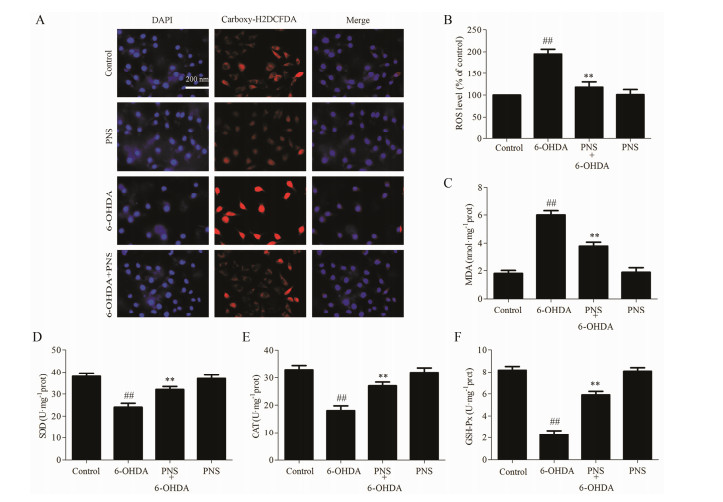 | Figure 3 Effects of PNS on 6-OHDA-induced oxidative stress in SH-SY5Y cells. A,B: PNS pretreat can inhibit 6-OHDA-induced increase of reactive oxygen species (ROS) in SH-SY5Y cells. C: PNS pretreat can inhibit the increase of malondialdehyde (MDA) induced by 6-OHDA in SH-SY5Y cells. D,E,F: PNS pretreat can inhibit 6-OHDA-induced decrease of superoxide dismutase (SOD),catalase (CAT) and glutathione peroxidase (GSH-Px) activity in SH-SY5Y cells. ##P < 0.01 vs control group; **P < 0.01 vs 6-OHDA group |
为探讨三七总皂苷的神经细胞保护作用机制,本研究考察了三七总皂苷对SH-SY5Y细胞Nrf2/HO-1信号通路的影响。Western blot结果表明,三七总皂苷预孵育能够显著降低SH-SY5Y细胞胞浆内Nrf2蛋白表达,增加核内Nrf2蛋白表达,显著增加SH-SY5Y细胞浆中HO-1的蛋白表达水平 (图 4A和4B)。为考察HO-1在三七总皂苷神经保护中的作用,采用HO-1活性抑制剂锡原卟啉 (SnPP) 预处理SH-SY5Y细胞,观察SnPP对三七总皂苷介导的抗凋亡作用的影响,发现SnPP能够明显抑制三七总皂苷介导的神经保护作用 (图 4C),提示HO-1在三七总皂苷介导的神经保护中发挥重要作用。
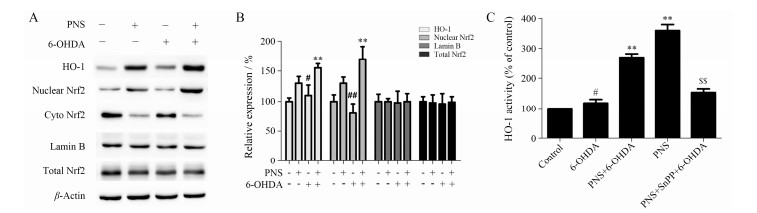 | Figure 4 Effect of PNS on expression of Nrf2 and HO-1 in SH-SY5Y cells. A,B: PNS pretreat can up-regulate nuclear Nrf2 and HO-1 in SH-SY5Y cells. C: The neuroprotective effects of PNS can be reversed by HO-1 inhibitor Sn-protoporphyrin (SnPP). #P < 0.05,##P < 0.01 vs control group; **P < 0.01 vs 6-OHDA group; $$P < 0.01 vs 6-OHDA+PNS group |
用MTT检测原人参二醇类皂苷成分原人参二醇 (PPD)、人参皂苷Rb1,原人参三醇类皂苷成分原人参三醇 (PPT)、三七皂苷 (R1和R2)、人参皂苷 (Re和Rg1) 对SH-SY5Y细胞活力的影响。发现所有原人参二醇类皂苷成分在50 μg·mL−1浓度以上孵育SH-SY5Y细胞24 h都能显著降低细胞活力,提示原人参二醇类皂苷成分在50 μg·mL−1浓度以上对SH-SY5Y细胞具有毒性作用 (图 5A和5B)。同时发现,所有原人参三醇类皂苷成分 (100 μg·mL−1) 孵育SH-SY5Y细胞24 h,对细胞活力无影响,提示原人参三醇类皂苷成分在100 μg·mL−1浓度以下对SH-SY5Y细胞没有毒性作用 (图 5C~5G)。
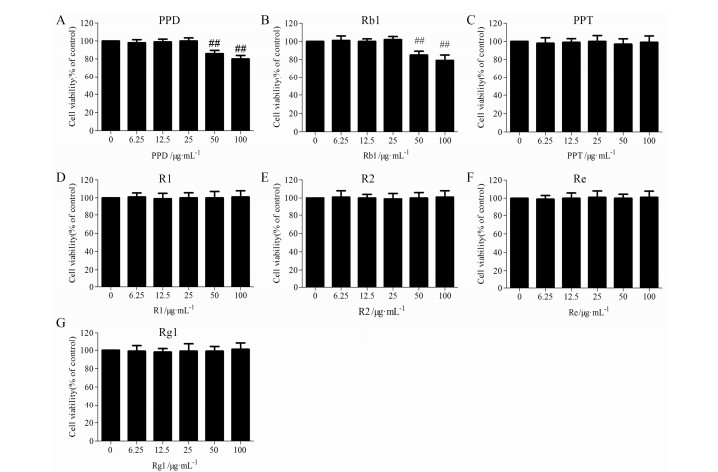 | Figure 5 Effect of a variety of ingredients in PNS on cell viability of SH-SY5Y cells. A: Protopanaxadiol (PPD); B: Ginsenoside Rb1 (Rb1); C: Protopanaxtriol (PPT); D: Notoginsenoside R1 (R1); E: Notoginsenoside R2 (R2); F: Ginsenoside Re (Re); G: Ginsenoside Rg1 (Rg1). ##P < 0.01 vs control group |
进一步检测了原人参二醇类皂苷成分和原人参三醇类皂苷成分对6-OHDA诱导SH-SY5Y细胞损伤的影响。与对照组相比,6-OHDA能显著降低SH-SY5Y细胞活力 (图 6A~6G ,P < 0.01),不同浓度的原人参二醇类皂苷成分 (6.25、12.5和25 μg·mL−1) 预孵育SH-SY5Y细胞24 h能明显提高细胞活力,呈剂量依赖性 (图 6A和6B)。然而,原人参二醇类皂苷成分在50和100 μg·mL−1浓度时不能抑制6-OHDA诱导的SH-SY5Y细胞损伤 (图 6A和6B)。而不同浓度的原人参三醇类皂苷成分 (6.25、12.5、25、50和100 μg·mL−1) 预孵育SH-SY5Y细胞24 h能明显提高细胞活力,呈现剂量依赖性 (图 6C~6G ,P < 0.01)。
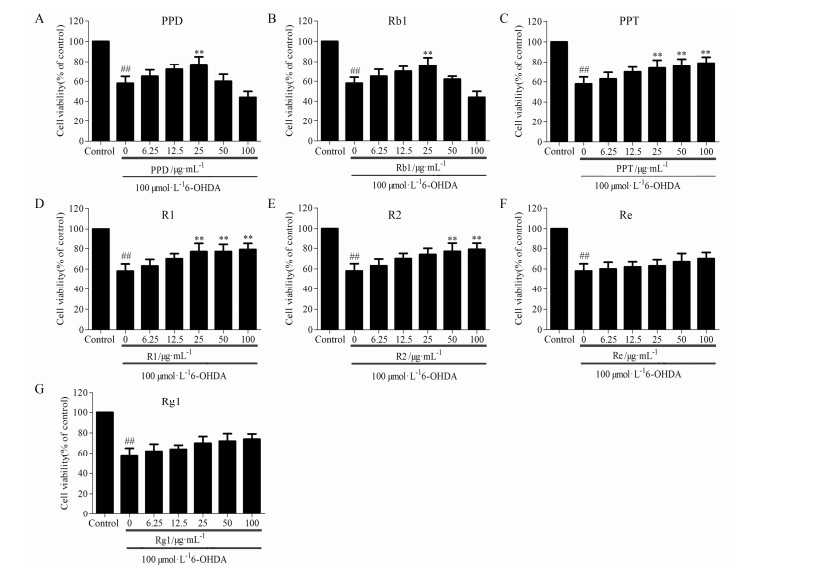 | Figure 6 Effects of a variety of ingredients in PNS on 6-OHDA-induced cell viability decrease in SH-SY5Y cells. A: PPD; B: Rb1; C: PPT; D: R1; E: R2; F: Re; G: Rg1. ##P < 0.01 vs control group,**P < 0.01 vs 6-OHDA group |
6-OHDA与多巴胺转运体的结合能力很高,所以能够选择性杀死多巴胺能神经元[7]。6-OHDA一旦进入神经元,通过自氧化和酶降解产生过氧化氢、超氧化物和羟基自由基等,从而导致脂质过氧化、蛋白质和DNA氧化,最终导致氧化应激,线粒体功能失调和凋亡[8]。所以6-OHDA被广泛认定为神经毒剂,用来建立体内体外帕金森病模型[9, 10, 11]。此次实验采用6-OHDA诱导SH-SY5Y细胞损伤模型考察了三七总皂苷的神经保护作用及其机制。
结果发现,三七总皂苷能够显著抑制6-OHDA诱导SH-SY5Y细胞存活率的下降和LDH漏出,减轻DNA断裂,并抑制线粒体膜电位的下降和caspase-3活化,表明三七总皂苷能够显著抑制6-OHDA诱导SH-SY5Y细胞凋亡。
氧化应激介导了6-OHDA的神经毒性,损伤多巴胺能神经元,导致黑质−纹状体发生退行性病变。氧化应激是一种ROS的产生超过了细胞抗氧化能力的状态。内源性抗氧化酶系统如SOD、CAT和GSH-Px等功能异常,导致过量ROS产生,引起脂质过氧化产生MDA、蛋白羰基化和DNA断裂[2]。本研究发现6-OHDA能够诱导SH-SY5Y细胞内ROS和MDA过量产生,而抗氧化酶SOD、CAT和GSH-Px活力显著降低,提示在6-OHDA的作用下,SH-SY5Y细胞处于氧化应激状态。然而,三七总皂苷预处理能够明显缓解6-OHDA诱导SH-SY5Y细胞氧化应激。
进一步探讨三七总皂苷抑制6-OHDA诱导SH- SY5Y细胞氧化应激的分子机制。机体在抗氧化应激过程中产生了很多防御性机制,其中Nrf2/ARE信号通路的活化是关键环节。HO-1是一种最广泛存在的抗氧化防御酶,可代谢血红素生成CO、胆红素和游离铁,在神经细胞抵抗氧化应激中发挥重要的作用[12]。HO-1等抗氧化酶的转录表达由Nrf2调控,在静息状态下,Nrf2与Keap1结合滞留在胞浆中,当Nrf2被激活,它从Nrf2-Keap1复合物中解离出来,转位至核内,与抗氧化反应元件结合,促进Ⅱ型解毒酶的表达[13]。结果发现三七总皂苷显著增加细胞核内Nrf2蛋白表达水平,并显著上调HO-1的蛋白表达。而且,HO-1活力抑制剂SnPP预孵育则能抑制三七总皂苷介导的神经细胞保护作用。这些结果表明,三七总皂苷可能是通过活化Nrf2/HO-1信号通路发挥神经细胞保护作用。但是,Nrf2从Keap1-Nrf2复合体中释放的分子机制,需要后续实验进行确证。
作为天然植物提取物,三七皂苷在治疗神经系统相关疾病方面具有独特的优势。已有大量研究表明雌激素具有神经保护作用[14]。然而雌激素的不良反应也是不可忽视的[15]。三七皂苷具有拟雌激素样活性,如三七皂苷R1[16]和人参皂苷Rb1[17]都被证明具有雌激素样活性。因此,三七皂苷治疗神经系统疾病具有较大的发展空间。目前作者对三七总皂苷保护6-OHDA诱导的SH-SY5Y细胞损伤作用及机制有了初步了解,但对三七皂苷中不同单体成分配伍或三七皂苷与其他中药配伍来发挥神经保护作用仍需进行大量的体内外实验进一步研究。
| [1] | Li JY, Ma SS, Huang QY, et al. The function of neuroinflammation in Parkinson disease[J]. Prog Physiol Sci (生理科学进展), 2015, 46:175-179. |
| [2] | Yan MH, Wang X, Zhu X. Mitochondrial defects and oxidative stress in Alzheimer disease and Parkinson disease[J]. Free Radic Biol Med, 2013, 62:90-101. |
| [3] | Wang Q, Zheng H, Zhang ZF, et al. Ginsenoside Rg1 modulates COX-2 expression in the substantia nigra of mice with MPTP-induced Parkinson disease through the P38 signaling pathway[J]. J South Med Univ (南方医科大学学报), 2008, 28:1594-1598. |
| [4] | Kim KH, Song K, Yoon SH, et al. Rescue of PINK1 protein null-specific mitochondrial complex IV deficits by ginsenoside Re activation of nitric oxide signaling[J]. J Biol Chem, 2012, 287:44109-44120. |
| [5] | Kumar H, Koppula S, Kim IS, et al. Nuclear factor erythroid 2-related factor 2 signaling in Parkinson disease:a promising multi therapeutic target against oxidative stress, neuroinflammation and cell death[J]. CNS Neurol Disord Drug Targets, 2012, 11:1015-1029. |
| [6] | O'Connell MA, Hayes JD. The Keap1/Nrf2 pathway in health and disease:from the bench to the clinic[J]. Biochem Soc Trans, 2015, 43:687-689. |
| [7] | Tufekci KU, Civi Bayin E, Genc S, et al. The Nrf2/ARE pathway:a promising target to counteract mitochondrial dysfunction in Parkinson's disease[J]. Parkinsons Dis, 2011, 2011:314082. |
| [8] | Wang P, Niu L, Guo XD, et al. Gypenosides protects dopaminergic neurons in primary culture against MPP+-induced oxidative injury[J]. Brain Res Bull, 2010, 83:266-271. |
| [9] | Zhang GL, Deng JP, Wang BH, et al. Gypenosides improve cognitive impairment induced by chronic cerebral hypoperfusion in rats by suppressing oxidative stress and astrocytic acti vation[J]. Behav Pharmacol, 2011, 22:633-644. |
| [10] | Nixon RA, Wegiel J, Kumar A, et al. Extensive involvement of autophagy in Alzheimer disease:an immuno-electron microscopy study[J]. J Neuropathol Exp Neurol, 2005, 64:113-122. |
| [11] | Chu CT. Autophagic stress in neuronal injury and disease[J]. J Neuropathol Exp Neurol, 2006, 65:423-432. |
| [12] | Ye F, Li X, Li L, et al. The role of Nrf2 in protection against Pb-induced oxidative stress and apoptosis in SH-SY5Y cells[J]. Food Chem Toxicol, 2015, 86:191-201. |
| [13] | Uttara B, Singh AV, Zamboni P, et al. Oxidative stress and neurodegenerative diseases:a review of upstream and downstream antioxidant therapeutic options[J]. Curr Neuropharmacol, 2009, 7:65-74. |
| [14] | Cao DC, Zhi DS, Zhang S. The nerve protective effect of estrogen and progesterone[J]. Chin J Cerebrovasc Dis (中国脑血管病杂志), 2005, 2:90-92. |
| [15] | Tan Z, Wang TH. Mechanisms of estrogen action[J]. Chin J Pathol (中国病理生理杂志), 2003, 19:1422-1426. |
| [16] | Song ZB, Zhu CL, Shi FY, et al. The study on antioxidant capacity of ginsenoside Re in vitro and its effect for serum deprived nerve cell[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2012, 18:225-228. |
| [17] | Hashimoto R, Yu J, Koizumi H, et al. Ginsenoside Rb1 prevents MPP+-induced apoptosis in PC12 cells by stimulating estrogen receptors with consequent activation of ERK1/2, Akt and inhibition of SAPK/JNK, p38 MAPK[J]. Evid Based Complement Alternat Med, 2012, 2012:693717. |
 2016, Vol. 51
2016, Vol. 51


