冠状动脉疾病是导致因心血管事件而猝死的重要原因,发病机制是冠状动脉粥样硬化斑块的损伤或脱落诱发血小板活化和聚集,促发心肌梗死。血小板在斑块破裂后血栓形成的发病机制中起关键作用,这个过程是血小板激活。
血小板激活剂包括凝血酶、二磷酸腺苷 (ADP)、血栓烷A2 (TxA2)、肾上腺素和胶原等,活化的血小板发生变形,分泌颗粒成分,并在表面表达激活的糖蛋白IIb/IIIa受体,与循环血中的纤维蛋白原结合,导致血栓形成。凝血酶作为重要的激活剂激活了血 小板表面的G蛋白偶联受体,即蛋白酶激活受体 (protease activated receptor,PAR)。人类有4种PAR亚型,广泛分布于组织中,其中PAR-1又称凝血酶受 体,在血小板聚集和血栓形成中起着最主要的作用。沃拉帕沙是首创的口服PAR-1小分子抑制剂。
2 体外模型的建立应用纯化的人血小板膜作为PAR-1的来源,配体是对凝血酶受体有强结合作用的3H标记的活性肽 ([3H]haTRPA,Kd = 5 nmol·L-1),筛选和评价化合物对PAR-1的竞争性结合作用。
3 天然产物喜巴辛为先导化合物天然产物喜巴辛 (1,himbacine) 是从木兰科植物Galbulimima baccata树皮中分离的生物碱。最初研究喜巴辛的目的是寻找抗阿尔茨海默病药物,发现1对乙酰胆碱毒蕈碱受体M2有强效抑制作用,IC50 = 4.5 nmol·L-1,选择性强于M1约10倍。为获得活性更强选择性更高的M2受体拮抗剂,合成了喜巴辛的类似物,经深入研究构效关系,揭示出含内酯的三环体系是影响活性的重要组成部分。
先灵葆雅研究所在研究全合成方法中,构建了关键中间体,实现了喜巴辛改构物的平行合成。喜巴辛及其类似物的全合成对于研究M2受体拮抗剂以及后来随机筛选并转轨研发PAR-1抑制剂提供了方法和物质保障 (Chackalamannil S,Davies RJ,Asberom T,et al. A highly efficient total synthesis of (+)-himbacine.J Am Chem Soc,1996,118: 9812-9813)。
4 吡啶环类似物的优化在普筛中发现含吡啶环的改构物2对PAR-1抑制活性IC50 = 300 nmol·L-1,甲基在其他位置活性均降低,6-甲基变换为其他烷基,如6-乙基(化合物3) 活性显著提高,IC50 = 85 nmol·L-1,6位是极性基团时活性下降或消失。化合物2和3是消旋化合物,拆分成 (+)-2和 (+)-3,手性中心与天然的喜巴辛相反的化合物活性提高,IC50分别为150和20 nmol·L-1,而它们的对映体活性弱10倍。化合物 (+)-3进而用食蟹猴做半体内 (ex-vivo) 实验,注射剂量10 mg·kg-1后可以完全抑制haTRPA引起的血小板聚集,然而 (+)-3的口服生物利用度很低 (大鼠F = 3%),代谢也很快 (iv,t1/2 < 1 h)。

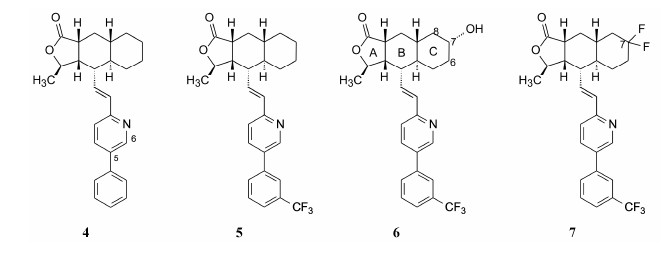
药物的活性与药代是密不可分的,优化结构应体现在活性与药代之间最佳配置,在改造上述吡啶类似物中,为了改善药代性质,在抑制活性上作了“牺牲”。由于吡啶环上5-OCH3和5-Bn取代的化合物活性强于相应的6位,特别是 (+)-5-Ph化合物 (4) IC50 = 27 nmol·L-1,而 (±)-6-Ph无活性,因而探索5-位芳基取代的活性和药代性质,化合物4大鼠灌 胃后4 h内迅速代谢。在苯环上加入取代基 (如不同位置上烷基、烷氧基、卤素、氰基、磺酰胺基和三氟甲基等),评价IC50和大鼠药代的AUC和Cmax,发现 (+)-m-CF3-Ph化合物 (5) IC50 = 11 nmol·L-1,AUC = 6 116 nmol·L-1·h,Cmax = 2.3 μmol·L-1。用猴作半体内实验评价化合物5的抑制血小板聚集活性,显示有剂量依赖性的抑制作用,而且时间持久。此外5不影响凝血时间,说明不是作用于凝血酶和蛋白酶环节上。5对PAR-2和PAR-4的功能也没有影响。然而5是CYP酶诱导剂,更加快对它的代谢,还存在药物-药物相互作用问题 (Charckalamannil S,Xia Y,Greenlee WJ,et al. Discovery of potent orally active thrombin receptor (protease activated receptor 1) antagonists as novel antithrombotic agents.J Med Chem,2005,48:5884-5887)。
6 由代谢产物引发的新一轮优化为了克服化合物5的药代问题,用大鼠肝细胞与5温孵或猴体内给药,发现在三环的C环6、7和8位碳原子发生了羟基化,催化该氧化代谢的酶是CYP2A和CYP2B,生成单羟基化合物都有两种构型α-OH和β-OH。为验证是否发生了代谢活化,合成并评价了这些代谢产物,发现 (+)-7α-羟基化合物 (6) 活性最强 (IC50 = 17 nmol·L-1),与化合物5活性相近,但药代性质优于5。由于合成方便,同时也制备了(+)-7,7-二氟代化合物 (7) (IC50 = 37 nmol·L-1)。
由代谢产物6以及衍变出的7作为新一轮的先 导物进行优化,将苯环上的三氟甲基替换为2-或3-氟、氯或甲基,化合物的抑制PAR-1活性除二氟系 列的苯环为2-氯或3-氯化合物的IC50分别达到11 和12 nmol·L-1外,其余的活性都没有超过化合物6 (Clasby MC,Chackalamannil S,Czarniecki M,et al. Metabolism-based identification of a potent thrombin receptor antagonists. J Med Chem,2007,50: 129-138)。
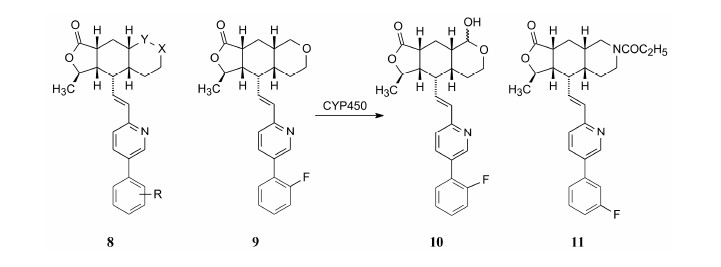
7 C环的优化—克服代谢问题和增加分子的极性化合物6的体内外药效虽然很好,但在体内迅 速代谢为7,8-二羟基化合物而失活,为解决这个代谢问题,对C环的C7做杂原子的电子等排置换,这样也可以增加分子的极性。为此设计合成了通式为8 的一系列化合物,其中Y和X分别是CH2,O; CH2,S; CH2,SO; CH2,SO2; CH2,NHCO2C2H5等,末端苯环的R为o-、m-卤素、氰基或三氟甲基等。结果表明,虽然体外抑制PAR-1大多有较高的活性,但仍未避免代谢不稳定问题,例如X为S的硫杂环己烷可被CYP氧化成亚砜或砜而失去活性。不过四氢吡喃化合物9的IC50 = 26 nmol·L-1,大鼠AUC = 850 ng·h·mL-1,仍被CYP代谢,C8被羟基化,生成环状半缩醛10。半缩醛是有反应活性的亲电性基团,故化合物9不宜开发。
化合物11有强效的体外活性 (IC50 = 11.5 nmol·L-1),由此又合成了一系列十氢异喹啉类似物,构效关系提示化合物11为最佳。猴灌胃11可迅速吸收,生物利用度为62%,半体内实验6 h内100% 抑制PAR-1,24 h仍有70% 的抑制率,11的半衰期为6.2 h。小鼠实验显示,11具有代谢稳定性,灌胃8天也无CYP酶诱导作用 (Chelliah MV,Chackalamannil S,Xia Y,et al. Heterotricyclic himbacine analogs as potent,orally active thrombin receptor (protease activated receptor-1) antagonists.J Med Chem,2007,50: 5147-5160)。
研究至此,已经聚焦于C7的基团变换成为优化活性强度和药代的位点。由于C7易于发生氧化代谢,用氨基取代并进行酰化、烷氧羰基化或脲基得到了系列化合物,结果表明C7为R构型的化合物体外抑制PAR-1的活性都很高,其中化合物12和13的体外活性IC50分别为8.1和13 nmol·L-1,两个化合物的结构都是氨基甲酸乙酯,犹如将化合物11的氨基甲酸乙酯从环内拉出。12和13的结构差异只在苯环的间位分别为F或CF3。进而用猴半体内实验确定了化合物12和13活性都很强而持久,分别灌胃0.1和1 mg·kg-1,可100% 抑制猴血小板聚集,持续时间超过24 h。由于F原子的亲脂性低于CF3,决定将化合物12作为候选化合物。12的大鼠药代动力学表明,口服生物利用度F = 33%,半衰期t1/2 = 5.1 h; 猴的F = 86%,t1/2 = 13 h (Chackalamannil S,Wang YG,Greenlee WJ,et al. Discovery of a novel,orally active himbacine-based thrombin receptor antagonist (SCH 530348) with potent antiplatelet activity.J Med Chem,2008,51: 3061-3964)。
默沙东公司决定开发12,定名为硫酸沃拉帕沙 (vorapaxar sulfate),经临床III期试验,于2014年5月经FDA批注上市,成为首创的作用于PAR-1的口服抗血栓药物,用于心脏病发作或动脉堵塞的患者,以降低心脏病进一步发作、中风等死亡危险。
 2016, Vol. 51
2016, Vol. 51
