2. 北京中医药大学东方医院, 北京 100078;
3. 中国科学院微生物研究所, 北京 100101
2. Dongfang Hospital of Beijing University of Chinese Medicine, Beijing 100078, China;
3. Institute of Microbiology, Chinese Academy of Science, Beijing 100101, China
药用鹿茸 (Cornu Cervi Pantotrichum) 为梅花鹿 (Cervus nippon Temminck) 或马鹿 (Cervus elaphus Linnaeus) 的雄性未骨化密生茸毛的幼角[1]。传统中医认为鹿茸具有补肾壮阳作用。鹿茸中含有丰富的生长因子、多糖类、蛋白质等活性成分。其中蛋白质类占鹿茸的49.54%~54.68%,比其他成分含量相对较高。研究表明,鹿茸蛋白质成分具有显著药理活性[2]。Xiu等[3]通过对体外培养的兔骨髓间质干细胞 (marrow derived marrow stem cells,MSCs) 在特定培养液作用下向软骨细胞表型分化的实验研究,发现MSCs在特定培养条件下能向软骨细胞表型分化,并且鹿茸多肽对其定向软骨分化有明显的促进作用。Chen等[4]研究鹿茸多肽对大鼠心肌缺血损伤的保护作用,发现鹿茸多肽不仅能降低血清肌酸激酶、乳酸脱氢酶、血清及心肌组织丙二醛含量,而且能增加血清及心肌组织超氧化物歧化酶 (SOD) 活性。鹿茸多肽对大鼠心肌缺血损伤具有保护作用。Luo等[5]研究了鹿茸多肽对小鼠抗疲劳能力和耐缺氧的影响,结果显示鹿茸多肽能显著增加小鼠常压缺氧存活时间、爬杆时间和负重游泳时间、断头喘气时间; 并能显著降低游泳后血清乳酸增加量。结果说明,鹿茸多肽能够提高小鼠抗疲劳和耐缺氧的能力。因此,蛋白质的研究对于研究鹿茸的活性、制剂工艺指标极为重要。
相对和绝对定量同位素标记 (isobaric tags for relative and absolute quantitation,iTRAQ) 技术是美国应用生物系统公司在2004年推出的一项新的体外同位素标记技术[6],原理是利用iTRAQ试剂标记多肽的N-末端氨基及每个赖氨酸侧链氨基[7],将不同状态的蛋白组样品分别用含不同报告基团的iTRAQ试剂标记,如113、114、115、116、117、118、119及121,标记完后混合所有样品。当混合后的肽片段经过串联质谱分析后,通过产生的报告离子峰面积对不同标记的蛋白进行定量。该方法可同时测定8个蛋白组样品,且蛋白覆盖率高、可同时比较和分析蛋白质,具有定量准确、可信度高的优势[8]。如今,iTRAQ技术已经在蛋白质组学的定量研究中得到了极其广泛的应用。Zhu等[9]使用iTRAQ技术鉴定了芸苔属植物保卫细胞中的相对蛋白成分。他们用相对定量方法在经脱落酸处理过的对照组中和样品中鉴定出了431种蛋白质,在含量丰度相对上调的66种蛋白质中,与应激和防御有关的蛋白质占有大多数,38种蛋白的含量丰度下调了,其中许多都与新陈代谢和合成途径有关。Golovan等[10]利用iTRAQ技术鉴定了猪肝细胞中1 476种蛋白,对其中880种蛋白进行功能分析,发现与能量代谢、生物合成、分解代谢、电子传递、氧化还原、酶类反应等有关的蛋白含量都显著增加,这些蛋白在肝脏作为化学和能量工厂这一角色中都起着重要的作用。
本研究利用iTRAQ技术对不同加工工艺鹿茸差异蛋白质组学进行研究,以期发现不同加工工艺鹿茸的蛋白质含量及活性变化规律。建立针对蛋白质成分的质量评价和研究方法,从而为鹿茸加工工艺的优选提供理论依据。
材料与方法 仪器 5415R 离心机(艾本德Eppendorf公司); 5800 MALDI TOF/TOFTM质谱仪 (AB SCIEX公司); Surveyor Plus液相色谱仪 (赛默飞世尔公司); nano LC-2D (Eksigent Technologies); C18色谱柱250 mm × 4.6 mm column (5 µm 110A) (Phenomenex公司); NanoLC column 75 μm × 15 cm (Michrom Bioresources,Auburn,CA); NanoLC Trap column 5 mm × 0.3 mm (安捷伦300 SB,5 μm),EASYpureII超纯水机 (Barnstead公司)。WLF-520型低温粉碎机 (廊坊市冠通机械有限公司)。LGJ-12冷冻干燥机 (北京松源华兴科技发展有限公司)。Lyo-5型真空冷冻干燥机 (上海东富龙科技有限公司)。JMS-50型胶体磨 (廊坊正瑞机械有限公司)。
药品及试剂鹿茸购买自长春市茸生鹿产品有限公司的梅花二杠鹿茸。iTRAQ-8Plex Multiplex Kit及iTRAQ Buffer kit (上海质数公司); 胰蛋白酶 (Sigma公司); CHCA基质 (Sigma公司); 质谱级水 (Honeywell公司); 质谱级乙腈 (Honeywell公司)。
样品制备鹿茸鲜品: 取自−80 ℃冷冻保存的鲜鹿茸,液氮保护下低温粉碎成细粉。直接冻干品: 取−80 ℃冷冻保存的鲜鹿茸,直接用小型冻干机冻干,然后在液氮保护下低温粉碎成细粉。鹿茸匀浆品: 取−80 ℃冷冻保存的鲜鹿茸,液氮保护下低温粉碎成细粉,然后加入2倍量去离子水混匀后胶体磨匀浆5 min,收集匀浆液。冻干品 ( 加冻干保护剂): 取鹿茸匀浆 品,加入10% 冻干保护剂海藻糖,搅拌溶解,分装于片剂模具中进行冷冻干燥,制备冻干加保护剂鹿茸样品。冻干品 (未加冻干保护剂): 取鹿茸匀浆品,直接分装于片剂模具中进行冷冻干燥,制备冻干未加保护剂鹿茸样品。冻干品 (加冻干保护剂) 并于40 ℃ 10天: 取加有保护剂的鹿茸冻干品放入烘箱,40 ℃保存10天备用。煮炸鹿茸: 取−80 ℃冷冻 保存的鲜鹿茸,按传统煮炸工艺用沸水煮炸4、5次,60~80 s/次,待血从鹿茸另一侧完全渗出后取出,60~70 ℃烘干8 h,冷却后液氮保护下低温粉碎成细粉。
蛋白质酶解各样品经Bradford法测定蛋白质浓度[11]。取经准确浓度测定后的蛋白质样品200 µg于离心管中,加入还原剂三羧甲基磷酸 (TCEP) 4 µL,37 ℃水浴反应1 h,加入烷基化试剂甲基甲基硫代 甲砜 (MMTS) 2 µL,室温放置20 min。将还原烷基化后的蛋白溶液加入到10K超滤管中,离心 (12 000 r·min−1) 25 min。加入100 mmol·L−1三乙基碳酸氢铵 (TEAB) 溶液100 µL重复洗涤3次。更换新的收集管,向超滤管中加入胰蛋白酶2~4 µg,37 ℃反应过夜。次日离心 (12000 r·min−1),收集含有酶切肽段的滤过液。加入100 mmol·L−1的TEAB 50 µL洗涤,合并滤液,抽干冻存。
多肽的iTRAQ标记从冰箱中取出8 Plex iTRAQ试剂的113号~121号,平衡到室温,将iTRAQ试剂离心至管底,每管加入异丙醇150 µL,涡旋振荡,离心至管底。取上步被抽干的多肽样品100 µg,113号加入到a: 鲜品; 115号加入到c: 煮炸; 116号加入到d: 直接冻干; 117号加入到e: 匀浆; 118号加入到f: 冻干加保护剂; 119号加入到g: 冻干未加保护剂; 121号加入到h: 冻干加保护剂40 ℃ 10天。离心 (12000 r·min−1) 3 min,室温反应2 h。每管加入去离子水100 µL终止反应。将8个标记后的多肽样品混合,抽干备用。
第一维高pH值反相色谱分级对iTRAQ标记后的多肽混合物,首先采用高pH值的反相色谱进行一维分离。采用C18色谱柱 (250 mm × 4.6 mm,5 µm,110 Ǻ) 分离样品,流速为500 µL·min−1。流动相A: 水加10 mmol甲酸铵,氨水调至pH10; 流动相B: 乙腈−10 mmol甲酸铵 (pH 10)。梯度条件为: 0~10 min,2% B; 10~60 min,2%~35% B; 60~80 min,35%~80% B; 80~90 min,80% B; 90~100 min,2% B。收集80份洗脱组分,并根据色谱峰规律合并为10份。抽干备用。
第二维纳升液相色谱分离对高pH值反相柱分离的多肽组分,进一步采用低pH值纳升液相色谱进行第二维分离。将样品用0.1% TFA溶解,用自动进样器上样于Trap柱 (安捷伦300 SB,5 mm × 0.3 mm,5 μm) 除盐,然后在纳升级色谱柱 (75 μm × 15 cm,Michrom Bioresources,Auburn,CA) 分离,流速为300 nL·min−1。流动相A: 2% 乙腈/0.1% 三氟乙酸; 流动相B: 98% 乙腈,0.1% 三氟乙酸。液相梯度如下: 0~1 min,0~5% B; 1~85 min,5%~7% B; 85~155 min,7%~25% B; 155~156 min: 25%~43% B; 156~166 min,43%~80% B; 166~167 min,80% B; 167~177 min,2% B。
MALDI TOF/TOF质谱鉴定点在LC-MALDI靶上的肽片段用AB Sciex公司的5800 MALDI-TOF/ TOF质谱仪 (Foster City,CA) 进行分析。质量数范围设置为800~4 000,以反射阳离子模式和200 Hz的激光重复频率采集MS谱图,每张谱图采集1 000个激光点 (laser shots)。以200 Hz的激光重复频率及1 kV电压采集MS/MS谱图,每张MS/MS采集750个激光点。选择MS谱中S/N > 10的最强的30个峰进行MS/MS分析。同时,对iTRAQ标记肽的碎片离子谱在113~121范围的base peak进行定量评估。采用AB Sciex公司Protein Pilot软件 (Version 4.5) 的Paragon algorithm算法进行数据库搜索。将一维分离产生的80个组分经LC-MALDI-TOF/TOF进一步分析产生的质谱数据合并,搜索从NCBI下载的偶蹄目 (Artiodactyla) 蛋白序列数据库。搜索参数设置为: 胰蛋白酶消化; MMTS烷基化修饰Cys; 采用8 Plex iTRAQ试剂标记肽片段。鉴定可信度 > 95% 及总的假阳性率 < 5% 的蛋白被用于进一步功能分析。
对于各种工艺产生的鹿茸蛋白样品组的iTRAQ标记情况如下: 113-鲜品、115-煮炸、116-直接冻干、117-匀浆、118-冻干加保护剂、119-冻干未加保护剂、121-冻干加保护剂且40 ℃放置10天。以m/z 113为对照,计算115∶113、116∶113、117∶113、118∶113、119∶113、121∶113的比值,选择差异 (P≤0.05) 的结果进行报告。以比值 > 1.50或 <0.60作为阈值选取差异蛋白。比值 > 1.50被认定为上调蛋白,比值 < 0.60为下调蛋白。最后将搜索结果进行合并处理。
生物信息学分析对于质谱分析得到的蛋白,采用Cluster3.0进行层次聚类 (hierarchy clustering) 分析,并通过Java Treeview 实现可视化。通过UniProKB (http://www.uniprot.org/uniprot/) 查找GO通路信息,并通过WEGO (http://wego.genomics.org.cn/cgi-bin/wego/index.pl) 对差异蛋白进行细胞成分、分子功能和生物进程聚类分类,根据注释信息讨论差异蛋白质功能。
结果 1 质谱分析通过用ProteinPilot软件进行数据库搜索和含量比较分析,质谱共分析得到1 015种蛋白,其中差异蛋白 (P≤0.05,含量差别 > 1.50或 <0.60) 有87种。其中,煮炸鹿茸组共57种、匀浆鹿茸组共10种、直接冻干组共7种、冻干加保护剂组共17种、冻干未加保护剂鹿茸组共15种、冻干加保护剂40 ℃ 10天组共6种。其中各个样品组与鲜品鹿茸组比较的差异上、下调蛋白数量经统计 (图 1),只有煮炸鹿茸组、匀浆鹿茸组、冻干未加保护剂鹿茸组下调蛋白数量多于上调蛋白数量,且煮炸鹿茸组对于鲜品鹿茸组差异蛋白数量最多,功能变化最大。而其他3组相对于鲜品组差异较小,上调蛋白数量居多。
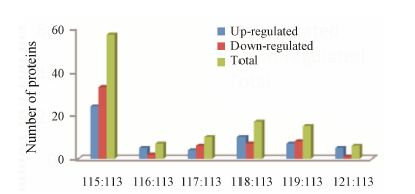
|
Figure 1 Numbers of different proteins by different processing methods of pilose antler compared with fresh pilose antler. 113: Fresh pilose antler; 115: Traditional fried process (TFP); 116: Directly freeze drying process; 117: Homogenate process (HP); 118: Freeze drying with protective agent (FDP); 119: Freeze drying without protective agent (FDNP); 121: Freeze drying with protective agent (FDP) for 40 ℃,10 days |
其中各个样品组与鲜品鹿茸组比较的差异蛋白数量经统计,煮炸鹿茸组功能显著的蛋白质中,下调蛋白有Heat shock cognate protein (HSP),Cofilin-1 (CFL1),FK506 binding protein 10 (FKBP10),Fibrinogen beta chain isoform 2 (FGB2)和Polyadenylate-binding protein (PABP),主要功能是蛋白质结合; 而蛋白质结合功能在治疗疾病领域有突出贡献。这些蛋白质经过煮炸工艺,相对 于鲜品鹿茸,相对含量下降。上调蛋白有载脂蛋白 (apolipoprotein,APO) A1、A4和乙酰辅酶A结合蛋白。APOA4的各种功能已经被逐步提出,包括参与脂类的分泌、代谢,调节食物摄入量和胃酸分泌的调制器,其抗氧化性能可防止炎症和动脉粥样硬化[12]。而APOA1和APOA2是高密度脂蛋白的主要成分 (HDL)[13, 14],A1约为75%,A2约为20%。APOA1质谱检测见图 2。

|
Figure 2 Mass spectrometry analysis for apolipoprotein A−I (APOA1) |
直接冻干鹿茸组功能显著的下调蛋白有VI型胶原蛋白α1 (collagen type VI alpha 1 protein,COL6A1),它是胎盘的新形式。COL6A1不仅代表一个结构蛋白提供组织的完整性,而且影响在植入部位滋养细胞的侵袭行为,抑制肿瘤发生[15]。上调蛋白是延长因子2 (elongation factor 2,EEF2),在造血细胞中活动有助于动脉粥样硬化的发生[16]。直接冻干工艺不仅使得有益功能强的蛋白受到影响,同时提高了对人体不利蛋白相对含量。
匀浆鹿茸组功能显著的下调蛋白有APOA1; 上调蛋白是血清磷酸丙糖异构酶 (triosephosphate isomerase,TPI),Yuan等[17]研究发现,TPI水平与疾病活动度评分呈明显正相关。TPI是类风湿关节炎新的疾病相关性自身抗原。
冻干加保护剂鹿茸组功能显著的下调蛋白是硫氧还蛋白 (thioredoxin,TRX),TRX是一种普遍存 在的抗氧化酶,参与保护生物抵抗各种氧化应激反应[18]。上调蛋白是靶向GTP酶 (Ras-related protein Rab-1A,RAB1A),转化生长因子-β诱导蛋白ig-h3 (transforming growth factor-beta-induced protein ig-h3,TGFBIp/beta ig-h3)、双糖链蛋白多糖 (biglycan,BGN)和核心蛋白聚糖 (decorin,DCN)。
冻干未加保护剂鹿茸组下调蛋白无显著功能; 上调蛋白有肿瘤转移蛋白 (ezrin) 和蛋白聚糖 (aggrecan core protein,ACAN),肿瘤转移蛋白在肿瘤转移中起重要作用。越来越多的研究表明,肿瘤转移蛋白表达水平很高与许多人类恶性肿瘤相关。肿瘤转移蛋白的高表达可能是胰腺导管癌的重要预测指标[19]。ACAN对正常软骨组织的形成和胚胎肢体发育过程中的生存起到重要的调节作用[20]。
冻干加保护剂组40 ℃ 10天鹿茸组功能显著下调的蛋白有APOA1,上调蛋白有前胶原C-endopeptidase增强子 (procollagen C-endopeptidase enhancer,PCPE-1) 和DCN。PCPE-1是一种细胞外基质糖蛋白。研究表明,PCPE-1可能参与了肿瘤生长、神经退行性疾病和血管生成[21]。冻干加保护剂40 ℃ 10天鹿茸经过加热,长时间贮存后,功能显著的有益蛋白受到破坏,而对于参与肿瘤生长的蛋白质反而优化,相对含量增高。
1.2 不同加工工艺差异极显著(P≤0.001) 蛋白种类及功能 统计结果显示,煮炸鹿茸组相对于鲜品鹿茸组趋势图只有4种差异极显著蛋白比例值>1,这些蛋白质分别为HPCB1_000595044、网钙结合蛋白3 (RCN3)、ATP合酶 (ATP synthase,EC) 和APOA1。煮炸鹿茸组相对于鲜品鹿茸组的极显著下调蛋白质共有7种。这些蛋白质功能见表 1,多参与ATP代谢及合成、钙离子结合等。冻干加保护剂鹿茸组与冻干未加保护剂鹿茸组中,相对于鲜品鹿茸组比较,差异极显著蛋白均>1,均为上调蛋白质,其中名称为XII型胶原蛋白,在冻干加保护剂鹿茸组为极显著上调蛋白,在煮炸鹿茸组为下调蛋白质,说明煮炸加热工艺可能会使胶原蛋白受到破坏。另外一个极显著上调蛋白为II型胶原蛋白. II型胶原蛋白是软骨组织的特殊部分、可使软骨组织线性生长和具有抵抗压力的能力,对于骨骼的正常发育必不可少。这些成分在冻干加保护剂工艺中得到保存。冻干未加保护剂鹿茸组差异极显著蛋白为Uncharacterized Protein LOC524810; ECa。功能见表 1。直接冻干鹿茸组无差异极显著蛋白质。匀浆鹿茸组APOA1为差异极显著下调蛋白。
|
|
Table 1 Molecular function of significant different proteins compared with fresh pilose antler. 115: Traditional frying process (TFP),117: Homogenate process (HP),118: Freeze drying with protective agent (FDP),119: Freeze drying without protective agent (FDNP),121: Freeze drying with protective agent (FDP) for 40 ℃,10 days. ↑: Up-regulate; ↓: Down-regulate. aThe duplicate protein in each group |
对各组与鲜品鹿茸组比较,挑选差异极显著蛋白 (P≤0.001阈值在 > 1.50或 <0.60) 在各组进行统计 (表 1)。
2 GO通路信息分析 2.1 全体差异蛋白质GO通路分析本研究对87种差异蛋白进行GO通路分析,通过WEGO进行细胞成分、分子功能和生物进程分类,讨论分析相对于鲜品鹿茸,其他加工工艺鹿茸的差异蛋白质组学信息。其中表现在细胞成分上的有44类,分子功能有7类,生物进程有21类,排名前三位的生物进程是细胞过程 (52.7%)、代谢过程 (46.2%)和定位过程 (26.4%); 细胞成分是参与细胞组成 (45.1%)、穿透细胞内成分 (42.9%)、细胞器成分 (37.4%); 分子功能是结合功能 (52.7%)、催化活性功能 (25.3%)、结构分子活性 (6.6%)及转运功能 (6.6%),结果见图 3。

|
Figure 3 Go information of different proteins compared with Fresh pilose antler |
用Cluster 3.0实现各组相对于鲜品鹿茸组差异蛋白质的定量数据的样本维和基因维的分层聚类计算(图 4)。结果表明: 第一类为煮炸鹿茸组,第二类为直接冻干鹿茸组与冻干未加保护剂鹿茸组,第三类为匀浆鹿茸组,第四类为冻干加保护剂鹿茸组与冻干加保护剂40 ℃ 10天鹿茸组。结果说明,冻干加保护剂组及冻干加保护剂40 ℃ 10天组为近似,而煮炸鹿茸蛋白质的变化最大。这与WEGO数据相符。

|
Figure 4 Cluster analysis of different proteins by different processing methods of pilose antler compared with fresh pilose antler. 113: Fresh pilose antler; 115: TFP; 116: Directly freeze drying process; 117: HP; 118: FDP; 119: FDNP; 121: FDP for 40 ℃,10 days |
讨论
中药鹿茸早在《神农本草经》就有记载。鹿茸的蛋白质成分是重要活性成分之一。目前研究蛋白质相对定量的传统方法是凝胶电泳法,但这种方法操作费时费力,难以实现与质谱的直接联用。而且对于特定蛋白质不能达到完全分离,因此限制了应用范围。而iTRAQ技术可以对任何类型的蛋白质都能进行分离定量。使用该技术可以寻找差异表达蛋白,并分析其蛋白功能。可同时使8个样本相对量化,大大降低了实验过程中所引入的技术误差。目前此技术多应用于微生物及血浆研究领域,应用到中药领域目前还尚未普及。本研究应用iTRAQ标记技术考察不同加工工艺鹿茸的差异蛋白质组学。相对于鲜品鹿茸,共检测出差异蛋白质87种。这些差异蛋白质通过Wego分析,功能多为结合功能、催化活性功能、结构分子活性及转运功能。
通过比较各个加工工艺的差异蛋白质变化规律。为鹿茸工艺的优选提供依据。其中煮炸工艺需要经过加热及去血处理,差异蛋白相对于鲜品鹿茸组来说,相对含量变化大,并且下调蛋白明显多于上调蛋白。煮炸过程中,参与结合功能的蛋白质受到影响,而蛋白质结合功能经研究表明与很多炎症、疾病治疗预防相关: 经研究表明重组人可溶性DR5蛋白可以有效阻断TRAIL诱导的细胞凋亡作用,显示DR5在TRAIL诱导Jurkat细胞凋亡作用中起着十分关键的作用[22]。Zhang等[23]研究端粒重复序列结合蛋白质1 (telomeric-repeat binding factor-1,TRF1) 和端粒重复序列结合蛋白质2 (telomeric-repeat binding factor-2,TRF2) 基因表达异常在原发性干燥综合征 (primary Sjogren’s,pSS) 发病中可能的作用,结果表明,TRF2转录水平可能参与了pSS患者端粒酶激活和端粒缩短的调节; TRF2、TRF1可能参与了pSS炎症免疫调节,且与pSS的发病机制有关。具有参与ATP的合成与结合、蛋白质结合、异构酶活性等功能的蛋白质也受到严重破坏,这些功能都是人体重要的代谢过程。说明煮炸使得蛋白质成分受到较大影响。Cluster聚类分析也显示煮炸鹿茸为单独一类,与其他各组差异较大。
冻干工艺的鹿茸中,只有冻干未加保护剂鹿茸组蛋白质相对于鲜品鹿茸组来说下调蛋白多于上调蛋白,说明对蛋白质的破坏相对较大。冻干加保护剂鹿茸组与冻干未加保护剂鹿茸组,与鲜品鹿茸组比较,均使得蛋白质含量有所增加,其中名称为XII型胶原蛋白,在冻干加保护剂鹿茸组为极显著上调蛋白,在煮炸鹿茸组为下调蛋白。说明这一成分在冻干加保护剂工艺中得到优化,而在煮炸过程中遭到破坏。另外一个极显著上调蛋白为II型胶原蛋白。II型胶原蛋白是软骨组织的特殊部分,说明这些成分在冻干加保护剂工艺中都得到保存及优化。而且,经筛选出的具有显著功能的上调蛋白质中,TGFBIp/ beta ig-h3经研究表明TGFBIp在血小板活化过程里起着重要的作用[24]。BGN调节纤维细胞生长因子从而有助于精原细胞的维护[25]。DCN是一种小的富含亮氨酸的蛋白多糖家族的一员,在间质细胞和上皮细胞发挥多功能作用。越来越多的证据表明,DCN使多种人类肿瘤的表达失调,影响肿瘤细胞的生物学过程[26]。冻干加保护剂工艺有利于活化血小板、维护精原细胞、使肿瘤细胞表达失调等显著功能蛋白质优化,使其含量相对增加。因此冻干加保护剂工艺有效保护、优化了蛋白质成分及功能。
直接冻干鹿茸组使得有益蛋白质成分 (collagen type VI alpha 1 protein) 含量降低,也使得在造血细胞中活动有助于动脉粥样硬化的发生的不益蛋白质成分EEF2含量提高。虽然在加工过程中,直接冻干工艺是直接应用小型冻干机冻干,然后在液氮保护下低温粉碎,操作简便快捷,但是这种工艺并不能起到优化鹿茸活性能力。
在匀浆工艺中,下调蛋白数目多于上调蛋白数目,并且匀浆鹿茸组仅有一个差异极显著蛋白,相对含量下降。匀浆工艺是冻干工艺中间环节,但缺少冻干过程,这使得蛋白质成分的变化较直接冻干工艺以及冻干加保护剂工艺鹿茸来说,受到一定程度破坏。
本研究从蛋白质组学角度研究不同加工工艺鹿茸的蛋白质含量及功能变化规律。但是对于筛选出的具有差异极显著或功能显著的蛋白质,其体内成分代谢过程以及功能蛋白质的药效学验证还需进一步研究。
| [1] | Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China(中华人民共和国药典)[S]. 2010 ed. Vol 1. Beijing:China Medical Science Press, 2010:303. |
| [2] | Fan YL, Xing ZT, Wei GQ, et al. A study on the extraction separation and anticancer activity of velvet antler protein[J]. J Econ Anim(经济动物学报), 1998, 01:30-34. |
| [3] | Xiu ZB, Lin JH, Wu ZY, et al. Effect of pilose antler polypeptides(PAP) on chondrogenic phenotype differentiation of bonemarrow-derived mesenchymal stem cells(MSCs) of rabbit in vitro[J]. China J Orthop Trauma(中国骨伤), 2007, 20:31-33. |
| [4] | Chen XG, Wang Y, Wu Y, et al. Protective effects of pep-tides from velvet antler of Cervus Nippon on acute ischemic myocardial injury in rats[J]. China J Chin Mater Med(中国中药杂志), 2009, 34:1971-1974. |
| [5] | Luo XD, Pan FG, Zhang TF, et al. Effects of pilose antler polypeptide on ability of mice anti-anoxia and anti-fatigue[J]. Food Sci(食品科学), 2008, 29:386-388. |
| [6] | Ross PL, Huang YN, Marchese JN, et al. Multiplexed protein quantitation in Saccharomyces cerevisiae using amine-reactive isobaric tagging reagents[J]. Mol Cell Proteomics, 2004, 12:1154-1169. |
| [7] | Xie XZ, Wang X, Liu LH, et al. ITRAQ technology and its application in proteomics[J]. Chin J Biochem Mol Biol(中国生物化学与分子生物学报), 2011, 27:616-621. |
| [8] | Chen J. iTRAQ Quantitation Technique and Label Free Quantitation Technique to Study the Differences in Protein Expression of Liliopsida's Chloroplast(iTRAQ及非标定量 方法分析百合纲类植物叶绿体差异蛋白)[D]. Shanghai:Fudan University, 2012. |
| [9] | Zhu M, Simons B, Zhu N, et al. Analysis of abscisic acid responsive proteins in Brassica napus guard cells by multiplexed isobaric tagging[J]. J Proteomics, 2010, 73:790-805. |
| [10] | Golovan SP, Hakimov HA, Verschoor CP, et al. Analysis of Sus scrofa liver proteome and identification of proteins differentially expressed between genders, and conventional and genetically enhanced lines[J]. Comp Biochem Physiol Part D Genomics Proteomics, 2008, 3:234-242. |
| [11] | Jin MY, Dong L, Dai JD, et al. Determination of the con-tent of protein in pilose antler processed by different methods with bradford method[J]. Chin Arch Tradit Chin Med(中华中医药学刊), 2015, 33:592-594. |
| [12] | Orsó E, Schmitz G. Apolipoprotein A-IV in the follicle-associated epithelium:a further piece in the puzzle[J]. Dig Dis Sci, 2014, 59:2609-2610. |
| [13] | McGuire KA, Davidson WS, Jonas A. High yield overex-pression and characterization of human recombinant proapoli-poprotein A-I[J]. J Lipid Res, 1996, 37:1519-1528. |
| [14] | Sontag TJ, Reardon CA. Polymorphisms of mouse apolipo-protein A-II alter its physical and functional nature[J]. PLoS One, 2014, 9:e88705 |
| [15] | Oefner CM, Sharkey A, Gardner L, et al. Moffett A2 colla-gen type IV at the fetal-maternal interface[J]. Placenta, 2015, 36:59-68. |
| [16] | Zhang P, Riazy M, Gold M, et al. Impairing eukaryotic elongation factor 2 kinase activity decreases atherosclerotic plaque formation[J]. Can J Cardiol, 2014, 30:1684-1688. |
| [17] | Yuan JZ, Wu YZ. A novel antigen for rheumatoid arthritis:triosephosphate isomerase[J]. J Clin Med Pract(实用临床医药杂志), 2012, 16:8-12. |
| [18] | Kang T, Wan H, Zhang Y, et al. Comparative study of two thioredoxins from common cutworm(Spodoptera litura):cloning, expression, and functional characterization[J]. Comp Biochem Physiol B Biochem Mol Biol, 2015, 182:47-54. |
| [19] | Piao J, Liu S, Xu Y, et al. Ezrin protein overexpression predicts the poor prognosis of pancreatic ductal adenocarci-nomas[J]. Exp Mol Pathol, 2014, 98:1-6. |
| [20] | Lauing KL, Cortes M, Domowicz MS, et al. Aggrecan is required for growth plate cytoarchitecture and differentiation[J]. Dev Biol, 2014, 396:224-236 |
| [21] | Salza R, Peysselon F, Chautard E, et al. Extended in-teraction network of procollagen C-proteinase enhancer-1 in the extracellular matrix[J]. Biochem J, 2014, 457:137-149. |
| [22] | Du YW, Liu GC, Zhao YP, et al. Isolation and purify of recombinant human soluble DR5 and detection of its biological activity[J]. J Henan Univ Med Sci(河南大学学报 医学版), 2007, 26:25-27, 31. |
| [23] | Zhang MY, Zhou JG, Qing YF, et al. Expression of TRF1 and TRF2 mRNA in the peripheral blood mononuclear cells of patients with primary Sjogren's syndrome[J]. Chin J Clin(中华临床医师杂志电子版), 2013, 21:9485-9488. |
| [24] | Kim HJ, Kim PK, Bae SM, et al. Transforming growth factor-β-induced protein(TGFBIp/β ig-h3) activates platelets and promotes thrombogenesis[J]. Blood, 2009, 114:5206-5215. |
| [25] | Winge SB, Nielsen J, Jørgensen A, et al. Biglycan is a novel binding partner of fibroblast growth factor receptor 3c(FGFR3c) in the human testis[J]. Mol Cell Endocrinol, 2015, 399:235-243. |
| [26] | Shi X, Liang W, Yang W, et al. Decorin is responsible for progression of non-small-cell lung cancer by promoting cell proliferation and metastasis[J]. Tumour Biol, 2015, 36:3345-3354. |
 2015, Vol. 50
2015, Vol. 50


