牛筋果 [Harrisonia perforate (Blanco) Merr.] 为苦木科 (Simaroubaceae) 牛筋果属植物,主要分布于我国的福建、广东和海南等地,马来半岛、中南半岛、菲律宾、印度尼西亚等也有分布; 其根、茎、叶均可入药,味苦,性凉,有清热解毒作用,对防治疟疾有一定效果[1]。之前作者曾报道从牛筋果枝叶的95% 乙
醇提取物中分离得到了16个化合物[2],这次又从其中分离鉴定了6个化合物,分别为harriperfin E (1)、kihadanin A (2)、kihadanin B (3)、6α-acetoxyobacunol acetate (4)、gardaubryone C (5) 和β-sitosterol methyl ether (6)。其中化合物1为一新的色原酮化合物 (图 1),化合物2~6为首次从该植物中分离得到。
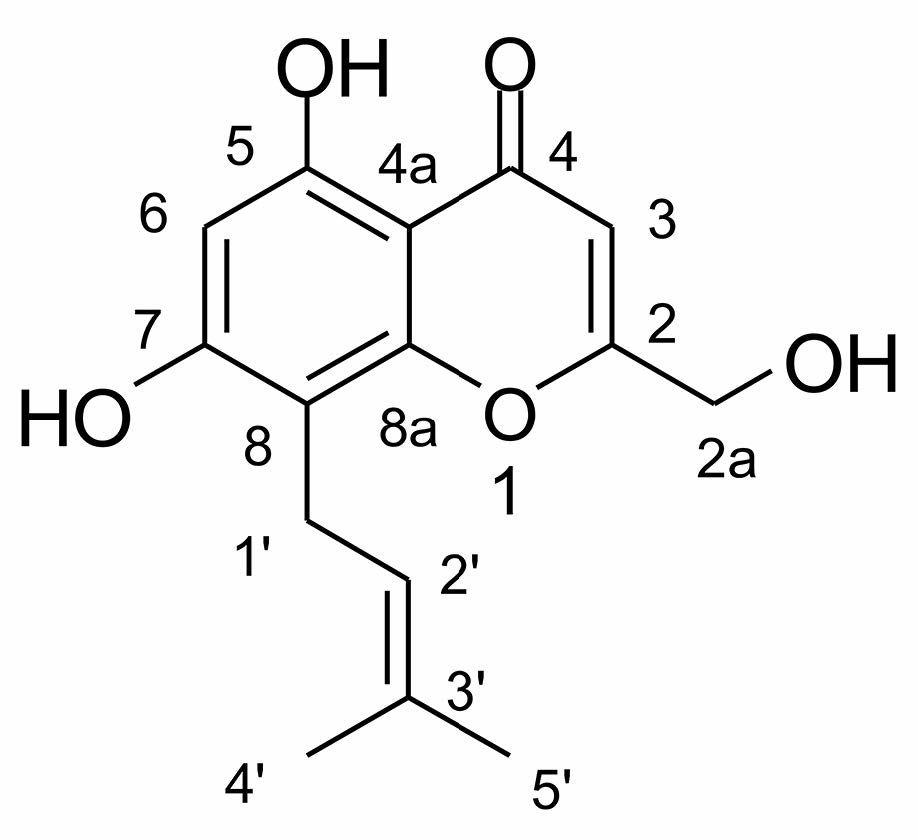
|
Figure 1 Chemical structure of compound 1 |
化合物1 浅黄色针晶 (甲醇),mp 244~246 ℃,UV光谱在209、257 nm处有最大吸收; IR光谱提示化合物中存在羟基 (3 320 cm-1)、羰基 (1 651 cm-1)、苯环 (1 563,1 454 cm-1)。HR-ESI-MS显示m/z 277.107 0 [M+H]+(calcd. for C15H17O5,277.107 1),确定化合物的分子式为C15H16O5。1H NMR (400 MHZ,pyridine-d5) 谱中显示含有3个不饱和质子信号 [δH 6.79 (1H,s,H-3),6.66 (1H,s,H-6),5.77 (1H,t,J = 7.1 Hz,H-2')]、2个亚甲基质子信号 [δH3.82 (2H,d,J = 7.1 Hz,H-1'),4.69 (2H,s,H-2a)]、2个甲基信号 [δH 1.94 (3H,s,H-4'),1.72 (3H,s,H-5')]。13C NMR和DEPT谱中显示共有15个碳信号,分别为8个季碳信号 (δC183.4,171.1,163.9,160.4,156.8,131.7,112.9,105.4)、3个次甲基碳信号 (δC 123.8,106.6,94.1),2亚甲基碳信号 (δC 61.1,22.6) 和2个甲基碳信号 (δC 26.2,18.4) (表 1)。以上数据与已知化合物5-羟基-7-甲氧基-2-甲基-8-异戊烯基色原酮核磁数据[3]非常相似,区别在于化合物1中少了一个甲氧基碳信号,一个甲基变成了连氧的亚甲基碳信号 (δC 61.1)。再综合HSQC、1H-1H COSY、HMBC谱数据,可以完成对化合物1碳氢信号的全归属 (表 1)
|
|
Table 1 NMR data of compound 1. 1H at 400 MHz; 13C at 100 MHz. Pyridine-d5,δ in ppm,J in Hz |
在HMBC谱中,[δH 6.79 (H-3)] 与 [δC 171.1 (C-2),105.4 (C-4a),61.1 (C-2a)] 相关; [δH 6.66 (H-6)] 与 [δC 105.4 (C-4a),156.8 (C-5),163.9 (C-7),112.9 (C-8)] 相关,进一步确定了该化合物为一色原酮类化合物,苯并吡喃酮骨架上C-2,C-5,C-7,C-8位的氢原子被取代,且确定了碳2位连有羟甲基。[δH 1.94 (H-4'),1.72 (H-5')] 分别与 [δC123.8 (C-2'),131.7 (C-3')]有相关,[δH 3.82 (H-1')]与 [δC 163.9 (C-7),112.9 (C-8),160.4 (C-8a),123.8 (C-2'),131.7 (C-3')] 相关,通过这些相关信号,可以确定化合物1中存在1个异戊烯基片段,且该基团与C-8位相连,由碳5位和7位均为季碳信号 [δC 156.8 (C-5),163.9 (C-7)],再结合分子式可以确定碳5位和7位上有羟基取代,从而确定了该化合物的结构。综合以上解析,鉴定化合物1为一新的色原酮类化合物,命名为harriperfin E。
实验部分X-5型显微熔点测定仪 (温度未校正); Agilent 6210 LC/MSD TOF型质谱仪; Finnigan LCQ Advantage MAX质谱仪; Jasco V-550紫外/可见光谱仪; Jasco FT/ IR-480 Plus傅里叶变换红外光谱仪 (KBr压片); Bruker AV 400超导核磁共振仪; Agilent 1200分析型高效液相色谱仪; Cosmosil C18色谱柱 (250 mm × 10 mm,5 μm ); Phenomenex Lux5u-cellulose-1色谱柱(250 mm × 4.6 mm,5 μm); 柱色谱用硅胶 (青岛海洋化工厂); RP-18 F254薄层预制板和ODS RP-18柱色谱材料 (Merck公司); 硅胶GF254薄层预制板 (烟台化学工业研究所)。
实验所用牛筋果于2010年7月采集于海南尖峰岭,经海南大学生物工程研究中心黄世满植物学高级工程师鉴定为牛筋果Harrisonia perforata (Blanco) Merr.的枝叶,样品现存放于暨南大学药学院标本室,编号为2010070501。
1 提取与分离牛筋果干燥枝叶19.3 kg,用150 L 95% 的乙醇渗漉提取4次,减压浓缩得浸膏0.9 kg。浸膏经4倍量水混悬后,依次用等体积的乙酸乙酯、正丁醇萃取3次,分别回收,得到乙酸乙酯部位约274 g,正丁醇部位约320 g,水部位约300 g。
乙酸乙酯部位 (约260 g) 经硅胶柱色谱 (石油醚-丙酮系统),TLC分析并合并,得到12个流分(Fr.1~12),Fr.9 (31.25 g) 经硅胶柱色谱、Sephadex LH-20凝胶柱色谱以及制备型HPLC等技术分离纯化,得到化合物2 (12.6 mg)、3 (6.3 mg)、4 (15.4 mg)、5 (8.2 mg) 和6 (7.8 mg)。Fr.10 (30.76 g) 经硅胶柱色谱、Sephadex LH-20凝胶柱色谱以及制备型HPLC等技术分离纯化,得到化合物1 (5.2 mg)。
2 结构鉴定 化合物1浅黄色针晶 (甲醇); mp 244~246℃; UV (CH3OH): 209、257 nm; IR (KBr) νmax/cm-1: 3 320、2 913、1 651、1 563、1 454、1 171; HR-ESI-MS: m/z 277.107 0 [M+H]+; NMR数据见表 1。
化合物2淡黄色块晶 (甲醇); IR (KBr) νmax/ cm-1: 3 405、2 959、1 758、1 279、1 118; ESI-MS: m/z 487.3 [M+H]+; 1H NMR (400 MHZ,pyridine-d5) 和 13C NMR (100 MHZ,pyridine-d5) 数据与文献[4]报道的kihadanin A数据一致,故鉴定化合物2为kihadanin A。
化合物3淡黄色块晶(甲醇); mp 255~257 ℃; IR (KBr) νmax/cm-1: 3 429、1 749、1 681、1 282、1 030、824; ESI-MS: m/z 487.4 [M+H]+; 1H NMR (400 MHZ,CDCl3) 和13C NMR (100 MHZ,CDCl3) 数据与文献报道的kihadanin B的数据一致[4],故鉴定化合物3为 kihadanin B。
化合物4淡黄色块晶 (甲醇); IR (KBr) νmax/cm-1: 3 450、2 931、1 747、1 370、1 235、1 027; ESI-MS: m/z 579.4 [M+Na]+; 1H NMR (400 MHZ,CDCl3) 和13 C NMR (100 MHZ,CDCl3) 数据与文献[5]报道的6α-acetoxyobacunol acetate数据一致,故鉴定化合物4为6α- acetoxyobacunol acetate。
化合物5白色针晶 (甲醇); IR (KBr) νmax/cm-1: 3 392、2 939、2 870、1 707、1 455、1 377; ESI-MS: m/z 499.5 [M+Na]+; 1H NMR (400 MHz,CD3OD) 和13C NMR (100 MHz,CD3OD) 数据与文献[6]报道的gardaubryone C数据一致,故鉴定化合物5为 gardaubryone C。
化合物6白色粉末; IR (KBr) νmax/cm-1: 3750、3 648、2 932、2 870、1 463、1 375; ESI-MS: m/z 413.4 [M+H]+; 1H NMR (400 MHz,CDCl3) 和13C NMR (100 MHz,CDCl3) 数据与文献报道的β-谷甾醇的数据相似[7],相比β-谷甾醇多了一个甲氧基,少了一个羟基,故鉴定化合物6为β-sitosterol methyl ether。
| [1] | Editorial Committee of Flora of China of Chinese Academy of Sciences. Flora of China(中国植物志)[M]. Beijing:Science Press, 1997, 43:15. |
| [2] | Liu G, Zheng RR, Liu ZW, et al. Enantiomeric chromones from Harrisonia perforate[J]. Phytochem Lett, 2014, 10:295-299. |
| [3] | Wang GQ, Zhang MS, Zhu YL. Chemical constituents of Harrisonia perforate Blanco Merr.[J]. Acta Pharm Sin(药学学报), 1983, 18:113-118. |
| [4] | Fernandar RG, Walmir SG, Maura TT, et al. Limonoids from Trichilia elegans SSP. Elegans[J]. Phytochemistry, 1997, 45:141-148. |
| [5] | Madhu KJ, Raymond JA, Ellen KM, et al. Limonoids from the Fijian medicinal plant Dysoxylum richii[J]. Can J Chem-Revue Can De Chim, 1989, 67:257-260. |
| [6] | Grougnet R, Magiatis P, Mitaku S, et al. Dammarane triterpenes from Gardenia aubryi Vieill[J]. Helv Chim Acta, 2011, 94:656-661. |
| [7] | Hai LQ, Xu JJ, Kai SE, et al. Chemical constituents of Hedysarum austrosibiricum b. Fedtsch[J]. West Chin J Pharm Sci(华西药学杂志), 2006, 21:47-48. |
 2015, Vol. 50
2015, Vol. 50


