丝状病毒 (filovirus) 为单链负链RNA病毒,属于丝状病毒科 (Filoviridae),包括埃博拉病毒 (Ebola virus)、马尔堡病毒 (Marburg virus) 和奎瓦病毒 (Cueva virus)[1, 2]。埃博拉病毒和马尔堡病毒可引发危害公共安全和人类健康的重大烈性传染病,被列为A类生化武器[3]。埃博拉病毒是流行程度最广的丝状病毒,通过体液接触或飞沫等途径在人群中传播,致死率25%~90%[4]。自1976年首次在非洲扎伊尔和苏丹出现至今,埃博拉病毒病已出现十余次有规模的爆发流行,2014年3月在西非爆发的新一轮埃博拉疫情是迄今为止最严重的一次,死亡人数超过1万人[5]。埃博拉病毒病临床表现为高热、头痛、肌痛、多器官出血衰竭[6],目前尚无疫苗、无药物上市,研发抗埃博拉病毒药物迫在眉睫。
埃博拉病毒有囊膜,表面有包膜糖蛋白 (glycolprotein,GP),是唯一负责病毒进入宿主的病毒蛋白,中心为螺旋状核衣壳,包括基因组RNA及其他6 种病毒蛋白。目前已确定5种亚型,分别为扎伊尔 型 (Zaire-EBOV)、苏丹型 (Sudan-EBOV)、莱斯顿 型 (Reston-EBOV)、科特迪瓦泰森林型 (Taï Forest- EBOV) 和乌干达本迪布焦型 (Bundibugyo-EBOV)[1, 4],其中扎伊尔型恶性程度最强,死亡率50%~90%,苏丹型恶性程度次之,死亡率50%~70%。引起2014年埃博拉病毒病的病毒隶属于扎伊尔亚型[7]。
基于上述研究背景,本文应用细胞水平重组病毒技术[8, 9, 10],制备了以丝状病毒表面糖蛋白GP为外膜蛋白包裹HIV核心的重组病毒,共建立了扎伊尔型埃博拉病毒 (EBOV-Zaire GP/HIV-luc)、苏丹型埃博拉病毒 (EBOV-Sudan GP/HIV-luc) 和马尔堡病毒 (Marburg GP/HIV-luc) 三种细胞水平重组病毒药理筛选模型。应用该模型对已报道的丝状病毒进入抑制剂氯喹 (chloroquine)[11, 12]进行检测,数据与文献报道相符,证实模型构建成功。埃博拉病毒和马尔堡病毒被世界卫生组织列为危险性四级病毒,活病毒研究需要生物安全四级 (Biosafety Level 4,BSL-4) 实验研究条件[13],细胞水平重组病毒技术是国际上用于检测高危病毒的经典研究方法,本文构建的丝状重组病毒进入模型靶点明确,可在BSL-2级实验条件下用于抗丝状病毒进入的活性化合物筛选评价,将有利于抗丝状病毒药物的高通量筛选和研发。
材料与方法 细胞和质粒人肾上皮细胞系293T细胞购自 中国医学科学院基础医学研究所; 编码优化的丝 状病毒包膜糖蛋白GP基因由上海生工生物工程有 限公司合成; 携带荧光素酶报告基因的HIV-1质粒 (pNL4-3.Luc.R-E-) 和水泡性口膜炎病毒外壳糖蛋白 (vesicular stomatitis virus glycoprotein,VSV-G) 质粒由美国伊利诺伊大学Dr. Lijun Rong惠赠。
试剂DMEM细胞培养基和胎牛血清购自Invitrogen公司; 荧光素酶检测试剂盒、细胞裂解液购自Promega公司; jetPEI转染试剂购自Polyplus- transfection公司; 兔抗EBOV-Zaire GP多克隆抗体购自苏州杰恩生物公司; 小鼠抗β-actin单克隆抗体、辣根酶标记山羊抗小鼠IgG和辣根酶标记山羊抗兔IgG购自北京中杉金桥生物技术公司; λDNA/Hind III Marker购自Fermentas公司; 蛋白预染marker、限制性内切酶Kpn I和BamH I购自NEB公司; HIV-1 p24抗原ELISA试剂盒购自ZeptoMetrix公司; 依法韦仑 (efavirenz) 购自Sigma-Aldrich公司; 氯喹购自上海陶素生物公司; 其他试剂均为分析纯。
埃博拉病毒GP蛋白的表达检测根据jetPEI转染试剂说明书将EBOV-Zaire GP质粒转染至293T细胞,同时设置293T细胞空白对照组及仅转染pcDNA3.1(+) 空载体质粒的Mock对照组。培养48 h后裂解细胞,将细胞裂解物于4 ℃,13000 r∙min-1离心10 min收集上清液,按常规Western blot方法[14]检测GP蛋白的表达 (一抗: 兔抗EBOV-Zaire GP多克隆抗体; 二抗: 辣根酶标记山羊抗兔IgG),同时检测细胞内的β-actin蛋白表达,作为内参对照(一抗: 小鼠抗β-actin单克隆抗体; 二抗: 辣根酶标记山羊抗小鼠IgG)。
重组病毒的制备转染前一天,按照细胞数2×106接种293T细胞至100 mm培养皿中,转染当天用jetPEI试剂进行质粒共转染,将5 µg HIV-luc核心质粒 (pNL4-3.Luc.R-E-) 分别与5 µg EBOV-Zaire GP质粒、5 µg EBOV-Sudan GP质粒、5 µg Marburg GP质粒或3 µg VSV-G质粒共转染至293T细胞,转染后16 h更换新鲜细胞培养基,并继续培养32 h,收集上清液并经0.45 µm滤膜过滤,即获得重组病毒EBOV- Zaire GP/HIV-luc、EBOV-Sudan GP/HIV-luc、Marburg GP/HIV-luc和VSVG/HIV-luc。
病毒滴度的测定感染前一天,按每孔细胞数6×104接种293T细胞至24孔板中,将重组病毒液以不同稀释比 (1∶2、1∶4、1∶8、1∶16、1∶32和1∶64) 感染细胞。感染48 h后,弃去细胞上清,向细胞孔中加入细胞裂解液50 µL于4 ℃裂解细胞10 min后,将荧光素酶底物30 µL与细胞裂解物30 µL混合并于FB15荧光检测器 (Sirius) 测定细胞中荧光素酶活性,以荧光素酶相对活性 (relative luciferase units,RLUs) 表示。
重组病毒的HIV-1p24抗原测定将重组病毒原液进行倍比稀释,各取450 µL,用裂解液50 µL进行裂解,按照p24抗原ELISA试剂盒说明书测定并计算重组病毒原液的p24抗原浓度[15, 16]。
模型的确证按每孔细胞数6×104接种293T细胞至24孔板中,培养24 h。用DMSO溶解氯喹和依法韦伦,于感染前15 min加入细胞培养液中,DMSO溶剂作空白对照,再加入病毒液 (将病毒原液稀释至含p24抗原浓度为0.5 ng∙mL-1) 0.5 mL。重组病毒感染后,继续培养48 h,去除细胞上清液,每孔加入细胞裂解液50 µL于4 ℃裂解细胞10 min,将荧光素酶底物30 µL与细胞裂解物30 µL混合并于FB15荧光检测器测定细胞中荧光素酶相对活性,以DMSO组测定值为对照,计算药物半数抑制浓度IC50值。通过比较丝状重组病毒组EBOV-Zaire GP/HIV-luc、EBOV-Sudan GP/HIV-luc、Marburg GP/HIV-luc与模型对照组VSVG/HIV-luc的检测结果,进行化合物的特异性评价。
高通量筛选模型实验方法的适用性通过Z'因 子值评价,Z '因子值通过公式计算[17]: Z ' = 1 - [(3σc+ + 3σc-) / |μc+-μc-|],其中μc-和σc-分别表示阴性对照组 (即DMSO溶剂组) RLUs的平均值和标准差; μc+和 σc+分别表示阳性药对照组 (即氯喹30 μmol∙L-1组) RLUs的平均值和标准差。Z '因子值大于0.5时,高通量筛选模型实验方法较为理想,Z '因子值越接近1提示阴性对照组及阳性药对照组之间分离间距越大,即该方法越适用于高通量筛选。
数据分析及统计实验数据由Excel统计软件分析,浓度-活性/感染率数据作散点图并用指数非线性拟合得到作用曲线,根据公式计算药物半数抑制浓度IC50值,同一实验重复3次,计算均值及标准偏差 (x± s)。
结果 1 扎伊尔型埃博拉重组病毒EBOV-Zaire GP/HIV-luc的构建 1.1 编码EBOV-ZaireGP基因的质粒构建扎伊尔型埃博拉病毒GP基因(EBOV-Zaire GP,Mayinga株,Genbank L11365,2 031 bp) 按照人密码子优化基因序列[18]并合成基因,将所合成的带有Kpn I和BamH I酶切位点的DNA克隆至真核表达载体pcDNA3.1(+) 中。EBOV-Zaire GP质粒经测序及酶切鉴定序列正确 (图 1A)。

|
Figure 1 Identification of EBOV-Zaire GP expression. A: Electrophoresis of double enzymatic digested product of EBOV- Zaire GP plasmid. Lane 1: λDNA/HindIII Marker; 2: Double enzymatic digested product of EBOV-Zaire GP plasmid by KpnI and BamHI. B: Identification of EBOV-Zaire GP protein expression. Lane 1: Blank: cell lysates of 293T cells alone; 2: Mock: cell lysates of 293T cells transfected with pcDNA3.1(+) vector; 3: Cell lysates of 293T cells transfected with EBOV-Zaire GP plasmid. The plasmid of pcDNA3.1(+) vector or EBOV- Zaire GP was transfected to 293T cells respectively,forty-eight hours after transfection,the cell lysates were collected and detected by Western blot. The GP expression was detected by rabbit anti-EBOV Zaire GP polyclonal antibody,and the cellular β-actin expression was detected by mouse anti-β-actin monoclonal antibody |
埃博拉病毒包膜蛋白GP是病毒表面负责入侵宿主的唯一元件,GP以三聚体形式镶嵌于病毒表面,每个单体GP由GP1和GP2两个亚基组成,通过一对二硫键相连接。在构建模型时,首先检测了GP蛋白在细胞中的表达。 将EBOV-Zaire GP质粒转染至293T细胞,48 h后将细胞裂解并离 心收集细胞裂解物,经观察表达GP对细胞有轻微毒性,但对细胞形态无显著影响 (图略)。将样品进行SDS-PAGE电泳并进行Western blot检测,结果显示,GP蛋白可在细胞中表达,糖基化GP1亚基大小约为130 kD (图 1B),与文献[19]报道一致。
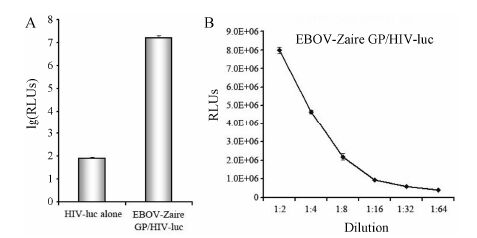
1.3 EBOV-ZaireGP/HIV-luc重组病毒模型的建立应用重组病毒技术[8, 9, 10],共转染EBOV-Zaire GP质粒和HIV-luc质粒至293T细胞,包装为重组病毒颗粒EBOV-Zaire GP/HIV-luc,同时进行只转染HIV-luc质粒的空白对照组。转染后48 h收集细胞上清液,并进行病毒滴度测定。将含有病毒的上清液倍比稀释后加入293T细胞培养基,经观察感染重组病毒的细胞未见细胞毒性。孵育48 h后裂解细胞,测定细胞中的荧光素酶相对活性。由于HIV-luc空白对照组没有外膜蛋白包裹,因此无法进入宿主细胞; 而EBOV-Zaire GP/HIV-luc重组病毒颗粒可通过病毒表面的GP蛋白识别宿主受体进入细胞,释放病毒HIV-luc核心进入胞浆,并在细胞中表达荧光素酶,因此可通过检测感染细胞中荧光素酶报告基因的表达水平,判断病毒的感染力。经测定病毒滴度,EBOV-Zaire GP/HIV-luc重组病毒感染细胞的荧光素酶相对活性 (RLUs) 达到107单位,比HIV-luc空白对照组高1000倍以上 (图 2A)。EBOV-Zaire GP/HIV-luc重组病毒感染细胞的荧光素酶相对活性与加入的病毒量呈剂量依赖型关系 (图 2B)。被感染细胞中报告基因的表达水平可以体现病毒的感染水平。
|
Figure 2 Establishment of EBOV-Zaire GP/HIV-luc pseudovirions. A: EBOV-Zaire GP/HIV-luc and HIV-luc alone (no Env) pseudovirions were generated in 293T cells. The virions were separately incubated with 293T cells for 48 h,and the luciferase activities were represented as lg (relative luciferase units,RLUs). Data represents an average of three independent experiments. Values are means of triplicate samples ± SD. B: The titer evaluation of EBOV-Zaire GP/HIV-luc pseudovirions. The pseudovirions containing supernatant was serially diluted to 1∶2,1∶4,1∶8,1∶16,1∶32 and 1∶64. The infectivity represented as RLUs was tested. Data represents an average of three independent experiments |
通过检测HIV-1的p24抗原在重组病毒颗粒中 的浓度可判断重组病毒是否成功包装[15, 16]。经测 定,扎伊尔型埃博拉重组病毒颗粒p24抗原浓度为 5 ng∙mL-1,说明此重组病毒颗粒具有较高感染能力,将病毒原液稀释至含p24抗原浓度0.5 ng∙mL-1作为感染剂量进行化合物的筛选评价。
2 应用EBOV-Zaire GP/HIV-luc重组病毒模型对化合物筛选评价EBOV-Zaire GP/HIV-luc重组病毒的特点是外膜蛋白为埃博拉病毒GP,包裹的核心为携带荧光素酶的HIV,当对化合物进行初筛时,经EBOV-Zaire GP/ HIV-luc重组病毒模型筛选得到的有效化合物包含两类情况,一类是特异性埃博拉病毒进入抑制剂,另一类是作用于HIV复制环节或干扰荧光素酶活性的抑制剂,即假阳性化合物。因此,在得到初筛有效化合物后,还需应用模型对照组VSVG/HIV-luc重组病毒[9]进行化合物的进一步评价。VSVG/HIV-luc重组病毒颗粒的外膜蛋白为水泡性口膜炎病毒的外膜糖蛋白VSV-G ,是VSV病毒表面唯一的蛋白,负责识别结合宿主受体。VSV病毒的宿主受体类型多样,在多种细胞内广泛存在[20],因此VSVG/HIV-luc重组病毒可进入不同种属及组织来源的细胞系。利用此特点,VSVG/ HIV-luc重组病毒进入细胞后可体现HIV病毒的特性,因此将其作为特异性对照模型。当化合物仅对埃博拉重组病毒的进入有抑制,而对VSV重组病毒的进入没有影响时,视其为特异性埃博拉病毒进入抑制剂; 而当化合物对两种重组病毒的感染均有抑制时,则判断其作用环节为HIV-luc核心,即影响HIV复制或荧光素酶活性的抑制剂,即为假阳性化合物。
基于上述模型构建理论,分别以文献报道的EBOV进入抑制剂氯喹[11, 12]和HIV复制抑制剂依法韦仑[21]对模型进行了验证。
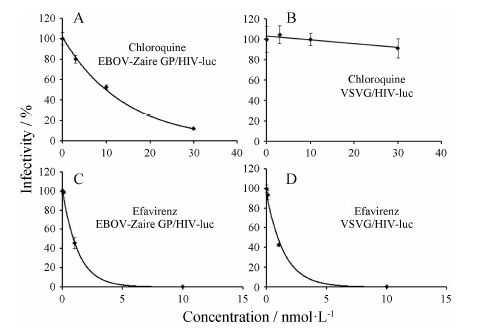
2.1EBOV进入抑制剂的EBOV-Zaire GP/HIV-luc重组病毒模型检测氯喹是常用抗疟药物,同时也具有体外和体内抗埃博拉病毒感染的作用。因此,将氯喹作为抗EBOV阳性药物对EBOV-Zaire GP/HIV-luc重组病毒及VSVG/HIV-luc重组病毒模型进行了检测。结果显示,氯喹可显著抑制EBOV-Zaire GP/HIV-luc重组病毒对细胞的感染,IC50为 (12.4 ± 2.5) μmol∙L-1 (图 3A),与文献报道数值相符 (IC50: 4.7 μmol∙L-1[11]~15.3 μmol∙L-1[12]),氯喹对VSVG/HIV-luc重组病毒的感染无抑制作用 (图 3B),提示氯喹为特异性抑制埃博拉病毒进入抑制剂,可作为EBOV-Zaire GP/HIV-luc重组病毒模型阳性对照药,在氯喹30 μmol∙L-1浓度条件下计算Z ' 因子值为0.87,提示本模型符合高通量筛选实验方法标准,精确度较高,稳定性较好。
|
Figure 3 Effect of chloroquine (A,B) or efavirenz (C,D) on the entry of EBOV-Zaire GP/HIV-luc and VSVG/HIV-luc pseudovirions. Compounds were added into 293T cells at indicated concentrations 15 min prior to adding pseudovirions. Infected cells were lysed 48 h post-infection,and the luciferase activity was measured. DMSO as a solution control whose infectivity was defined as 100%. Data represents an average of three independent experiments |
重组病毒模型检测 应用EBOV-Zaire GP/HIV-luc重组病毒及VSVG/HIV-luc重组病毒模型对HIV复制 抑制剂依法韦伦进行了检测。结果显示,依法韦伦对EBOV-Zaire GP/HIV-luc重组病毒及VSVG/HIV-luc重组病毒的感染均有显著抑制作用,IC50分别为 (0.91 ± 0.01) nmol∙L-1和 (0.93 ± 0.01) nmol∙L-1,即这两种均以HIV-luc为病毒核心的重组病毒在遇到对HIV复制有抑制作用的化合物时显示同样的抑制作用 (图 3C,3D)。因此,在进行抗埃博拉病毒药物筛选时,参考特异性模型对照VSVG/HIV-luc重组病毒模型的结果可以筛选并去除由于对HIV核心复制有效而在初筛中显示有效的假阳性化合物。
3 多种丝状重组病毒模型的构建及化合物检测参照扎伊尔型埃博拉重组病毒模型的制备方法,还构建了苏丹型埃博拉重组病毒模型EBOV-Sudan GP/HIV-luc和马尔堡重组病毒模型Marburg GP/HIV- luc,并对化合物进行了检测。
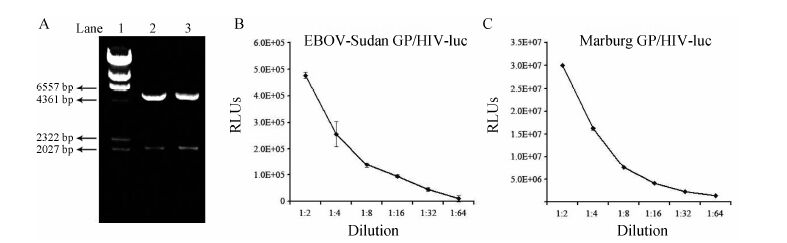
3.1 苏丹型埃博拉重组病毒和马尔堡重组病毒模型的构建编码密码子优化的苏丹型埃博拉病毒GP基因 (EBOV-Sudan GP,Boniface株,Genbank FJ968794.1,2 031 bp) 和马尔堡病毒GP基因 (Marburg GP,Musoke株,Genbank NC_001608.3,2 046 bp) 经人工合成基因序列后连接入真核表达载体pcDNA3.1(+) 中,基因测序及酶切鉴定序列正确 (图 4A)。模型构建方法同扎伊尔型埃博拉重组病毒。结果显示,EBOV- Sudan GP/HIV-luc和Marburg GP/HIV-luc重组病毒感染细胞的荧光素酶相对活性分别达到106单位和107单位 (图略),比空白对照组HIV-luc高1 000倍以上,两株重组病毒感染细胞的荧光素酶相对活性随着病毒感染量的增加呈线性变化 (图 4B,4C)。经检测,EBOV-Sudan GP/HIV-luc和Marburg GP/HIV-luc重组病毒颗粒p24抗原浓度分别为2和20 ng∙mL-1,分别将病毒原液稀释至p24抗原浓度0.5 ng∙mL-1作为感染剂量进行化合物的筛选评价。
|
Figure 4 Establishment of EBOV-Sudan GP/HIV-luc and Marburg GP/HIV-luc pseudovirions. A: Electrophoresis of double enzymatic digested product of EBOV-Sudan GP or Marburg GP plasmid. Lane 1: λDNA/HindIII Marker; 2: Double enzymatic digested product of EBOV-Sudan GP plasmid by KpnI and BamHI; 3: Double enzymatic digested product of Marburg GP plasmid by KpnI and BamHI. The titer of EBOV-Sudan GP/HIV-luc (B) or Marburg GP/HIV-luc (C) pseudovirions was tested. The pseudovirions containing supernatant was serially diluted to 1∶2,1∶4,1∶8,1∶16,1∶32 and 1∶64. The infectivity represented as RLUs was tested. Data represents an average of three independent experiments |
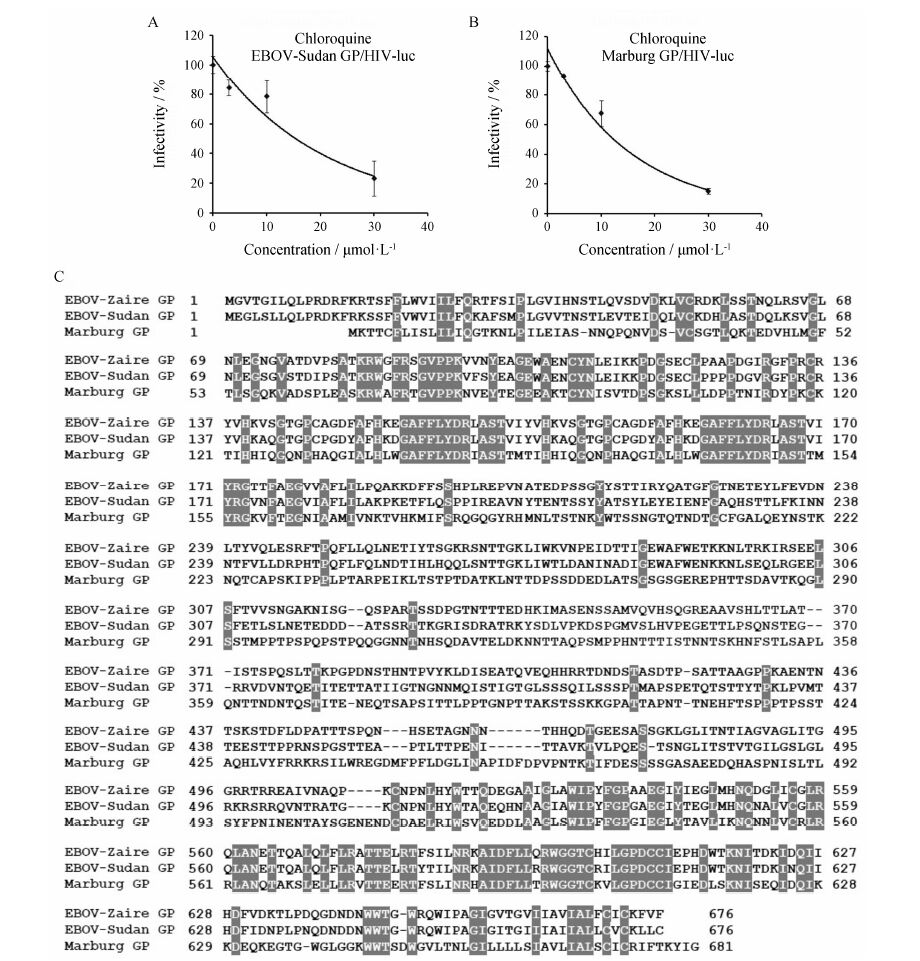
应用EBOV-Sudan GP/HIV- luc和Marburg GP/HIV-luc重组病毒模型对氯喹进行检测。结果显示,氯喹可抑制苏丹型埃博拉病毒和马尔堡病毒进入宿主,IC50分别为 (15.4 ± 4.1) μmol∙L-1和 (12.4 ± 0.3) μmol∙L-1 (图 5A,5B)。其中,氯喹抗马尔堡病毒进入的IC50数据与文献[11]报道相符 (IC50: 5.5 μmol∙L-1),对于氯喹抗苏丹型埃博拉病毒进入的检测数据为首次报道,本研究提示,氯喹有广谱抗丝状病毒作用,可作为EBOV-Sudan GP/HIV-luc和Marburg GP/HIV-luc重组病毒模型阳性对照药,在氯喹30 μmol∙L-1浓度条件下计算Z '因子值分别为0.83和0.87,提示此两种模型均符合高通量筛选实验方法标准,精确度较高,稳定性较好。
|
Figure 5 Effect of chloroquine on the entry of EBOV-Sudan GP/HIV-luc (A) and Marburg GP/HIV-luc (B) pseudovirions. The compound was added into 293T cells at indicated concentrations 15 min prior to adding pseudovirions. Infected cells were lysed 48 h post-infection,and the luciferase activity was measured. DMSO as a solution control whose infectivity was defined as 100%. Data represents an average of three independent experiments. C: Protein sequence alignments of EBOV-Zaire GP,EBOV-Sudan GP and Marburg GP. The conserved residues were highlighted by grey |
通过蛋白序列比对结果可见,两株埃博拉病毒与马尔堡病毒GP蛋白的序列同源性仅为23% (图 5C)。应用多株系丝状病毒模型评价化合物将有利于广谱抗丝状病毒药物的发现,并将有助于药物的作用机制研究。
讨论丝状病毒进入宿主细胞是病毒入侵的第一步,阻断此过程就可有效抑制丝状病毒感染,研发丝状病毒进入抑制剂是抗丝状病毒药物的重要研究方向。本文应用细胞水平重组病毒技术,以丝状病毒包膜表面唯一负责病毒进入的糖蛋白GP作为外壳蛋白,包裹携带报告基因的HIV核心,组装为丝状重组病毒颗粒。由于HIV基因组敲除了env、vpr和nef基因[22],此病毒颗粒仅可单次感染宿主细胞,因此是安全有效的药理筛选模型,可用于BSL-2级生物实验安全条件下操作,有利于对化合物的大规模筛选评价。本文针对丝状病毒科中恶性程度强、有代表性的病毒株系,共建立了三株丝状重组病毒模型,分别为扎伊尔型埃博拉重组病毒EBOV-Zaire GP/HIV-luc、苏丹型埃博拉重组病毒EBOV-Sudan GP/HIV-luc和马尔堡重组病毒Marburg GP/HIV-luc,同时应用VSVG/ HIV-luc重组病毒作为模型对照,便于进行假阳性化合物的筛查。丝状病毒GP/HIV重组病毒模型用于化合物筛选在国外已有应用[23, 24],而在国内尚属首次报道。多株系丝状病毒进入模型的建立将为寻找特异性丝状病毒进入抑制剂提供药物筛选评价平台,并将有利于药物作用机制的研究,对研发抗丝状病毒药物有重要意义。
| [1] | Feldmann H, Geisbert TW. Ebola haemorrhagic fever[J]. Lancet, 2011, 377:849-862. |
| [2] | Negredo A, Palacios G, Vázquez-Morón S, et al. Discovery of an ebolavirus-like filovirus in europe[J]. PLoS Pathog, 2011, 7:e1002304. |
| [3] | Centers for Disease Control and Prevention. Bioterrorism agents/diseases[EB/OL]. 2010-3-20. http://www.bt.cdc.gov/agent/agentlist-category.asp#a. |
| [4] | Sanchez A, Geisbert TW, Feldmann H. Filoviridae:Mar-burg and Ebola viruses. Fields virology[M]. Philadelphia:Lippincott Williams & Wilkins, 2006:1409-1448. |
| [5] | World Health Organization. Ebola Situation Report[EB/OL]. 2015-3-18. http://apps.who.int/ebola/current-situation/ebola-situation-report-18-march-2015. |
| [6] | Streether LA. Ebola virus[J]. Br J Biomed Sci, 1999, 56:280-284. |
| [7] | WHO Ebola Response Team. Ebola virus disease in West Africa-the first 9 months of the epidemic and forward projections[J]. N Engl J Med, 2014, 371:1481-1495. |
| [8] | Guo Y, Rumschlag-Booms E, Wang J, et al. Analysis of hemagglutinin-mediated entry tropism of H5N1 avian influenza[J]. Virol J, 2009, 6:39. |
| [9] | Cao YL, Guo Y. Screening of HIV-1 replication inhibitors by using pseudotyped virus system[J]. Acta Pharm Sin(药学学报), 2008, 43:253-258. |
| [10] | Zhang C, Cao YL, Zhong W, et al. Establishment of a cell-based 2009 H1N1 influenza neuraminidase inhibitors evaluation system[J]. Acta Pharm Sin(药学学报), 2010, 45:383-387. |
| [11] | Madrid PB, Chopra S, Manger ID, et al. A systematic screen of FDA-approved drugs for inhibitors of biological threat agents[J]. PLoS One, 2013, 8:e60579. |
| [12] | Kouznetsova J, Sun W, Martínez-Romero C, et al. Identification of 53 compounds that block Ebola virus-like particle entry via a repurposing screen of approved drugs[J]. Emerg Microbes Infect, 2014, 3:e84. |
| [13] | US Department of Health and Human Services. Biosafety in Microbiological and Biomedical Laboratories(BMBL) 5th Edition[M]. USA:HHS Publication, 2009:251-256. |
| [14] | Burnette WN. "Western blotting":electrophoretic transfer of proteins from sodium dodecyl sulfate-polyacrylamide gels to unmodified nitrocellulose and radiographic detection with antibody and radioiodinated protein A[J]. Anal Biochem, 1981, 112:195-203. |
| [15] | Cao YL, Li SX, Chen H, et al. Establishment of pharmacological evaluation system for non-nucleoside reverse-transcriptase inhibitors resistant HIV-1[J]. Acta Pharm Sin(药学学报), 2009, 44:355-361. |
| [16] | Guo JM, Guo Y. The in vitro HAART pharmacodynamics study with dolutegravir as the "anchor"[J]. Acta Pharm Sin(药学学报), 2015, 50:50-58. |
| [17] | Zhang JH, Chung TD, Oldenburg KR. A simple statistical parameter for use in evaluation and validation of high throughput screening assays[J]. J Biomol Screen, 1999, 4:67-73. |
| [18] | Grote A, Hiller K, Scheer M, et al. JCat:a novel tool to adapt codon usage of a target gene to its potential expression host[J]. Nucleic Acids Res, 2005, 33:W526-W531. |
| [19] | Manicassamy B, Wang J, Jiang H, et al. Comprehensive analysis of ebola virus GP1 in viral entry[J]. J Virol, 2005, 79:4793-4805. |
| [20] | Pak CC, Puri A, Blumenthal R. Conformational changes and fusion activity of vesicular stomatitis virus glycoprotein:[125I] iodonaphthyl azide photolabeling studies in biological membranes[J]. Biochemistry, 1997, 36:8890-8896. |
| [21] | Ford N, Mofenson L, Kranzer K, et al. Safety of efavirenz in first-trimester of pregnacy:a systematic review and meta-analysis of outcomes from observational cohorts[J]. AIDS, 2010, 24:1461-1470. |
| [22] | Petropoulos CJ, Parkin NT, Limoli KL, et al. A novel phe-notypie drug susceptibility assay for human immunodeficiency virus type 1[J]. Antimicrob Agents Chemother, 2000, 44:920-928. |
| [23] | Basu A, Li B, Mills DM, et al. Identification of a small-molecule entry inhibitor for filoviruses[J]. J Virol, 2011, 85:3106-3119. |
| [24] | Yermolina MV, Wang J, Caffrey M, et al. Discovery, synthesis, and biological evaluation of a novel group of selective inhibitors of filoviral entry[J]. J Med Chem, 2011, 54:765-781. |
 2015, Vol. 50
2015, Vol. 50


