2. 默克雪兰诺北京医药研发有限公司, 北京 100022;
3. 北京法马苏提克咨询有限公司上海分公司, 上海 200021;
4. 科文斯医药研发 (北京) 有限公司, 北京 100022
2. Merck Serono (Beijing) Pharmaceutical Distribution Co., Ltd., Beijing 100022, China;
3. Pharmaceutical Product Development (Beijing), Inc., Shanghai 200021, China;
4. Covance Pharmaceutical Research and Development (Beijing) Co. Ltd., Beijing 100022, China
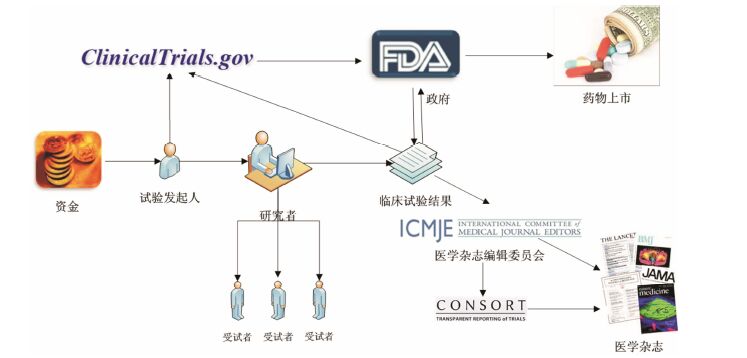
药物临床试验是指任何在人体 (患者或健康志愿者) 进行的系统性研究,其基本过程如图 1所示,目的是评估研究药物的疗效与安全性[1]。试验设计是药物临床试验的灵魂,试验数据是其申报上市的主要依据。在传统模式中,临床试验系统都是专用系统,其数据仅来源于临床试验目的本身。而随着医院信 息系统,尤其电子病历系统在医院的部署和普及,大量日常诊疗数据被存储在医院信息系统中,为药物临床试验提供了潜在的数据来源[2]。据《2013年我国卫生和计划生育事业发展统计公报》提供的数据,我国2013年总诊疗人次达73.1亿人次,入院人次达 19 215万人次。另据《中国医院信息化发展研究报告2008-2013》提供的数据: 2012年,我国电子病历系统普及率就已经达到46.67%。有研究显示,超过40%的临床试验需要采集的数据同时也存在于医院电子病历系统中。这些数据的互联互通将极大促进临床试验的效率。
|
图 1 临床试验基本流程及成果 |
临床试验数据的互联互通大体可以分为3个层次。第一个层次是物理上联通,但是语义不通。比如每个连接在互联网上的系统都可以说是联通了,但是大部分系统除了简单的管理信息,相互之间并不理解对方的内容。第二个层次是有一个公用的标准, 通过这个公用标准的“参照作用”,系统之间的内容可以经过翻译相互识别。第三个层次是各个系统从构建开始即遵循统一的标准,相互之间不需要翻译即可以相互交流、汇总数据。目前所讲的互联互通主要指第二个层次的互联互通。因为不同的实体和系统之间,其基本的数据结构和内部标准一般是不同的,但是只要有一个大家共同认可的公共标准,就可以进行系统间数据的转换、识别、交互、融合。
2 临床试验数据的主要标准临床试验数据的互联互通主要依赖于统一的标准。目前的临床数据标准主要分为两类: 一类是数据交换标准,用于不同系统、不同机构、不同地区甚至国家之间的数据交换和整合。一类是语义标准,在 指称同一事物的时候,确保使用规范的词语和唯一的编码,相互之间不会有交叉和歧义。国际上电子病历数据交换类标准主要有: HL7 (Health Level 7,HL7 卫生信息交换标准),OpenEHR (open domain-driven platform for developing flexible e-health systems),医学数字影像与通讯标准 (digital imaging and communications in medicine,DICOM) 等; 语义类标准主 要有: 医学系统命名法-临床术语 (systematized nomenclature of medicine-clinical terms,SNOMED CT),国际疾病分类 (international classification of diseases,ICD),观测指标标识符逻辑命名与编码 (logical observation identifiers names and codes,LOINC),临床药学标准术语 (normalized names for clinical drugs,RxNORM),医疗通用操作编码系统 (healthcare common procedure coding system,HCPCS)/医疗操作术语 (current procedural terminology,CPT) 等。不同的医疗机构使用着各种各样不同
的标准,即使是名称相同的标准,在细节上也可以有细微差异,如ICD编码的6位后编码可以由使用单 位根据自身情况自由定制。总之,各种标准间兼容性差,不同机构电子病历系统间的互联互通困难重重。临床研究的数据标准主要是CDISC (clinical data interchange standards consortium) 标准[3]。该标准由非营利性机构CDISC协会开发维护。美国FDA已 经声明在2016年12月17日以后,将全部强制“新药临床试验”的电子数据采用CDISC的数据标准进行提交。
目前,NCI (national cancer institute,美国国家 癌症研究院)、FDA、CISCS、HL7等多个标准组织正在建设一个“BRIDG (biomedical research integrated domain group)”模型[4],该模型主要在CDISC和HL7参考信息模型 (reference information model,RIM) 之间建立映射关系,以便于遵循不同协议标准的数据之间的语义互通。
3 临床试验数据互联互通的最新进展国内外在该领域均做了许多有益的探索。其中 美国的临床数据互联互通的研究多是以大学为主 体进行,主要的平台包括: 斯坦福大学医学中心的STRIDE[5]; 杜克大学综合癌症研究中心的caTRIP[6]; 俄亥俄州州立大学医学中心的IW[7]; NIH资助的i2b2[8]等。其中i2b2是一个由NIH资助的生物计算国家研究中心,致力于临床数据分析应用。该系统是开源系统,包含很多组件。该系统的许多组件,目前在该领域多个平台中得到应用。欧洲的临床数据互联互通的项目多以欧盟资助的形式存在,代表性的项目和平台主要有: EHR4CR (electronic health records for clinical research)[9] 、EMIF (2013-2017)、Linked2 Safety (2011-2014) 等。
从2007年开始,美国FDA依托ClinicalTrials.gov网站采集的数据,与杜克大学合作,启动了一个临床试验转化创新 (clinical trials transformation initiative,CTTI) 项目,致力于将ClinicalTrials.gov网站的临 床试验注册数据以及临床试验结果数据进行分析利用[10]。该项目建立了一个AACT (aggregate analysis of clinicaltrials.gov) 数据库,这个数据库定期更新,这些数据免费向包括美国以外的公众开放,目前提供经过整理的Oracle关系数据库格式、文本格式以及SAS格式的数据下载。
我国在该领域也开始了积极的探索和尝试。上 海申康公司的医联网平台已经连接了34家上海地区的医院,采集的信息主要服务于医保和患者转诊,目前实现了上海地区34家医院的检查报告查询。2015年5月26日在北京大学医学部成立了国家医疗数据中心 (国家卫生计生委医管中心支持)。2015年5月28日在四川电子科技大学成立了医疗健康大数据研究院 (国家卫生计生委信息中心支持)。2015年6月CDISC中国协调委员会成立了互联互通工作组 (China CDISC Coordinating Committee (C3C) Healthcare LinkWork Group),专门研究临床研究数据的互联互通及医院临床数据二次利用问题。但是总体来看,国内该领域的研究还刚刚起步,大多研究还是在单个或隶属于同一系统的医院中进行。
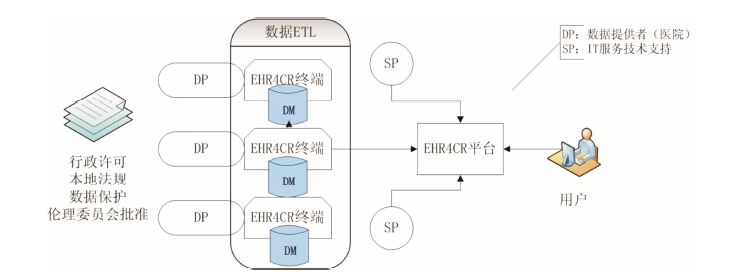
4 欧洲最大的临床试验数据互联互通项目—— EHR4CR在医院电子病历系统数据互联互通的探索中,有示范意义的是欧洲的EHR4CR (electronic health records systems for clinical research) 项目[9, 11]。该项目是一个由创新药物行动 (innovative medicine initiative,IMI) 资助的项目 (2011-2015)。总投资额为1 600万欧元,其目标是“为将电子病历数据应用于临床研究,开发可重用、可扩展的方案、工具和服务”。目前有34个成员 (包括10家制药企业以及11家医院),横跨德国、法国、英国、瑞士和波兰5个国家。该项目从欧盟先前的以及其他的类似项目中汲取了很多有益的元素,形成具有自己风格的中间件,安全组件,查询引擎,数据分析组件等功能组件。该系统平台的基本结构如图 2所示。
|
图 2 EHR4CR平台结构简图 |
接入EHR4CR平台的终端医院需要安装部署EHR4CR代理软件,该套软件分为3部分: ① 医院本地数据库 (指医院本身的电子病历系统) 的数据提取。② 医院本地数据与EHR4CR平台的接口,负责将医院电子病历数据库与EHR4CR平台进行互联。接口层的主要工作之一是将“EHR4CR核心术语”与“医院本地术语”进行映射。③ EHR4CR数据集市 (DM,data mart),负责存储完全符合EHR4CR平台信息模型的数据,直接向EHR4CR大平台提供可识别的信息。
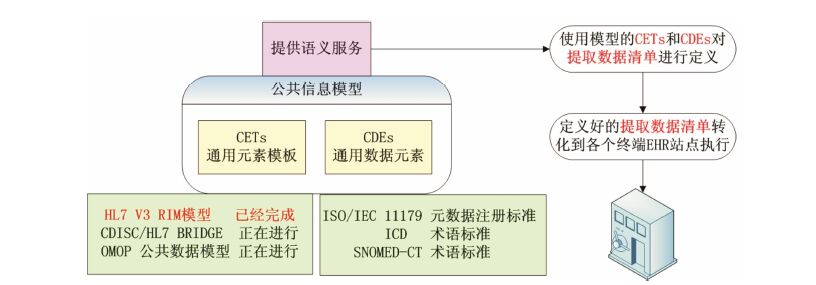
EHR4CR的公共信息模型是各接入医院之间数据互通的基础,如图 3所示,该模型以业界公用标准 (如ISO/HL7 V3 RIM,ISO/IEC 11179 MDR [Metadata RegistryStandard,元数据注册标准],ICD,SNOMED- CT,CDISC/HL7 BRIGE等) 为基础,形成“通用数据模板 (common element templates,CETs)”和“通用数据元素 (common data elements,CDEs)”两个基础模块。这两个基础模块是构成EHR4CR平台的公共信息模型 (common information model,CIM) 的基本元素,是可以由机器处理的标准化语义组件。由公共信息模型为各组成部分之间的语义交互提供参照。
|
图 3 EHR4CR平台公共信息模型结构 |
目前该平台已经在5个欧洲国家的11家医院中进行了系统可行性测试。EHR4CR平台相关终端软 件在11个医院终端站点进行了部署,在12个临床试验的受试者招募中进行了测试,筛选处理了超过500万个患者的匿名化数据。测试表明,该系统可以加速
受试者的招募速度,提高寻找目标受试者的准确性,同时降低临床试验费用[12]。以上测试局限在受试者招募过程,平台对于临床试验的全程支持尚未最终完成。2016年,该项目将转为欧洲制药工业联合会 (European Federation of Pharmaceutical Industries and Associations,EFPIA) Champion Program,由参加该项目的每个医药公司全资或部分资助3~5家医院,目标是在2015~2016年间,在EHR4CR平台上新接入25~30家医院。
5 对临床试验数据互联互通的展望随着移动终端 (手机、PDA) 以及各种可穿戴设备的普及,使“对人体各种生理指标进行持续的、伴随性的动态数据采集和处理”已经成为现实,这些数据对于慢病监测和管理有着重要的意义[13]。但是这些移动健康数据的特点是“数据量更大,数据类型更多,数据标准更不统一”,甚至它们采集到数据的准度和精度都有待规范[14]。因此对这些数据的整合利用目前还存在很大的难度。除了需要解决的技术问题以外,还有伦理学问题,数据利用与个人隐私保护的矛盾处理以及“数据公用的利益协调机制”等。目前限制临床数据互联互通共享利用的瓶颈主要包括“技术平台”、“社会环境”以及“商业模式”等三个方面。解决这些问题,将是一个长期的过程。不受限制的互联互通是不存在的,需要在数据利用、技术水平、隐私保护、运行成本等几个方面找到最佳平衡点。这些需要政府部门 (如卫生计生委、SFDA等)、行业协会、标准组织、医院以及商业公司等几方的共同努力。如由政府负责搭台,营造大环境并出台各种激励措施; 行业协会和标准组织负责建立符合实际的、不断维护更新的、中文版本的可落地标准; 医院负责提供符合标准要求的数据; 商业公司负责提供资助和进行商业运作,最终形成一个多方共赢的,可持续发展的临床数据共享利用生态环境。可以预见,随着各种临床试验相关数据的互联互通共享,我们将迎来药物临床试验领域革命性的改变。现有的以随机抽样为基础的统计分析方法将面临新的挑战,以群体大数据与个人大数据为基础的“精准医疗”也许不再遥远。
| [1] | Zou C, Jiang M, Liu F, et al. Discussion on management of new drug clinical trials project [J]. Chin J New Drugs Clin Rem (中国新药与临床杂志), 2013, 22: 915-917. |
| [2] | Weiskopf NG, Weng C. Methods and dimensions of electronic health record data quality assessment: enabling reuse for clinical research [J]. J Am Med Inform Assoc, 2013, 20: 144-151. |
| [3] | Lu F, Gao R, Tang XD, et al. Applications and prospects of data management standards in Clinical Data Interchange Standards Consortium in clinical research [J]. Chin New Drugs J (中国新药杂志), 2011, 20: 2400-2404. |
| [4] | Fridsma DB, Evans J, Hastak S, et al. The BRIDG project: a technical report [J]. J Am Med Inform Assoc, 2008, 15: 130-137. |
| [5] | Lowe HJ, Ferris TA, Hernandez PM, et al. STRIDE-an integrated standards-based translational research informatics platform [J]. AMIA Annu Symp Proc, 2009, 2009: 391-395. |
| [6] | Mcconnell P, Dash RC, Chilukuri R, et al. The cancer translational research informatics platform [J]. BMC Med Inform Decis Mak, 2008, 8: 60. |
| [7] | Kamal J, Liu J, Ostrander M, et al. Information warehouse-a comprehensive informatics platform for business, clinical, and research applications [J]. AMIA Annu Symp Proc, 2010, 2010: 452-456. |
| [8] | Murphy SN, Weber G, Mendis M, et al. Serving the enterprise and beyond with informatics for integrating biology and the bedside (i2b2) [J]. J Am Med Inform Assoc, 2010, 17: 124-130. |
| [9] | De Moor G, Sundgren M, Kalra D, et al. Using electronic health records for clinical research: the case of the EHR4CR project [J]. J Biomed Inform, 2015, 53: 162-173. |
| [10] | Tenaerts P, Madre L, Archdeacon P, et al. The clinical trials transformation initiative: innovation through collaboration [J]. Nat Rev Drug Discov, 2014, 13: 797-798. |
| [11] | Ouagne D, Hussain S, Sadou E, et al. The electronic healthcare record for clinical research (EHR4CR) information model and terminology [J]. Stud Health Technol Inform, 2012, 180: 534-538. |
| [12] | Doods J, Bache R, Mcgilchrist M, et al. Piloting the EHR4CR feasibility platform across Europe [J]. Methods Inform Med, 2014, 53: 264-268. |
| [13] | Xu L, Chen MY. Application of wearable medical device in medical monitoring system [J]. China Digit Med (中国数字医学), 2015, 10: 23-24. |
| [14] | Cui HE, Yao SW. Key technology and quantity control of wearable medical devices [J]. Chin J Med Instrum (中国医疗器械杂志), 2015, 39: 113-117. |
 2015, Vol. 50
2015, Vol. 50


