2. 中国科学院上海高等研究院, 上海 201210;
3. 北京百奥知信息科技有限公司, 北京 100098
2. Shanghai Advanced Research Institute, Chinese Academy of Science, Shanghai 201210, China;
3. Beijing Bioknow Information Technology Co, Ltd., Beijing 100098, China
每一次信息技术的发展都会给各行业带来革新性的变化,临床研究也不例外。实际上,自上世纪50年代,计算机便被用于处理临床研究数据。上个世纪80年代,个人电脑的普及极大地促进了它在临床研究领域的应用; 90年代中期互联网技术的发明,彻底改变了临床研究的方式与方法。临床数据从由纸质病例报告表 (CRF) 的填写后,再录入到早期单机版的数据管理系统,发展到基于网络的多中心电子数据采集 (EDC); 随机化也从最早的信封发放发展到基于电话的应答处理,以及今天的基于网络以至于基于移动通讯(如手机或iPAD) 的随机。今天,信息化技术的应用对临床研究的过程管理、文档管理以及临床数据的采集、管理、报告与分析等都产生了积极影响。信息技术的运用已经彻底改变了临床研究的过程与方法,极大地提高了临床研究的效率与质量[1]。
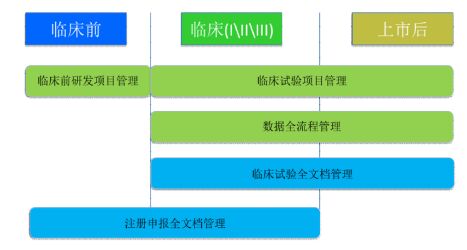
1 数据管理过程与文档管理临床研究涉及临床研究机构、研究者、伦理委员会、医学部、监查部、质量部、统计部、数据管理部等部门,临床研究所使用的计算机化系统主要包括临床研究项目管理 (CTMS)、临床试验受试者管理系统、EDC系统、数据管理系统、随机化与药物管理 (RTSM)、患者报告结局 (ePRO)、临床试验不良事件管理报告系统 (PV)、临床研究全文档管理系统 (TMF) 以及注册申报管理系统 (eCTD) 等。从药物临床试验质量管理规范 (GCP) 的角度来看[2, 3],临床研究主要关注的要素是数据、过程与文档。数据贯穿于临床研究的各个阶段,它是用于统计分析的基础,而临床研究的过程管理包括临床前、临床与上市后的过程管理,主要是确保临床研究的过程符合法规的要求; 临床研究的文档则是记录临床研究过程的文件化的证据,以便重塑临床研究的过程 (图 1)。
|
图 1 临床研究中的过程管理与文档管理 |
临床研究的信息化管理是用现代信息技术管理临床研究的数据、过程与文档。它通过技术手段整合内外部资源,以完善临床研究的方式与流程,提高临床研究的效率和效益以及临床研究的质量[1, 4, 5]。
临床研究的信息化管理主要分为三个层次: ① 最低要求: 数据能收集,文档可保存、可查询等,如Excel、Epidata; ② 中等要求 (主要是合规): 符合法规要求的电子采集与管理规范,支持质量控制,逻辑核查,原始数据核查 (source data verification,SDV),稽查轨迹,版本控制,支持电子签名等; ③ 高等要求 (一体化): 遵守国际标准与国际规范,涵盖药物研发以及临床研究的整个过程,实现数据与过程的可溯源性,并实现系统间信息的互联互通与实时交换,同时支持移动互联网。
临床研究要实现信息化管理必须解决的几个难题: ① 电子化: 信息化管理的首要要求必须是电子化,基于纸质的临床研究做不到电子化。基于电子化的源数据与电子化的数据采集系统为信息化管理提供了必要的物质基础与应用基础; ② 标准化: 缺乏标准将很难实现数据的识别与交换; ③ 关联性: 也叫交互性,主要指的是系统间信息/数据的互联互通,这是一体化的基础; ④ 可扩展性: 主要指的是系统必须具有强大的灵活性以容纳来自其他系统的信息。
3 国内外临床研究信息化水平比较欧美发达国家凭借其技术优势已经走在临床研究信息化与一体化应用的前列,并取得了巨大的成功。我国由于临床研究起步较晚,所使用的技术也相对落后[6, 7, 8, 9, 10, 11],基本还处于纸质与手工阶段,如临床监察员 (CRA) 和项目经理 (PM) 需要花费大量时间,手工整理各项目的进展、入组汇总、文件归档等,数据的准确性无法溯源,有时也有缺失等; 数据/文档散落分布,有的使用文件服务器管理 (缺乏版本控制),有的因员工离职导致资料丢失。但是,随着国家对科技创新的大力支持,国内各制药企业在药物研发方面的投入力度也越来越大,与此同时,国内的信息化技术与水平也在不断地提高 (表 1)。
|
|
表 1 国内外临床研究信息化水平比较 |
国外一直在追求信息技术的一体化并付出了不少的努力,但是,由于种种原因,一体化始终没有很好实现,各系统间缺乏高效的互联互通,数据整合采用更多的是系统外的手工操作,或者是建立更大的数据仓库。
4 一体化信息技术应用于临床研究的优势一体化信息技术应用于临床研究的主要优势包括在表 2中。
|
|
表 2 一体化信息技术应用于临床研究的主要优点 |
此外,一体化信息系统有利于具有创新能力与创新意志的企业可以更容易地采纳国际标准与规范技术,充分利用信息技术带来的便利,为开拓国际市场并创建产品的大数据仓库和数据挖掘提供基础。
5 一体化信息技术的必然性药物研发的过程越来越复杂,产生的数据越来越多。传统的药物研发管理模式已经无法适应复杂的流程与海量的信息。信息在采集、管理、整合、共享、汇总与监控等方面给管理者带来了越来越大的压力。信息的准确与及时将为研发管理者的决策提供可靠的数据基础。因此,利用信息化技术管理临床研究过程与数据目前已经成为我国临床研究的一个迫切要求,很多制药企业也在此领域投入了大量的人力物力,并初步显现出显著性的质量与效率的提升。
电子数据采集系统是最受重视的信息化技术,因其在效率、质量与成本等方面的诸多优势,它在我国临床研究中的使用率不断提高。但我国目前的EDC系统尚存功能不完善、操作不规范以及缺乏验证等问题[9, 10]。为此,我国药监部门正在制订电子数据采集技术指南,以规范EDC的使用。
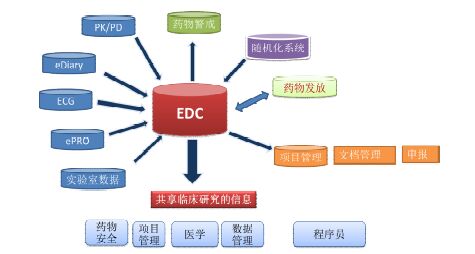
目前,临床研究一体化信息技术,特别是移动互联网技术与云平台,将药物研发过程中各个阶段有机地整合在一起,将数据采集、随机化、药物发放、ePRO、数据管理、医学编码、数据报告、项目管理、药物安全警戒、eTMF以及eCTD等融为一体,实现对研发过程、数据以及质量的全面管理 (图 2)。
|
图 2 一体化信息技术在临床研究中的应用 |
一体化信息技术在临床研究中的应用,很大程度上得益于我国的后发优势,通过吸取西方国家的教训,走出适合我国国情的信息化之路。
| [1] | Yan CC. Data Management in Clinical Research (医药临床 研究中的数据管理) [M]. Beijing: Science Press, 2011: 1-11. |
| [2] | Society of Clinical Data Management. Good Clinical Data Management Practices [S]. 2013. |
| [3] | ICH. E6 Good Clinical Practices [S]. 1997. |
| [4] | Marks RG, Conlon M, Ruberg SJ. Paradigm shifts in clinical trials enabled by information [J]. Statist Med, 2001, 20: 2683-2696. |
| [5] | McFadden ET, Lopresti F, Bailey LR, et al. Approaches to data management [J]. Control Clin Trials, 1995, 16: 30S-65S. |
| [6] | Palm U. Controlling the increased complexity of electronic clinical data collection and management technology by data modeling and system engineering [J]. Drug Inf J, 2002, 36: 683-692. |
| [7] | Kush RD, Bleicher P, Kubick WR, et al. eClinical Trials, Planning & Implementation [M]. Boston, MA: CenterWatch Inc., 2003. |
| [8] | Maloy J. Tipping the scale toward success-technology [J]. The Monitor, 2003, 17: 18-23. |
| [9] | Li QN, Lu F, Gao R, et al. Current investigation of e-data management in TCM clinical research [J]. Chin J Inf Tradit Chin Med (中国中医药信息杂志), 2014, 21: 6-9. |
| [10] | Deng YZ, Yu J, Liu C, et al. Current status and trend of clinical data management at electronization time [J]. Chin J New Drugs (中国新药杂志), 2014, 8: 879-884. |
| [11] | Goldfarb NM. Clinical research information technology: the future is here [J]. J Clin Res Best Pract, 2015, 11: 1-3. |
 2015, Vol. 50
2015, Vol. 50


