2. 中国药科大学药学院, 江苏 南京 211100
2. College of Pharmacy, China Pharmaceutical University, Nanjing 211100, China
全身性炎症反应综合征 (systemic inflammatory response syndrome,SIRS) 大多是由严重感染、严重创伤及胰腺炎等诱发,能引起与重症炎症或局部炎症无直接关系的肺、肝脏、肾脏等多脏器功能障碍,病情严重时还会造成死亡。在伴有SIRS的脏器功能障碍中,急性肺损伤最难治疗[1, 2]。临床上表现为继发性急性呼吸窘迫综合征。近年研究发现,中性粒细胞释放的弹性蛋白酶参与弹性蛋白、O型胶原、蛋白多糖等细胞外基质主要构成成分的降解过程,与各种急性肺损伤的发病和炎症反应关系密切[3, 4, 5],因此,弹性蛋白酶抑制药在治疗SIRS并发的肺损伤中有广阔的应用前景。
西维来司他钠水合物是人体中性粒细胞弹性蛋白酶竞争性抑制剂[6, 7, 8, 9],为全球首个急性肺损伤治疗药物,于2002年在日本上市,以静脉滴注方式给药。与内源性蛋白酶抑制物比较,低分子质量的西维来司他能够到达中性粒细胞和组织的间隙,并且其抑酶活性也不受活性氧影响,可在炎症局部位置有效抑制弹性蛋白酶[10, 11, 12]。该药主要在肝脏经酯酶水解代谢,生成XW-IMP-A,由尿液排泄。为研究西维来司他在人体的药动学,需建立灵敏分析方法测定血浆中西维来司他及其代谢物。
本实验旨在建立准确、快速、灵敏的HPLC-MS/ MS法同时测定人血浆中西维来司他及其代谢物,并将确证后的方法应用于注射用西维来司他钠的人体药动学研究。
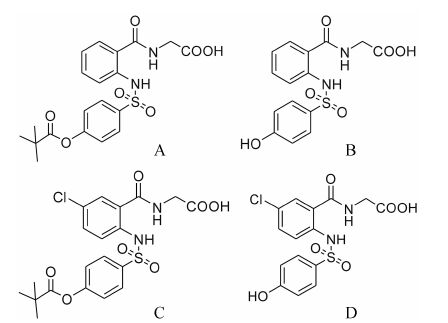
材料与方法 对照品与试剂西维来司他钠水合物对照品 (批号XW-130703-B1,含量99.7%)、XW-CL对照品 (批号130621,含量96.7%)、XW-IMP-A对照品 (批号130329,含量99.7%) 和XW-CL-A对照品 (批号130626,含量97.9%) 均由上海汇伦生命科技有限公司提供。4个化合物的结构见图 1。甲醇 (德国Merck公司)、乙腈 (德国Merck公司) 和醋酸铵 (美国ROE公司) 均为色谱纯。人空白血浆 (曙光医院临床试验机构)。
|
Figure 1 Structures of sivelestat (A,MW 434.46),XW-IMP-A (B,MW 350.35),XW-CL (C,MW 468.91),XW-CL-A (D,MW 384.79) |
API 4000型三重四极杆串联质谱仪,配备电喷雾电离源 (ESI源),美国AB SCIEX公司; 岛津液相色谱系统 (包括DGU-20A3型脱气机、LC-20AD型二元输液泵、SIL-20AC型自动进样器和CTO-20A型柱温箱),日本岛津公司。
色谱条件分析柱: Capcell PAK C18 (4.6 mm × 100 mm,5 μm,日本资生堂公司); 预柱: C18保护柱 (4.0 mm × 3.0 mm,5 μm,美国Phenomenex公司); 流动相: A相 (5 mmol·L-1醋酸铵水溶液),B相 (甲醇-乙腈,7∶3); 梯度洗脱: 0~0.5 min,45% B; 0.5~0.51 min,45%~70% B; 0.51~2.5 min,70% B; 2.5~2.51 min,70%~45% B; 2.51~6 min,45% B。流速: 0.7 mL·min-1。柱温: 25 ℃。进样量: 10.0 µL。
质谱条件离子源: 电喷雾电离源 (Turbo Ionspray); 离子化方式: 负离子模式; 喷雾电压: -4 200 V; 加热毛细管温度: 500 ℃; 离子源气体1 (N2) 压力为50 psi (1 psi ≈ 6.9 kPa); 离子源气体2 (N2) 压力为50 psi; 气帘气体 (N2) 压力为10 psi; 扫描方式为多反应监测 (MRM),碰撞气压力为8 psi; 扫描方式: 选择反应监测; 扫描时间为100 ms; 用于检测的各待测物 的离子反应分别为: m/z 433→m/z 389 (西维来司他)、m/z 467→m/z 423 (XW-CL)、m/z 349→m/z (175+148) (XW-IMP-A)、m/z 383→m/z 182 (XW-CL-A)。
标准系列样品和质控样品的制备分别精密 称取西维来司他和XW-IMP-A对照品各两份,用乙腈-水 (1∶1) 溶解并定容,分别获得质量浓度约为1.00 mg·mL-1的西维来司他和XW-IMP-A的储备液。一份用于标准系列样品的配制,另一份用于质控 (QC) 样品的配制。用人空白血浆稀释西维来司他和XW-IMP-A储备液,得标准系列样品的血浆质量浓度分别为10.0/2.50、 30.0/5.00、100/10.0、300/25.0、1 000/100、3 000/200、7 500/500和15 000/1 000 ng·mL-1; 质控样品的血浆质量浓度分别为10.0/2.50 (LLOQ)、25.0/6.00 (LQC)、2000/150 (MQC)、12 000/800 (HQC) ng·mL-1。QC样品于 -20 ℃下储存。
血浆样品预处理取人血浆100 μL,分别加入乙腈-水溶液 (1∶1) 50 μL、内标溶液 (2 μg·mL-1 XW- CL用于西维来司他测定; 1 μg·mL-1 XW-CL-A用于XW-IMP-A测定) 25 μL和200 μL乙腈,涡流1 min,离心5 min (14 000 r·min-1)。取上清液100 μL于另一干净试管中,加入5 mmol·L-1醋酸铵水溶液100 μL,涡流30 s,取10 μL进行HPLC-MS/MS分析。
方法学验证 选择性分别取6个不同来源的人空白血浆以及相应空白血浆配置的LLOQ样品进行HPLC-MS/MS分析。考察血浆中内源性物质是否干扰待测物及其内标测定。
标准曲线按“血浆样品预处理”项下操作,以每个待测物浓度为横坐标,待测物与内标物的峰面积比值为纵坐标,用加权 (W = 1/x2) 最小二乘法进行回归运算,求得的直线回归方程即为标准曲线。
精密度与准确度取低、中、高3个浓度 (西维来司他/XW-IMP-A的血浆量浓度分别为25.0/6.00、 2 000/150和12 000/800 ng·mL-1) 的QC样品,按“血浆样品预处理”项下操作,每浓度进行6样本分析,连续测定3天,求得日内、日间精密度与准确度。
基质效应分别取6份不同来源的人空白血浆和1份空白溶血血浆,除不加内标外,按“血浆样品预处理”项下操作,取全部上清液,加入相应浓度对照质控溶液 (西维来司他/XW-IMP-A的溶液分别是50.0/12.0和24 000/1 600 ng·mL-1) 和内标溶液,涡 流混匀后,取100 μL上清液于另一干净试管中,加入5 mmol·L-1醋酸铵水溶液100 μL,涡流混匀,每一浓度进行三样本分析,获得相应的平均峰面积。同法以水代替空白血浆,按上述方法处理,每一浓度进行三样本分析,获得相应的平均峰面积。以两种处理方法的峰面积比值计算待测物的基质效应。
回收率取人空白血浆配制低、中、高三浓度的质控样品,按“血浆样品预处理”项下操作,每一浓度进行6样本分析。同时另取人空白血浆100 µL,除不加内标溶液外,按“血浆样品预处理”项下操作,取全部上清液,加入相应浓度对照质控溶液 (西维来司他/XW-IMP-A的溶液分别是50.0/12.0、4 000/300和24 000/1 600 ng·mL-1) 和内标溶液,涡流混匀后,取100 μL上清液于另一干净试管中,加入5 mmol·L-1醋酸铵水溶液100 μL,涡流混匀后进样分析。以每一浓度两种处理方法的峰面积比值计算处理回收率。
稳定性血浆样品储存和预处理均在避光条件下进行。本实验考察了西维来司他及其代谢物低、高两浓度 (西维来司他/XW-IMP-A分别为25.0/6.00和12 000/800 ng·mL-1) 血浆样品处理后避光室温放置48 h稳定性、人血浆样品避光室温放置6 h、经历3次冷冻-解冻循环和 -20 ℃长期放置的稳定性。
稀释实验本实验考察了血浆浓度超出定量上限的样品,经空白人血浆稀释后的准确度。取西维来司他/XW-IMP-A的稀释质控样品 (西维来司他和XW-IMP-A血浆质量浓度为30 000和2 000 ng·mL-1),用空白人血浆稀释4倍后,按“血浆样品预处理”项下操作,进行6样本分析,根据当日标准曲线计算每一样本测得浓度。
药动学研究临床试验经苏州大学附属第一医院伦理委员会批准,10名健康受试者,分别给予1.0 mg·kg-1·h-1注射用西维来司他钠,静滴2 h。在给药前和给药后0.5、1.0、1.5、2.0、2.25、2.5、3.0、4.0、6.0、8.0、10.0、12.0、24.0、36.0和48.0 h静脉取血3 mL。血样在采集后置于含肝素的抗凝管中,立即于4 ℃以3 500 r·min-1离心10 min,获得的血浆样品于 -20 ℃冷冻保存。
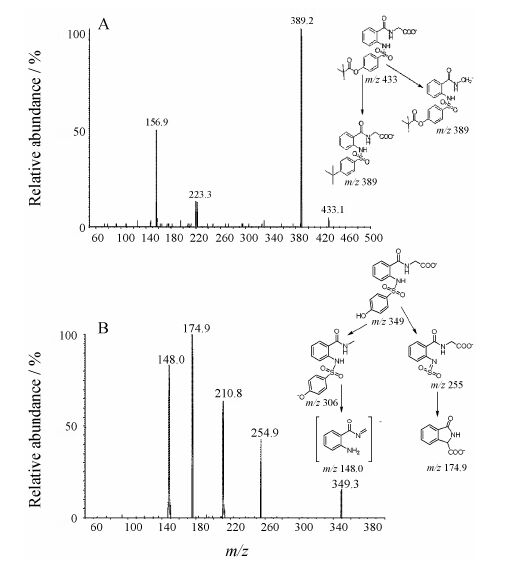
结果 1 质谱分析西维来司他、代谢物XW-IMP-A、内标XW-CL和内标XW-CL-A主要生成m/z 433、m/z 349、m/z 467和m/z 383的[M-H]-峰。4个化合物的结构见图 1。选择性对[M-H]-峰进行产物离子扫描,西维来司 他和内标XW-CL的主要碎片为m/z 389和m/z 423,XW-IMP-A和内标XW-CL-A产生的主要碎片离子为m/z (175+148) 和m/z 182,将这些主要碎片作为定量分析时检测的产物离子。待测物及内标的产物离子扫描质谱图及可能的断裂方式见图 2。
|
Figure 2 Product mass spectra of [M-H]- ions of sivelestat (A),XW-IMP-A (B) and their proposed fragmentation pathways |
空白人血浆中的内源性物质不干扰待测物西维来司他、XW-IMP-A和内标XW-CL、XW- CL-A的测定。典型色谱图见图 3。

|
Figure 3 Typical MRM chromatograms of XW-IMP-A (I),XW-Cl-A (II),sivelestat (III),XW-Cl (IV) in human plasma. A: Blank plasma; B: Blank plasma spiked with 2 000 ng·mL-1 XW-Cl and 1 000 ng·mL-1 XW-Cl-A; C: Blank plasma spiked with 10 ng·mL-1 sivelestat,2.5 ng·mL-1 XW-IMP-A,2 000 ng·mL-1 XW-Cl and 1 000 ng mL-1 XW-Cl-A; D: A plasma sample from No.1 human volunteer 2.5 h after an intravenous drip administration of 0.2 mg·kg-1·h-1 sivelestat |
用加权 (W = 1/x2) 最小二乘法进行回归运算,求得的标准曲线的相关系数 (r2) 均大于0.99。根据标准曲线,测定人血浆西维来司他和XW-IMP-A的线性范围分别为10.0~15 000和2.50~1 000 ng·mL-1。典型标准曲线回归方程为: 西维来司他,y = 0.000 834 x + 0.001 66 (r = 0.998 5); XW-IMP-A,y = 0.003 14 x + 0.002 86 (r = 0.999 4)。
取空白血浆配制LLOQ样品 (西维来司他/XW- IMP-A血浆质量浓度为10.0/2.50 ng·mL-1),进行6样本分析,连续测定3天,并根据当日标准曲线求得每一样本测得浓度。结果表明LC-MS/MS法测定人血浆中西维来司他和XW-IMP-A的定量下限分别可达10.0和2.50 ng·mL-1。
2.3 精密度与准确度西维来司他和XW-IMP-A 每一浓度水平QC样品的日内精密度 (RSD) 均小于8.5%,日间精密度 (RSD) 均小于9.0%,准确度 (RE) 在 -1.3%~1.4% 之间; XW-IMP-A每一浓度水平QC样品的日内精密度 (RSD) 均小于7.3%,日间密度 (RSD) 均小于6.9%,准确度 (RE) 在 -0.8%~2.5% 之间。
2.4 回收率采用沉淀蛋白法处理血浆样品可获得较高的回收率。西维来司他在低、中、高三浓度的回收率分别为 (86.2 ± 3.7) %、(83.9 ± 1.0) % 和 (89.0 ± 1.6) %; XW-IMP-A在低、中、高三浓度的回收率分别为 (82.6 ± 4.9) %、(89.2 ± 1.7) % 和(84.7 ± 1.0) %。
2.5 基质效应西维来司他在低、高两浓度的基 质效应分别为95.5% 和94.3%,相对标准差分别为2.8% 和3.8%; 内标XW-CL的基质效应为104%,相对标准差为1.7%。XW-IMP-A在低、高两浓度的基质效应分别为99.6% 和100%,相对标准差分别为2.9% 和1.6%; 内标XW-CL-A的基质效应为105%,相对标准差为3.9%。结果表明,待测物及其内标在本实验选择的色谱和质谱条件下,可忽略基质效应的影响。
2.6 稳定性西维来司他及其代谢物XW-IMP-A低、高两浓度血浆样品经预处理后避光室温放置24 h 稳定 (西维来司他和XW-IMP-A的RE分别在0.8%~4.1% 和0.2%~3.5% 之间); 血浆样品避光室温放置 6 h (西维来司他和XW-IMP-A的RE分别在 -5.6%~2.5% 和2.0%~7.3% 之间)、经历3次冷冻-解冻循 环 (西维来司他和XW-IMP-A的RE分别在 -0.7%~4.4% 和2.3%~4.7% 之间) 和 -20 ℃放置101天(西维来司他和XW-IMP-A的RE分别在 -4.9%~-2.4% 和-3.5%~6.2% 之间) 条件下均稳定。
2.7 稀释实验西维来司他稀释质控样品经4倍稀释后测得的精密度和准确度 (RE) 分别为1.3% 和 -8.6%。XW-IMP-A稀释质控样品经4倍稀释后测得的精密度和准确度 (RE) 分别为2.2% 和2.5%。结果表明,人血浆样品经空白人血浆稀释4倍后测定不影响结果的准确度。
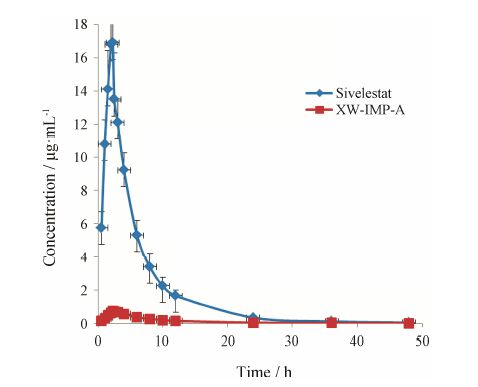
3 药动学研究将所建立并经过验证的方法应用于注射用西维来司他的人体药动学研究。健康受试者给予1.0 mg·kg-1·h-1注射用西维来司他钠静滴2 h,西维来司他和XW-IMP-A的药时曲线见图 4。
|
Figure 4 Mean plasma concentration-time curves of sivelestat and XW-IMP-A after an intravenous drip administration of 1.0 mg·kg-1·h-1 sivelestat to 10 male volunteers |
西维来司他和代谢物XW-IMP-A分子结构中均含有碱性氮原子和羧基,使得它们在正、负离子模式下均有响应,实验结果显示在负离子模式下响应更高,信号更稳定,另外发现西维来司他及其代谢物XW-IMP-A在APCI源下的响应均明显小于ESI,所以最终选择用ESI源负离子检测。
西维来司他结构中含有酯键,血浆中的酯酶、光照、pH均可能影响其稳定性,而导致定量分析结果的偏差。本文在方法建立时重点对药物的稳定性进行了考察。分别将低、高浓度的西维来司他溶液和XW- IMP-A溶液各3份置于光照条件下,24 h后测定浓度。结果表明,低、高浓度的西维来司他溶液分别降低了22% 和18%,同时还有部分XW-IMP-A生成,而XW- IMP-A溶液未检测到明显变化。将上述西维来司他和XW-IMP-A工作液置于避光的条件下,结果显示西维来司他和XW-IMP-A溶液均稳定。因此,为了保持待测物的稳定性,本实验的所有操作都在避光条件下进行。另外,实验中也考察了待测物在样品处理过程中pH值对稳定性的影响。经乙腈沉淀蛋白后的 上清液以不同pH值 (3、5、7和9) 的缓冲液等体积稀释,室温放置24 h后测定其稳定性。结果发现,在pH小于5或大于9体系下待测物响应均不稳定。因此 ,本实验采用5 mmol·L-1醋酸铵水溶液等体积稀释上清液以维持pH值在6~8之间,室温可放置至 少24 h。血浆稳定性结构表明,西维来司他不受血浆中酯酶影响。
在色谱条件优化时,发现以甲醇作为流动相的有机相时,西维来司他的质谱响应和浓度的线性关系良好,但代谢物XW-IMP-A高浓度响应易饱和。以 乙腈作为流动相的有机相时,出现相反结果。考虑到甲醇和乙腈在色谱分离能力和离子化上各有优缺点,并结合人血浆样品中西维来司他和XW-IMP-A的浓度范围,本实验尝试了以不同比例的甲醇-乙腈作 为有机相。西维来司他 (logP = 2.96) 和代谢物XW- IMP-A (log P = 1.53) 的极性相差较大,为保证两个待测物尽可能在较短时间内实现同时测定,本实验采用梯度洗脱方式,以确保两个待测物均获得良好的峰形和足够的响应。本实验也比较了两者在Atlantis C18柱 (4.6 mm × 100 mm,5 μm) 和Capcell PAK C18柱 (4.6 mm × 100 mm,5 μm) 的保留行为,结果显示待测物在前者上的出峰时间较早且基质效应严重,在后者上有较好的保留和峰形。
| [1] | Tamakuma S, Ogawa M, Aikawa N, et al. Relationship between neutrophil elastase and acute lung injury in humans [J]. Pulm Pharmacol Ther, 2004, 17: 271-279. |
| [2] | Du GH, Wu S, Feng WH. Sivelestat sodium in the treatment of acute lung injury research [J]. Chin Pharm J (中国药学杂志), 2004, 39: 321-324. |
| [3] | Ryugo M, Sawa Y, Takano H, et al. Effect of a polymorphonuclear elastase inhibitor (sivelestat sodium) on acute lung injury after cardiopulmonary bypass: findings of a double- blind randomized study [J]. Surg Today, 2006, 36: 321-326. |
| [4] | Ding LJ, Dong Z, Le LL, et al. Protective effect of sodium sivelestaton cerebral ischemia/reperfusion injury in rats and its mechanism [J]. Chin Pharmacol Bull (中国药理学通报), 2011, 27: 54-58. |
| [5] | Sakashita A, Nishimura Y, Nishiuma T, et al. Neutrophil elastase inhibitor (sivelestat) attenuates subsequent ventilator- induced lung injury in mice [J]. Eur J Pharmacol, 2007, 571: 62-71. |
| [6] | Yoshikawa S, Tsushima K, Koizumi T, et al. Effects of a synthetic protease inhibitor (gabexate mesilate) and a neutrophil elastase inhibitor (sivelestat sodium) on acid-induced lung injury in rats [J]. Eur J Pharmacol, 2010, 641: 220-225. |
| [7] | Hagio T, Matsumoto S, Nakao S. Sivelestat, a specific neutrophil elastase inhibitor, prevented phorbol myristate acetate-induced acute lung injury in conscious rabbits [J]. Pulm Pharmacol Ther, 2005, 18: 285-290. |
| [8] | Matsumoto S, Shingu C, Koga H, et al. The impact of oxidative stress levels on the clinical effectiveness of sivelestat in treating acute lung injury: an electron spin resonance study [J]. J Trauma, 2010, 68: 796-801. |
| [9] | Iwata K, Doi A, Ohji G, et al. Effect of neutrophil elastase inhibitor (sivelestat sodium) in the treatment of acute lung injury (ALI) and acute respiratory distress syndrome (ARDS): a systematic review and meta-analysis [J]. Intern Med, 2010, 49: 2423-2432. |
| [10] | Cao LL, Zheng XY, Du GH et al. Application of sivelestat in the treatment of acute lung injury [J]. Her Med (医药导报), 2004, 23: 207-209. |
| [11] | Aikawa N, Kawasaki Y. Clinical utility of the neutrophil elastase inhibitor sivelestat for the treatment of acute respiratory distress syndrome [J]. Ther Clin Risk Manag, 2014, 10: 621-629. |
| [12] | Kawabata K, Hagio T, Matsuoka S. The role of neutrophil elastase in acute lung injury [J]. Eur J Pharmacol, 2002, 451: 1-10. |
 2015, Vol. 50
2015, Vol. 50


