2. 中国食品药品检定研究院, 北京 100050
2. National Institutes for Food and Drug Control, Beijing 100050, China
对化学药品中的杂质谱分析是当前药品质量控制的热点[1, 2]。药品中诸杂质的种类与含量被总称为杂质谱 (impurity profiles)[1]。理想的控制理念应是针对药品中的每一个杂质,依据其生理活性逐一制定其质控限度[2],这就要求所建立的药品杂质分析方法能够检测出药品中的所有已知杂质。目前,欧洲药典 (EP) 和美国药典 (USP) 已经在其品种各论中列出了与品种相关的主要已知杂质,如USP36版的头孢地尼原料各论中列出了8种特定杂质,并采用相对保留时间对其在HPLC色谱图中的位置进行定位[3]。但在质量源于设计 (QbD) 理念的指导下,不断有新的药物杂质被发现。如在头孢地尼原料中已经发现超过8个降解杂质与工艺杂质 (图 1)[4]。每年有大量的药物新杂质被发现,但由于文献中采用的杂质分析方法通常与药品标准中的色谱分析方法不同,在得不到杂质对照品的情况下,通常无法知道新杂质在药品质控色谱系统中的保留值,即无法判断利用现有的药品质控方法能否实现对新杂质的控制。
定量结构-性质关系 (quantitative structure property relationships,QSPR) 是通过测量或计算有机物的特征参数,建立相关性模型,对有机物的理化性质进行预测的重要方法[5, 6]。QSPR的基本假设是: 结构相似的有机物会表现出相似的性质; 根据结构或从拓扑指数到电子或量子化学性质的各种参数[7, 8, 9, 10] (这些参数通常被称作分子描述符[11]),可以精确构建各类相应的模型,并通过这些模型预测化合物的生物活性或性质。基于QSPR发展的定量结构-色谱保留相关 (quantitative structure - retention relationship,QSRR) 技术,已经用于预测物理化学性质与保留特性、选择分离条件及深入探索色谱保留机制等方面的研究[12, 13, 14,]。当流动相和固定相确定后,相互保留作用的差异主要在于物质分子的结构不同,运用QSRR模型预测化合物的气相色谱保留指数 (gas chromatographic retention indices,GC-RI) 已取得较理想结果[14, 15, 16]。
药品中的杂质 (残留的反应起始物、副产物或降解物),从其化学结构角度通常均与药物自身的结构具有一定的相似性。本文基于QSPR原理,采用化学计算软件,选择特定的分子描述符表征药物杂质的结构,建立特定色谱系统中杂质QSRR模型,用于预测新杂质在该色谱系统中的保留值,为评价药品质控方法的有效性提供了新的思路。
材料与方法 仪器与试剂ADMET Predictor软件V6.5.0010为美国Simulations Plus公司产品。HPLC分析系统: Waters 2695型液相色谱仪、PDA检测器; LC-MS分析系统: 资生堂 NanoSpace S1-2 HPLC、AB公司Q Trap 3200 MS-MS。
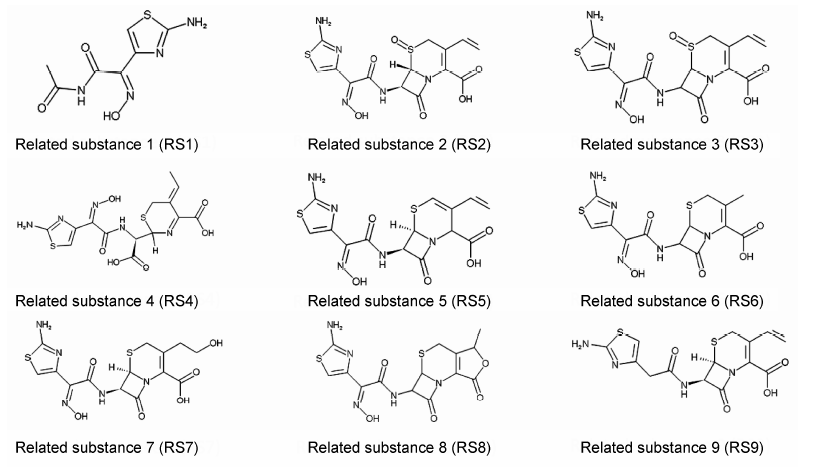
甲醇、乙腈为色谱纯,为Fisher公司产品; 10%四甲基氢氧化铵、磷酸和乙二胺四乙酸二钠为北京化工厂产品。头孢地尼分散片 (批号20120302) 为中国食品药品检定研究院的检验留样。头孢地尼杂质对照品 (杂质A: 噻唑乙酰基甘氨酸肟; 杂质B: 噻唑基乙酰基甘氨酸肟缩醛; 杂质C: 3-甲基头孢地尼; 杂质D: 头孢地尼相关化合物A; 杂质E: 头孢地尼内酯; 杂质F: 头孢地尼异唑类似物; 杂质G: E-头孢地尼; 杂质H: 头孢地尼脱羧开环内酯; 其中杂质D有4种异构体,杂质H有两种异构体) 由中国食品药品 检定研究院提供,其他诸杂质如图 1所示。
|
Figure 1 The structure of cefdinir related substances |
构建QSRR模型 建立QSRR关系的首要步骤就是对化合物的分子结构进行有效的数值表征。将诸杂质结构导入ADMET工作站,计算表征分子结构的分子描述符。目前常用的分子描述符包括原子电子拓扑结构函数 (E-state)、亲和亲电福井函数 (Fukui) 和巴拉班指数 (Balaban distance connectivity index) 等多个体系。ADMET软件通过不同的计算体系可以得到超过300个表征分子结构的分子描述符,在构建QSRR模型前,需要对这些分子描述符进行筛选,包括: ① 剔除非数性无效数据。分子描述符的计算以分子结构为基础,采用通用无监督计算过程,因此在计算过程中算法对某些特定的分子结构可能出现无法计算或不适用计算的情况,产生无效数据; 另外,部分分子描述符属于性质或聚类型参数,不适用直接用于QSRR建模计算。② 剔除无变异信息。由不同分子结构中的相似结构产生的分子描述符数值相近,这些分子描述符在建模过程中几乎没有贡献,为简化建模的复杂程度,这些分子描述符也应予以剔除。③ 合并高度相关的分子描述符。由不同计算体系得到的分子描述符可能表述相同的结构信息,同一计算体系产生的不同分子描述符也可能出现高度一致或直接相关的情况,这些分子描述符在建模前应进行合并。
对ADMET工作站产生的分子描述符以上述筛选原则为判断依据,进行无监督筛选至80个左右,采用人工神经网络算法进行50次重复建模。人工神经网络算法具有随机性选择变量的特性,通过对诸模型中各分子描述符与模型的相关性分析,选出约30个与模型最相关的分子描述符,再采用多元线性回归法 (MLR) 建模; 建模过程中再逐步淘汰不相关的变量 (分子描述符),建立最终的QSRR模型。
HPLC分析方法[3]按USP36版头孢地尼有关物质项下方法实验。采用色谱柱: Diamonsil C18 (4.6 mm × 150 mm,5 μm) 色谱柱; 以0.1% 四甲基氢氧化铵溶液1 L中加入0.1 mol·L-1乙二胺四乙酸二钠溶液0.4 mL为流动相A,以0.1% 四甲基氢氧化铵溶液 (用磷酸调节至pH 5.5)-乙腈-甲醇(500∶300∶200) 1 L中加入0.1 mol·L-1乙二胺四乙酸二钠溶液0.4 mL为流动相B,梯度洗脱 (起始比例A为97.5%-B为2.5%、25 min A为87.5%-B为12.5%、37 min A为75%-B为25%、43 min始恢复为起始比例至58 min); 流速为1.0 mL·min-1; 柱温为40 ℃; UV检测波长为254 nm; 进样体积为10 μL。
LC-MS分析方法[4]采用柱切换的方法,将色谱系统1用于对头孢地尼中的杂质进行分离,诸杂质经六通阀逐一被切换至色谱系统2,经脱盐、洗脱后进行MS分析。色谱系统1为USP36版HPLC方法,进样体积为50 µL。色谱系统2采用Diamonsil C18 (4.6 mm × 150 mm,5 μm) 色谱柱; 流动相C为含有0.5% 甲酸的水溶液,流动相D为乙腈-0.5% 甲酸溶液 (90∶10); 梯度洗脱 [起始至5.6 min (C为100%- D为0%) 用于对目标杂质的脱盐处理、20 min至60 min (C为0%-D为100%) 用于经脱盐的目标杂质洗脱至MS系统]。切换用定量环体积为500 µL。MS分析条件: 扫描模式: 增强全扫描 (+EMS) 和增强离子扫描 (+EPI),一级质谱 (+Q1) 和二级质谱 (+MS2); 扫描范围: 10~500 m/z; 气帘气 (curtain gas); 20 L·h-1; 喷雾电压 (IS): +4.5 kV; 温度 (TEM): 500.00 ℃; 雾化气 (GS1): 60 L·h-1; 辅助气 (GS2): 65 L·h-1; 碰撞气 (CAD): Medium; 去簇电压 (DP): +37.5 V; 入口电压 (EP): +6.0 V; 碰撞室入口电压 (CEP): +19.0 V; 碰撞电压 (CE): +15.0 V; 碰撞室出口电压 (CXP): +3.0 V。
结果与讨论 1 建立头孢地尼QSRR模型
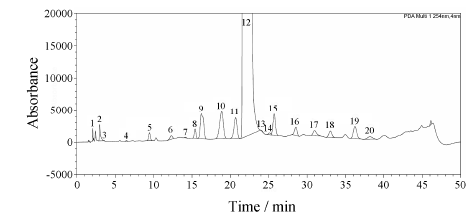
采用HPLC法分析头孢地尼杂质,经杂质对照品和LC-MS确认,其典型的色谱图如图 2所示。选择头孢地尼与美国药典36版 (USP36版) 收录杂质A、B、C、E、F、G、H为模型训练集,以对头孢地尼的相对保留时间 (RRT) 作为溶质保留值参数,采用lgRRT与相应的分子描述符 (表 1) 建立多元线性回归模型。
筛选过程依次为: ① 非数性描述符剔除 (non- numberic inputs); ② 低方差描述符剔除 (identical and low variance inputs); ③ 无代表性描述符剔除 (underrepresented inputs); ④ 对筛选后诸描述符与建模训练集数据进行相关性分析,筛选高敏感、高相关性描述符 (highly correlated inputs); ⑤ 区间线性灵敏度分析 (sensitivity by truncated linear analysis)。通过筛选的分子描述符以模型训练集为依据建立多元线性回归模型,并进行验证和误差分析。
|
Figure 2 The typical chromatogram of cefdinir related substances. 1: Impurity A; 2: Impurity B; 3: RS1; 4: RS2; 5: RS3; 6: RS4; 7: RS5; 8: Impurity C; 9: RS6 and RS7; 10/11/13: Impurity D; 12: Cefdinir; 14: RS8; 15: Impurity E; 16: Impurity G; 17: RS9; 18: Impurity F; 19/20: Impurity H |
|
|
Table 1 The molecular descriptors and results of cefdinir related substances. F_AFRBWF: Average value of the freely rotatable bond weight factor; Blbn_J: Balaban distance connectivity index J of the hydrogen-suppressed molecular graph; SsCH3: Atom-type E-state index for -CH3 groups; SssCH2: Atom-type E-state index for -CH2- groups; SsNH2: Atom-type E-state index for -NH2 groups; SssNH: Atom-type E-state index for -NH- groups; SssS: Atom-type E-state index for -S- groups; SHdCH2: Atom-type hydrogen E-state index for =CH2 groups; EEM_AFc: Sum of absolute values of sigma Fukui indices on C; EEM_Afpl: Sum of absolute values of sigma Fukui indiceson polar atoms; EEM_XFpl: Maximum sigma Fukui index on polar atoms; Pi_MaxQ: Maximum Hückel pi atomic charge |
最终的QSRR模型包括F_AFRBWF、Blbn_J、SsCH3、SssCH2、SsNH2、SssNH、SssS、SHdCH2、EEM_AFc、EEM_AFpl、EEM_XFpl和Pi_MaxQ 12个分子描述符 (表 1): lgRRT = 0.442 964 × F_AFRBWF - 0.347 1 × Blbn_J + 0.004 033 × SsCH3 - 0.144 05 × SssCH2 - 0.023 14 × SsNH2 + 0.064 803 × SssNH + 0.188 527 × SssS - 0.044 77 × SHdCH2 + 0.055 475 × EEM_AFc - 0.059 72 × EEM_AFpl + 0.491 649 × EEM_XFpl + 5.322 131 × Pi_MaxQ - 2.823 21。比较诸溶质实测RRT与预测结果的相关性,以实测相对保留时间RRT为横坐标 (x),预测结果lgRRT为纵坐标 (y),对数回归方程为y = 0.448 1 ln(x) + 0.003 9,对应R2 = 0.983 6,即构建的QSRR模型可准确预测头孢地尼杂质的色谱保留行为。
2 对头孢地尼QSRR模型的验证计算头孢地尼有关物质1~9所对应的QSRR模型参量分子描述符,带入QSRR模型预测各杂质的RRT,并与实测值进行比较,验证模型的预测能力。头孢地尼有关物质1~9中的实测相对保留时间与预
测的相对保留时间的最大差异值为0.103 (表 2); 提示所建立的QSRR模型对未参与建模杂质的保留行为具有较好的预测性。
|
|
Table 2 The comparison between true values and predictions of cefdinir in QSRR |
在美国药典36版 (USP36版) 收录的头孢地尼有关物质中,杂质D为4个非对映异构体的总称,4个异构体彼此间的色谱行为具有较大差异。采用头孢地尼杂质D作为验证集样本,评价模型对非对映异构体的预测情况。QSRR模型预测的USP杂质D的RRT为1.172; 在USP36版的色谱系统中,归属于USP杂质D的3个有关物质峰的实测相对保留时间分别为0.865、0.962和1.100; 与预测值的差值 (ΔRRT) 分别为0.307、0.210和0.072。
目前鲜有利用分子描述符建立色谱保留行为预测的报告,缺乏对这类算法模型最大允许误差值的权威依据。根据本类模型建立与应用的特征,对于模型训练集数据,模型预测各物质间的相对保留时间RRT的顺序应与实测数据一致,即能够准确预测各物质在相应色谱系统中的出峰顺序,对于模型的验证数据除保证各物质间RRT的大小关系一致外,应对预测RRT与实测RRT的差值ΔRRT进行评价,当验证集样本ΔRRT的差值不大于模型训练集样本ΔRRT的最大值时,认为模型具有良好的预测能力。
汇总建模中的全部数据,可见头孢地尼QSRR模型对一般杂质具有较好的预测能力,但对仅分子空间构型不同的非对映异构体杂质的预测误差可能较大。由于在建立QSRR模型中选择分子描述符的过程采用无监督的敏感度筛选运算,相较于差异较大的平面结构,空间差异所引起分子描述符值的变化具有更小的权重,在建模中易被系统淘汰。这也就导致了上述QSRR模型对于空间结构差异的不敏感。
3 头孢地尼QSRR模型的应用QSRR模型的一个重要作用在于当药品中有新的杂质被确认时,可以预测该杂质在色谱系统中的保留值,进而评价目前的色谱系统是否可以对新杂质进行控制。头孢地尼通常以7-AVCA (C9H10N2O3S) 与头孢地尼活性酯 (C14H10N4O3S3) 为起始原料,经缩合产生中间体 (C16H15N5O6S2),再经水解后获得头孢地尼粗品[17]。利用上述头孢地尼有关物质QSRR模型,预测USP色谱方法是否可以控制头孢地尼合成过程中残留的起始原料和中间体。
利用ADMET软件,计算QSRR模型预测需要的7-AVCA、头孢地尼活性酯 (cefdinir AE) 和中间体 (intermediate) 的分子描述符,利用模型计算它们在USP36头孢地尼有关物质分析方法中的RRT值,其分别为0.296,0.790和1.605。采用USP36版方法 测定7 -AVCA、头孢地尼活性酯与中间体,7-AVCA实测保留时间为8.076 min,RRT为0.361,与预测结 果的差值 (ΔRRT) 为0.065; 活性酯实测保留时间为13.616 min,RRT为间0.634,ΔRRT为0.156; 中间体实测保留时间为31.881 min,RRT为1.483,ΔRRT为0.122。ΔRRT值均小于建模样本的最大误差,说明头孢地尼有关物质QSRR模型可用于预测头孢地尼合成工艺中的起始原料及中间体的保留值。USP36版收载的方法可以控制头孢地尼合成工艺中残留的反应起始物和中间体,即在无法获得相应杂质对照品时,可通过物质的结构信息,预测其在特定色谱系统中的保留值,进而对色谱系统的有效性和通用性进行科学评价。
头孢地尼杂质U是在酸性降解条件下产生的特定新杂质,根据质谱分析结果,推测出了杂质U的可能结构 (图 3),利用QSRR模型预测其在USP36头

|
Figure 3 The MS results of cefdinir impurity U and fragmentation pathways |
孢地尼有关物质色谱系统中的RRT为2.234。采用USP36版方法测定杂质U的实测相对保留时间为46.199 min,对应的RRT为2.118,与预测结果的差值 (ΔRRT) 为0.116,小于建模样本的最大误差。
结论QSRR模型以分子描述符为依据,构建物质结构与色谱行为的关系模型,用于特定色谱条件下物质保留值的预测。本研究建立头孢地尼有关物质的QSRR模型,可以预测头孢地尼杂质在USP36版色谱条件下的保留值,虽然对仅空间结构存在差异的差向异构体的预测准确性略差,但当药品中有新的杂质被确认时,通过对该杂质在色谱系统中保留值的预测,可以评价目前的色谱系统是否可以对该杂质实现有效控制。应用该模型,对头孢地尼合成过程中的起始原料7-AVCA、头孢地尼活性酯、中间体和新酸降解杂质U的色谱保留值进行了预测,预测值与实测数据基本一致,结果也提示,目前USP36头孢地尼有关物质分析方法可以检测到上述杂质。
| [1] | Görög S. The importance and the challenges of impurityprofiling in modern pharmaceutical analysis [J]. Trends AnalChem, 2006, 25: 755-757. |
| [2] | Hu CQ. Current situation and the trend in impurity control ofchemical drugs [J]. Sci Sin Chim (中国科学: 化学), 2010,40: 679-687. |
| [3] | US Pharmacopeia Convention. The United States Pharmacopoeia[S]. 36th ed. Rockville, MD, 2013. |
| [4] | Li J, Wang LX, Yao SC, et al. Characterization of impuritiesin cefdinir bulk material by online column-switching liquidchromatography and tandem mass spectrometry [J]. CurrPharm Anal, 2013, 9: 145-158 |
| [5] | Katritzky AR, Kuanar M, Slavov S, et al. Quantitativecorrelation of physical and chemical properties with chemicalstructre: utility for prediction [J]. Chem Rev, 2010, 110:5714-5789. |
| [6] | Huuskonen J, Rantanen J, Livingstone D. Prediction ofaqueous solubility for a diverse set of organic compoundsbased on atom-type electrotopological state indices [J]. Eur JMed Chem, 2000, 35: 1081 -1088. |
| [7] | Faulon JL, Bender A. Handbook of Chemoinformatics Algorithms[M]. London: Chapman & Hall/CRC Press, Taylor &Francis Group, 2010. |
| [8] | Godavarthy SS, Robinsin RL Jr. Improved structure-propertyrelationship models for prediction of critical properties [J].Fluid Phase Equilibria, 2008, 264: 122 -136. |
| [9] | Kier LB, Hall LH. Molecular Structure Description: theElectrotopological State [M]. New York: Academic Press,1999: 67. |
| [10] | Balaban AT. Highly discriminating distance-based topologicalindex [J]. Chem Phys Lett, 1982, 89: 399 -404. |
| [11] | Todeschini R, Consonni V. Handbook of Molecular Descriptors[M]. Weinheim (Germany): Wiley-Vch, 2002: XI-XIV. |
| [12] | Kang JJ, Cao CZ, Li Z, et al. Quantitative structure-retentionrelation (QSRR) studies for predicting the gas chromatographyretention indices of polycyclic hydrocarbons (PAH): quasilengthof carbon chain and pseudo-conjugated surface [J]. J ChromtogrA, 1998, 799: 361-367. |
| [13] | Yang GS, Yuan SL, Lin XJ, et al. The study of chiraldiscrimination of organophosphonate derivatives on pirkle typechiral station-ary phase by molecular modeling [J]. Talanta,2004, 64: 320-325. |
| [14] | Liu FP, Liang YZ, Cao C, et al. QSPR study of GC retentionindices for saturated esters on seven stationary phases basedon novel topological indices [J]. Talanta, 2007, 72: 1307 -1315. |
| [15] | Wang Y, Liu SS, Zhao JS, et al. Prediction of gas chromatographicretention indices of organophosphates by electrotopologicalstate index [J]. Acta Chim Sin (化学学报), 2006,64: 1043-1050. |
| [16] | Tong JB, Zhang SW. Molecular electronegativity-distancevector for quantitative structure-retention relationship oforganophosphates [J]. J Mol Sci (分子科学学报), 2007, 23:271-275. |
| [17] | Li Jin, Wang LX, Zhang DS, et al. Comparison of analyticalmethods for cefdinir related substances [J]. Chin J Antibiot(中国抗生素杂志), 2012, 37: 610-614. |
 2015, Vol. 50
2015, Vol. 50


