2. 海南省食品药品检验所, 海南 海口 570100
2. Hainan Provincial Institute for Drug and Food Control, Haikou 570100, China
尼麦角林 (10α-甲氧基-1, 6-二甲基麦角林-8β-甲醇基-5-溴-3-吡啶羧酸酯, 图 1), 是20世纪60年代 开发的血管活性药, 可用于治疗阿尔茨海默病、血管痴呆、脑动脉硬化、脑中风、短暂性脑缺血、外周血管病等疾病[1, 2, 3, 4]。近期研究发现其还具有促进角膜上皮伤口愈合[5]和抗氧化[6]的作用, 不良反应小且多为短暂性[7]。因此尼麦角林在临床虽已使用40多年, 仍然具有良好的临床价值。最新的欧洲药典、英国药典和日本药局方均收载了该品种, 药典方法及文献[8, 9, 10, 11]报道均采用高效液相色谱法对尼麦角林进行有关物质检查。但未见尼麦角林有关物质的系统鉴定研究报道, 也未见针对不同厂家原料和制剂有关物质的比较分析报道。本文研究建立了适用于尼麦角林及其制剂中有关物质检查的高效液相色谱−质谱联用分析方法, 检出了尼麦角林中16个主要的有关物质, 并结合对照品比对、二级质谱裂解解析、合成工艺分析 [12, 13, 14, 15], 鉴定了它们的结构, 可为尼麦角林生产工艺控制和质量保障提供参考依据。
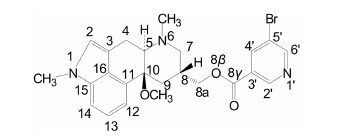 | Figure 1 Chemical structure of nicergoline |
1290 Infinity液相色谱-6224飞行时间质谱仪 (美国安捷伦科技公司); TSQ Quantum Ultra AM型LC-MS/MS联用仪 (美国热电公司); BS210电子天平 (德国赛多利斯)。
试药与试剂
尼麦角林 (美国Pfizer公司、捷克IVAX公司), 杂质A、B、C、D、F、G和H对照品 (欧洲药典8.0), 尼麦角林片 (齐都天迈/Qidu, 1303003, 10 mg/片, 山东齐都药业有限公司; 思尔明/Pfizer 1200103, 10 mg/片, 美国Pfizer公司), 尼麦角林胶囊 (庆普/Qingpu 130401, 30 mg/粒, 重庆福安药业集团庆余堂制药有限公司)。
色谱条件
采用Phenomenex Gemini-NX C18 (4.6 mm × 250 mm, 5 μm) 色谱柱, 以0.2% 乙酸铵 缓冲液 (取乙酸铵2.0 g, 加水900 mL溶解后, 用氨水调节至pH 7.0, 加水稀释至1 L)−甲醇−乙腈 (45∶25∶30) 为流动相等度洗脱, 流速1 mL·min−1, 柱温35 ℃, 检测波长为288 nm, 进样20 μL。
TOF/MS测定条件
电喷雾正离子化, 喷雾电压3.5 kV, 雾化气压力240 kPa, 流量8 L·min−1, 温度350 ℃, 碎片电压175 V, 参比离子m/z 121.050 873 (质子化嘌呤, C5H5N4+) 和m/z 922.009 798 (质子化氟代膦嗪HP-921, C18H19O6N3P3F24+), 质量数扫描范围 m/z 100~1 500。
MS/MS测定条件
三重四极质谱电喷雾正离子化, 喷雾电压5 kV, 雾化气压力240 kPa, 辅助气压力70 kPa, 毛细管温度350 ℃, CID氩气0.2 Pa, 碰撞能量20~35 eV。
供试品溶液
取尼麦角林或尼麦角林片/胶囊 细粉适量 (约相当于尼麦角林10 mg), 精密称定, 置 10 mL量瓶中, 加流动相溶解并稀释至刻度, 摇匀, 滤过, 取续滤液即得; 精密量取上述各溶液适量, 加流动相定量稀释, 分别制成1% 和0.1% 的自身对照溶液。
对照品溶液
取已知杂质对照品 (杂质A~D、F~H) 各适量, 分别精密称定, 加流动相溶解并定量稀释成约含10 μg·mL−1的溶液作为杂质对照溶液。
强制降解实验溶液
取尼麦角林约10 mg, 经 1 mL 0.1 mol·L−1盐酸溶液60 ℃水浴30 min、1 mL 1 mol·L−1氢氧化钠溶液60 ℃水浴30 min、或1 mL 5% 过氧化氢溶液25 ℃水浴10 min, 分别处理, 放冷 (酸碱处理溶液先中和) 后, 加流动相溶解并稀释至10 mL, 制成约含1 mg·mL−1的强制降解实验溶液。同时进行空白溶剂实验。
结果1 有关物质检查
建立了尼麦角林有关物质检查的挥发性流动相HPLC分析法, 并适用于有关物质的联用质谱鉴定。该色谱条件下尼麦角林原料药、制剂以及强制降解实验供试溶液中的各有关物质均分离良好。
采用该方法对尼麦角林的2批原料药 (图 2a, b) 与3批制剂 (图 2c~e) 进行有关物质分析, 结果表明 (表 1) 它们含有16个主要有关物质 (按保留时间顺次编号为1~16)。强制降解实验结果 (图 3) 表明, 本品在强碱条件下 (图 3c) 主要降解为有关物质1和2; 在氧化条件下 (图 3d) 主要降解为有关物质5和8; 而在强酸条件下 (图 3b) 主要降解为有关物质7和9。
 | Figure 2 HPLC-UV chromatograms of the related substances in nicergoline API (active pharmaceutical ingredient) and preparations.a: Pfizer API; b: IVAX API; c: Pfizer tablets; d: Qidu tablets; e: Qingpu capsules |
 | Figure 3HPLC-UV chromatograms of the degradation impurities in nicergoline from stress tests. a: Normal; b: Acid; c: Base; d: Oxidation |
|
|
Table 1 Quantitative data of the related substances found in nicergoline API and preparation. A, B, C, D, F, G and H were compared with the reference substance |
HPLC-ESI+-TOF/MS测得各有关物质母离子的准确质量与离子组成, 三重四极质谱获取二级质谱碎片信息, 通过与已知有关物质对照品对照和质谱解析, 鉴定各有关物质结构。结果见表 2。
|
|
Table 2 Related substances identified in nicergoline by HPLC-TOF/MS and MS/MS |
2.1 已知有关物质的确证
通过有关物质对照品对照 (保留时间) 及质谱定性, 确证有关物质1、2、6、10、11、14和15分别与已知有关物质D、C、B、H、A、F和G对应。对尼麦角林以及各已知有关物质的二级质谱碎片进行裂解途径和规律分析, 可以辅助未知杂质结构的推断与鉴定。尼麦角林二级质谱裂解规律 (图 4) 总结如下: ① 在母离子P+ 中, 10位甲氧基/羟基极易脱去, 生成质量数为 [P-32]+/[P-18]+ 的碎片离子峰, 可据此推测10位的基团; ② 尼麦角林5-卤代烟酸基团较稳定, 易与吲哚并喹啉基团脱离, 因而尼麦角林及其已知杂质的主要碎片离子来自于吲哚并喹啉基团; ③ 吲哚并喹啉基团较易脱去CH2=CH2、CH3CH3、CH3NH2、CH2=C=CH2、CH3N=CH2等中性小分子, 生成质量数分别为 [P-28]+、[P-30]+、[P-31]+、[P-43]+、[P-40]+ 的碎片离子峰; 偶尔会脱去CH4产生质量数为 [P-16]+ 的碎片离子峰或失去一个甲基自由基, 产生质量数为 [P-15]+ 的奇电子碎片离子峰; ④ 质谱中常会产生220/221/222、194/196、181/182/183/184、167/168等多组与尼麦角林结构相关的碎片离子峰簇, 可用于结构推断准确性的验证。
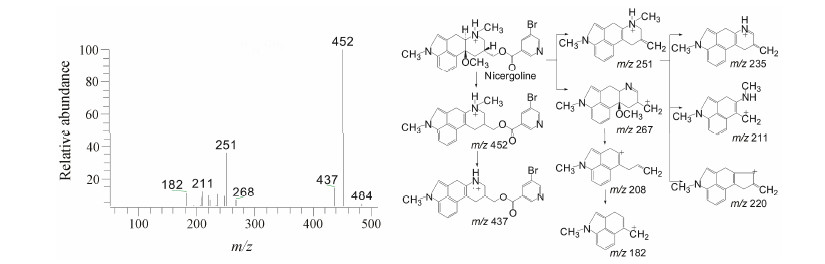 | Figure 4 MS/MS spectra of nicergoline [M+H]+ (m/z 484) ion and its fragmentation pathways |
2.2 未知有关物质的鉴定
根据质谱信息, 结合合成工艺[12, 13, 14, 15]以及裂解规律, 对各有关物质进行综合分析, 鉴定其结构。
有关物质3和4: TOF/MS测得有关物质3 [M+H]+ 的准确质量为315.206 2, 与离子式C19H27N2O2+相应, 保留时间为5.7 min; 有关物质4[M+H]+的准确质量为343.201 9, 与离子式C20H27N2O3+ 相应, 保留时间为6.3 min。两者的分子量均较尼麦角林小, 均无典型[M+H+2]+同位素峰, 提示两者均不含有5-卤代烟酸结构。主要碎片离子 (m/z 251、211、196等) 均与尼麦角林一致, 都含有 [P-32]+ 碎片离子 (分别为m/z 311、283), 提示两者均含有吲哚并喹啉结构。结合合成工艺, 推定有关物质3为甲基化反应的副产物, 而有关物质4为溴烟酸酯化步骤的反应副产物。
有关物质5、8和12: TOF/MS测得有关物质5 [M+H]+的准确质量为500.118 9, 保留时间为8.4 min; 有关物质8 [M+H]+ 的准确质量为500.117 0, 保留时间为12.5 min。有关物质5和8的 [M+H]+ 与 [M+H+2]+ 丰度比均为1∶1, 均与离子式C24H27BrN3O4+对应并比尼麦角林多一个O原子; 强制降解实验结果表明, 有关物质5和8在氧化破坏条件下含量均明显增加。对尼麦角林的结构进行分析, 结合化学反应规律, 其氧化反应易发生在化学活性较高的吲哚基团2位 (吲哚的亲电取代反应多发生在3位与2位, 3位没 有氢原子, 故发生在2位[16]) 或者生成氮氧化物。根据MS/MS主要碎片离子信息以及相应结构的极性 (与色谱保留大小相关), 推测有关物质5为尼麦角林吲哚基团2位羟基化的产物 (图 5), 而有关物质8 则为尼麦角林喹啉基团6位脂肪氨基的氮氧化物。TOF/MS测得有关物质12 [M+H]+的准确质量为514.132 2, [M+H]+与[M+H+2]+丰度比为1∶1, 与离子式C25H29BrN3O4+对应, 较尼麦角林大30 (元素组成与CH3O取代对应), 保留时间为22.4 min; MS/MS
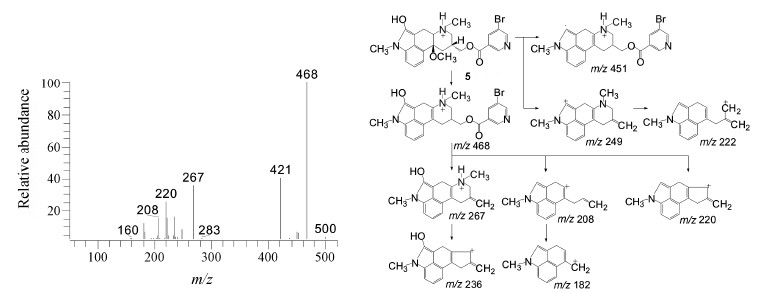 | Figure 5 MS/MS spectrum of related substance 5 [M+H]+ (m/z 500) ion and its fragmentation pathways |
主要碎片离子均比尼麦角林多30, 进一步证明CH3O取代。根据裂解规律, 结合合成工艺, 鉴定有关物质12为吲哚基团2位甲氧基化的副产物 (图 6)。
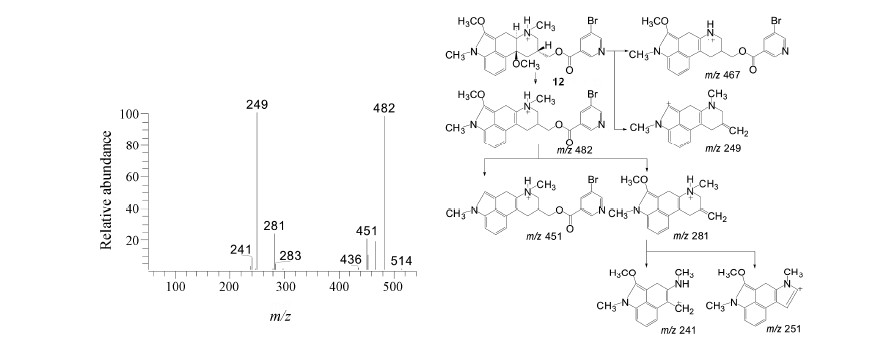 | Figure 6 MS/MS spectrum of related substance 12 [M+H]+ (m/z 514) ion and its fragmentation pathways |
有关物质13和16: TOF/MS测得有关物质13 [M+ H]+的准确质量为498.138 5, [M+H]+与[M+H+2]+丰度比为1∶1, 与离子式C25H29BrN3O3+ 对应, 比尼麦角林多1个甲基取代; 有关物质16[M+H]+的准确质量为518.085 3, 同位素峰 [M+H]+、[M+H+2]+和[M+H+4]+的丰度比约为77∶100∶24, 与离子式C24H26BrClN3O3+对应, 比尼麦角林多1个Cl取代; 两者的反向色谱保留均比尼麦角林大而极性降低, 主要碎片离子 (m/z 251、235、220、211和208) 均与尼麦角林的一致, 表明两者均含有吲哚并喹啉母核结构, 而取代均发生在尼麦角林的取代基单元上。有关物质13有m/z 452 [P-46]+ 的特征碎片离子, 根据裂解规律和合成工艺, 推测其为乙氧基取代尼麦角林的甲氧基而产生的副产物; 有关物质16的氯原子取代应在5-卤代烟酸基团上, 根据有机化学反应规律, 推断氯原子取代在6'位, 是由起始原料5-溴-3-吡啶羧酸中的杂质参与反应而产生的副产物。
有关物质7和9: TOF/MS测得酸降解杂质7和9 [M+H]+的准确质量均为470.108 3, [M+H]+与[M+H+ 2]+丰度比均为1∶1, 与离子式C23H25BrN3O3+ 对应, 两者的分子量均比尼麦角林小14, 元素组成少CH2。保留时间分别为9.9和12.5 min。两者的部分碎片离子 (m/z 251、235、221/220、211、208、196/194和182) 与尼麦角林一致, 提示两者均含有吲哚并喹啉结构; 两者均含有m/z 452 [P-18]+ 特征碎片离子, 推测结构中均含有游离羟基。有关物质9含量增加较明显, 根据化学反应规律, 推测其为10位甲氧基醚水解的产物, 而有关物质7则由10位甲氧基消除后与H2O加成而成, 根据碎片离子 (主要依据m/z 325和144) 判定羟基加成发生在5位。
讨论据药典和文献 [8, 9, 10, 11]报道, 本品有关物质检查通常采用非挥发性缓冲盐作为流动相, 不适用于电喷雾离子化的质谱分析。本文研究建立的挥发性流动相液−质联用方法, 尼麦角林与检测出的16个主要有关物质均可有效分离。缓冲溶液pH为影响分离的关键因素, pH增大, 保留增强, 有利于改善分离, 经优化选择缓冲溶液pH 为7.0。通过调整有机相的组成和比例可获得理想的保留和分离, 兼顾分离和电喷雾离子化的效率, 优化确定了流动相比例为乙酸铵缓冲液−甲醇−乙腈 (45∶25∶30) 等度洗脱, 色谱分离良好。
检出并鉴定了尼麦角林及其制剂中的16个主要有关物质, 其中7个 (有关物质1、2、6、10、11、14和15) 为已知杂质。其余9个未知杂质均具有吲哚并喹啉结构。根据杂质来源可将其分为2类, 即工艺杂质 (反应副产物) 和降解杂质。有关物质3、6和12为甲基化反应步骤的副产物, 有关物质4为酯化反应步骤的副产物, 有关物质10、11和16为起始原料所引入杂质参与反应的副产物, 有关物质13为重结晶过程的副产物 (与选取的重结晶溶剂相关), 有关物质14为尼麦角林的非对映异构体杂质, 而有关物质15则为甲醇取代反应步骤的副产物。有关物质1和2是尼麦角林酯键水解的两个降解产物; 有关物质5和8在氧化条件下含量增加明显, 尤其是有关物质5, 其在制剂中含量较高, 为制剂工艺过程及贮藏过程中的氧化杂质; 有关物质7和9为酸降解产物。
| [1] | Winblad B, Fioravanti M, Dolezal T, et al. Therapeutic use of nicergoline [J]. Clin Drug Invest, 2008, 28: 533-552. |
| [2] | Saletu B, Garg A, Shoeb A. Safety of nicergoline as an agent for management of cognitive function disorders [J]. BioMed Res Int, 2014, http://dx.doi.org/10.1155/2014/610103. |
| [3] | Caraci F, Chisari M, Frasca G, et al. Nicergoline, a drug used for age-dependent cognitive impairment, protects cultured neurons against h-amyloid toxicity [J]. Brain Res, 2005, 1047: 30-37. |
| [4] | Mizuno T, Kuno R, Nittab A, et al. Protective effects of nicergoline against neuronal cell death induced by activated microglia and astrocytes [J]. Brain Res, 2005, 1066: 78-85. |
| [5] | Kim SY, Choi JS, Joo1 CK. Effects of nicergoline on corneal epithelial wound healing in rat eyes [J]. Invest Ophthal Visual Sci, 2009, 50: 621-625. |
| [6] | Vairetti M, Battaglia A, Carfagna N, et al. Antioxidant properties of MDL and MMDL, two nicergoline metabolites, during chronic administration of haloperidol [J]. Eur J Pharmacol, 2002, 453: 69-73. |
| [7] | Fioravanti M, Nakashima T, Xu J, et al. A systematic review and meta-analysis assessing adverse event profile and tolerability of nicergoline [J]. BMJ Open, 2014, 4: e005090, doi:10.1136/bmjopen-2014-005090. |
| [8] | Yalcın G, Yuktas FN. An efficient separation and method development for the quantifying of two basic impurities of nicergoline by reversed-phase high performance liquid chromatography using ion-pairing counter ions [J]. J Pharm Biomed Anal, 2006, 42: 434-440. |
| [9] | Ahmad AK, Kawy MA, Nebsen M. First derivative ratio spectrophotometric, HPTLC-densitometric, and HPLC determination of nicergoline in presence of its hydrolysis-induced degradation product [J]. J Pharm Biomed Anal, 2002, 30: 479-489. |
| [10] | Banno K, Horimoto S. Separation and quantitation of nicergoline and related substances by high-performance liquid chromatography/atmospheric pressure ionization mass spectrometry [J]. Chromatographia, 1991, 31: 50-54. |
| [11] | Qiu LY, Zhang D. Determination of the contents and related substances in nicergoline for injection by HPLC [J]. West China J Pharm Sci (华西药学杂志), 2006, 21: 572-574. |
| [12] | Liu CL, Fan XS, Wang FL, et al. Method for preparing nicergoline: CN 103159756 [P]. 2011-12-11. |
| [13] | Guan D, Zhou AX, Chen XM, et al. Method for preparation of nicergoline: CN 102718761 [P]. 2012-05-29. |
| [14] | Liu XL, Mu ZY, Liao XH, et al. Method for producing nicergoline: CN 101781296 [P]. 2010-02-10. |
| [15] | Giovanni I, Daniele L. Process for the 1-methylation of lysergol derivatives, and its use in the preparation of nicergoline: CH 671398 [P]. 1986-07-31. |
| [16] | Eicher T, Hauptmann S. The chemistry of Heterocycles Structures, Reactions, Synthesis and Applications (杂环化学-结构、反应、合成与应用) [M]. 2nd ed. Beijing: Chemical Industry Press, 2005: 82-83. |
 2015, Vol. 50
2015, Vol. 50