2. 南京中医药大学 江苏省方剂高技术研究重点实验室, 江苏 南京 210023;
3. 江苏大学药学院, 江苏 镇江 212013
2. Jiangsu Key Laboratory for High Technology Research of TCM Formulae, Nanjing University of Chinese Medicine, Nanjing 210023, China;
3. School of Pharmacy, Jiangsu University, Zhenjiang 212013, China
糖尿病是一种胰岛素缺乏或胰岛素生物功能缺失而引起的糖、脂肪和蛋白质代谢紊乱的代谢性疾 病,可引起多种严重的并发症[1]。作为一种“综合征”,糖尿病很难用单一的评价指标来反映其复杂的发病机制。代谢组学是通过组群指标分析生物体整体或组织细胞系统代谢动态变化,通过对血清或血浆、尿液等生物体终端代谢物的整体动态变化进行分析,从而反映生物体体内的生物学变化过程[2, 3, 4, 5, 6]。
桑叶为桑科 (Moraceae) 桑属植物桑 (Morus alba L.) 的干燥叶,其性寒、味甘苦,具有疏散风热、清肺润燥、清肝明目的功效,是临床常用中药之一。自古就有治疗消渴症的记载,并且大量研究表明,桑叶中主要的生物活性成分为生物碱类、黄酮类、多糖类成分[7, 8, 9],药理活性评价表明,其具有显著调节血糖及防治糖尿病并发症的作用[10,11]。本研究以糖尿 病模型小鼠为研究对象,应用代谢组学方法对模型小鼠血浆代谢物的整体变化进行研究,分析鉴定其血浆中潜在的生物标志物,在此基础上研究桑叶生物碱类、黄酮类、多糖类提取物干预后的代谢扰动规律及代谢表型的变化,从而探讨其干预糖尿病的生物学机制。
材料与方法 实验动物SPF级ICR小鼠36只,均为雄性,体重20~30 g,购自南京市江宁区青龙山动物繁殖场,合格证号SCXK (苏) 2012-0004。小鼠分笼饲养,置于温度 (25 ± 2) ℃、湿度50%~60% 的饲养室。每日光照8 h。饮水为高温灭菌水,饲料为常规饲料。动物均自由饮水、进食。
桑叶生物碱类、多糖类、黄酮类提取物实验室自制。戴安Ultimate 3000超高效液相色谱仪,双压线性离子阱串联高分辨质谱Orbitrap Velos Pro (Thermo公司)。乙腈 (色谱纯,Tedia公司); 甲酸(色谱纯,Merck公司); 甲醇 (色谱纯,江苏汉邦科技有限公司)。
桑叶样品制备与分析方法桑叶生物碱类、黄酮类、多糖类提取物的制备方法参照文献[12]进行。生物碱类成分采用UPLC-TQ/MS/MS方法测定含量; 多糖提取物采用硫酸-苯酚法测定总糖含量; 黄酮类成分采用HPLC方法进行分析。
生物碱类成分的分析条件色谱条件: 色谱柱为Acquity UPLC BEH Amide (100 mm × 2.1 mm,1.7 μm); 流动相: A为含5 mmol·L-1甲酸铵、乙酸铵和0.2% 甲酸的水溶液; B为含1 mmol·L-1甲酸铵、乙酸铵和0.2% 甲酸的乙腈溶液。梯度洗脱 (0~3 min,10% A; 3~9 min,10%~18% A; 9~15 min,18%~20% A,15~16 min,20%~46% A,16~18 min,46% A)。流速: 0.4 mL·min-1,柱温: 35 ℃,进样量: 1 μL。质谱条件: 离子化模式: ESI+; 检测方式: 多反应检测 (MRM); 毛细管电压: 3.0 kV; 离子源温度: 150 ℃; 脱溶剂气温度: 550 ℃; 脱溶剂气流量: 1 000 L·h-1; 锥孔气流量: 50 L·h-1; 碰撞气流量: 0.15 mL·min-1; 取样锥孔电压: 20 V; 碰撞能量: 22 eV。
黄酮类成分的分析条件色谱柱: Dimonsiol C18色谱柱 (250 mm × 4.6 mm,5 μm); 检测波长: 358 nm; 流动相: 乙腈 (A)-0.5% 磷酸溶液 (B),梯度洗脱 (0~5 min,10% A; 10 min,18% A; 13 min,22% A; 30 min,22% A); 流速: 0.8 mL·min-1; 柱温: 30 ℃; 进样体积: 10 μL。
多糖类成分的分析方法精密量取样品 (20 mg·mL-1) 100 μL,置于15 mL干燥具塞试管中,加水补足至1.0 mL,另取水1.0 mL作空白对照。加入5% 苯酚溶液2.0 mL,混匀后,加入浓硫酸7.0 mL,冷却后充分混匀,置沸水浴中加热20 min。迅速冷却至室温,混匀,在最大吸收波长处 (490 nm) 测定吸光度。
小鼠造模方法及给药小鼠随机分为正常对照组6只与糖尿病模型组30只。对照组小鼠以普通饲料喂养,模型组小鼠以高糖高脂饲料 (为普通饲料基础上添加10% 猪油、10% 蛋黄粉和20% 蔗糖) 喂养。喂养6周后,模型组腹腔注射四氧嘧啶200 mg·kg-1,每隔2天连续追加四氧嘧啶3次进行造模,空白对 照组注射等剂量的生理盐水。一周后检测模型组小鼠空腹血糖 (FBG) ≥ 7.0 mmol·L-1,表明造模成功。将造模成功小鼠随机分为4组,其中3组为给药组,一组为模型对照组。实验前一天禁食12 h,不禁水,给药8 h后统一进食,给药5天。精密称定桑叶多糖提取物179.86 mg、桑叶生物碱提取物180.30 mg、桑叶黄酮提取物181.08 mg,将其溶解在9 mL水中,按0.1 mL/10 g剂量灌胃给药。
血浆样本收集与处理给药后2 h取血,置于肝素钠抗凝管中,离心15 min (3 500 r×min-1),分离血浆,于 -80 ℃冷冻保存。精密吸取血浆样品100 μL,加入甲醇300 μL,涡旋2 min,13 000 r×min-1离心10 min,吸取上清液在37 ℃水浴上氮气吹干。残渣用流动相100 μL复溶,涡旋2 min,13 000r×min-1离心10 min后,取上清液用于分析。
血浆样品的分析条件色谱条件: 色谱柱为ACQUITYTM UPLC BEH C18柱 (1.7 μm,2.1 mm × 100 mm,美国Waters公司),流动相为A 0.1% 甲酸水溶液,B乙腈。梯度洗脱: 0~1 min,95% A; 1~15 min,95%~10% A; 16~17 min,10%~95% A; 17~18 min,95% A。 流量: 0.4 mL·min-1; 进样量2 µL,柱温35 ℃。质谱条件: 采用电喷雾正、负离子源 (ESI+/ESI-),鞘气流速: 35 arb,辅助气流速: 15 arb,毛细管温度: 275 ℃,喷雾电压: 3.5 kV,管透镜电压水平: 65%,毛细管电压: 35 V,扫描范围: m/z 100~1 000; 质量分辨率: 60000。二级质谱分析: 裂解模式: 高能诱导解离 (HCD); 隔离宽度: 2.0 Da; 归一化碰撞能量: 35; 激活时间: 30 ms; 碰撞气: 高纯氮气。
代谢组学数据处理和分析所有数据应用SIEVEx64软件进行总离子流图提取、峰对齐及归 一化等处理,得到碎片离子的信息列表,将其导入EZinfo 2.0软件进行有监督的偏最小二乘判别法 (PLS-DA) 分析。利用Thermo XReport软件统计内 源性代谢产物的峰面积等相对含量信息。采用SPSS 16.0软件进行统计学处理,两组间比较采用t检验,检验标志性代谢物组间差异的显著性,结果以x± s表示,P < 0.05为差异具有统计学意义。
潜在标志物的结构推导主要包括以下步骤: ① UPLC-Orbitrap MS正离子模式下采集潜在生物标志物的准分子离子; ② 根据准确分子质量利用Chemspider来预测化合物的元素组成以及结构式,然后利用文献及数据库检索候选代谢物; ③ 根据得到的多级质谱信息 (MSn) 来排除一些候选代谢物,进一步缩小候选代谢物的范围; ④ 利用标准样品或者参考文献信息来确认候选代谢物,并验证鉴定结果的可靠性。
结果 1 桑叶提取物含量分析 1.1 线性范围取对照品工作液,按相应条件检测,以各成分进样浓度 (X,μg·mL-1) 为横坐标,峰面积 (Y) 为纵坐标进行线性回归,得回归方程,结果见表 1。
|
|
Table 1 Calibration curves of nine compounds. DNJ: Deoxynojirimycin; DNJ-GLC: 2-O-α-D-Glc-DNJ |
取对照品溶液重复进样6次,以峰面积为指标计算RSD (n = 6),考察方法精密度; 样品溶液间隔0、1、2、4、8、12和24 h进样,以峰面积为指标计算RSD (n = 6),考察样品的稳定性,在已知各成分含量的样品溶液中加入对照品工作液,考察方法的平均回收率 (n = 6)。结果表明,各成分精密度RSD≤4.55%,稳定性RSD≤4.32%,平均回收率为94.63%~103.05%,均符合分析要求。
1.3 含量分析桑叶黄酮类提取物中含有新绿原酸、绿原酸、隐绿原酸、芦丁、异槲皮苷、紫云英苷6种主要活性成分,其含量分别为6.3%、8.3%、5.5%、1.7%、2.3%、0.7%; 桑叶生物碱类提取物含有Fagomine、DNJ和DNJ-GLC等3种主要活性成 分,含量分别为3.2%、24.4% 和1.8%; 桑叶多糖类提取物中总多糖含量为27.6%。
2 糖尿病模型小鼠生化指标检测
造模后,模型组空腹血糖值明显升高 [(18.52 ± 0.68) mmol·L-1],与空白组 [(5.03 ± 0.51) mmol·L-1] 比较具有显著性差异 (P < 0.01)。桑叶黄酮类、生物碱类、多糖类提取物给药后,FBG值均呈下降趋势,具有显著性差异 (P < 0.01)。其中桑叶黄酮给药组FBG为 (12.21 ± 1.02) mmol·L-1,桑叶生物碱给药组FBG为(12.05 ± 0.8) mmol·L-1,桑叶多糖给药组FBG为(12.34 ± 0.56) mmol·L-1。
3 造模前后小鼠血浆代谢物分析
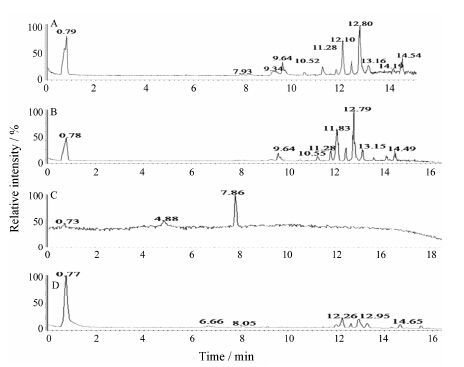
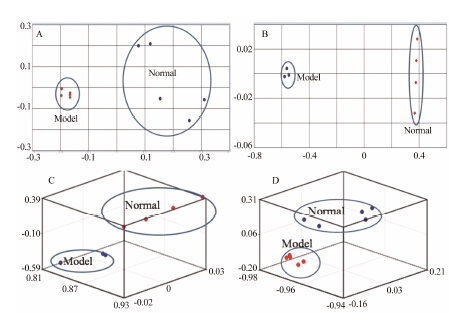
采用UPLC-Orbitrap MS分别在正、负离子模式下采集血浆样品的代谢信息。图 1分别为正、负离子模式下糖尿病模型小鼠与正常小鼠的典型总离子流图。为了考察糖尿病模型小鼠体内代谢物的整体变化,采用PCA方法对正常组和模型组小鼠血浆代谢物谱数据进行模式识别,得到样品分布图,它能够反映样品之间的相似性、差异程度,图谱差异小的样品在散点图中的位置相互靠近; 反之,差异较大的样品距离较远。图 2为模型组小鼠血浆代谢谱的分类,可看出糖尿病模型组与正常组得到明显区分,说明与正常组相比糖尿病模型小鼠机体内发生代谢异常。
|
Figure 1 Normal and diabetic model mice plasma typical UPLC LTQ-MS/MS profile. A: ESI+ mode samples from normal mice; B: ESI+ mode samples from model mice; C: ESI- mode samples from normal mice; D: ESI- mode samples from model mice |
|
Figure 2 Normal and diabetic mice plasma PCA plot. A: ESI+ mode 2D PCA plot; B: ESI- mode 2D PCA plot; C: ESI+ mode 3D PCA plot; D: ESI- mode 3D PCA plot |
采用偏最小二乘判别法 (PLS-DA) 考察正常组与糖尿病模型组血浆代谢模式的差别,得到其PLS-DA载荷图。图中每一个点代表一个变量,变量对分类的重要程度 (VIP,variable importance in the projection) 由其值的大小来衡量,并依据VIP值对变量进行筛选。VIP值大于1者可作为潜在生物标志物。
对潜在的生物标志物根据质荷比在METLIN (http://metlin.scripps.edu/),HMDB (www.hmdb.ca) 及KEGG (www.genome.jp/kegg/ligand.html) 数据库中进行检索和确认,并与文献进行比较,共鉴定出8个潜在的生物标志物,其质谱数据信息及在正常组与糖尿病模型组小鼠血浆中的变化见表 2。对该8种潜在生物标志物的相对含量进行t-检验,它们在两组小鼠间存在显著性差异 (P < 0.05)。模型小鼠体内该8种代谢物均下调,这些变化预示着糖尿病模型小鼠体内的氨基酸与鞘脂代谢发生异常。
|
|
Table 2 Diabetes mice plasma potential biomarker identification results. VIP (variable importance in the projection) values were obtained from cross-validated PLS-DA models with a threshold of 1. P < 0.05,**P < 0.01 vs normal group |
5 桑叶中生物碱类、黄酮类、多糖类提取物干预糖尿病模型小鼠的效应评价
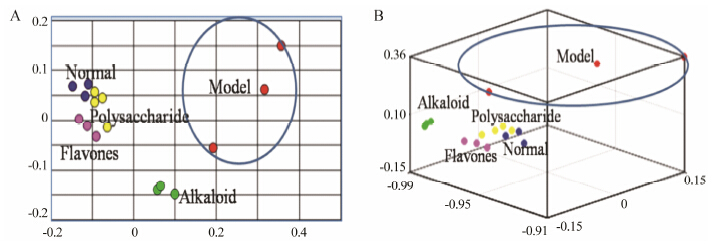
采用PCA分析法对正常组、模型组、给药组进行多元数据分析,从图 3可看出,正常组、模型组和给药组小鼠血浆样品分别聚为一类,各样品间能够明显区分。研究结果提示,经桑叶提取物干预后,糖尿病模型小鼠体内异常代谢有所改善。
|
Figure 3 ESI + model of mulberry leaves three extracts after the intervention in plasma PCA plot (A: 2D; B: 3D) |
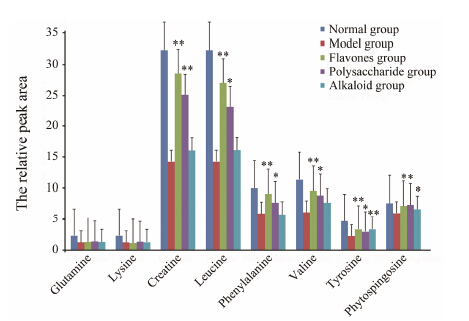
对正常组、模型组、给药组小鼠血浆中8种生物标记物的相对含量进行t检验,结果表明: 模型组血浆中8种潜在生物标记物的代谢水平下调,而给药组均具有不同程度的回调。模型组与3个药物干预组相比,桑叶黄酮类提取物组给药后肌酸、亮氨酸、苯丙氨酸、缬氨酸、酪氨酸显著上调 (P < 0.01),4-羟双氢鞘氨醇也明显上调 (P < 0.05),具有统计学意义; 桑叶多糖类提取物给药组肌酸显著上调 (P < 0.01),亮氨酸、苯丙氨酸、缬氨酸、酪氨酸、4-羟双氢鞘氨醇明显上调 (P < 0.05),具有统计学意义; 桑叶生物碱类提取物给药组酪氨酸显著上调 (P < 0.01),4-羟双氢鞘氨醇也明显上调 (P < 0.05),具有统计学意义。见图 4所示。
|
Figure 4 Differences of eight kinds of potential biomarkers in plasma |
6 桑叶多组分干预糖尿病模型小鼠的代谢途径与机制探讨
将鉴定的8种生物标志物输入到MetPA (http:// metpa.metabolomics.ca./MetPA/faces/Home.jsp) 数据库中,构建代谢通路,从中选出4条代谢通路作为潜在的糖尿病模型通路 (Raw P < 0.01),分别为赖氨酸降解 (lysine degradation)、丙氨酸,天门冬氨酸和谷氨酸代谢 (alanine,aspartate and glutamate metabolism)、缬氨酸,亮氨酸和异亮氨酸降解 (valine,leucine and isoleucine degradation)、苯丙氨酸代谢 (phenylalanine metabolism)。从代谢通路分析可知,丙氨酸、天冬氨酸和谷氨酸代谢通路、赖氨酸降解通路、苯丙氨酸代谢通路影响值相对较高,分别为0.21、0.15和0.12。苯丙氨酸在结构上与酪氨酸相似,在体内经苯丙氨酸羟化酶作用生成酪氨酸,酪氨酸在酪氨酸羟化酶的作用下生成3,4-二羟基苯丙氨酸,通过多巴脱羧酶作用生成多巴胺,因此它们均为神经介质儿茶酚胺生物合成的前体物质。血浆中酪氨酸水平下降,可能是由于高血糖使得肝脏的糖异生增加所致。
讨论本研究采用代谢组学的方法对四氧嘧啶所致糖尿病模型小鼠血浆进行分析,结果发现模型小鼠血浆中谷酰胺酸、赖氨酸、肌酸、亮氨酸、苯基氨基酸、缬氨酸、酪氨酸、4-羟双氢鞘氨醇等代谢产物水平均下降,这一趋势与相关报道一致[13]。桑叶黄酮类、生物碱类、多糖类提取物干预后对糖尿病小鼠氨基酸代谢具有明显的调节作用,三者均可调节缬氨酸,亮氨酸和异亮氨酸降解以及苯丙氨酸代谢通路,提示桑叶可促进胰岛素分泌,抑制糖异生,并且有利于阻止糖尿病并发症的发生。这与研究报道,桑叶可促进胰岛素分泌,改善胰岛素抵抗[14, 15, 16]的结果相一致。
此外,4-羟双氢鞘氨醇属于鞘脂类化合物,在鞘脂合成中具有重要作用。二氢鞘氨醇是神经酰胺的重要合成前体,而神经酰胺是半乳糖鞘氨醇、葡糖苷酰鞘氨醇和鞘磷脂的前体。其中鞘磷脂代谢失调可能导致细胞死亡,并且与胰岛素相关疾病密切相关[17]。桑叶黄酮类、生物碱类、多糖类提取物干预后4-羟双氢鞘氨醇明显上调,提示可能对脂类代谢起到一定调节作用,其作用机制尚需进一步深入研究。
| [1] | Hansen KB, Vilsboll T, Knop FK. Incretin mimetics: a novel therapeutic option for patients with type 2 diabetes-a review [J]. Diabetes Metab Syndr Obes, 2010, 3: 155-163. |
| [2] | Zhu C, Hu P, Liang QL, et al. Integration of metabonomics technology and its application in modernization of traditional Chinese medicine [J]. Acta Pharm Sin (药学学报), 2008, 43: 683-689. |
| [3] | Huang XC, Su SL, Duan JA, et al. Application and thinking of metabonomics in some scientific problems of traditional Chinese medicine [J]. Chin Tradit Herb Drugs (中草药), 2014, 45: 147-153. |
| [4] | Su SL, Duan JA, Wang PJ, et al. Metabolomic study of biochemical changes in the plasma and urine of primary dysmenorrhea patients using UPLC-MS coupled with a pattern recognition approach [J]. J Proteome Res, 2013, 12: 852-865. |
| [5] | Liu P, Duan JA, Su SL, et al. Biomarkers of primary dysmenorrhea and herbal formula intervention: an exploratory metabonomics study of blood plasma and urine [J]. Mol Biosyst, 2013, 9: 77-87. |
| [6] | Huang XC, Su SL, Duan JA, et al. Simultaneous determination of paeoniflorin, albiflorin, ferulic acid, tetrahydropalmatine, protopine, typhaneoside, senkyunolide I in Beagle dogs plasma by UPLC-MS/MS and its application to a pharmacokinetic study after oral administration of Shaofu Zhuyu Decoction [J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2014, 1: 75-81. |
| [7] | OuYang Z, Chen J. Progress in mulberry chemical composition and pharmacological effects [J]. J Jiangsu Univ (江苏大学学报), 2003, 24: 39-44. |
| [8] | Mohammad I, Hamayun K, Mohibullah S, et al. Chemical composition and antioxidant activity of certain Morus species [J]. J Zhejiang Univ Sci B, 2010, 11: 973-980. |
| [9] | Cheng FY, Ye SY. Mulberry treating diabetic research overview [J]. J Pharm Pract (药学实践杂志), 2005, 23: 71-74. |
| [10] | Liu XM, Xiao GS, Chen WD. Research and development progress of mulberry leaves [J]. J Chin Med Mater (中药材), 2001, 24: 144-147. |
| [11] | Lu GB, Ren CJ, Cui WZ, et al. The preliminary structure of polysaccharide MLP Ⅱ from mulberry leaves and its hypoglycemic effect on rat model of diabetes [J]. Sci Seric, 2011, 37: 1053-1060. |
| [12] | Yang Y, OuYang Z, Chang Y, et al. Study on hypoglycemic effects of components in mulberry leaves [J]. Food Sci (食品科学), 2007, 28: 454-456. |
| [13] | Guo WX, Zhang JQ, Dong AM, et al. The 11th National Endocrinology Conference Proceedings of the Chinese Medical Association (中华医学会第十一次全国内分泌学学术会议 论文汇编) [C]. Guangzhou: Chinese Medical Association, 2012: 219. |
| [14] | Zhao YL, Huang YQ. The research of mulberry resources on diabetes mellitus [J]. Strait Pharm J (海峡药学), 2009, 21: 13-15. |
| [15] | Zhou YX, Liao ST, Liu XM, et al. Diabetic therapy effects of mulberry resources on diabetes mellitus [J]. Nat Prod Res Dev (天然产物研究与开发), 2004, 16: 265-268. |
| [16] | Xing DX, Liao ST, Liu JP. The research of mulberry medicinal resources on diabetes [J]. J Chin Med Mater (中药材), 2006, 29: 1253-1257. |
| [17] | Tian QL. Plasma Phospholipid Metabolic Profiling and Biomarkers of Type 2 Diabetes Mellitus Based on UPLC/Q-TOF/MS (基于UPLC/Q-TOF/MS的T2DM大鼠血浆中 磷脂代谢轮廓分析及标志物识别) [D]. Guangzhou: Guangdong Pharmaceutical University, 2012. |
 2015, Vol. 50
2015, Vol. 50


