2. 南京中医药大学国家教育部中药炮制规范化及标准化工程研究中心, 江苏 南京 210023;
3. 北京大学药学院天然药物及仿生药物国家重点实验室, 北京 100191
2. Engineering Center of State Ministry of Education for Standardization of Chinese Medicine Processing, Nanjing University of Chinese Medicine, Nanjing 210023, China;
3. State Key Laboratory of Natural and Biomimetic Drugs, School of Pharmaceutical Sciences, Peking University Health Science Center, Beijing 100191, China
川芎始载于《神农本草经》,为伞形科植物川芎 (Ligusticumchuanxiong Hort.) 的干燥根茎。其性辛、温; 归肝、胆、心包经; 具有活血行气、祛风止痛的功效[1]。临床主要用于治疗气滞血瘀所导致的胸痹心痛、胸胁刺痛、跌扑肿痛、月经不调、经闭痛经、癥瘕腹痛、头痛、风湿痹痛等,是中医处方常用中药,也是许多中成药的重要原材料[2]。川芎的主要成分包括苯酞类、酚酸类、生物碱类等,其中苯酞类药理活性与川芎活血行气、祛风止痛的传统功效密切相关,具有明显的舒张血管、改善微循环、抑制血小板聚集、拮抗动脉粥样硬化的形成以及抗实验性脑缺血等方面的作用[3, 4]。酚酸类成分除上述作用外,还具有明显的清除自由基、增强免疫功能等药理活性。2010年版《中国药典》(一部) 在川芎项下仅以阿魏酸作为其检测指标,尽管阿魏酸在川芎中含量较高,但单一成分终究难以真正体现和全面保障川芎的内在质量。川芎苯酞类成分中的丁烯基苯酞结构稳定,价廉易得,已被列为国家法定的对照品[5],而其他苯酞类成分的稳定性较差,且较难以分离。因此,本研究选用丁烯基苯酞作为内参物,应用单标多组分HPLC定量分析(HPLC-QAMS) 法,以酚酸类成分 (阿魏酸) 以及苯酞类成分 (洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A、藁本内酯、丁烯基苯酞) 为研究对象,建立丁烯基苯酞与其他成分间的相对校正因子 (RCF),同时应用外标法测定各成分的含量,对实测值和计算值进行分析比较以验证HPLC-QAMS法的准确性; 通过改变液相色谱系统、色谱柱、流速、柱温等来考察RCF的耐用性,以其结果来评价HPLC-QAMS法的系统适用性[6, 7, 8, 9, 10]。根据HPLC-QAMS法的准确性和适用性来探讨HPLC-QAMS在川芎饮片不同类型成分同时含量测定中应用的合理性及其在质量评价应用中的可行性。
材料与方法材料
Waters e2695-2489型高效液相色谱仪 (美国Waters公司); Varian 920-LC型高效液相色谱仪 (美国Varian公司); Shimadzu LC-2010A型高效液相色谱仪 (日本Shimadzu公司); AG 285型电子天平 (瑞士Mettler Toledo公司); KQ-500型超声波清洗器 (昆山市超声仪器有限公司); TGL-16B型离心机 (上海安亭科学仪器厂); 超纯水制备仪 (南京易普易达科技发展有限公司)。
阿魏酸(ferulic acid,批号: A-002-121011)、洋川芎内酯I (senkyunolide I,批号: Y-084-130113)、阿魏酸松柏酯 (coniferyl ferulate,批号: A-001-140727)、藁本内酯 (Z-ligustilide,批号: G-010-140728) 和丁烯基苯酞 (butylidenephthalide,批号: D-057-130708) 对照品均购自成都瑞芬思生物科技有限公司; 洋川芎内酯A (senkyunolide A,批号: 140225) 对照品购自成都克洛玛生物科技有限公司。上述对照品经HPLC面积归一化法检测,其质量分数 (纯度) 均大于98%,符合含量测定的要求。甲醇 (色谱纯,德国CNW公司),乙腈 (色谱纯,德国CNW公司),甲酸 (分析纯,南京化学试剂有限公司),水为实验室自制超纯水,其他试剂均为分析纯。
23批不同批号的川芎饮片收集于其道地产区及各大药房 (样品编号: 1~23),各批次川芎饮片经北京大学药学院天然药物及仿生药物国家重点实验室屠鹏飞教授鉴定,均为伞形科植物川芎 (Ligusticum chuanxiong Hort.) 的干燥根茎。
色谱条件ODS HYPERSIL色谱柱 (250 mm × 4.6 mm,5 μm),流动相A为0.2% 甲酸水,流动相B为乙腈,梯度洗脱 (0~10 min,95%→70% A; 10~16 min,70%→60% A; 16~30 min,60% A; 30~45 min,60%→40% A; 45~48 min,40% A; 48~49 min,40%→10% A; 49~54 min,10%→0% A; 54~60 min,0%→20% A),流速1.0 mL·min-1,检测波长为252 和266 nm,柱温30 ℃,进样量20 μL。理论塔板数以丁烯基苯酞计应不小于4 000。
供试品溶液的制备取川芎饮片,粉碎,过3号筛,精密称定约0.5 g,置于具塞锥形瓶中,精密加入60%甲醇25 mL,密塞,称定重量,超声 (500 W,40 kHz) 提取60 min,放冷,再称定重量,用60% 甲醇补足减失的重量,摇匀,于12 000 r·min-1转速下离心5 min,取上清液,用0.45 μm微孔滤膜滤过,取续滤液,即得。
混合对照品溶液的制备分别精密吸取一定量的各对照品甲醇储备液于10 mL棕色量瓶中,用甲醇稀释并定容至刻度,摇匀,配制成阿魏酸71 000.0 ng·mL-1、洋川芎内酯I 33 855.0 ng·mL-1、阿魏酸松柏酯122 892ng·mL-1、洋川芎内酯A 312 360 ng·mL-1、藁本内酯898 500 ng·mL-1和丁烯基苯酞21 608.0 ng·mL-1的混合对照品溶液1#,采用逐级稀释的方法依次得稀释倍数分别为2、4、8、16、32的系列浓度溶液,作为混合对照品溶液2#~6#,备用。
色谱峰的定位单标多组分HPLC定量分析法色谱峰的准确定位一般可以采用保留时间差或相对保留值等参数,同时结合色谱图的整体特征以及每个色谱峰的紫外吸收特征来定位其余待测成分的色谱峰。保留时间差是待测成分i与内参物s之间保留时间的差值,计算公式为: ΔtRis = tRi - tRs; 相对保留值是指各待测成分i与内参物s之间保留时间的比值,计算公式为: ris = tRi/tRs。
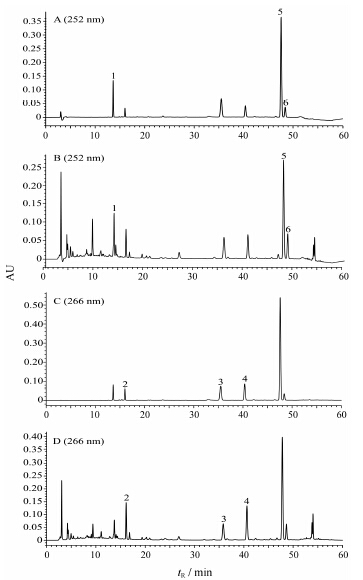
结果 1 方法学考察 1.1 HPLC色谱图典型的混合对照品溶液和供试品溶液在252 nm和266 nm的HPLC色谱图见图 1。
|
Figure 1 Typical HPLCchromatograms of mixed reference substances (A,C) and samples (B,D) at 252 nmand 266 nm. Peaks 1: Ferulic acid; 2: Senkyunolide I; 3: Coniferylferulate; 4: Senkyunolide A; 5: Z-ligustilide; 6: Butylidenephthalide |
精密吸取上述混合对照品溶液1#~6#,分别进样20 μL,每个浓度测定3次,取平均值。以峰面积积分值为纵坐标 (Y),对照品浓度 (ng·mL-1) 为横坐标 (X),绘制标准曲线,以偏最小二乘法计算回归方程。结果表明,混合对照品溶液在一定范围内线性关系良好,各对照品回归方程、相关系数及线性范围见表 1。
|
|
Table 1 Linear results of sixmarker compounds in Chuanxiong Rhizoma |
取4#混合对照品溶液,在上述色谱条件下连续进样6次,记录各组分色谱峰的峰面积并计算其RSD值。阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A、藁本内酯和丁烯基苯酞的RSD值依次为0.82%、3.0%、1.0%、0.87%、0.92% 和0.69%,表明仪器的精密度良好。
1.4 重复性精密称取川芎10号样品粉末6份,按“供试品溶液的制备”项下方法平行制备6份供试液,在上述色谱条件下进样分析,计算各组分的含量及其RSD值。阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A、藁本内酯和丁烯基苯酞6种组分含量的RSD值依次为2.4%、2.1%、2.8%、2.9%、2.3% 和2.0%,表明方法的重复性良好。
1.5 稳定性取同一份供试品溶液,室温放置,分别于0、2、4、8、10、12、24 h进样分析,测定各组分的峰面积并计算其RSD值。阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A、藁本内酯和丁烯基苯酞的RSD值依次为2.7%、1.6%、2.4%、1.6%、1.2% 和0.82%,表明供试品溶液在室温下24 h内稳定。
1.6 加样回收率取已知含量的川芎10号样品粉末,精密称定,约0.25 g。每份精密加入相当于0.25 g样品含量的6种对照品,按“供试品溶液的制备”项下方法操作,在上述色谱条件下进样分析,计算得阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A、藁本内酯和丁烯基苯酞的平均加样回收率分别为101.2%、98.5%、101.0%、102.0%、98.5% 和100.2%,RSD值分别为3.0%、1.6%、2.7%、1.4%、1.3% 和1.2%,表明方法的准确度较高。
2 相对校正因子计算 2.1 川芎中待测成分相对校正因子的计算根据公式Ci = fsi × Cs × Ai / As,以丁烯基苯酞为内标,计算丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间的相对校正因子,结果见表 2。
|
|
Table 2 Relative correction factorsof six compounds in Chuanxiong Rhizoma (n = 3). a: Ferulic acid; b: SenkyunolideI; c: Coniferyl ferulate; d: Senkyunolide A; e: Z-ligustilide; f:Butylidenephthalide |
针对可能影响相对校正因子耐用性的主要因素,设计以下一系列实验,重点考察测定条件的微小波动对相对校正因子重现性的影响。
2.2.1 不同仪器对相对校正因子的影响在不同实验室进行实验,采用ODS HYPERSIL色谱柱 (250 mm × 4.6 mm,5 μm),分别考察3种不同高效液相色谱系统 (Waters e2695-2489、Varian 920-LC、Shimadzu LC-2010A) 对相对校正因子的影响。结果显示,同一品牌色谱柱应用于3种不同高效液相色谱系统后,丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间相对校正因子的RSD值依次为: 1.9%、3.4%、1.4%、3.9% 和2.1%,表明在此影响因素下各成分相对校正因子的重现性良好。
2.2.2 不同色谱柱对相对校正因子的影响在不 同实验室进行实验,采用3种不同高效液相色谱系统 (Waters e2695-2489、Varian 920-LC、Shimadzu LC-2010A),分别考察3种不同品牌色谱柱 (ODS HYPERSIL、Purospher® STAR LP RP-18、Hypersil ODS) 对相对校正因子的影响。结果显示,对于3种不同高效液相色谱系统,分别应用3种不同品牌色谱柱后,丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间相对校正因子的RSD值在1.1%~5.0% 之间,表明在此影响因素下各成分相对校正因子的重现性良好。
2.2.3 不同流速和不同柱温对相对校正因子的影响在同一实验室进行实验,采用Waterse2695- 2489高效液相色谱系统和ODS HYPERSIL色谱柱 (250 mm × 4.6 mm,5 μm),分别考察不同流速 (0.8、1.0、1.2 mL·min-1) 和不同柱温 (25 ℃、30 ℃、35 ℃) 对相对校正因子的影响。结果显示,针对同一高效液相色谱系统和同一品牌色谱柱,应用不同流速后,丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间相对校正因子的RSD值依次为:4.5%、2.0%、4.7%、2.4% 和4.2%; 应用不同柱温后,丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间相对校正因子的RSD值依次为:2.2%、4.5%、4.9%、4.0% 和2.1%,表明在此影响因素下各成分相对校正因子的重现性良好。
2.3 待测组分色谱峰的定位本研究主要考察了相对保留值在3种不同高效液相色谱系统 (Waters e2695-2489、Varian 920-LC、Shimadzu LC-2010A) 中分别应用3种不同品牌色谱柱 (ODS HYPERSIL、Purospher® STAR LP RP-18、Hypersil ODS) 后的重现性。结果显示,相对保留值的波动在不同高效液相色谱系统和不同品牌色谱柱之间不明显,丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间相对保留值的RSD值在0.29%~4.5% 之间,表明采用相对保留值法进行川芎中酚酸类和苯酞类待测成分色谱峰的定位是可行的。
2.4 HPLC-QAMS法与外标法测定结果的比较精密称取23批川芎饮片粉末各约0.5 g,按“供试品溶液的制备”项下方法制备供试品溶液,采用外标法 (ESM) 对川芎进行多成分同步含量测定,每批样品平行测定3次,取其平均值。再用所建立的 HPLC-QAMS法,以测得的丁烯基苯酞结果为基础,根据其与其他成分间的RCF来计算其他各成分的含量,取其平均值。两种方法所得结果比较见表 3。通过分析比较可见,外标法实测值与HPLC-QAMS法计算值之间无明显差异,RSD值均小于5%。
|
|
Table 3 Contents (mg·g-1)analysis andcomparison ofsix analytes in Chuanxiong Rhizoma samples by ESM and HPLC-QAMS (n = 3). a: Ferulic acid; b:Senkyunolide I; c: Coniferyl ferulate; d: Senkyunolide A; e: Z-ligustilide;f: Butylidenephthalide |
本研究在优选供试品溶液的提取条件时,采用不同提取方法 (超声提取、索氏提取、回流提取)、不同提取溶剂 (60%、80%、100% 乙醇和60%、80%、100% 甲醇)、不同提取时间(30、60、90和120 min) 以及不同提取体积 (20、50、100和200倍) 制备供试品溶液,最终确定的最佳提取条件为: 50倍量的60% 甲醇超声提取60 min。在此条件下,目标成分的提取效率较高,干扰的杂质峰较少,且方法简单,成本较低。
实验通过考察甲醇-水溶液、甲醇-0.1% 甲酸水溶液、乙腈-水溶液、乙腈-0.1% 甲酸水溶液、乙腈- 0.2% 甲酸水溶液等流动相洗脱系统,综合比较基线噪声、拖尾、分离度等因素,最终选择乙腈-0.2% 甲酸水溶液系统作为流动相。在此条件下,供试品溶液出峰较多,所测定的色谱峰形状和各峰之间的分离度符合含量测定要求,而且杂质峰较少,基线较为平稳。实验同时对供试品溶液进行全波长扫描,根据扫描结果确定阿魏酸、藁本内酯和丁烯基苯酞的检测波长为252 nm; 洋川芎内酯I、洋川芎内酯A和阿 魏酸松柏酯的检测波长为266 nm。此外,还通过实 验对柱温、流速和进样量等进行了优选,并最终确定了最佳色谱条件。
在建立丁烯基苯酞与阿魏酸、洋川芎内酯I、阿魏酸松柏酯、洋川芎内酯A和藁本内酯之间的相对校正因子时,设计了一系列实验用于考察不同高效液相色谱系统、不同类型色谱柱、不同流速和不同柱温对RCF耐用性的影响。结果表明,测定条件的微小改变对RCF影响不大,RCF的重现性良好,应用所
建立的HPLC-QAMS法得到的RCF比较稳定,具有较高的可信度,可利用其在对照品缺乏的情况下实现川芎的多指标定量分析和质量评价。另外,本研究同时测定的6个成分中,除了5个成分同为苯酞类 成分外,阿魏酸属于酚酸类成分。由实验结果可知,两种方法所测得的阿魏酸含量之间的RSD值均小于2.5%,改变测定条件后,阿魏酸与内参物 (丁烯基苯酞) 之间RCF的RSD值均小于4.8%,所有差异均在误差允许的范围内。由此可以推断,HPLC-QAMS法不仅适用于同种类型成分间含量的同时测定,亦有望用于不同类型成分间含量的同时测定。在今后的研究中,可以适当拓宽单标多组分HPLC定量分析法的应用范围,但是需要更加谨慎地优选色谱条件,考察测定条件(高效液相色谱系统、色谱柱、检测波长、流速、柱温以及对pH值有特殊要求的需考察pH值) 发生微小改变时相对校正因子的耐用性。尤其对于不同的高效液相色谱系统,由于检测器以及积分方式的不同等因素可能会带来影响。因此建议: 如果结果中各高效液相色谱系统间的RCF差异较大,则应考虑缩小所建不同成分间RCF的应用范围,同时根据RCF的RSD值大小限定所适用的高效液相色谱系统,从而最大程度地减少HPLC-QAMS应用的误差。
| [1] | Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典) [S]. 2010 ed. Vol 1. Beijing: China Medical Science Press, 2010: 38. |
| [2] | Li SL, Lin G, Chung HS, et al. Study on fingerprint ofrhizoma Chuanxiong by HPLC-DAD-MS [J]. Acta Pharm Sin (药学学报), 2004, 39: 621-626. |
| [3] | Peng SH, Zhou TH. Investigation on in vivo metabolism of n-butylphthalide [J]. Acta Pharm Sin (药学学报), 1996, 31: 780-784. |
| [4] | Xu HL, Feng YP. Effects of 3-n-butylphthalide on thrombosis formation and platelet function in rats [J]. Acta Pharm Sin (药学学报), 2001, 36: 329-333. |
| [5] | Liu YH, Yi JH, Shao HW, et al. Determination of butylphthalide and ligustilide in Chuanxiong Rhizoma by substitution method of reference substance [J]. Chin J Pharm Anal (药物分析杂志), 2012, 32: 758-762. |
| [6] | Lou YJ, Cai H, Liu X, et al. Multi-component analysis in sun-dried and sulfur-fumigated Angelicae Sinensis Radix by single marker quantitation and chemometric discrimination [J]. Pharmacog Mag, 2014, 10: s189-s197. |
| [7] | Lu TL, Shi SM, Cai BC, et al. Advances in studies on multi-component determination of Chinese materia medica by QAMS [J]. Chin Tradit Herb Drugs (中草药), 2012, 43: 2525-2529. |
| [8] | Wang ZM, Qian ZZ, Zhang QW, et al. Technical guide for quantitative analysis of multi-components by single marker [J]. China J Chin Mater Med (中国中药杂志), 2011, 36: 657-658. |
| [9] | Wang ZM, Gao HM, Fu XT, et al. Multi-components quantitation by one marker new method for quality evaluation of Chinese herbal medicine [J]. China J Chin Mater Med (中国中药杂志), 2006, 31: 1925-1928. |
| [10] | Gao HM, Song ZH, Wang ZM, et al. Overview on quantitative analysis of multi-components by single-marker [J]. China J Chin Mater Med (中国中药杂志), 2012, 37: 405-416. |
 2015, Vol. 50
2015, Vol. 50


