黄芩苷 (baicalin,BC) 是传统中药黄芩的主要成分,属于黄酮类化合物,它在清除氧自由基、减轻组织的缺血再灌注损伤和调节免疫等多方面具有显著功效[1]。随着生物技术的发展以及中药化学成分分离水平的进步,黄芩苷在抗氧化、抗肿瘤及治疗心血管疾病等方面具有潜在的开发应用价值[2]。中药中的某些活性成分可以和金属元素形成配合物,从而使其药理作用得到加强,此现象已有大量文献佐证。BC分子结构中因含有羟基或羰基等基团而与金属离子有较强的螯合作用,其母核的4位羰基上的氧原子具有很强的配位能力,同时黄芩苷的空间结构也有利于金属配合物的合成[3]。目前已有关于黄芩苷-金属配合物 (BMC) 的报道[4],本课题组进行的BMC研究显示,黄芩苷与金属离子配合后,生物利用度提高,药理活性有不同程度的提升[5]。而药物的体内过程可表现为吸收、分布、代谢及排泄4个过程,其中分布过程包含药物的输运,是药物发挥药效的关键过程之一。在药物的体液输运中,主要是其与血清蛋白 (BSA) 分子的相互作用过程。但关于BMC-BSA的相互作用研究尚不够深入,亟需进一步完善。
目前生物活性小分子/离子与蛋白质分子的相互作用机制研究是国内外的热点研究领域[6, 7],荧光光谱[8, 9]、紫外光谱[10, 11]和红外光谱[12]等分析手段的应用促进了该研究领域的不断深入。相对于这些经典 方法而言,电化学分析法具有快捷、高选择性、高灵敏度、能应用于没有光谱信号的浑浊溶液体系等特 点[13],目前电化学方法应用于相互作用的研究已见报道[14],但多是具有电活性小分子药物-药物的相互作用研究,传统电极很难对蛋白质大分子 (如血清蛋白) 表现出电化学活性,故建立新的方法分析小分子药物与生物大分子的相互作用很有必要。通过电 极修饰可以将蛋白质等大分子与活性小分子/离子的非共价相互作用的反应信号放大,进而可以针对反应体系的电化学行为特征变化来研究相互作用,这是一种行之有效的新方法。碳纳米管 (multi-walled carbon nanotubes,CNTs) 具有良好的导电性、催化活性和较大的比表面积,尤其对过电位的明显降低及对部分氧化还原蛋白质的直接电子转移现象,因此被广泛用于修饰电极的研究[15, 16]。碳纳米管的发现时间并不长,其作为电极用于化学反应时能促进电子转移,在分析药物与血清蛋白相互作用的应用也刚起步,但作为一种新型的电极修饰材质,由于其本身所拥有的独特性质,决定它具有广阔的应用前景。
本文利用CNTs的分子结构特征,建立一种研究BMC与BSA分子作用机制的分析新方法,并将物理的一些理论方法应用于相互作用研究,建立BMC与BSA相互作用的结合模型,进而推求热力学结合常数和动力学参数,分析BMC与BSA的作用机制,为进一步了解BMC在生物体内的代谢过程提供有价值的信息。
材料与方法 试剂与仪器CHI660C电化学工作站 (上海辰华仪器有限公司); 三电极系统: 玻碳电极 (glassy carbon electrode,GCE,φ = 3 mm) 为工作电极,饱和甘汞电极(saturated calomel electrode,SCE) 为参比电极,铂电极为对电极; SK3210HP超声波清洗器 (上海科导超声仪器有限公司)。
黄芩苷 (≥96%,baicalin,BC,上海金穗生物科技有限公司),BMC (本实验室合成与表征,纯度 > 95%)[17],多壁碳纳米管 (CNTs,纯度 > 95%,中国科学院成都化学有限公司),牛血清白蛋白 (BSA,纯度≥98%,上海神航生物科技有限公司)。其他试剂均为分析纯,实验用水为二次蒸馏水。分别配制0.2 mol·L-1的Na2HPO4和NaH2PO4溶液,pH值分别是5.8、6.0、6.5、7.0、7.5、8.0的磷酸缓冲液 (PBS),并用PBS配制1×10-5 mol·L-1 BSA储备液,相同pH值的PBS和二甲基亚砜 (DMSO,≤0.4%) 配制1×10-4 mol·L-1 BMC溶液。
碳纳米管修饰电极的制备与表征多壁碳纳米管 (CNTs) 40 mg放入200 mL浓HCl中,磁力搅拌 下加热回流7 h,以去除金属催化剂。纯化后的CNTs放入80 mL浓混酸 (HNO3∶H2SO4 = 1∶3) 中,室温超声反应10 h。蒸馏水洗至中性,得到羧基化的F-CNTs[18],干燥成粉末备用。
玻碳电极分别用0.3和0.05 μm的A12O3粉末 在抛光布上进行抛光,采用大量二次蒸馏水冲洗,然后在超声清洗仪中分别用二次蒸馏水、无水乙醇和二次蒸馏水超声清洗 (5 min/次),室温晾干。取10 mg羧基化的F-CNTs溶于N,N-二甲基甲酰胺 (DMF) 中,超声10 min使其分散均匀,取F-CNTs溶液5 µL,采用滴涂法修饰玻碳电极表面,50 ℃烘干,得F-CNTs/ GCE修饰电极。
制备的F-CNTs/GCE采用循环伏安法进行电化学性能表征。在5 mmol·L-1 K3Fe(CN)6 + 0.1 mol·L-1 KCl溶液中,0.6~-0.2 V电位内,进行循环伏安扫描获取伏安图; 频率范围0.01~100 000 Hz,振幅0.005 V,以5.0 mmol·L-1 [Fe(CN)6]4-/3- 为氧化还原探针,于0.1 mol·L-1 KCl电解质溶液中,进行电化学阻抗表征,绘制等效电路,分析F-CNTs/GCE的电 学特性。
BMC-BSA的相互作用分析在pH 7.5的PBS中,分别对1.0×10-5 mol·L-1 BC和1.0×10-5 mol·L-1 BC-Ce3+、BC-La3+、BC-Y3+、BC-Co2+、BC-Ni2+和BC-Cu2+配合物溶液进行循环伏安分析 (-0.3~0.6 V, 扫速为0.1 V·s-1),数据拟合建立模型,并获取热力学常数; 根据物理原理,由实验数据分析获得动力学参数。
结果与讨论 1 修饰电极的电化学表征新型F-CNTs/GCE电极进行电化学阻抗表征,交流阻抗谱如图 1所示。
 |
Figure 1 The cyclic voltammograms (CA) of different electrodes in [Fe(CN)6]4-/3--KCl solution (cyclic voltammetric responses at different electrodes). (a) Bare GCE; (b) F-CNTs/GCE. GCE: Glassy carbon electrode; F-CNTs: Functionalized multi-walled carbon nanotubes |
氧化还原峰在各电极上呈对称形,说明探针离子在修饰电极上的电化学反应是准可逆过程。探针[Fe(CN)6]4-/3- 在F-CNTs/GCE (图 1b曲线) 上的峰电流比裸电极 (图 1a曲线) 大,这是因为电极表面修饰了F-CNTs后,其比表面积明显增加,证明F-CNTs有利于电子的转移,有效改善原基底电极的性能。裸电极在高频区出现了弧形,低频区呈线性,说明电极过程受电子转移和扩散联合控制,裸电极的界面电子传递阻力 (Ret) 很大。F-CNTs修饰电极表面后,电子传递阻力明显减少,这是因为功能化的碳纳米管极易被溶剂润湿,能形成较好的电极/溶液界面,加速电子传递。黄芩苷配合物在修饰电极上有灵敏的还原峰,而在裸玻碳电极上并不明显。正是碳纳米管的吸附性能增加了电极表面的药物与蛋白的浓度,最终导致出现了明显的峰电流。
用Zview软件对上述电极交流阻抗谱 (图 1) 进行拟合,其等效电路如图 2所示,R1表示电极外表面和参比电极之间的溶液电阻,CPE1为表征双电层电容的常相位元件,CPE2为表征法拉第反应过程双电层电容的常相位元件,R2为电子迁移阻抗,R3为Warburg阻抗。拟合得到的参数值如表 1所示。
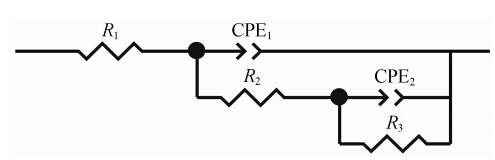 |
Figure 2 Equivalent circuit model of electrochemical impedance spectra of GCE and F-CNTs/GCE |
|
|
Table 1 The equivalent circuit parameters of GCE and F-CNTs/GCE |
从表 1可知,电极的阻抗谱高频端均为一偏心半圆的容抗弧,表明体系出现弥散效应,这是由于电极表面与溶液界面的不均匀所致。两种电极均在含5 mmol·L-1 K3Fe(CN)6 的0.1 mol·L-1 KCl溶液中进行测试,因此溶液电阻R1相差不大,电流较易在参比电极与修饰电极间传输。由于采用F-CNTs为基质材料,修饰电极的电子转移电阻R2明显小于表面没有任何增强电子转移物质的裸电极,说明碳纳米管可极大提高电子传递速率。双电层的电化学行为趋向于 一个等效元件CPE,用n (0~1) 来表示弥散效应的大小,n值越小弥散效应越大,电极表面越粗糙,当n = 1时无弥散效应。各电极中,裸电极CPE1的n值最大(0.883 4),表明其弥散效应较小,F-CNTs/GCE CPE1的n值为0.405 1,小于裸电极,说明F-CNTs/GCE表面较粗糙,提高了电极的敏感度,有利于BMC与BSA的分子作用机制分析。
由于pH值对BMC与BSA相互作用影响较大,故配制一系列BMC的不同pH (5.0~8.7) PBS溶液,利用循环伏安法测定F-CNTs/GCE的氧化峰电流。在缓冲溶液的pH值为7.5时,峰形最好,且峰电流绝对值最大; 当缓冲溶液pH < 7.5,氧化还原峰形较宽; 当pH过大时,氧化还原峰形不明显。故后续实验选用pH为7.5的PBS缓冲液。
BMC的峰电位随着溶液pH的增加逐渐负移,说明有质子参与BMC在电极上的氧化反应。同时BMC氧化峰电位与pH呈良好的线性关系(图 3)。BMC氧化峰电位与pH的线性回归方程斜率接近 -59 mV/pH, 说明BMC在电极上发生了等电子质子反应。
 |
Figure 3 The linear relationship between pH and the oxidation peak potentials of baicalin metal complexes (BMC) |
循环伏安法实验选择0.2 mol·L-1 PBS缓冲溶液 (pH 7.5) 为底液,ipc与cBMC在1.0×10-6~5.0×10-4 mol·L-1内呈良好的线性关系,检出限均可达1×10-7 mol·L-1。在1.0×10-5 mol·L-1 BMC的PBS溶液中 加入定量的BSA后,峰电流的降低值同BSA量在1.0×10-6~6.0×10-6 mol·L-1内呈线性关系,BSA的检出限为6×10-7 mol·L-1 (S/N = 3)。对1×10-6 mol·L-1 BSA进行8次平行测定,RSD为3.6%。
2 BMC与BSA相互作用的热力学机制在生物大分子-活性小分子相互作用研究中,结合参数的求取具有重要意义,结合本工作的具体实验数据,分别建立BMC与BSA相互作用的结合模型,进而理论推求结合常数 (β) 和结合位点数 (n)。
设定BSA与BMC生成复合物BSA-nBMC,
BSA + nBMC 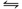 BSA-nBMC BSA-nBMC
|
(1) |
则β可表示为:
| β = [BSA-nBMC] / [BMC]n [BSA] | (2) |
其中,[BSA]、[BSA-nBMC]、[BMC]分别代表溶液中未结合BMC的BSA浓度、结合BMC的BSA浓度、自由的BMC浓度,又根据物料平衡,得到溶液中BSA的总浓度 (cBSA):
| (cBSA) = [BSA] + [BSA-BMC] | (3) |
同样可得到溶液中BMC的总浓度[BMC]0:
| [BMC]0 = [BMC] + n[BSA-nBMC] | (4) |
在实验条件下,峰电流 (I) 与电极反应体系中的BMC浓度呈正比,其可表示为:
| I = K [BMC] | (5) |
其中,K为比例常数,当温度及反应条件确定时,其为定值,I[BMC]0和I[BMC]分别表示不加入和加入BSA时BMC峰电流值,其差值可表示为:
| ΔI = I[BMC]0- I[BMC] | (6) |
将公式 (4) 和 (5) 带入公式 (6) 中:
| ΔI = K([BMC]0-[BMC]) = Kn[BSA-nBMC] | (7) |
即ΔI与 [BSA-nBMC] 呈正比。当 [BSA-nBMC] 达到最大值,即形成复合物的浓度达到极值时,ΔI 达到峰值,即ΔImax。当复合物浓度达到极值时,[BSA-nBMC]max应等于cBSA。
| ΔI = Kn[BSA-nBMC]max = KncBSA | (8) |
公式 (8) 和 (7) 相减,得到:
| ΔImax- ΔI = Kn(cBSA- [BSA-nBMC]) = Kn[BSA] | (9) |
公式 (7) 和 (9) 带入公式 (2) 中,得到:
| lg[ΔI /(ΔImax- ΔI)] = lgβ + nlg[BMC] | (10) |
由方程式 (10) 即可计算蛋白质大分子与BMC相互作用的结合常数及结合位点数。依据实验数据,以lg[ΔI/(ΔImax-ΔI)] 对lg[BMC] 作图,可说明lg[ΔI/ (ΔImax-ΔI)] 对lg[BMC] 确实存在方程式 (10) 的关系,实验结果验证了建议的理论方程。同时根据线性方程求得β和n,详见表 2。
|
|
Table 2 The relationship between lg[ΔI/(ΔImax-ΔI)] and lg[BMC] in BMC-BSA solution system (n = 7). BSA: Bovin serum album; BC: Baicalin |
由表 2可见,BMC-BSA的结合位点数在1.7左右,其中BC-Co2+-BSA的结合位点数最小 (1.3),其次为BC-Y3+-BSA的结合位点数为1.6,其他BMC-BSA与BC-BSA的结合位点数相同 (1.7)。
3 BMC与BSA相互作用的动力学机制为研究BMC与BSA的相互作用,采用循环伏 安法来检测。图 4为BMC-BSA的循环伏安图。从 图 4可见,在 -0.3~0.6 V内均出现氧化还原峰。由于BMC峰电位差ΔEp > (59/n) mV,峰电流之比Ipc/Ipa ≈ 1,表明碳纳米管修饰电极在选定缓冲溶液体系中的 氧化还原反应为准可逆反应过程。在电位扫描范围 内未出现新峰,但氧化还原电流均下降,而峰电位基本不变,且随着BSA浓度的增加,峰电流的降低值随之增加。说明BMC和BSA结合形成没有电化学 活性的超分子化合物,使得BMC的电化学活性基团隐于BSA内部,使溶液中游离的BMC浓度下降,对应的氧化还原峰电流下降。实验表明,新构建的F-CNTs/GCE可用于研究BMC-BSA的相互作用。
 |
Figure 4 The cyclic voltammograms of BC-BSA,BMC-BSA in PBS (pH 7.5). PBS: Phosphate buffer solution |
以循环伏安法研究扫描速度对BMC氧化峰电 流和峰电位的影响,如图 5所示。图 5为扫描速度在50~350 mV·s-1之间BMC在F-CNTs/GCE上CV图。从图 5可见,BC和BMC的氧化峰电流 (Ipa) 与扫描速度 (v) 在50~400 mV·s-1之间呈良好的线性关系。根据Laviron理论[19],当循环伏安峰电流与扫描速率一次方有线性关系时,物质在电极上的吸附符合Langmuir吸附等温式 (11),即:
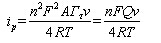
|
(11) |
其中Q = nFAΓτ ,为循环伏安单一过程的峰面积 (以电量计)。上式表明,无需知道电极表面吸附量及电极面积的绝对值,只需测得某扫描速率下循环伏安图上的峰面积即可求得n。本实验在100 mV·s-1扫速下测得BMC的氧化峰电流和峰面积,可得各物质参与电极反应的电子数n为2。
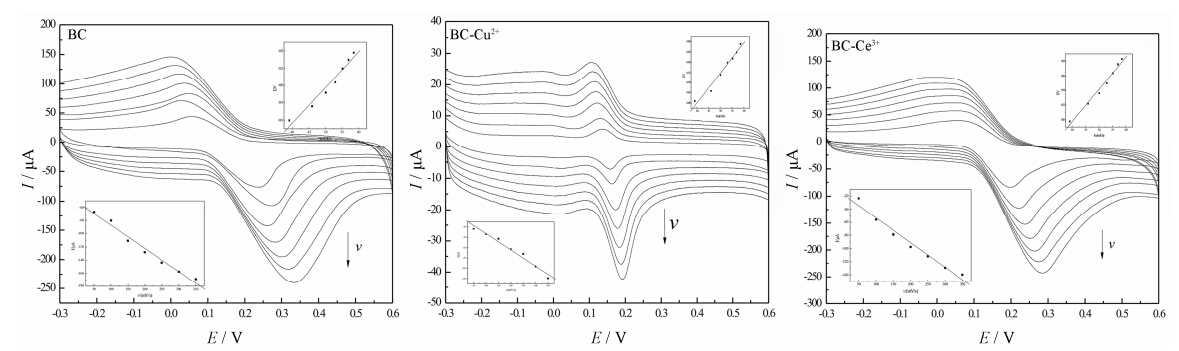 |
Figure 5 Cyclic voltammograms of BC or BMC at different scan rates. Scan rate: 0.05,0.1,0.15,0.2,0.25,0.3,0.35 V·s-1; CBC = 1.0×10-4 mol·L-1,CBMC = 1.0×10-4 mol·L-1. The CV curve of BC-Ni2+,BC-CO2+ similar as the BC-Cu2+; the CV curve of BC-La3+,BC-Y3+ similar as the BC-Ce3+ |
图 5表明BMC在F-CNTs/GCE上的电化学氧 化过程是受吸附控制的电极反应过程。由图 5可见,BMC的峰电位 (Epa) 和扫描速度 (lnv) 呈线性关系,线性方程列于表 3。根据Laviron理论,由斜率求出电子传递系数 (α),则电子转移速率常数 (ks) 可由公式 (12) 算出[20]:

|
(12) |
当v = 0.1 V·s-1时,计算各电极体系氧化峰电位及还原峰电位差ΔEp,获得ks,见表 3。
|
|
Table 3 Equation of the effect of scan rate on the oxidation peak potential of BMC (n = 7) |
当BMC与BSA相互作用后,同样获得Epa与lnv关系图,由斜率求得α,进而可计算得到ks,结果见表 4。
|
|
Table 4 Equation of the effect of scan rate on the oxidation peak potential of BMC-BSA (n = 7) |
通过实验和计算,BMC的电极反应电子数为2, 而BMC与BSA相互作用后,应用同样的方法计算BMC的电极反应过程电子转移数也为2,结果发现BC和BMC的电极反应过程电子转移数没有变化[21],说明无论BSA是否存在,BC和BMC的电极反应没有变化,只是体系游离的BC和BMC浓度降低,使峰电流降低,证明BMC与BSA作用后形成了一种非电化学活性的超分子化合物。
4 BMC与BSA结合反应机制的探讨BC属于黄酮类化合物,它的基本结构是两个芳香环 (A和C),由含氧六元环 (B) 连接而成 (图 6)。BC分子中的羟基在一定条件下可以被氧化,但因为羟基的空间位置不同,其氧化还原反应的活性和电化学可逆性差异较大,其中C环上两个邻羟基的电活性最大,是抗氧化作用的主要官能基团。由此可知,图 4的氧化还原峰为BC的C环上5,6位羟基发生 氧化还原反应而得到,进而可得电化学机制如图 6所示。结果表明,BSA的加入使得BC和BMC的峰电流降低,证明BC和BMC与BSA存在一定的相互作用。其可能的电化学反应机制推断如下: BSA的空间结构由3个结构域组成,每个结构域由2个亚结构域以槽口相对的方式形成圆筒状结构,几乎所有的疏水性氨基酸残基都包埋在圆筒的内部,构成疏水性腔[22]。当BSA加入到BMC体系中,BMC的电化学参数无显著变化。因此推断BMC与BSA作用后形成了一种非电活性的超分子化合物,BMC分子的部分结构片段会插入BSA分子内部,造成其活性基团被包埋于BSA的疏水腔内,而不易在电极上发生氧化还原反应,导致BMC的氧化还原峰电流降低。
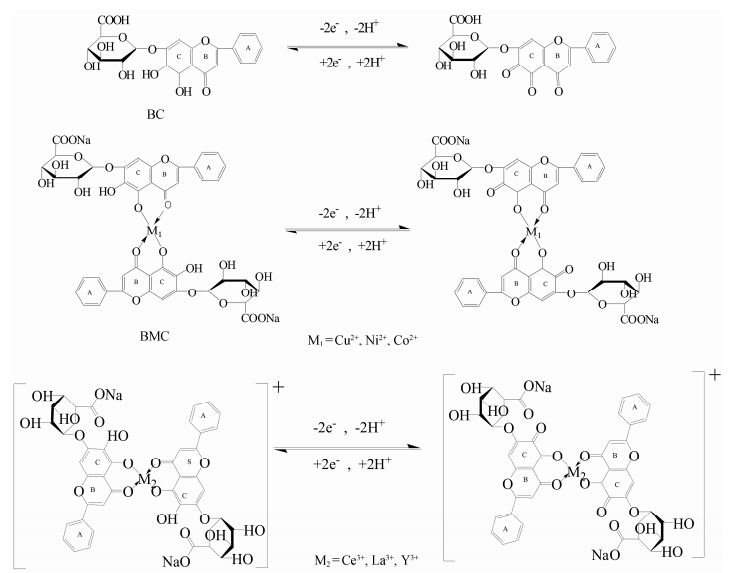 |
Figure 6 The redox reaction mechanism of BMC |
本文将碳纳米管修饰电极成功用于分析BMC与BSA相互作用机制,药物与蛋白质分子相互作用的药理过程中,宏观分析得出微观的实验结果与实际的药效机制存在一定的差别,但是,宏观的作用机制与体外药效实验分析也是药物与蛋白质分子相互作用研究中的内容,其可以从不同角度提供药物的药效及作用机制的诸多信息。结果显示,BMC与BSA相互作用前后电极反应过程中电子转移数未发生显著变化。表明BMC与BSA相互作用形成非电化学活性的超分子化合物,使氧化还原反应的峰电流下降。本文运用物理学等效电路模型结合相互作用原理,将不同研究领域知识交叉应用,建立了F-CNTs/GCE交流阻抗谱的等效电路模型,数据模拟分析获得电极体系电学阻抗谱等效电路模型为R1(CPE1(R2(CPE2(R3)))),计算等效电路各元件参数证明等效电路能有效模拟电极检测机制。本工作尝试将物理学中的等效电路应用于药物相互作用研究。本文所得结果也说明修饰电极能放大BMC与血清蛋白质分子非共价相互作用的反应信号,获得BMC-BSA的结合位点数在1.7左右,其中BC-Co2+-BSA的结合位点数最小 (1.3),其次为BC-Y3+-BSA的结合位点数为1.6,其他BMC-BSA与BC-BSA的结合位点数相同 (1.7)。BMC的电极反应过程电子转移数没有变化,说明无论BSA是否存在,BMC的电极反应没有变化,只是体系游离的BMC浓度降低,使峰电流降低,证明BMC与BSA作用后形成了一种非电化学活性的超分子化合物。本工作阶 段尚未发现不同金属形成的不同BMC与BSA的结合过程存在特征性差异,并不能完全肯定不存在,因此,关于BMC与BSA的相互作用还需进一步研究。BMC是一类很有前途的药物,目前,BMC在某些方面比BC具更高的活性,是否与金属离子产生的协同作用还需进一步研究,BMC的生物药剂学和药代动力学方面的研究也未见报道。本工作只通过电化学 的方法进行了BMC与BSA的结合机制分析,对以 后研究电化学与其他分析方法结合具有一定的参考价值。本阶段成果可为进一步研究BMC的药理作用机制提供理论前期基础,为生物活性分子/离子与蛋白质分子的相互作用机制提供了一种快速、简单和 有效的方法,对探讨非共价相互作用具有一定的参考价值。
| [1] | Orzechowska B, Chaber R, Wiśniewska A, et al. Baicalin from the extract of Scutellaria baicalensis affects the innate immunity and apoptosis in leukocytes of children with acute lymphocytic leukemia [J]. Int Immunopharmacol, 2014, 23: 558-567. |
| [2] | Chen HJ, Gao Y, Wu JL, et al. Exploring therapeutic potentials of baicalin and its aglycone baicalein for hematological malignancies [J]. Cancer Lett, 2014, 354: 5-11. |
| [3] | Tarahovsky YS, Kim YA, Yagolnik EA, et al. Flavonoid- membrane interactions: involvement of flavonoid-metal complexes in raft signaling [J]. Biochim Biophys Acta, 2014, 1838: 1235-1246. |
| [4] | Li DJ, Zhu M, Xu C, et al. Characterization of the baicalein- bovine serum albumin complex without or with Cu2+ or Fe3+ by spectroscopic approaches [J]. Eur J Med Chem, 2011, 46: 588-599. |
| [5] | Guo M, Wu ZL, Gao XY. Relationship between toxicity of baicalin-metal complexes on human hepatoma SMMC-7721 cells and interaction of baicalin-metal complexes with hepatoma cell DNA [J]. Chin J Pharm Toxicol (中国药理学与毒理学杂志), 2014, 28: 536-549. |
| [6] | Seyed DM, Panahi AV, Rasoulifard MH. Interaction between deferiprone and human serum albmin: multi-spectroscopic, electrochemical and molecular docking methods [J]. Eur J Pharm Sci, 2014, 20: 9-17. |
| [7] | Yu ZQ, Dong SY, Huang TL, et al. Electrochemical studies on interaction between quercetin and bovine serum albumin at different pH [J]. Chem World (化学世界), 2010, 51: 135-139. |
| [8] | Hu XJ, Li YZ, Xiong YD, et al. Progress of study on interaction of small molecules with bovine serum albumin by spectroscopy [J]. Phys Test Chem Anal (Part B: Chem Anal) (理化检验 (化学分册)), 2010, 46: 583-588. |
| [9] | Knmari M, Maurya JK, Tasleem M, et al. Probing HAS-ionic liquid interaction by spectroscopic and molecular docking methods [J]. J Photochem Photobiol B: Biol, 2014, 138: 27-35. |
| [10] | Li Y, Ma X, Lu GH. Systematic investigation of the toxic mechanism of difenoconazole on protein by spectroscopic and molecular modeling [J]. Pesticide Biochem Physiol, 2013, 105: 155-160. |
| [11] | Pei MY, Zheng XF, Cao HY, et al. Spectroscopic studies on interaction between 3-bromopyruvic acid and human serum albumin [J]. Chin J Anal Chem (分析化学), 2010, 38: 948- 952. |
| [12] | Jiang XY, Li WX, Chen JW. Binding of quercetin, myricetin with bovine serum albumin in the presence of Zn2+ [J]. Chin J Inorg Chem (无机化学学报), 2008, 24: 1588-1595. |
| [13] | Suprum EV, Shumyantseva VV, Archakov AI. Protein electrochemistry: application in medicine. A review [J]. Electrochim Acta, 2014, 140: 72-82. |
| [14] | Zhao Y, Hong B, Fan LZ. Electrodeposition of gold nanoparticle clusters on multi-wall carbon nanotubes and the direct electrochemistry of hemoglobin [J]. Acta Chim Sin (化学学报), 2013, 71: 239-245. |
| [15] | Yan JX, Guan HN, Yu J, et al. Acetylcholinesterase biosensor based on assembly of multiwall carbon nanotubes onto liposome bioreactors for detection of organophosphates pesticides [J]. Pesticide Biochem Physiol, 2013, 105: 197-202. |
| [16] | Li JH, Kuang DZ, Feng YL, et al. Preparation of glucose biosensor based on the nanocomposite film of titanium dioxide/ carbon nanotubes/chitosan [J]. Chin J Inorg Chem (无机化学学报), 2011, 27: 2172-2178. |
| [17] | Guo M, Wu ZL, Wang CG, et al. Synthesis and anti-tumor activity of baicalin-metal complex [J]. Acta Pharm Sin (药学学报), 2014, 49: 337-345. |
| [18] | Zhao XF, Jiang Q, Guo YN, et al. Effect of synthesis scanning rate on the electrochemical capacitance of the PANI/CNTs composite [J]. J Funct Mater (功能材料), 2010, 41: 139- 143. |
| [19] | Laviron E. General expression of the linear potential sweep voltammogram in the case of diffusionless electrochemical systems [J]. J Electroanal Chem Interfac Electrochem, 1979, 101: 19-28. |
| [20] | Zhang ZX, Wang EK. Principles and Methods of Electrochemistry (电化学原理与方法) [M]. Beijing: Science Publishing Company, 2000: 439. |
| [21] | How GT, Pandikumar A, Ming HN, et al. Highly exposed {001} facets of titanium dioxide modified with reduced grapheme oxide for dopamine sensing [J]. Sci Rep, 2014, Article number: 5044. |
| [22] | Yu XY, Liao ZX, Yao Q, et al. The investigation of the interaction between tropicamide and bovine serum albumin by spectroscopic methods [J]. Spectrochim Acta Mol Biomol Spectros, 2014, 118: 331-336. |
 2015, Vol. 50
2015, Vol. 50


