胃排空速度对口服药物的吸收和代谢有明显影响,通过评价药物在胃中的排空速度不仅可以反映其吸收速度,还能够在一定程度上为其代谢动力学研究提供依据。目前评价胃排空的方法主要有插管法、放射学法、对乙酰氨基酚吸收实验、胃磁图、实时超声、上腹阻抗测定、呼吸实验、磁共振成像术、核素显像法等。每种方法都各有优缺点,其中放射学法被认为是目前检测胃排空的金标准,但需多次暴露于X射线而使检查受限。对乙酰氨基酚吸收法是一种安全、简单、经济的方法,已被证实能够准确反映胃排空,且易被受试者接受[1, 2]。
对乙酰氨基酚 (扑热息痛) 是临床上广为应用的一种苯胺类解热镇痛药,口服后在胃内几乎不吸收,小肠吸收迅速而完全,即其吸收速度取决于经胃排空速度。因此,测定小鼠血清对乙酰氨基酚浓度能够间接反映其胃排空功能[3]。早在上世纪90年代,Feng等[4]就将该方法应用于糖尿病患者的胃轻瘫诊断,并以此评价红霉素对其胃排空的影响。此外,Sanaka等[5]通过比较人唾液和血浆中对乙酰氨基酚的药代动力学参数,发现测定唾液对乙酰氨基酚浓度也是一种评价胃排空的方法。
胰高血糖素样肽-1 (glucagon-like peptide-1,GLP-1) 是目前开发抗糖尿病药物的重要靶点,已有Exenatide、Liraglutide和Lisexnatide等先后上市。文献[6, 7, 8]已证实该类药物能够明显抑制胃排空。对乙酰氨基酚吸收法也被应用于评价该类药物对胃排空的影响,主要以血清对乙酰氨基酚浓度曲线、达峰时间和药时曲线下面积 (AUC) 作为评价指标。
目前关于血清 (浆) 对乙酰氨基酚浓度的测定主要采用高效液相色谱法。毕小平等[9]基于对乙酰氨基酚本身荧光较弱,在弱碱性条件下经光化学反应后荧光强度明显增加的现象,采用光化学荧光法测定血浆对乙酰氨基酚浓度。Maida等[10]采用酶法测定小鼠血清对乙酰氨基酚浓度,评价二甲双胍对小鼠胃排空的影响。本文为采用重氮化法测定血清对乙酰氨基酚浓度的方法学研究。主要原理为: 对乙酰氨基酚在酸性条件下水解生成对氨基苯酚,然后与亚硝酸钠发生重氮化反应生成重氮化合物,在312 nm处有特异吸收峰,最后以312 nm处吸收度与对氨基苯酚浓度绘制标准曲线,计算对乙酰氨基酚浓度。此外,本研究还采用该方法测定小鼠血清对乙酰氨基酚浓度,计算AUC,评价新型长效GLP-1类似物GW002对小鼠胃 排空的影响,并采用经典碳素墨汁迁移法对其进行验证。
材料与方法 实验材料与仪器正常ICR小鼠 (雄性,体重20~22 g) 购自北京维通利华实验动物有限公司,许可证编号SCXK (京) 2002-0003,饲养于中国医学科学院药物研究所SPF级动物房。实验材料包括对乙酰氨基酚对照品 (中国食品药品检定研究院)、0.5和1 mol·L-1盐酸、2% 亚硝酸钠溶液、2% 尿素溶液、20% 三氯醋酸 (TCA)。多功能酶标仪 (BIO-TEK)。GW002为一种将GLP-1的C端与人血清白蛋白 (human serum albumin,HSA) 的N端通过连接肽融合后产生的新型长效GLP-1类似物,由江苏泰康生物医药有限公司提供。
对乙酰氨基酚溶液精密称量对乙酰氨基酚1 mg,加入蒸馏水1 mL,于40 ℃水浴溶解,即含对乙酰氨基酚1 mg·mL-1,现用现配。
对氨基苯酚溶液精密称取对乙酰氨基酚25 mg,加入0.5 mol·L-1盐酸溶液40 mL溶解,于90 ℃ 水浴2.5 h,冷却至室温后转移至50 mL量瓶中定容,按对乙酰氨基酚计算即为500 μg·mL-1,棕色瓶4 ℃保存。
标准曲线吸取对氨基苯酚溶液 (500 μg·mL-1),用生理盐水倍比稀释为160、80、40、20和10 μg·mL-1的对照溶液及空白溶液,取50 μL加入0.5 mol·L-1 盐酸100 μL和2% 亚硝酸钠溶液25 μL反应(4 ℃) 5 min,加入2% 尿素溶液25 μL,振荡15 min,除去气泡,测定312 nm处吸收度值,拟合回归方程。
血清对测定的影响分别吸取空白血清、对乙酰氨基酚和对氨基苯酚溶液,配制含不同质量浓度对乙酰氨基酚和对氨基苯酚 (160、80、40、20、10、5和0 μg·mL-1) 的血清溶液适量,加入1/10体积TCA (20%) 振荡后静置15 min,4 000 r·min-1离心10 min; 取上清液,加入等体积1 mol·L-1盐酸,混匀,于90 ℃水浴加热2.5 h,4 000 r·min-1离心5 min; 取上清液 50 μL,按照以上步骤,测定312 nm处吸收度值,拟合回归方程。
回收率分别吸取空白血清、对乙酰氨基酚和对氨基苯酚溶液,配制含20、40和80 μg·mL-1对乙酰氨基酚和对氨基苯酚的血清溶液各3份,按照以上步骤去蛋白后进行重氮化反应,测定312 nm处吸收度值,计算回收率。
小鼠血清对乙酰氨基酚浓度的测定取对乙酰氨基酚1片 (0.5 g) 研磨加水混悬,定容至10 mL (50 mg·mL-1)。正常ICR小鼠10只,禁食过夜 (自由饮水) 后尾尖采血,灌胃对乙酰氨基酚 (500 mg·kg-1,10 mL·kg-1),于灌胃后0.25、0.5、1、1.5、2 h采血,6 000×g离心2 min,血清按照上述步骤去除蛋白和进行重氮化反应,测定312 nm处吸收度值。根据标准曲线计算血药浓度,并绘制药时曲线。
对乙酰氨基酚法评价GW002对小鼠胃排空的影响正常ICR小鼠随机分为两组: 一组皮下注射生理盐水作为正常对照组 (Nor,n = 10),一组皮下注射GLP-1类似物GW002 (9 mg·kg-1,n = 9) 作为给药组。各组小鼠禁食过夜 (自由饮水) 后尾尖采血,于给药后24 h灌胃对乙酰氨基酚 (500 mg·kg-1,10 mL·kg-1),0.5 和1 h后分别采血,6 000×g离心2 min,按照上述步骤测定312 nm处吸收度值。根据标准曲线计算血药浓度,绘制药时曲线并计算AUC。
经典碳素墨汁迁移法验证GW002对小鼠胃排空的影响两组正常ICR小鼠 (给药和处理同前),于给药后24 h灌胃碳素墨汁 (10 mL·kg-1),15 min后脱颈椎处死,分离小肠,测量小肠的长度和碳素墨汁在小肠中的迁移长度,计算碳素墨汁在小肠中的迁移率。碳素墨汁迁移率 = (碳素墨汁在小肠中的迁移长度/小肠的长度)×100。
统计学分析所有数据均以均值±标准差表示,相关数据以t检验进行统计学分析,P < 0.05表示数据间有统计学差异。
结果 1 方法学考察 1.1 标准曲线对乙酰氨基酚水解产物对氨基苯酚在0~160 μg·mL-1内发生重氮化反应的线性关系良好,回归方程为y = 0.018 1 x + 0.010 4,R2 = 0.999 7。
1.2 血清对对乙酰氨基酚和对氨基苯酚测定的影响含血清的对乙酰氨基酚及其水解产物对氨基苯酚在0~160 μg·mL-1内发生重氮化反应的线性关系良好,回归方程分别为y = 0.004 5 x + 0.046 2 (R2 = 0.998 2) 和y = 0.006 x + 0.037 4 (R2 = 0.998 9)。表明血清用约2% 三氯乙酸去除蛋白后不影响对乙酰氨基酚的测定。
1.3 血清中对乙酰氨基酚及其水解产物的回收率含血清的对乙酰氨基酚20、80和160 μg·mL-1的平均回收率为97.4%~116.7%; 其水解产物对氨基苯酚20、80和160 μg·mL-1的平均回收率为98.0%~110.8%,均符合生物样品分析的要求。
2 在评价胃排空功能中的应用 2.1 正常ICR小鼠单次给予对乙酰氨基酚后血药浓度的测定正常ICR小鼠灌胃对乙酰氨基酚 (500 mg·kg-1) 后,其血药浓度迅速增加,在给药后30 min达峰,随后逐渐降低 (图 1)。因此,为减少动物个体差异和测定误差,在依据血清对乙酰氨基酚浓度评价药物对小鼠胃排空影响的实验中,分别在给予对乙酰氨基酚0、30和60 min时采血,测定其血清浓度,绘制药时曲线。
 |
Figure 1 The serum acetaminophen concentration-time curve in normal ICR mice. n = 10,x± s |
与正常对照组 (Nor) 相比,长效GLP-1类似物GW002给药后24 h,能够明显降低正常小鼠血清对乙酰氨基酚浓度及AUC值,降低幅度达28.4%。结果见图 2。
 |
Figure 2 Effect of GW002 on the gastric emptying of ICR mice evaluated through determination of serum acetaminophen. GW002: A prolonged GLP-1 analog. A: Blood acetaminophen concentration-time curve; B: Area under the concentration-time curve (AUC) of blood acetaminophen. n = 9,x± s. ***P < 0.001 vs Nor |
对小鼠胃排空的影响 与正常对照组 (Nor) 相比,GW002给药24 h后能够明显抑制碳素墨汁在正常小鼠小肠中的迁移长度和迁移率,抑制百分数分别为32.9% 和34.9%。与GW002对小鼠血清对乙酰氨基酚浓度-时间曲线下面积的降低百分数28.4% 基本一致。提示采用重氮化法测定血清对乙酰氨基酚浓度可以用于评价药物对胃排空的影响。结果见图 3。
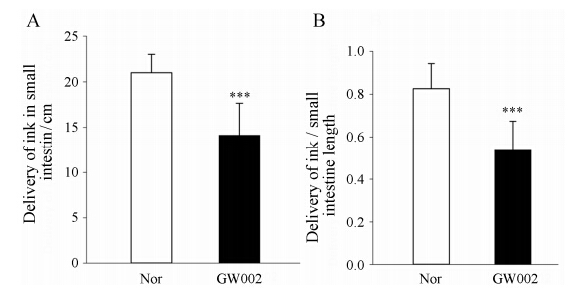 |
Figure 3 Effect of GW002 on the gastric emptying of ICR mice evaluated by the ink transferring method. A: Transferring length of ink; B: Relative transferring rate of ink. n = 10,x± s. ***P < 0.001 vs Nor |
对乙酰氨基酚在酸性溶液中水解后暴露芳伯胺基,在酸性条件下与亚硝酸钠发生重氮化反应,生成的重氮化合物在312 nm处有特征吸收峰。但是亚硝酸钠中亚硝酸根离子在特征峰后有明显杂峰,加入尿素反应可以消除该杂峰,使特征峰更加明显。一份专利[11]指出,对乙酰氨基酚在10% 盐酸中、90 ℃水浴加热2 h即可完全水解为对氨基苯酚。结合重氮 化反应所需的酸性条件,经过摸索,确定对乙酰氨基酚的水解条件为0.5 mol·L-1盐酸中90 ℃水浴加热2.5 h,重氮化反应后过量的亚硝酸采用尿素分解。
在血清样品的测定中,由于蛋白成分在90 ℃水浴加热变性,使溶液呈褐色,明显影响312 nm处吸收度,所以需要去除血清蛋白。本研究分别考察了无水乙醇 (1∶1) 和不同浓度三氯乙酸 (1%、2%、5%、10% 和15%) 的去蛋白效果及对血清样品回收率的影响,发现无水乙醇 (1∶1) 和2% 三氯 乙酸都能够明显去除血清中的蛋白成分,且回收率高。但采用无水乙醇沉淀蛋白后会有部分残留,增加了排除后续反应孔中气泡的难度,同时从成本考虑,最终采用2% 三氯乙酸。
采用该方法分别测定含有不同浓度对乙酰氨 基酚及其水解产物对氨基苯酚的血清样品,都具 有良好的回归曲线,回归系数 (R2) 分别为0.998 2和0.998 9,提示采用重氮化法测定血清对乙酰氨基酚浓度线性关系良好。回收率实验结果显示,该方法具有良好的准确性,可以用于血清对乙酰氨基酚的浓度测定。
对乙酰氨基酚具有一定肝毒性,且口服吸收迅速而完全,约45 min后血药浓度便开始下降。研究分别采用对乙酰氨基酚200、350和500 mg·kg-1灌胃给予正常ICR小鼠,观察各组动物均无明显异常; 采用重氮化法测定血清对乙酰氨基酚浓度,发现其血药浓度于给药后30 min达峰,随后逐渐降低 [30 min: (49.4 ± 5.2) μg·mL-1,60 min: (38.8 ± 4.2) μg·mL-1,120 min: (23.9 ± 3.6) μg·mL-1]。因此,确定对乙酰氨基酚的给药剂量为500 mg·kg-1,并分别于给药前 (0 min)、给药后30和60 min采血,测定其血药浓度,计算AUC,并以此作为指标评价药物对小鼠胃排空的影响。
研发长效GLP-1类似物是目前国内外开发抗糖尿病药物的重要手段之一,文献报道该类药物能够通过延缓胃排空发挥辅助降低餐后血糖的作用。GW002是一种新型的长效GLP-1类似物,在评价其单次给药对胃排空的作用及作用时程中,如果采用经典碳素墨汁迁移法,则需要使用多批动物分别在给药后不同时间处死动物分离小肠,而如果采用重氮化法测定血清对乙酰氨基酚浓度,则可以仅使用一批动物分别在给药后不同时间给予对乙酰氨基酚,不需处死动物。这样不仅可以减少动物的使用量,符合实验伦理学要求,还有利于动态监测药物对胃排空的影响。
| [1] | Näslund E, Bogefors J, Grybäck P, et al. Gastric emptying: comparison of scintigraphic, polyethylene glycol dilution, and paracetamol tracer assessment techniques [J]. Scand J Gastroenterol, 2000, 35: 375-379. |
| [2] | He XP, Zhu RM. Methods for measuring gastric emptying [J]. J Med Postgrad (医学研究生学报), 2003, 16: 389-390, 392. |
| [3] | Clements JA, Heading RC, Nimmo WS, et al. Kinetics of acetaminophen absorption and gastric emptying in man [J]. Clin Pharmacol Ther, 1978, 24: 420-431. |
| [4] | Feng B, Li Y, Li C. Acetaminophen absorption test for determination of diabetic gastroparesis and effects of erythromycin on gastric emptying [J]. Chin J Intern Med (中华内科杂志), 1996, 35:178-181. |
| [5] | Sanaka M, Kuyama Y, Nishinakaqawa S, et al. Use of salivary acetaminophen concentration to assess gastric emptying rate of liquids [J]. J Gastroenterol, 2000, 35: 429-433. |
| [6] | Jelsing J, Vrang N, Hansen G, et al. Liraglutide: short-lived effect on gastric emptying - long lasting effects on body weight [J]. Diabetes Obes Metab, 2012, 14: 531-538. |
| [7] | Ionut V, Zheng D, Stefanovski D, et al. Exenatide can reduce glucose independent of islet hormones or gastric emptying [J]. Am J Physiol Endocrinol Metab, 2008, 295: E269-E27. |
| [8] | Peixoto EML, Froud T, Gomes LS, et al. Effect of exenatide on gastric emptying and graft survival in islet allograft recipients [J]. Transplant Proc, 2011, 43: 3231-3234. |
| [9] | Bi XP, Xie Y, Zhang TQ, et al. Determination of plasma paracetamol by photochemical fluorescence method [J]. J Shanxi Med Univ (山西医科大学学报), 2007, 38: 1002-1004. |
| [10] | Maida A, Lamont BJ, Cao X, et al. Metformin regulates the incretin receptor axis via a pathway dependent on peroxisome proliferator-activated receptor alpha in mice [J]. Diabetologia, 2011, 54: 339-349. |
| [11] | Li JS, Yang Y. Determination of paracetamol based on the diazo coupling reaction: CN, 101446559A [P]. 2009-06-03. |
 2015, Vol. 50
2015, Vol. 50


