阿司匹林是乙酰水杨酸,相对分子质量180.16,一个非常简单的有机化合物,诞生一百多年来,仍然被广泛地应用,是个“神奇”的药物。
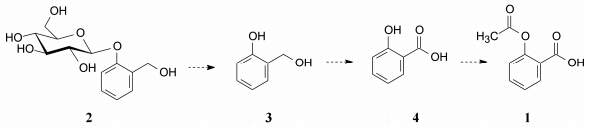
1 由天然产物水杨苷发明了阿司匹林阿司匹林 (1) 的诞生起源于水杨酸的解热止痛作用,后者可追溯到更久远的柳树皮的应用。早在古埃及的Ebers药书就记载了柳树皮的浸液可治疗风 湿痛,到18世纪确定浸液中的有效成分是水杨苷 (2,salicin),后来证明水杨苷在体内水解成葡萄糖和水杨醇 (3),水杨醇经体内氧化成水杨酸 (4) 而发挥解热止痛作用。
1897年德国拜耳药厂的化学家霍夫曼 (Felix Hoffmann) 合成了水杨酸的衍生物,纯化后首次得到乙酰水杨酸,其父率先用来治疗风湿性关节炎,表明仍有止痛效果,而对胃的刺激性低于水杨酸。1899年命名为阿司匹林 (aspirin),治疗疼痛和解热,在20世纪50年代成为销售非常成功的药物。但是到20世纪60年代,由于众多的解热镇痛药上市,应用阿司匹林日益减少。
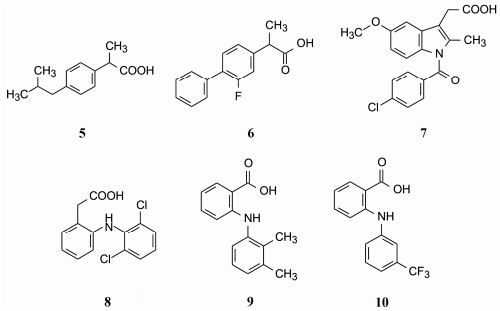
2 后继的非甾体抗炎药由水杨酸和阿司匹林的引领,研发出一批解热止痛药物,被称作非甾体抗炎药 (NSAIDs),例如芳丙酸类药物布洛芬(5,ibuprofen) 和氟比洛芬 (6,flurbiprofen); 芳乙酸类类吲哚美辛 (7,imdomethacin) 和双氯芬酸 (8,diclofenac); 氨基芳甲酸类甲芬那酸 (9,mefenamic acid) 和氟芬那酸 (10,flufenamic acid) 等数十种,作为解热镇痛药物,阿司匹林失去了原有的优势。
重新引起人们对阿司匹林的关注,是临床发现长期服用阿司匹林的人极少有冠状动脉阻塞和冠脉供血不足的症候,继之发现阿司匹林具有阻止血小板聚集,防止血栓形成的作用,这些与后来发现前列腺素、环氧合酶及其催化花生四烯酸代谢有密切关系。
1971年John Vane (1982年获诺贝尔奖) 发现了前列腺素,证明阿司匹林的作用是阻止前列腺素在体内的生成,是由于抑制了环氧合酶的缘故 (Shuker SB,et al. Science,1996,274: 1531)。环氧合酶是催化花生四烯酸合成前列腺素的酶系。
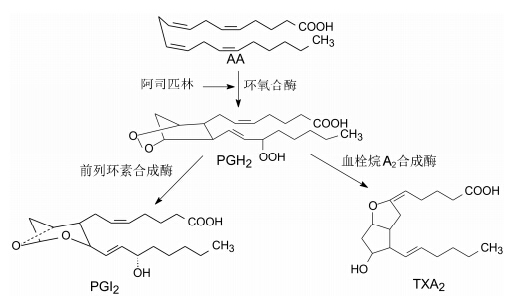
花生四烯酸 (AA) 是组成细胞膜磷脂的降解产物,在体内经过环氧合酶催化氧化,生成PGH2,再经一系列的生化反应,生成前列腺素 (PGs)、前列环素 (PGI2) 和血栓烷A2 (TXA2) 等 (图 1)。炎症细胞中含有大量的前列腺素,阿司匹林的抗炎作用在于抑制了前列腺素的生成。
|
图 1 阿司匹林抑制环氧合酶 |
阿司匹林抑制血小板聚集和血栓的生成是与PGI2和TXA2的生成相关。就引发冠状动脉疾患而言,PGI2具有舒张血管抑制血小板聚集的功能,是花生四烯酸“好的”代谢物; TXA2促进血管收缩和血小板聚集,是“坏的”代谢物,正常状态下,PGI2与TXA2的功能处于相互制约状态,维持血管的正常功能。阿司匹林抑制环氧合酶的功能,即使在低剂量下也阻断血栓烷的合成途径和血栓的形成,并且由于以不可逆方式抑制环氧合酶功能,TXA2的体内合成要等到新的环氧合酶生成后才发生。然而PGI2在其他组织仍可以产生,从而对抗和“压制”了TXA2的血栓形成。阿司匹林这个特异性功能开辟了预防性治疗心脏病和卒中的新适应证。据不完全统计,全球每年生产的阿司匹林4万吨以上。
4 阿司匹林的作用机制阿司匹林的解热止痛不是由于在体内水解成水杨酸而起效的,所以不是水杨酸的前药。它对环氧合酶的作用机制不同于水杨酸和其他NSAIDs。阿司匹林与环氧合酶发生共价键结合,是个不可逆抑制剂,而其他NSAIDs与环氧合酶都是可逆性结合。
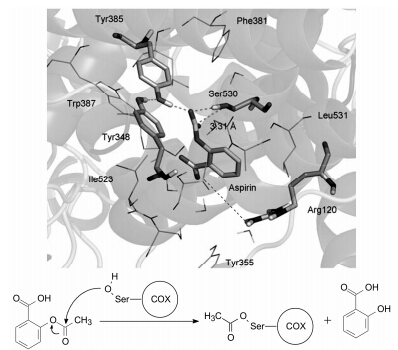
阿司匹林与环氧合酶的结合位点在花生四烯酸发生反应所处的通道内,苯环与Tyr348发生π-π叠 合作用; 1位的羧基与Arg120形成盐键 (其他非甾体抗炎药的羧基也形成盐键); 2位的乙酰基与丝氨酸残基Ser530先发生氢键结合,然后乙酰基转移到丝氨酸的羟基上,产生不可逆性结合 (图 2),乙酰化后的环氧合酶失去了催化功能,阻止了后续的级联反应 (Tosco P and Lazzarato L. ChemMedChem,2009,4: 939)。从有机化学反应分析,Ser530的羟基被阿司匹林的乙酰 (氧) 基酯化,即在脂肪醇羟基与酚羟基酯之间发生了不可逆性的酯交换,通常这是很难进行的有机反应 (充其量呈可逆的平衡态),但何以在环氧合酶的活性中心处发生?这是因为该不可逆反应的推动力 (driving force) 是诸多氢键、盐键、π-π相互作用,以及某些氨基酸残基的协同作用,不仅提高了乙酰基的亲电性,也提升了Ser530羟基的亲核性。烧瓶中的有机反应没有这样的微环境。
阿司匹林作为超小分子 (相对分子质量低于200) ,结构中没有冗余的原子,分子的每个组成部分都为参与结合和反应出力,因此阿司匹林具有不可复制性,上百年来没有类似的药物跟踪和超越,这个神奇的分子迄今无可替代。
|
图 2 阿司匹林与环氧合酶的结合图 |
 2015, Vol. 50
2015, Vol. 50
