2. 江苏省食品药品监督检验研究院, 江苏 南京 210008
2. Jiangsu Institute for Food and Drug Control, Nanjing 210008, China
银翘解毒系列制剂共有5个剂型8个品种,分别为片剂、丸剂 (蜜丸、浓缩蜜丸、浓缩水丸)、颗粒剂、胶囊剂 (胶囊、软胶囊)、合剂。处方均由金银花、连翘、薄荷、牛蒡子、荆芥、淡豆豉等9味中药材组成[1,2,3,4]。其中金银花为君药,其质量优劣直接影响银翘解毒系列制剂的药效。金银花的活性成分主要为新绿原酸 (a)、绿原酸 (b)、隐绿原酸 (c)、咖啡酸 (d)、异绿原酸B (e)、异绿原酸A (f) 以及异绿原酸C (g) 等酚酸类成分。银翘解毒系列制剂的现行质控标准不统一,仅通过测定绿原酸的含量来控制其金银花的质量存在一定的局限性。因此,有必要为银翘解毒系列制剂制定统一的金银花的质量控制方法。
多指标的质量控制模式需要对照品的种类和数量均比较大,且部分对照品价格较昂贵、不易得。王智民等[5,6]提出了一测多评的多指标质控模式: 在缺少对照品的情况下,同时测定具有相同的紫外吸收光谱的同类 (母核同类) 多成分,可以用其中易得的某一化合物来实现其他多个化合物的同步监控。本研究中上述7个酚酸类成分结构类似,紫外吸收光谱接近,绿原酸对照品易得、价格便宜,其他酚酸类成分价格昂贵、不易得,适合用一测多评法。目前国外文献已有报道,如美国药典USP37-NF32的红车轴草、圣约翰草等[7],欧洲药典EP8.0的草本紫锥花及根等[8],以及关于大黄[9]、丹参[10]等中药材的相关研究。国内一测多评法多用于单味中药材[11,12,13,14],中成药较少,尤其是中药复方制剂。迄今仅有咳喘宁[15]、麦贞花颗粒[16]、双青咽喉片[17]、银黄片[18]、冠脉康胶囊[19]、热痹消颗粒[20],未见有系列复方制剂的文献报道。银翘解毒系列制剂有8个品种,含9味药材。色谱图中除待测峰外,还存在许多非待测峰,这些峰往往位置紧邻,给待测峰的定位造成困难。目前普遍采用相对保留时间 (RRT) 来定位各待测峰,这种定位方法必须基于待测峰前后没有干扰峰,否则当色谱柱和仪器发生变换时,很难保证待测峰定位的准确性,银翘解毒系列制剂即属于此种情况。本研究采用金银花对照提取物作银翘解毒系列制剂的随行对照,解决了RRT定位法的不足,确保了在不同色谱柱和仪器情况下峰定位的准确性。
材料与方法 仪器与试药日本Shimadzu LC-20AB,Agilent 1260,Dionex Ulitimate 3000; 色谱柱: Kromasil C18 (250 mm × 4.6 mm,5 μm),Waters SunFire C18 (250 mm × 4.6 mm,5 μm),Shiseido C18 (250 mm × 4.6 mm,5 μm)。乙腈为色谱纯,其他试剂为分析纯,水为超纯水。
对照品a (PA0819RA13,纯度≥ 98%)、c (ZF0226BA14,纯度≥ 98%)、e (20120921,纯度≥ 98%)、f (20130816,纯度≥ 98%) 和g (20120302,纯度≥ 98%) 均为上海源叶生物科技有限公司产品; b (110753-201314,96.60%) 和d (110885-200102,五氧化二磷减压干燥12 h以上) 为中国食品药品检定研究院产品。本实验所用对照药材均由北京同仁堂科技发展股份有限公司提供,金银花对照提取物为中国药科大学李会军老师提供。银翘解毒胶囊 (20120602,东莞广发制药有限公司)、银翘解毒片 (121006,湖北广仁药业有限公司)、银翘解毒颗粒 (121107,四川同人泰药业有限公司)、银翘解毒合剂 (12260484,北京同仁堂科技发展股份有限公司)、银翘解毒软胶囊 (120303,江苏康缘药业股份有限公司)、银翘解毒丸 (浓缩丸) (201007003,九芝堂股份有限公司)、银翘解毒丸 (浓缩蜜丸) (20120801,九芝堂股份有限公司)、银翘解毒丸 (大蜜丸) (120034,佛山冯了性药业有限公司)。
色谱条件Kromasil C18 (250 mm × 4.6 mm,5 μm) 色谱柱; 流动相: A为乙腈,B为0.05% 磷酸溶液。梯度洗脱,0~25 min,9% A; 25~27 min,9%~14% A; 27~45 min,14% A; 45~50 min,14%~17% A; 50~60 min,17%~20% A; 60~70 min,20%~30% A; 70~80 min,30%~50% A; 80~85 min,50%~55% A; 流速1 mL·min-1,检测波长为328 nm,柱温35 ℃,进样量10 μL。理论板数按绿原酸峰计算应不低于30 000。
对照品溶液精密称取a、b、c、d、e、f和g对照品适量置20 mL棕色量瓶中,用50% 甲醇定容,制得质量浓度分别为0.156 70、0.484 40、0.158 05、0.015 78、0.160 65、0.491 25和0.211 30 mg·mL-1的混合对照品溶液。
供试品溶液取本品适量 (固体制剂),研细,胶囊取0.25 g,片剂取0.5 g,颗粒剂取2 g,丸剂取1 g,精密称定,置50 mL量瓶中,加50% 甲醇40 mL超声处理45 min后,加50% 甲醇定容,摇匀,高速离心 (10 000 r·min-1,10 min),即得。
取软胶囊适量,混匀,精密称定0.25 g,置100 mL锥形瓶中,加石油醚 (30~60 ℃) 10 mL,超声20 min,倾去石油醚,残渣挥干,精密加50% 甲醇50 mL,称重,超声处理45 min,用50% 甲醇补足减失的重量,摇匀,0.45 μm微孔滤膜滤过,即得。
取本品适量 (液体制剂),混匀,精密吸取5 mL,置50 mL量瓶中,加50% 甲醇稀释至刻度,摇匀,高速离心 (10 000 r·min-1,10 min),即得。
阴性对照品溶液按处方组成称取除金银花的剩余药材适量,按供试品溶液 (固体制剂) 方法制备阴性对照品溶液。
对照提取物溶液取对照提取物适量,按供试品溶液 (固体制剂) 方法制备对照提取物溶液。
外标法方法学考察 专属性精密吸取上述对照品溶液、供试品溶液与阴性对照溶液各10 μL,分别注入液相色谱仪,比较其色谱图。
线性关系考察依次将混合对照品溶液稀释50%、25%、12.5%、6.25% 和1.56%,配成系列混合对照品溶液。取上述6个浓度的混合对照品溶液,每个浓度进样2次,记录峰面积,以每个浓度峰面积积分平均值Y为纵坐标,对照品溶液浓度X (mg·mL-1) 为横坐标,进行线性回归。以信噪比10的进样质量为定量限 (LOQ),以信噪比3的进样质量为定量限 (LOD)。
精密度精密吸取同一浓度的混合对照品溶液连续进样6次,记录峰面积。
重复性取银翘解毒颗粒,按供试品溶液制备方法,平行制备6份,每份进样2次,记录峰面积,计算各成分的含量。
稳定性取同一份银翘解毒颗粒供试品溶液,分别于0、4、8、12、24、48 h重复进样,记录峰面积。
加样回收率取银翘解毒颗粒1 g,精密称定,置50 mL量瓶中,精密加入混合对照品溶液5 mL (a,0.048 16; b,0.143 22; c,0.060 12; d,0.003 716; e,0.021 41; f,0.017 41; g,0.057 00 mg·mL-1),按供试品溶液制备方法,平行制备6份,进样测定。
一测多评法 RCF的计算及确定本研究以b为内参物来计算a、c、d、e、f、g的RCF。取上述线性关系考察中的6个浓度对照品溶液的峰面积按下述公式计算所得的平均值作为定量用相对校正因子。
| ${\rm{RCF}} = \frac{{{C_{\rm{i}}}{\rm{/}}{A_{\rm{i}}}}}{{{C_{\rm{s}}}{\rm{/}}{A_{\rm{s}}}}}$ |
式中As为内参物峰面积,Cs为内参物的浓度,Ai为待测成分对照品峰面积,Ci为待测成分对照品 的浓度。
RCF耐用性考察分别考察Kromasil C18、Waters SunFire C18、Shiseido C18三根色谱柱在同一台Agilent 1260 HPLC上; 同一根Kromasil C18色谱柱在Shimadzu LC-20AB、Agilent 1260、Dionex Ulitimate 3000三台HPLC上; Waters SunFire C18在Shimadzu LC-20AB、Shiseido C18在Dionex Ulitimate 3000等各条件下6个浓度点的平均值的RCF。计算其RSD,并运用SPASS软件中的ANOVA分析不同HPLC、不同色谱柱间各成分的RCF是否有显著性差异。
色谱峰的定位① 相对保留时间 (relative retention time,RRT) 法: 取上述线性关系考察中的6个浓度对照品溶液注入液相色谱仪,记录各成分在Kromasil C18、Waters SunFire C18、Shiseido C18三根色谱柱在同一台Agilent1260 HPLC上的保留时间,计算a、c、d、e、f、g相对于b的RRT。以6个浓度的平均RRT为各色谱柱的RRT,计算各成分在3根色谱柱 上RRT的RSD。② 对照提取物法: 采用金银花对照提取物来进行色谱峰随行定位。考察Kromasil C18、Waters SunFire C18和Shiseido C18色谱柱在同一台Agilent 1260 HPLC上的色谱峰情况。
外标法与一测多评法含量测定结果比较考察了用外标法和一测多评法分别测定a、b、c、d、e、f和g在银翘解毒胶囊、银翘解毒片、银翘解毒颗粒、银翘解毒合剂、银翘解毒软胶囊、银翘解毒丸 (浓缩丸)、银翘解毒丸 (浓缩蜜丸)、银翘解毒丸 (大蜜丸) 中的含量。比较两种方法测定结果的相对平均偏差。
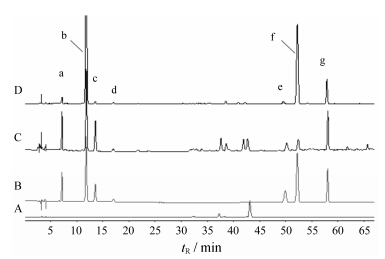
结果 1 外标法方法学考察 1.1 专属性测得色谱图如图 1所示。结果表明,阴性样品在7个目标成分的色谱峰位置无吸收,专属性良好。
|
Figure 1 HPLC chromatograms of negative sample without honeysuckle flower extract (A),reference substances (B),sample (C),honeysuckle flower (D). a: Neochlorogenic acid; b: Chlorogenic acid; c: 4-Caffeoylquinic acid; d: Caffeic acid; e: Isochlorogenic acid B; f: Isochlorogenic acid A; g: Isochlorogenic acid C |
结果见表 1。表明各成分标准曲线在线性范围内线性关系良好。
|
|
Table 1 The linear results of seven compounds |
7个化合物的峰面积RSD分别为0.36%、1.00%、0.98%、0.93%、0.42%、0.68%和1.35%。结果表明仪器的精密度良好。
1.4 重复性样品中7个化合物的平均含量分别为0.222 6、0.694 7、0.312 3、0.015 4、0.115 3、0.108 5和0.259 6 mg·g-1; RSD分别为0.82%、0.55%、0.46%、0.30%、0.87%、0.68% 和0.20%。结果表明本方法重复性良好。
1.5 稳定性7个化合物峰面积的RSD分别为0.94%、1.01%、0.71%、1.62%、0.53%、0.69% 和0.70%。结果表明供试品溶液在48 h内稳定性良好。
1.6 加样回收率7个化合物的平均加样回收率分别为99.57% (RSD = 1.16%)、100.39% (RSD = 1.05%)、99.69% (RSD = 0.68%)、100.63 (RSD = 1.77%)、96.85% (RSD = 0.79%)、99.88% (RSD = 1.38%) 和100.48% (RSD = 0.92%)。结果表明,本方法回收率良好。
2 一测多评法 2.1 RCF的计算及确定结果见表 2,a、c、d、e、f和g相对于b的RCF依次是1.088、1.109、0.592、0.940、0.871和0.799。
|
|
Table 2 Relative correction factors (RCF) of phenolic acids in Yinqiao Jiedu serial preparations |
各成分在不同色谱仪、不同色谱柱的RCF的RSD在0.80%~2.56%,小于3%。经ANOVA分析,在95% 的置信水平上,各成分P > 0.05。结果表明耐用性良好,不同色谱仪、不同色谱柱间各成分的RCF没有显著性差异。
2.3 色谱峰的定位 2.3.1 RRT法不同色谱柱间的RSD除a外,其他成分的RSD均大于3%,甚至有的超过50%。由于样品中杂质峰太多,采用RRT法很难进行准确定位各成分。
2.3.2 对照提取物法在不同色谱柱条件下,金银花对照提取物的7个峰均能与对照品完全吻合,表明该定位法准确。
3 外标法与一测多评法含量测定结果比较结果见表 3,表明两种方法在8个银翘解毒系列制剂中测得的各成分含量一致,相对平均偏差小于0.93%。因此,一测多评法可以成功用于8种银翘解毒系列制剂的含量测定。
|
|
Table 3 Comparison of result in Yinqiao Jiedu serial preparations by two methods. ES: External standard; QAMS: Quantitative analysis of multi-components by single-marker |
银翘解毒系列制剂为中药成方复方制剂,由于药味多,基质成分复杂,剂型间工艺和辅料不同,因此不同于单个品种的中药材,对于一测多评法的应用难度较大。本研究考察了不同浓度磷酸、不同梯度洗脱程序,结果表明在上述色谱条件下,8个银翘解毒系列制剂均具有良好的色谱行为,保证了含量结果的准确性和重复性,从而最终能建立统一通用的银翘解毒系列8个品种中君药金银花所含的7个酚酸类成分的测定方法。
本实验除上述RCF耐用性考察的3种色谱柱 外,还考察了另外两种常用C18柱,Shim-pack C18和Agela C18,结果也同样能获得良好的色谱分离行为,说明本实验建立的方法具有普适性。
有文献[11]表明使用一测多评法要满足RCF接近1。本研究中咖啡酸的RCF为0.592,但咖啡酸的含量在一测多评法和外标法间的相对平均偏差为0.93%,两种方法的含量测定结果具有一致性。表明有相同紫外吸收光谱的同类化合物其RCF与1相差较大时,一测多评法仍可适用。
采用一测多评法时需要进行色谱峰定位,文献普遍采用RRT法来定位各待测峰,但不同品牌色谱柱下各成分的相对保留时间相差较大,无法准确定位。因此本研究在一测多评法中采用金银花对照提取物作为随行对照并应用于中药复方系列制剂中,定位准确,克服了RRT法的不足。
本研究建立的一测多评法可成功应用于药味多、基质成分复杂、剂型间工艺和辅料不同的银翘解毒系列制剂的8个品种中对金银花酚酸成分的质量控制,为该系列制剂的标准通用和统一奠定了基础。
| [1] | Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典) [M]. 2010ed. Part I. Beijing: China Medical Science Press, 2010: 1086-1091. |
| [2] | China Drug Administration. The National Standard for Traditional Chinese Medicines Assembly [Department of internal medicine, respiratory system] (国家中成药标准汇编 内科、肺系一 ) [M]. Beijing: People's Medical Publishing House. |
| [3] | Chinese Pharmacopoeia Commission. Prescription Preparations of Chinese (中药成方制剂第十四册) [M]. Vol 14. Beijing: China Medical Science Press. |
| [4] | Chinese Pharmacopoeia Commission. Prescription Preparations of Chinese (中药成方制剂第十九册) [M]. Vol 19. Beijing: China Medical Science Press. |
| [5] | Wang ZM, Qian ZZ, Zhang QW, et al. Technical guide of quantitative analysis of multi-components by single marker [J]. China J Chin Mater Med (中国中药杂志), 2011, 36: 657-658. |
| [6] | Wang ZM, Gao HM, Fu XT, et al. Multi-components quantitation by one marker new method for quality evaluation of Chinese herbal medicine [J]. China J Chin Mater Med (中国中药杂志), 2006, 31: 1925-1928. |
| [7] | The United States Pharmacopeial Convention. The United States Pharmacopoeia 37-National Formulary32 [M]. Vol 4. Baltimore: United Book Press, Inc., 2014: 5523-5541. |
| [8] | The Directorate for the Quality of Medicines & Health Care of the Council of Europe (EDQM). European Pharmacopoeia 8.0 [M]. Vol 1. Nördlingen: Druckerei C. H. Beck, 2014: 1357-1361. |
| [9] | Gao XY, Jiang Y, Lu JQ, et al. One single standard substance for the determination of multiple anthraquinone derivatives in rhubarb using high-performance liquid chromatography-diode array detection [J]. J Chromatogr A, 2009, 1216: 2118-2123. |
| [10] | Hou JJ, Wu WY, Da Juan, et al. Ruggedness and robustness of conversion factors in method of simultaneous determination of multi-components with single reference standard [J]. J Chromatogr A, 2011, 1218: 5618-5627. |
| [11] | Gao HM, Song ZH, Wang ZM, et al. Overview of the on quality evaluation model of traditional Chinese medicine—QAMS [J]. China J Chin Mater Med (中国中药杂志), 2012, 37: 405-416. |
| [12] | Fan CJ. Application situation of multi-components quantitation by one marker new method for quality evaluation and control of Chinese herbal medicine [J]. Pharm Clin Chin Mater Med (中药与临床), 2013, 4: 18-20. |
| [13] | He FC, Li SC, Zhao ZQ, et al. Simultaneous quantitative analysis of four lignanoids in Schisandra chinensis by quantitative analysis of multi-components by single marker [J]. Acta Pham Sin (药学学报), 2012, 47: 930-933. |
| [14] | Zhu JJ, Wang ZM, Kuang YH, et al. A quantitative method using one marker for simultaneous assay of ginsenosides in Panax ginseng and P. notoginseng [J]. Acta Pham Sin (药学学报), 2008, 43: 1211-1216. |
| [15] | Liu YL, Li DM, Feng L, et al. Simultaneous assay of five kinds of alkaloid in kechuanning tablets by quantitative analysis of multi-component by single marker [J]. Tradit Chin Drug Res Clin Pharmacol (中国新药与临床药理), 2012, 23: 464-468. |
| [16] | Liu ZH, Gu W, Chang XJ, et al. Quantitative analysis of polytype components in maizhenhua granules by QAMS [J]. Tradit Chin Pat Med (中成药), 2012, 34: 2342-2347. |
| [17] | He B, Liu Y, Yang SY, et al. Simultaneous determination of 10 constituents in Shuangqing Yanhou Tablets by HPLC-QAMS [J]. Chin Tradit Herb Drugs (中草药), 2013, 44: 657-658. |
| [18] | Lin YQ, Xu LH, Wang SH, et al. Quantitative analysis on multi-components by single marker for simultaneous determination of six caffeoylquinic acids in Yinhuang Tablets [J]. Chin Tradit Herb Drugs (中草药), 2012, 43: 706-710. |
| [19] | Zou GX, You XM, Zhang Y, et al. The application of the determination the components in Guanmaikang capsules [J]. China J Chin Mater Med (中国中药杂志), 2008, 33: 1828-1831. |
| [20] | Chen XB, Zhou QM, Liu S, et al. Applicability of QAMS in quality control of rebixiao granule [J]. Chin J Inform Tradit Chin Med (中国中医药信息杂志), 2013, 20: 60-63. |
 2015, Vol. 50
2015, Vol. 50


