脑缺血 (cerebral ischemia) 是一种发病率高、致残率高、死亡率高和复发率高的脑血管疾病。临床研究表明脑缺血与谷氨酸兴奋性毒性介导的神经细胞损伤密切相关[1, 2]。PC12细胞为大鼠肾上腺嗜铬细胞瘤 (rat adrenal pheochromocytoma) 分化的PC12细胞,具有典型的交感神经元细胞特征。应用谷氨酸诱导PC12细胞损伤,已成为研究脑缺血的一种常用体外模型。
藁本内酯 (Z-ligustilide,LIG) 是中药川芎的主要成分之一,而川芎是经典复方通窍活血汤的主要组成药材。通窍活血汤有活血化瘀,通络开窍之效,临床上对缺血性中风、偏头痛、脑外伤性耳鸣等疾病的防治和改善具有良好的效果,疗效确切。课题组前期研究发现,通窍活血汤含药血清对谷氨酸诱导PC12细胞的损伤具有很好的保护作用[3],并在给予通窍活血汤的脑缺血大鼠的脑脊液中检测到了藁本内酯的成分。该成分对心脑血管有较强的药理作用,如脑神经保护、扩张血管和抑制血管平滑肌增殖等[4, 5, 6, 7]。已有研究证实藁本内酯能明显减少脑缺血再灌注引起的脑梗塞体积,改善脑神经功能,并且能减轻大鼠皮层神经元和海马神经元细胞的损伤[8, 9]。本研究在此基础上,旨在研究藁本内酯对谷氨酸诱导PC12细胞凋亡的保护作用,并探讨其可能的作用机制。
材料与方法 主要试剂PC12细胞 (中国科学院上海生命科学研究院细胞资源中心)。藁本内酯对照品购自成都科曼斯特生物科技有限公司 (纯度 ≥98%),先用DMSO溶解浓度为32 µmol·L-1的母液,再用无血清培养基稀释至所需浓度 (DMSO终浓度 < 0.3%)。丁苯酞 (合肥兰旭生物科技有限公司),DMEM高糖培养基、胎牛血清 (HyClone公司),MTT (Sigma公司),Annexin V-FITC凋亡试剂盒、核/胞浆蛋白提取试剂盒 (上海贝博生物公司),Caspase-3抗体、Bax、Bcl-2 (Santa Cruz公司),FITC 标记羊抗小鼠IgG、FITC标记羊抗兔IgG (北京中山金桥生物技术有限公司)。
主要仪器ELX800UV酶标仪 (Bio-TEK公司); CK2型倒置显微镜 (日本Olympus公司)。
PC12细胞培养及细胞存活率检测细胞培养于含有10% 胎牛血清的DMEM,置于37 ℃、5% CO2的培养箱中培养。取对数生长期的PC12细胞,以细胞数1×105/mL接种于96孔培养板内 (100 μL/孔),常规培养24 h后,将细胞分为正常对照组、模型对 照组、阳性对照组和LIG预处理后加谷氨酸组。正常对照组采用DMSO溶剂对照,谷氨酸处理组又分为5、10、15、20和25 mmol·L-1剂量组,以选择合适的造模浓度。各组DMSO终浓度 < 0.3%。阳性对照组为丁苯酞 (3-n-butylphthalide,NBP,10 µmol·L-1),LIG预处理组分为1、5和15 µmol·L-1剂量组,预处理3 h。作用24 h后,每孔加入MTT (5 mg·mL-1) 20 μL,再培养4 h后,小心吸弃上清液,每孔加入DMSO 150 µL溶解沉淀物,振荡器混匀后,酶标仪490 nm测定吸光度 (A) 值。MTT法检测细胞的存活率。按下式计算,细胞存活率 (%) = A实验组 / A正常对照组 × 100%,实验重复3次。
藁本内酯对谷氨酸损伤后PC12细胞凋亡的影响Annexin V-FITC/propidium iodide (PI) 双染法检测细胞凋亡造模结束后,去除细胞培养液,胰酶消 化,PBS洗细胞3次,按试剂盒说明书进行Annexin V和PI染色,经流式细胞仪检测,每组3个样本,采用FCS 4流式软件分析细胞凋亡率。
细胞内Ca2+含量检测细胞内钙离子浓度采用荧光染料Fluo-3/AM荧光探针法。造模结束后,加入Fluo-3/AM染色液 (5 μmol·L-1) 与37 ℃培养箱避光孵育30 min,用PBS洗涤细胞3次,以充分去除未进入细胞内的荧光探针。在荧光显微镜下随机选取不同区域的3个视野,观察并拍照。
Western blot检测线粒体和胞浆中Cyt C、Caspase-3、Bax和Bcl-2蛋白的表达取对数生长期的PC12细胞种于培养瓶中,分组处理后,收集细胞。① 提取细胞总蛋白质: 每组加入含1% 苯甲基磺酰氟 (PMSF) 的蛋白裂解液,冰上裂解30 min后,离心30 min,取上清液。② 提取胞浆和线粒体蛋白: 按胞浆/线粒体蛋白分离试剂盒说明书操作。③ SDS-PAGE凝胶电泳分离蛋白质,将蛋白带转移到硝酸纤维素膜上,5% 脱脂奶粉封闭2 h,一抗Cyt C/Caspase-3/Bcl-2/Bax (mouse monoclonal IgG ,1∶1 000) 4 ℃孵育过夜,PBST (含0.1% Tween 20的PBS) 洗3次,每次 10 min。加入对应的二抗室温孵育1.5 h,PBST洗3次,每次10 min。采用化学发光方法显影、定影,经AlphaView SA软件分析蛋白表达。
统计学处理
实验数据以![]() ± s表示,采用SPSS 17.0统计软件进行数据分析。多组间均数比较采用单因素方差分析,两组间均数比较采用Student’s t-test的方法,以P < 0.05为差异具有统计学意义。
± s表示,采用SPSS 17.0统计软件进行数据分析。多组间均数比较采用单因素方差分析,两组间均数比较采用Student’s t-test的方法,以P < 0.05为差异具有统计学意义。
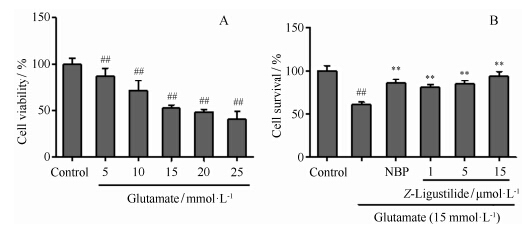
为选择谷氨酸损伤的最佳浓度,PC12细胞给予不同浓度的谷氨酸作用24 h。5~25 mmol·L-1谷氨 酸对PC12细胞活力呈剂量依赖的抑制作用 (图 1A)。在15 mmol·L-1谷氨酸作用下,PC12细胞的存活率为52.3%,因此选择15 mmol·L-1谷氨酸作为造模浓 度。但当藁本内酯 (1、5、15 µmol·L-1) 作用于损伤的PC12细胞后,细胞的存活率分别提高到80.0%、84.5% 和93.8% (图 1B)。
|
Figure 1 Effect of Z-ligustilide (LIG) on the viability of damaged PC12 cells elicited by glutamate. A: PC12 cells were treated with glutamate at concentrations of 5-25 mmol·L-1 for 24 h. B: PC12 cells were incubated with vehicle,LIG (1,5,15 μmol·L-1) or 10 µmol·L-1 3-n-butylphthalide (NBP) for 3 h,and then exposure to 15 mmol·L-1 glutamate for 24 h. The data are represented as means ± SD (n = 6). ##P < 0.01 vs control group; **P < 0.01 vs glutamate alone group |
为了定量检测藁本内酯对谷氨酸损伤的PC12细胞凋亡的影响,采用PI双染法检测细胞凋亡率。与正常对照组相比 (3.22%),谷氨酸单独给药组的细胞凋亡率为13.39%; 而藁本内酯给药组 (1、5、15 µmol·L-1) 使细胞的凋亡率减少到9.06%、6.48% 和3.82%。结果表明不同浓度的藁本内酯均可抑制谷氨酸诱导PC12细胞的凋亡。见图 2。

|
Figure 2 Effect of LIG on glutamate-induced PC12 cell apoptosis. Cells were incubated with different treatments,labeled with a combination of Annexin V-FITC/PI and measured by flow cytometry. (a) PC12 cells were incubated with culture medium only; (b) 15 mmol·L-1 glutamate alone; (c) 10 µmol·L-1 NBP + 15 mmol·L-1 glutamate; (d) 1 µmol·L-1 LIG + 15 mmol·L-1 glutamate; (e) 5 µmol·L-1 LIG + 15 mmol·L-1 glutamate; (f) 15 µmol·L-1 LIG + 15 mmol·L-1 glutamate. n = 3,x± s. ##P < 0.01 vs control group; **P < 0.01 vs glutamate alone group |
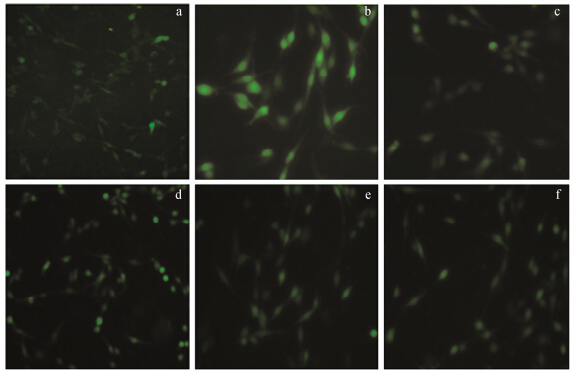
与模型对照组相比,正常对照组几乎见不到绿色荧光,而谷氨酸处理组绿色荧光非常强,藁本内酯干预后,绿色荧光减弱,表明藁本内酯可以抑制谷氨酸诱导所致PC12细胞钙离子的内流。见图 3。
|
Figure 3 Effect of LIG on glutamate-induced intracellular Ca2+ influx (magnification,×100). (a) PC12 cells were incubated with culture medium only; (b) 15 mmol·L-1 glutamate alone; (c) 10 µmol·L-1 NBP + 15 mmol·L-1 glutamate; (d) 1 µmol·L-1 LIG + 15 mmol·L-1 glutamate; (e) 5 µmol·L-1 LIG + 15 mmol·L-1 glutamate; (f) 15 µmol·L-1 LIG + 15 mmol·L-1 glutamate |
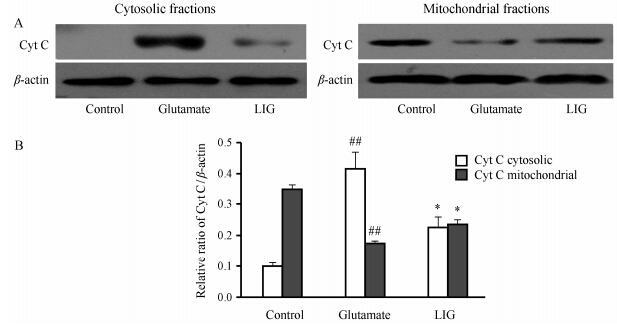
Western blot结果表明,正常对照组Cyt C主要 表达在线粒体中,线粒体中谷氨酸组Cyt C漏出量明显增多,而藁本内酯给药组Cyt C漏出量较谷氨酸组明显减少; 胞浆中谷氨酸组Cyt C表达明显增多,而藁本内酯给药组Cyt C表达较谷氨酸组明显减少。见图 4。
|
Figure 4 (A) Effect of LIG (15 µmol·L-1) on the expression levels of Cyt C in mitochondrial and cytosolic fractions of PC12 cells. (B) show densitometry analysis for the data from (A). n = 3,x± s. ##P < 0.01 vs control group; P < 0.05 vs glutamate (15 mmol·L-1) alone group |
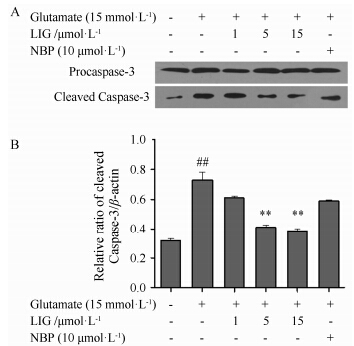
Western blot结果表明,正常对照组的活化Caspase-3 (cleaved-Caspase-3) 无表达,而谷氨酸组的活化Caspase-3表达明显上调,藁本内酯给药组的活化Caspase-3的表达与模型组相比显著降低 (图 5)。
|
Figure 5 (A) LIG suppressed glutamate-induced expression of cleaved-Caspase-3 in PC12 cells. (B) showed densitometry analysis for the data from (A). n = 3,x± s. ##P < 0.01 vs control group,**P < 0.01 vs glutamate alone group |
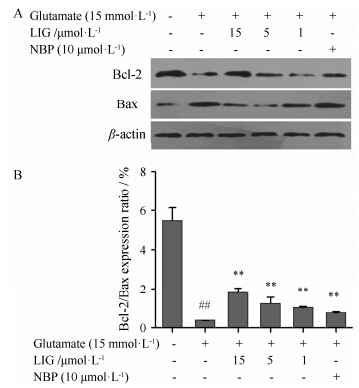
Western blot结果表明,与模型对照组相比,藁本内酯给药组的Bcl-2/Bax比率明显增高 (图 6)。结果表明,藁本内酯通过降低促凋亡蛋白Bax的表达和增加抗凋亡蛋白Bcl-2的表达抑制谷氨酸诱导的PC12细胞凋亡。
|
Figure 6 (A) Effect of LIG on the expression levels of Bcl-2 and Bax in PC12 cells. (B) showed densitometry analysis for the data from (A). n = 3,x± s. ##P < 0.01 vs control group,**P < 0.01 vs glutamate alone group |
谷氨酸是中枢神经系统中一类重要的兴奋性氨基酸 (excitatory amino acid,EAA),脑缺血时谷氨酸浓度的异常升高可过度激活离子型谷氨酸受体,引起细胞内钙离子浓度持续升高,导致“钙超载”现象发生,继而引起DNA损伤和细胞凋亡的级联反 应[10, 11]。已证实藁本内酯对缺血性脑损伤具有神经保护,而与藁本内酯具有相似化学结构的丁苯酞,是中国医学科学院药物研究所研制并开发的一类新型且具有前景的抗脑缺血药物,对急性缺血性脑卒中具有明显的疗效[12, 13]。已有研究证实丁苯酞能抑制神经细胞凋亡,保护缺血缺氧引起的神经细胞损伤[14]。作为丁苯酞的衍生物,藁本内酯与其化学结构相似,因此选择丁苯酞作为阳性对照药。
脑缺血时,氧、葡萄糖等物质的运输受限,能量骤减后导致离子梯度不可维持、膜电位下降、膜去 极化,细胞内电压依赖的Ca2+ 通道被激活使得细胞外Ca2+ 进入细胞内,同时因能量耗竭使钙泵功能失调,导致细胞内Ca2+ 排除障碍造成钙超载,导致线粒体损伤,引起Cyt C自线粒体释放致胞浆,活化Caspase-3,诱导细胞凋亡[15, 16]。而本研究结果表明,藁本内酯能明显逆转谷氨酸诱导的PC12细胞中Ca2+ 浓度的升高。
在谷氨酸所致PC12细胞凋亡机制研究中,有3条已知的凋亡途径: 线粒体凋亡途径、死亡受体途径 和内质网途径,其中线粒体凋亡通路是主要的途径,同时线粒体在细胞凋亡的过程中起着至关重要的作用[17, 18, 19]。Bcl-2和Bax是Bcl-2家族中两个主要的成员,Bcl-2家族主要调节细胞的凋亡和坏死。Bax作为细胞损伤和刺激的传感器,一般位于胞浆中,当细胞受到损伤和刺激后,Bax可以构成跨线粒体外膜的孔,导致膜电位的降低和Cyt C及其他凋亡诱导因子的外流,并激活Caspase-3,同时破坏正常状态下具有抗凋亡功能的Bcl-2蛋白。而抗凋亡蛋白Bcl-2是一种重要的细胞内组分,通过阻断Cyt C自线粒体释放和Caspase-3聚集抑制Bax的过表达,并且联系线粒体外膜,稳定膜的渗透性,保护线粒体的完整性,进而抑制细胞凋亡[20, 21]。两者在线粒体途径中起到重要的调节作用。因此,Bax/Bcl-2的比值被视为与凋亡相关的重要指标。由此,本研究检测了Bax和Bcl-2的表达变化,结果表明,藁本内酯阻止了Cyt C从线粒体释放到胞浆,参与上调Bcl-2蛋白和下调Bax蛋白的表达并抑制Caspase-3蛋白的过表达。提示藁本内酯通过调节抗凋亡蛋白Bcl-2和促凋亡蛋白Bax之间的平衡,抑制Caspase-3的活化,从而发挥抗凋亡作用。
本实验从分子水平上阐明了藁本内酯的神经保护作用,该作用可能通过抑制细胞内钙离子内流,抑制Cyt C自线粒体的释放,诱导了抗凋亡蛋白Bcl-2蛋白的表达增加,抑制促凋亡蛋白Bax和Caspase-3的过表达,最终抑制谷氨酸诱导的PC12细胞凋亡。
| [1] | Yu XY, Sun L, Luo XY, et al. Investigation of the neuronal deathmode induced by glutamate treatment in serum-, antioxidant-free primary cultured cortical neurons [J]. Brain Res Dev Brain Res, 2003, 145: 263-268. |
| [2] | Li Z, Lin XM, Gong PL, et al. Effects of Gingko biloba extract on glutamate-induced [Ca2+]i changes in cultured cortical astrocytes after hypoxia/reoxygenation, H2O2 or L-glutamate injury [J]. Acta Pharm Sin (药学学报), 2005, 40: 213-219. |
| [3] | Wang N, Deng Y, Wei W, et al. Serum containing Tongqiaohuoxue decoction suppresses glutamate-induced PC12 cell injury [J]. Neural Regen Res, 2012, 7: 1125. |
| [4] | Zuo AH, Wang L, Xiao HB. Research progress studies on pharmacology and pharmacokinetics of ligustilide [J]. China J Chin Mat Med (中国中药杂志), 2012, 37: 3350-3353. |
| [5] | Peng B, Zhao P, Lu YP, et al. Z-Ligustilide activates the Nrf2/HO-1 pathway and protects against cerebral ischemia– reperfusion injury in vivo and in vitro [J]. Brain Res, 2013, 1520: 168-177. |
| [6] | Feng ZB, Lu YP, Wu XM, et al. Ligustilide alleviates brain damage and improves cognitive function in rats of chronic cerebral hypoperfusion [J]. J Ethnopharmacol, 2012, 144: 313-321. |
| [7] | Qi HY, Han YF, Rong JH. Potential roles of PI3K/Akt and Nrf2–Keap1 pathways in regulating hormesis of Z-ligustilide in PC12 cells against oxygen and glucose deprivation [J]. Neuropharmacology, 2012, 62: 1659-1670. |
| [8] | Guo J, Shang EX, Duan JA, et al. Determination of ligustilide in the brains of freely moving rats using microdialysis coupled with ultra performance liquid chromatography/mass spectrometry [J]. Fitoterapia, 2011, 82: 441-445. |
| [9] | Kuang X, Yao Y, Du JR, et al. Neuroprotective role of Z-ligustilide against forebrain ischemic injury in ICR mice [J]. Brain Res, 2006, 1102: 145-153. |
| [10] | Pakhomova ON, Gregory B, Semenov I, et al. Calcium-mediated pore expansion and cell death following nanoelec-troporation [J]. Biochim Biophys Acta, 2014, 1838: 2547- 2554. |
| [11] | Reynolds IJ, Hastings TG. Glutamate induces the produc-tion of reactive oxygen species in cultured forebrain neurons following NMDA receptor activation [J]. J Neurosci, 1995, 15: 3318-3327. |
| [12] | Zhang LH, Yu WH, Wang YX, et al. DL-3-n-Butyl-phthalide, an anti-oxidant agent, prevents neurological deficits and cerebral injury following stroke per functional analysis, magnetic resonance imaging and histological assessment [J]. Curr Neurovasc Res, 2012, 9: 167-175. |
| [13] | Li JM, Li Y, Ogle M, et al. DL-3-n-Butylphthalide prevents neuronal cell death after focal cerebral ischemia in mice via the JNK pathway [J]. Brain Res, 2010, 1359: 216-226. |
| [14] | Chang Q, Wang XL. Effects of chiral 3-n-butylphthalide on apoptosis induced by transient focal cerebral ischemia in rats [J]. Acta Pharm Sin (药学学报), 2003, 24: 796-804. |
| [15] | Szydlowska K, Tymianski M. Calcium, ischemia and excitotoxicity [J]. Cell, 2010, 47: 122-129. |
| [16] | Zhao Q, Wang S, Li Y, et al. The role of the mitochondrial calcium uniporter in cerebral ischemia/reperfusion injury in rats involves regulation of mitochondrial energy metabolism [J]. Mol Med Rep, 2013, 7: 1073-1080. |
| [17] | Yu LC, Wang N, Zhang YF, et al. Neuro-protective effect of muscone on glutamate-induced apoptosis in PC12 cells via antioxidant and Ca2+ antagonism [J]. Neurochem Int, 2014, 70: 10-21. |
| [18] | Wang CY, Zhang SP, Xu Y, et al. Effect of safflor yellow B on vascular endothelial cells injury induced by angiotensin-Ⅱ [J]. Acta Pharm Sin (药学学报), 2012, 47: 811-815. |
| [19] | Ma J, Chen HM, Yan XJ, et al. Astaxanthin inhibits sodium azide-induced cytotoxicity in hepatocyte L-02 cells probably by H+ transferring function [J]. Acta Pharm Sin (药学学报), 2011, 46: 521-526. |
| [20] | Fu JJ, Huang HQ, Liu JJ, et al. Tanshinone ⅡA protects cardiac myocytes against oxidative stress-triggered damage and apoptosis [J]. Eur J Pharmacol, 2007, 568: 213-221. |
| [21] | Zhao H, Yenari MA, Cheng D, et al. Bcl-2 overexpression protects against neuron loss within the ischemic margin following experimental stroke and inhibits cytochrome C translocation and Caspase-3 activity [J]. J Neurochem, 2003, 85: 1026- 1036. |
 2015, Vol. 50
2015, Vol. 50


