2. 军事医学科学院 野战输血研究所, 北京 100850
2. Institute of Transfusion, Academy of Military Medical Sciences, Beijing 100850, China
铅污染以及铅中毒对人体健康的危害已经受到广泛关注。铅是人体非必需元素,主要通过呼吸道、消化道进入人体吸收,能够在体内蓄积,对全身各系统和器官有毒性作用,主要影响神经、消化、血液系统,铅污染和铅中毒是需要重点解决的公共卫生问题[1,2]。在治疗方面,依地酸二钠钙被作为首选药物用于临床[3]。依地酸二钠钙治疗铅中毒有良好的疗效,但在络合铅的同时,也络合排出体内的锌、钙、锰、铁、铜等,会造成体内必需微量元素的平衡失调,出现毒副作用,最重要的毒副作用是锌缺失引起的肾损害。
新促排灵 (Zn-DTPA) 又名二亚乙基三胺五乙酸三钠锌盐,与促排灵 (Ca-DTPA) 同属氨羧络合剂,于2004年8月由美国FDA批准同时上市,用于进入放射性核素严重污染场所工作或停留前以及放射性核素沾染后的治疗[4]。Zn-DTPA与Ca-DTPA在体内能选择性地与放射性核素镧 (140La)、铈 (144Ce)、钷(147Pm)、镅(124Am)、钚(239Pu) 等的阳离子形成稳定性的可溶性络合物,很快经肾脏排出体外,从而减少了体内放射性物质的沉积量。由于Ca2+ 同DTPA的络合常数要小于Zn2+ [5],Ca-DTPA中DTPA更易于与核素的阳离子络合,因此其促排作用强于Zn-DTPA。但毒理学研究显示,Ca-DTPA易造成内源性的锌缺失,从而使得与锌有关的酶的活性受到严重的影响,其中包括DNA与RNA聚合酶、羧肽酶、碳酸酐酶等,可造成肝肾、肠黏膜的损伤和造血抑制等不良反应[6,7]。Zn-DTPA的安全性较高,虽也能造成锰和镁等微量元素的缺失,但不会引起缺锌而产生严重的毒副作用,其毒性约为Ca-DTPA的1/10~1/30[8]。
在前期的研究中,本课题组采用石墨炉原子吸收分光光度计法测定铅含量,考察了Zn-DTPA对慢性铅中毒小鼠的促排作用[9]。本实验建立了小鼠急 性铅中毒模型,通过给予Zn-DTPA等药物治疗,用ICP-MS测定小鼠全血、尿液、股骨和脑中铅的含量,观察对铅的促排效果,为Zn-DTPA应用于铅中毒治疗提供依据和用药方案参考。 材料与方法
仪器 Agilent 7700x电感偶合等离子体质谱仪 (美国Agilent公司); LX3-64-01离心机 (北京医疗仪器修理厂); SZ-93A自动双重纯水蒸馏器 (上海亚荣生化仪器厂); Adventurer AR3130/C电子天平 (美国OHAUS公司); ES-1000E电子天平 (长沙湘平科技发展有限公司)。
药品与试剂 三水合乙酸铅 (国药集团化学试剂有限公司,分析纯,批号20120911); 新促排灵注射液(Zn-DTPA,军事医学科学院放射与辐射医学研究所研制,批号: 0909071); 促排灵注射液 (Ca-DTPA,军事医学科学院放射与辐射医学研究所研制,批号: 20110301); 硝酸 (国药集团化学试剂有限公司,分析纯,批号20130904); 0.9% 氯化钠注射液 (石家庄四药有限公司,批号121214403); 乙酸 (国药集团化学试剂有限公司,分析纯,批号20080823)。
TritonX-100 (Sigma-Aldrich公司,批号101326085); 肝素钠 (国药集团化学试剂有限公司,批号F20100521); ICP-MS元素分析含铅标准溶液和内标混合溶液 (Agilent公司); 硝酸 (Sigma公司); 异丙醇 (色谱级,批号: H41B17,J.T Baker公司)。三蒸水 (自制),用 于配制所有标准溶液与样品溶液; 氩气和氦气纯度≥99.99%; 样品配制均使用塑料容器。
实验动物 SPF级昆明小鼠,共72只,雌雄各 半,体重16~18 g,购自北京华阜康生物科技股份有限公司,动物合格证号: SCXK-(京) 2009-0004。
溶液的配制 称取三水合乙酸铅0.366 g,用0.9% 氯化钠注射液溶解,超声5 min后,滴加2~3滴乙酸并定容至40 mL,配成5 mg·mL-1乙酸铅溶液。取Zn-DTPA注射液 (100 mg·mL-1),用0.9% 氯化钠注射液稀释为50 mg·mL-1的Zn-DTPA受试液。取Ca-DTPA注射液 (100 mg·mL-1),用0.9% 氯化钠注射液稀释为50 mg·mL-1 Ca-DTPA受试液。
模型的建立 将72只小鼠随机分为4组,每组18只,分别为正常对照组、染铅模型组、Zn-DTPA给药组、Zn-DTPA与Ca-DTPA联用组。正常对照组小鼠每天腹腔注射0.2 mL 0.9% 氯化钠注射液,其余各组小鼠一次性腹腔注射乙酸铅溶液,每只小鼠染铅1 mg。
给药处理 染铅4 h后开始给药,其中染铅模型组小鼠每日腹腔注射0.9% 氯化钠注射液; Zn-DTPA给药组小鼠每日腹腔注射Zn-DTPA,剂量为50 mg·mL-1,0.1 mL/10 g; Zn-DTPA与Ca-DTPA联用组小鼠第 1、3和5天腹腔注射Ca-DTPA,第2和4天注射Zn-DTPA,剂量均为50 mg·mL-1,0.1 mL/10 g。给药开始后即收集每天尿液,各组小鼠于第2、4和6天分别取出6只,摘眼球取全血,处死后解剖采集双侧股骨和脑。
样品的采集与保存 尿液: 用10 mL聚乙烯树脂管收集尿液,置于4 ℃冰箱保存,尽快后续处理。全血: 小鼠摘眼球取血后,将血样收集于涂有1% 肝素钠的2 mL EP管中,置于4 ℃冰箱保存,尽快后续处理。组织: 小鼠处死后,取双侧股骨和脑,用0.9% 氯化钠注射液进行清洗,将组织表面的血液洗尽,晾干,于 -20 ℃冰箱中冷冻保存。
样品处理 尿液: 用0.1% TritonX-100将尿液定容至一定体积,取适量,加入5% HNO3溶液消解并稀释至合适浓度。全血: 取一定体积的血样,加入适量的浓HNO3,水浴加热消解后,用三蒸水稀释定容至合适浓度。组织: 称取组织湿重。加入适量的浓HNO3,水浴加热消解后,用三蒸水稀释定容至合适浓度。
样品测定 应用Agilent 7700x电感偶合等离子体质谱仪,采用八极杆碰撞/反应池氦气碰撞技术进行铅元素的定量扫描分析。采用两路蠕动泵进样,一路进样试剂空白、标准溶液和样品溶液,另一路始终进样混合内标溶液 (锂、钪、锗、钇、铟、铽、铋),两路液体采用雾化前混合的方法。采用ICP-MS测定标准溶液的计数值,以铅元素与混合内标元素计数值的比值为纵坐标、浓度为横坐标绘制标准曲线。
标准曲线的制备 标准曲线1: 精密量取含铅的标准储备液适量,用5% 硝酸逐级稀释成浓度0、1、2、5、10、20和50 ng·mL-1的对照样品溶液。同时精密量取含铅标准储备液同法制备低、中、高3个浓度 (浓度分别为2、20和40 ng·mL-1) 的质量控制 (QC) 样品,标准曲线测定时同法随行制备溶剂空白样品,在选定的工作条件下,对样品进行测定。标准曲线1用于测定小鼠全血、双侧股骨和脑样品。
标准曲线2: 精密量取含铅的标准储备液适量,用5% 硝酸逐级稀释成浓度0、1、2、5、10、20、50、100、200和500 ng·mL-1的标准溶液样品。同时精密量取含铅标准储备液同法制备低、中、高3个浓度 (浓度分别为2、100和400 ng·mL-1) 的质量控制 (QC) 样品,标准曲线测定时同法随行制备溶剂空白样品,在选定的工作条件下,对样品进行测定。标准曲线2用于测定小鼠尿液样品。
精密度 从乙酸铅标准溶液中精密量取一系列溶液,分别加入至一定体积空白小鼠的尿液、全血、股骨和脑的消化液中,配制成低、中、高3个浓度的乙酸铅标准生物样品,于第0、3、6、9和12 h分别进样分析,考察日内精密度; 连续测定3天,得到日间精密度。
方法回收率 从乙酸铅标准溶液中精密量取一系列溶液,分别加入至空白小鼠的尿液、全血、股骨和脑组织中,按“样品处理”项下消解处理,配制成低、中、高3个浓度的乙酸铅标准生物样品,进样分析,计算方法回收率。
重复性 取同种生物样品的同一浓度样品重复进样6次,计算RSD。
统计处理 所有数据以 (x± s) 表示,Excel表格t检验。 结果 1 方法学考察 1.1 标准曲线和定量下限
由表 1可见,标准曲线的线性范围是根据预实验中不同生物样品中铅含量不同而设立的,其中尿液样品标准曲线范围为1~500 ng·mL-1,定量下限为1 ng·mL-1; 全血样品、骨组织和脑组织标准曲线范围为1~50 ng·mL-1,定量下限为1 ng·mL-1。
|
|
Table 1 Standard curves of lead in urine,blood,femur and brain of mice |
小鼠尿液、全血、股骨和脑中低、中、高3个浓度的铅样品的日内和日间精密度RSD均小于15%,结果表明铅在小鼠尿液、全血、股骨和脑中精密度良好,符合方法学的测试要求,方法稳定。 1.3 方法回收率
小鼠尿液、全血、股骨和脑中空白样品和低、中、高浓度铅标准加入样品的方法回收率均在75%~103% 内,符合方法学的测试要求,方法准确可靠。 1.4 重复性
同一个生物样品,重复6次,RSD均小于3%,符合ICP-MS分析体内样品方法的要求。 2 Zn-DTPA对小鼠铅含量的影响 2.1 对尿铅的影响
小鼠腹腔注射Zn-DTPA,连续给药5天,每天尿铅排出量如图 1A所示。给药后小鼠尿液中的铅排出量较染铅模型组有显著性提高 (P < 0.05),在给药的初始2天内,Zn-DTPA的排铅作用更明显。Zn-DTPA与Ca-DTPA联合用药的效果优于Zn-DTPA单独用药。
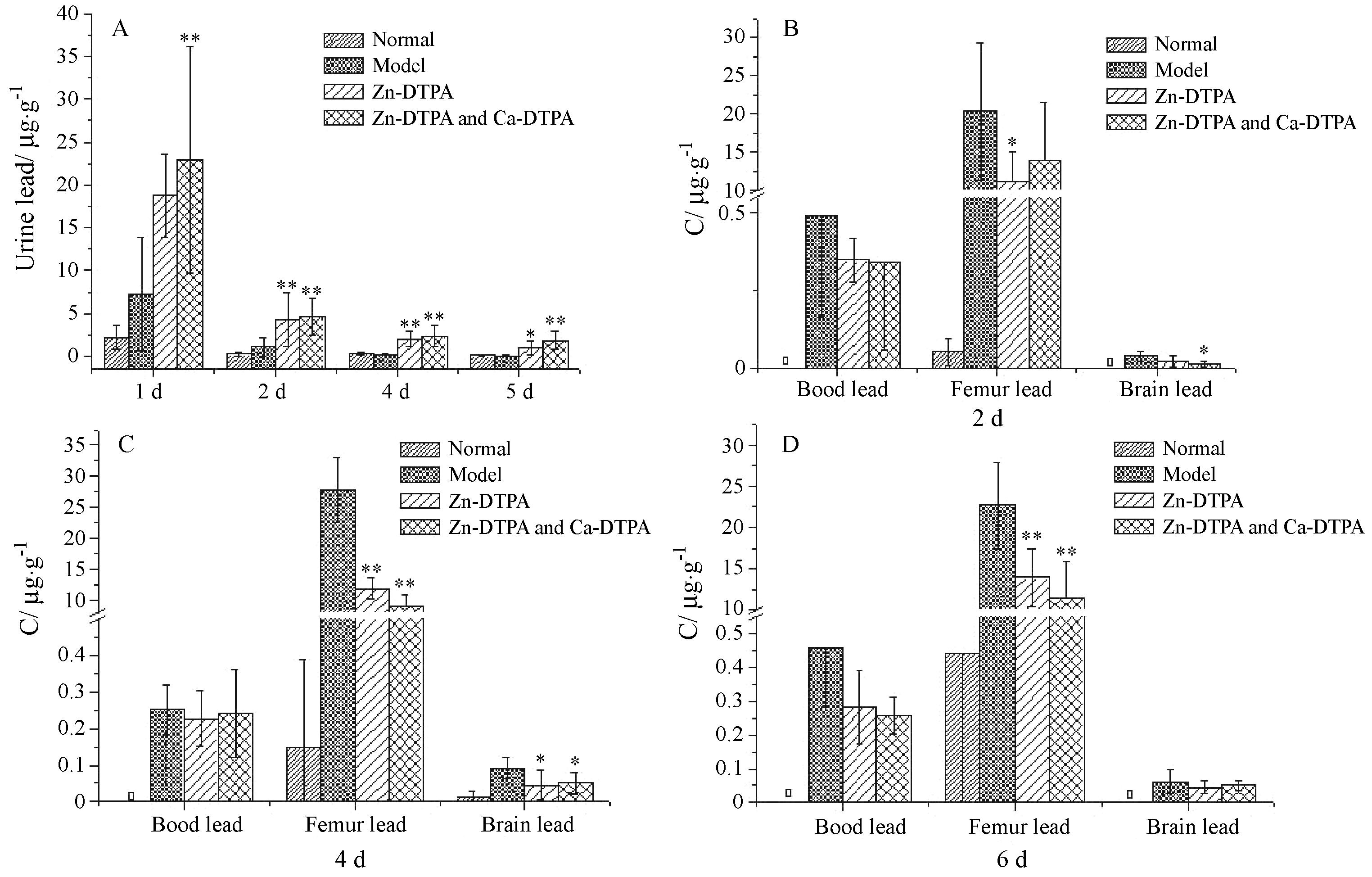 |
Figure 1 The effect of Zn-DTPA on lead content of mice. A: Urine lead of survived mice 1d (n = 18),2d (n = 12),4d (n = 6),5d (n = 6); B: Samples of mice killed at the second day (n = 6); C: Samples of mice killed at the fourth day (n = 6); D: Samples of mice killed at the sixth day (n = 6); P < 0.05,**P < 0.01 vs model. “0” represents no detected. x± s |
小鼠腹腔注射Zn-DTPA,连续给药5天,于第2、4和6天处死部分小鼠,小鼠血铅、骨铅和脑铅含量分别如图 1B、1C、1D所示。给药后小鼠血铅含量与染铅模型组相比较有降低,但没有显著性差异 (P > 0.05),Zn-DTPA与Ca-DTPA联合用药与Zn-DTPA单独用药相比,降低血铅的作用相当,差异不明显; 给药后小鼠骨铅含量与染铅模型组相比较有降低,在第4天和第6天处死的小鼠中,骨铅的降低有非常显著性差异 (P < 0.01)。提示Zn-DTPA可通过降低骨中铅的沉积并促进骨铅的释放和排出; 给药后小鼠脑铅含量与染铅模型组相比较有降低,在第4天处死的小鼠中,脑铅的降低有显著性差异 (P < 0.05)。 讨论
本文建立了小鼠急性铅中毒模型,观察了Zn- DTPA对急性铅中毒小鼠的促排铅的效果。结果表明Zn-DTPA可降低急性铅中毒小鼠血铅、骨铅和脑铅含量,与染铅模型组相比,对于骨铅和脑铅的降低有显著性差异。Zn-DTPA可显著增加尿中的铅含量,在给药的初始2天内,Zn-DTPA的排铅作用更明显。随着给药时间的延长,Zn-DTPA可通过降低骨中铅的沉积并促进骨铅的释放和排出。Zn-DTPA给药组和Zn-DTPA与Ca-DTPA联用组相比较,排铅作用相当,差异不明显。
以上研究结果表明,Zn-DTPA适宜单独用药治疗铅中毒,值得推广应用。Zn-DTPA用药时机很重要,越早使用,促排效果越明显。因为Zn-DTPA进入血液后能迅速地结合血液中的铅离子形成稳定性络合物,以尿铅的形式排出体外,从而降低血铅含量,使得进入骨和脑中的铅含量减少,减少了组织中的蓄积。Zn-DTPA安全性高,可以长期用药,为铅中毒治疗提供了一种更为安全的用药方案。
铅含量测定方法很多,除火焰原子吸收光谱法、氢化物发生原子吸收法、氢化物发生原子荧光法、双硫腙分光光度法和电感偶合等离子体质谱法外,还有荧光分光光度法、极谱法、电位溶出法。各种测定方法均有优点和不足。如火焰原子吸收光谱法不适合痕量分析。氢化物发生原子吸收法、氢化物发生原子荧光法灵敏度高,适合痕量分析但测定条件不易掌握。双硫腙分光光度法操作费时且使用试剂多不环保。随着仪器设备不断发展,ICP-MS测定生物样品 中铅的含量,具有灵敏度高、测量线性范围宽、分析简便快速等优点,并可进行血液、尿液中多元素同时分析,对复杂基体样品的分析具有很强的抗干扰能力。将成为铅测定的发展趋势[10,11]。通过ICP-MS技术分析生物样本中铅的含量,为核素促排药物的药效学研究提供了一定方法和参考。
| [1] | Hao FT, Du XQ, Niu YM, et al. Progress in research of the lead intoxication [J]. Chin J Ind Med(中国工业医学杂志), 2008, 21: 200-202. |
| [2] | Zhou QQ, Hu FF, Xia CY, et al. Study progress on health hazards in occupational lead-exposed workers [J]. Chin J Ind Med(中国工业医学杂志), 2013, 26: 353-356. |
| [3] | Zhou JY, Duan Z, Deng JX, et al. Clinical observation on chronic lead poisoning treated with different dosages of CaNa-EDTA [J]. Occup Health Emerg Resue(职业卫生与应急救援), 2002, 20: 159-160. |
| [4] | Cada DJ, Levien T, Baker DE. Pentetate calcium trisodium(Ca-DTPA)and pentetate zinc trisodium(Zn-DTPA)[J]. Hospital pharmacy, 2005, 40: 65-71. |
| [5] | Xue HL. The chelator treatment of common metal intoxication [J]. Chem Ind Occup Saf Health(化工劳动保护), 1989, 10: 22-26. |
| [6] | Shen BY, Ruan TM, Wu DC. Effect of Zn-DTPA on the decorporation of ultra-Uranium, ultra-Plutonium and Lanthanide and its application [J]. Foreign Med Sci(Radit Med Nucl Med)[国外医学(放射医学核医学分册)], 1988, 12: 70-74. |
| [7] | Zhao XC, Wu DC. Toxicity of DTPA and its application on the decorporation of nuclide [J]. Foreign Med Sci(Radit Med)[国外医学(放射医学分册)], 1980, 4: 211-215 |
| [8] | Zhang ZY, Xu XW, Zhu Z. Pentetate zinc trisodium [J]. Chin Pharm J(中国药学杂志), 2007, 42: 557-558. |
| [9] | Yang S, Chen L, Yin YY, et al. Study of the effect of pentetate zinc trisodium on excretion of lead in lead poisoned mice [J]. Pharm J Chin PLA(解放军药学学报), 2011, 27: 147-149. |
| [10] | Li JY, Shi L, Lu SH, et al. Progress of inductively coupled plasma mass spectrometry and its hyphenated techniques [J]. Chin J Inorg Anal Chem(中国无机分析化学), 2012, 2: 1-5. |
| [11] | He HL, Wang YF. Research progress of methods for lead determination [J]. Occup and Health(职业与健康), 2012, 28: 1395-1397. |
 2014, Vol. 49
2014, Vol. 49


