2. 海南师范大学化学与化工学院, 热带药用植物化学教育部重点实验室, 海南 海口 571158;
3. 西南大学生命科学学院, 重庆 400715;
4. 复旦大学药学院, 上海 201203
2. Key Laboratory of Tropical Medicinal Plant Chemistry of Ministry of Education, College of Chemistry and Chemical Engineering, Hainan Normal University, Hainan 571158, China;
3. School of Life Sciences, Southwest University, Chongqing 400715, China;
4. School of Pharmacy, Fudan University, Shanghai 201203, China
仁昌南五味子 (Kadsura renchangiana) 为五味子科 (Schisandraceae) 南五味子属 (Kadsura) 植物,主要分布于我国广西、贵州等地[1]。南五味子属植物常以果实或根茎入药,味辛微甘苦,性微温或平,主治风湿性关节炎、跌打损伤、胃和十二指肠溃疡、痛经、腹痛等疾病[2]。五味子科的主要成分联苯环辛烯类木脂素,具有抗肿瘤[3]、抗HIV[4,5,6]、抗肝损伤[7]、抗氧化[8]、抗脂质过氧化[9]、抑制Aβ42[10]和抗血小 板凝聚[11]等多方面生理活性。前期研究中,本课题 组从仁昌南五味子根茎中分离到4个新的联苯环辛烯类木脂素[12]和1个新的三萜类化合物[13]。进一步对仁昌南五味子根茎化学成分的研究,从中分离到 1个新的联苯环辛烯类木脂素,命名为仁昌南五味子戊素 (1)。 结果与讨论
将仁昌南五味子根茎95%乙醇提取物以乙醚萃取后,利用正相硅胶柱色谱及半制备HPLC分离得到一个新的联苯环辛烯类木脂素,命名为仁昌南五味子戊素 (1) (图 1)。
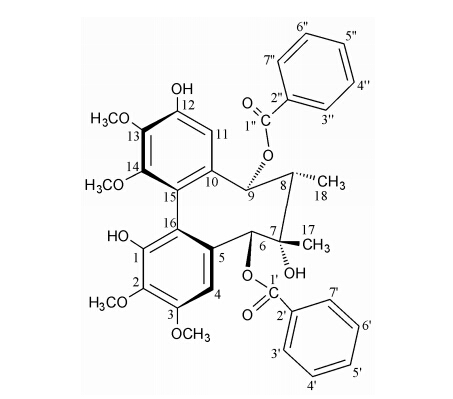 |
Figure 1 Structure of compound 1 |
化合物1为白色无定形粉末。HR-ESI-MS给出准分子离子峰m/z 667.214 85 [M+Na]+ (计算值为667.214 98),提示化合物的分子式为C36H36O11。紫外光谱 (UV) 显示在218、254、280 nm处分别有最大吸收。化合物1的1H NMR和13C NMR谱 (表 1)与tiegusanin D[14]相似,提示其为联苯环辛烯类木脂素。
|
|
Table 1 1H and 13C NMR data (400 and 100 MHz,respectively,in CDCl3) of compound 1 |
化合物1的1H NMR谱显示了1个单峰甲基信 号δH 1.44 (3H,s)、1个双峰甲基信号δH 1.42 (3H,d,J = 7.4 Hz) 和1个羟基信号δH 2.41 (1H,brs); δH 1.44的单峰信号提示与之相连的碳为季碳,HMBC谱 (图 2A) 上δH 2.41与δC 29.2的相关关系表明该季碳上 连接了羟基取代基; 两个甲基信号分别归属为CH3-17和CH3-18[12]。HMBC谱中,δH 6.05 (1H,s) 与δC 74.4 (C-7)、29.2 (CH3-17) 相关,δH 6.04 (1H,s) 与δC 43.6 (C-8)、17.7 (CH3-18) 相关,表明这两个H分别为H-6和H-9,且与含氧取代基相连,与已知化合物renchangianin A[12]相似。
 |
Figure 2 Key HMBC (A) and key ROESY correlations (B) of 1 |
1H NMR谱还显示了2个芳氢质子δH 6.89、δH 6.79 (各1H,s) 和4个甲氧基δH 4.00、3.40、3.30和3.21 (各3H,s) 信号。δH 6.05 (H-6) 与δC 107.5,δH 6.04 (H-9) 与δC 109.6的HMBC相关峰表明这两个碳信号分别为C-4和C-11。HMBC上H-4 (δH 6.79) 与δC 150.2和135.1相关,及H-11 (δH 6.89) 与δC 149.6和138.3相关表明这4个碳分别位于C-3、C-2、C-12和C-13。甲氧基δH 3.40、4.00、3.30和3.21分别与δC 135.1 (C-2)、150.2 (C-3)、138.3 (C-13)、148.9 (C-14) 的HMBC相关确定了甲氧基在苯环上的取代位置。
HSQC谱显示了2组质子信号δH 5.44和5.69 (各1H,brs),结合13C NMR谱在δC 100~102没有典型的亚甲二氧基碳信号,及红外光谱 (IR) 在3 431、3 568 cm-1,提示质子信号为苯环的2个羟基 取代基。由4组甲氧基分别在C-2、C-3、C-13和C-14上取代,故两个羟基分别在C-1和C-12取代,并由δH 5.44 (1-OH) 与δC 146.6 (C-1)、115.6 (C-16) 及δH 5.69 (12-OH) 与δC 149.6 (C-12)、109.6 (C-11) 的HMBC相关得到确认。
13C NMR谱还显示了12个芳香碳信号 (δC 127.8~132.9) 及羰基碳信号 (δC 164.2 × 2); 结合1H NMR谱显示了相应的10个芳香氢信号δH 7.26~7.51提示化合物中存在两个苯甲酰取代基。HMBC中 δH 6.04 (H-9) 及7.29 (H-3''/7'') 与酯基碳信号δC 164.2 (C-1'') 相关; δH 6.05 (H-6) 及δH 7.47 (H-3'/7') 与δC 164.2 (C-1') 相关,表明两个苯甲酰基分别是C-9和C-6上的取代基。HMBC显示了H-6与C-5 (δC129.2)和C-16 (δC 115.6),H-9与C-10 (δC 134.9) 和C-15 (δC 119.1) 的相关峰,以及ROESY谱中H-9与H-11的相关、H-6与H-4的相关 (图 2B) 进一步证实了两个苯甲酰取代基的位置。
化合物1的CD谱显示了在216 nm为 (-)-Cotton效应和252 nm为 (+)-Cotton效应,表明1为S-联苯结构[15]。ROESY谱H-4与H-6α、CH3-17与H-6,以及H-9β与H-11相关,表明环辛烯环为扭船椅式 (TBC) 构象。ROESY谱中其他H-11/H-9β、H-6α/H-4、H-6α/CH3-17、H-9β/8-H、OH-7α/H-6α、OH-7α/H-4、H-4/CH3O-2、H-11/H-8、HO-1/CH3O-2、HO-1/CH3O-14及HO-12/CH3O-13相关关系进一步确定了化合物1的取代位置和立体结构。综上所述,确定化合物1为 (aR,5S,6S,7S,8R)-5,8-dibenzoyloxy-5,7,8-trihydro-1,6,10-trihydroxy-2,3,11,12-tetramethoxy-6,7-dimethyl- dibenzo[a,c]cycloocten,命名为仁昌南五味子戊素,结构式见图 1。 实验部分
Avatar 360E.S.P型红外光谱仪 (美国Nicolet公司); UV-260型分光光度仪 (日本岛津公司); JASCO P-1020型旋光仪 (日本JASCO公司); JASCO J-715型圆二色谱仪 (日本JASCO公司); Bruker APEXⅢ 7.0 TESLA FTMS型高分辨质谱仪 (德国Bruker公司); Bruker DRX400型核磁共振仪 (德国Bruker公司,TMS为内标); Shimadzu LC-20A半制备型高效液相色谱仪 (日本岛津公司,检测器: UV); RP-C18 (YMC,10 μm,250 mm × 10 mm); 分析薄层色谱硅胶 (烟台市化学工业研究所); 柱色谱硅胶 (青岛海洋化工厂)。
仁昌南五味子药材于1997年9月采自广西壮族自治区龙胜县。由复旦大学药学院陈道峰教授鉴定 为K. renchangiana的干燥根茎,标本保存于复旦大学药学院生药学教研室植物标本室 (标本号: DFC- XT9701)。 1 提取与分离
干燥的仁昌南五味子根茎10 kg,粉碎,95%乙 醇室温下提取3次,合并提取液,减压浓缩,得到总浸膏650 g。将浸膏分散于1 L水中,用乙醚萃取7次,回收乙醚部分浓缩至干得190 g,再经硅胶色谱 (2 200 g) 分离,以石油醚-乙酸乙酯 (100∶0~0∶100) 梯度洗脱,得到15个组分 (Fr.1~15)。Fr.8 (石油醚-乙酸乙酯=7∶3) 经硅胶柱色谱,石油醚-乙酸乙酯洗脱 (10∶1~2∶1),得到4个亚组分。Fr.8-2经过半制备HPLC分离,流动相为甲醇-水 (30∶70),得到化合物1(3 mg,tR = 33.4 min)。 2 结构鉴定
化合物1 无定形粉末; [α]20D= +4.48 (c 0.174,MeOH); UV 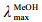 nm (logε): 280 (4.15),254 (4.09),218 (4.54); IR
nm (logε): 280 (4.15),254 (4.09),218 (4.54); IR 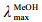 cm-1: 3 568,3 431,2 985,2 942,1 717,1 589,1 496,1 458,1 333,1 229,1 096,1 002,958,737; HR-ESI-MS m/z 667.214 85[M+Na]+ (calcd. C36H36O11Na,667.214 98); 1H NMR (400 MHz,CDCl3) 和13C NMR (100 MHz,CDCl3) 数据见表 1; CD
cm-1: 3 568,3 431,2 985,2 942,1 717,1 589,1 496,1 458,1 333,1 229,1 096,1 002,958,737; HR-ESI-MS m/z 667.214 85[M+Na]+ (calcd. C36H36O11Na,667.214 98); 1H NMR (400 MHz,CDCl3) 和13C NMR (100 MHz,CDCl3) 数据见表 1; CD 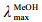 nm (Δε) 252 (-36.39),216 (+41.63)。
nm (Δε) 252 (-36.39),216 (+41.63)。
| [1] | Deng BL, Xie BX, Zhang C. Germplasm resources of Kadsura and their utilization in China (中南林业科技大学学报) [J]. J Central South Univ For Technol, 2008, 28: 90-94. |
| [2] | Dictionary of Chinese Traditional Medicines (中药大辞典) [M]. Shanghai: Shanghai People's Publishing House, 1977: 386-389, 1206-1207. |
| [3] | Chen M, Xu XM, Xu B, et al. Neglschisandrins E-F: two new lignans and related cytotoxic lignans from Schisandra neglecta [J]. Molecules, 2013, 18: 2297-2306. |
| [4] | Chen M, Kilgore N, Lee KH, et al. Rubrisandrins A and B, lignans and related anti-HIV compounds from Schisandra rubriflora [J]. J Nat Prod, 2006, 69: 1697-1701. |
| [5] | Yang GY, Wang RR, Mu HX, et al. Dibenzocyclooctadiene lignans and norlignans from fruits of Schisandra wilsoniana [J]. J Nat Prod, 2013, 76: 250-255. |
| [6] | Peng ZG, Xu LJ, Ye WC, et al. Effective components against HIV-1 replicative enzymes isolated from plants [J]. Acta Pharm Sin (药学学报), 2010, 45: 235-240. |
| [7] | Kuo YH, Wu MD, Huang RL, et al. Antihepatitis activity (anti-HBsAg and anti-HBeAg) of C-19 homolignans and six novel C-18 dibenzocyclooctadiene lignans from Kadsura japonica [J]. Planta Med, 2005, 71: 646-653. |
| [8] | Zhang LK, Chen HX, Tian JG, et al. Antioxidant and anti-proliferative activities of five compounds from Schisandra chinensis fruit [J]. Ind Crop Prod, 2013, 50: 690-693. |
| [9] | Yang XW, Hattori M, Namba T, et al. Anti-lipid peroxidative effect of an extract of the stems of Kadsura heteroclita and its major constituent, kadsurin, in mice [J]. Chem Pharm Bull, 1992, 40: 406-409. |
| [10] | Liu W, Yu R, Wu JH, et al. γ-Schisandrin inhibits production of amyloid β-protein 42 in M146L cells [J]. Acta Pharm Sin (药学学报), 2006, 41: 1136-1140. |
| [11] | Shi YM, Wang XB, Li XN, et al. Lancolides, antiplatelet aggregation nortriterpenoids with tricyclo [6.3.0.0 (2, 11)] undecane-bridged system from Schisandra lancifolia [J]. Org Lett, 2013, 15: 5068-5071. |
| [12] | Chen M, Liao ZX, Chen DF. Four new dibenzocyclooctene lignans from Kadsura renchangiana [J]. Helv Chim Acta, 2004, 87: 1368-1376. |
| [13] | Chen M, Chen DF. Renchanglactone A, a new triterpenoid lactone from Kadsura renchangiana [J]. Nat Prod Res, 2008, 22: 203-207. |
| [14] | Li XN, Pu JX, Du X, et al. Lignans with anti-HIV activity from Schisandra propinqua var. sinensis [J]. J Nat Prod, 2009, 72: 1133-1141. |
| [15] | Ikeya Y, Taguchi H, Yosioka I, et al. Constituents of Schizandra chinensis Baill.1. Isolation and structure determination of 5 new lignans, gomisin-a, gomisin-B, gomisin-C, gomisin-F and gomisin-G and the absolute structure of schizandrin [J]. Chem Pharm Bull, 1979, 27: 1383-1394. |
 2014, Vol. 49
2014, Vol. 49


