2. 南京农业大学动物医学院, 南京 210095;
3. 泰兴市鹏源养殖有限公司, 泰州 225400
2. College of Animal Medicine, Nanjing Agricultural University, Nanjing 210095, China;
3. Taixing Pengyuan Breeding Co. Ltd., Taizhou 225400, China
机体的氧化应激反应严重影响动物的繁殖性能,产蛋后期蛋鸡由于过度排卵,活性氧(ROS)大量积累,卵巢抗氧化能力减弱,卵泡闭锁增多,卵泡数量减少,加速了产蛋率的下降[1-2]。近年来,大量研究表明,饲粮中添加抗氧化剂可以减轻衰老引起的氧化应激,维持畜禽的繁殖能力。葡萄籽原花青素提取物可以增加衰老卵巢中的抗氧化酶活性及其基因表达来挽救抗氧化能力的下降,维持衰老卵巢中细胞增殖和凋亡之间的稳态[3]。虾青素可以提高蛋鸡的抗氧化能力,促进生殖激素的产生,通过降低卵泡闭锁来改善产蛋后期的繁殖性能[4]。戴宏建等[5]报道山楂叶黄酮可以通过提高蛋壳腺的抗氧化能力来提高产蛋后期种鸡的蛋壳品质。综上说明,通过提升蛋鸡抗氧化能力来延长产蛋周期、提升繁殖效率是可行的。
甜菜碱,又称三甲基甘氨酸,是一种高质量的饲料添加剂,在提高家禽生产性能、维持家禽健康状况等方面发挥重要作用。Omer等[6-7]研究发现,蛋鸡日粮中添加甜菜碱可以通过表观遗传调控肝的脂质代谢,促进肝中蛋黄前体物质的合成和释放,提升蛋鸡产蛋率。Shakeri等[8]发现,日粮中添加甜菜碱可以缓解热应激条件下肉鸡的氧化应激现象,提高谷胱甘肽过氧化物酶(GSH-Px)等抗氧化酶的活性。
颗粒细胞是卵泡内数量最多的细胞,参与激素的合成和分泌,并向卵母细胞传递信息,在卵泡的发育成熟过程发挥主要调控作用[9]。产蛋后期蛋鸡卵巢清除氧化物的能力减弱,日粮中添加甜菜碱是否通过缓解衰老蛋鸡卵巢的氧化应激及卵泡颗粒细胞微环境的变化来改善卵泡发育进而提升产蛋后期蛋鸡生产性能尚未有相关报道。因此,本研究在产蛋后期蛋鸡日粮中添加甜菜碱,研究其对产蛋后期蛋鸡生产性能和抗氧化能力的影响,为延长产蛋周期,提高经济效益提供参考。
1 材料与方法 1.1 试验设计与样品采集试验选取生理状态、产蛋率相近的108只海兰褐壳蛋鸡(500日龄),随机分为3组,每组3个重复,每个重复12只鸡。对照组饲喂基础日粮,试验组在基础日粮中分别添加1 000、3 000 mg·kg-1甜菜碱。基础日粮组成及营养成分见表 1。甜菜碱(C5H12NO2Cl含量≥98%)购自山东祥维斯生物科技股份有限公司。试验于2023年4月在江苏省泰州市泰兴市鹏源养殖有限公司进行。预试验1周,正式试验6周。试验期间,蛋鸡采用阶梯式笼养,自由采食和饮水,舍内光照维持16 h,黑暗8 h。每天7:00、13:30各饲喂1次。试验结束时,每组随机选取6只蛋鸡翅静脉采血,4 ℃、2 800×g离心10 min,分离获得的血清储存于-20 ℃备用。每组随机选择6只鸡,颈部放血处死,采集卵巢、直径为6~8 mm的小黄卵泡,分离颗粒层,液氮速冻后置于-80 ℃保存备用。
|
|
表 1 基础日粮组成和营养组成水平 Table 1 Composition and nutrient levels of basal diets |
每天记录各组各重复的产蛋数和蛋重,计算饲养日产蛋率。每天记录各组各重复的采食量,计算料蛋比。
| $ \begin{gathered} \text { 饲养日产蛋率 }=\frac{\text { 统计期内的总产蛋量 }}{\text { 实际饲养鸡只数的累加 }} \times 100 \% ; \\ \text { 料蛋比 }=\frac{\text { 统计期内饲料总耗量 }}{\text { 统计期内总产蛋量 }}。\end{gathered} $ |
试验结束时每个重复收集6枚蛋,每组18枚蛋。使用游标卡尺和螺旋测微器(日本三丰公司)测定蛋形指数和蛋壳厚度;使用蛋壳强度测定仪(北京天翔飞域科技有限公司)测定蛋壳强度;使用多功能蛋品质自动分析仪(日本Touhoku Rhythm Co. Ltd.公司)测定蛋白高度、哈氏单位、蛋黄颜色;分离蛋黄蛋清,蛋黄称重。
1.3 血清激素、抗氧化水平及卵巢抗氧化水平相关指标的测定使用ELISA试剂盒(南京奥青生物技术有限公司)检测血清中雌二醇(E2)、促卵泡生成素(FSH)、黄体生成素(LH)、孕酮(Prog)含量,按照试剂盒说明书进行操作。
使用试剂盒(南京奥青生物技术有限公司)测定蛋鸡血清和卵巢中总抗氧化能力(T-AOC)、谷胱甘肽过氧化物酶(GSH-Px)、超氧化物歧化酶(SOD)、过氧化氢酶(CAT)活性和丙二醛(MDA)含量,按照试剂盒说明书进行操作。
1.4 总RNA的分离和qRT-PCR使用TRIzol试剂(南京诺唯赞生物科技股份有限公司)从小黄卵泡颗粒层样品中提取总RNA。使用5×All-In-One RT MasterMix试剂盒(爱必梦生物科技有限公司)将RNA反转录为cDNA,反应体系为:400 ng总RNA、反转录酶4 μL,加去离子水至20 μL; 反应条件: 37 ℃ 15 min,60 ℃ 10 min。通过荧光定量PCR检测目的基因的表达水平,反应体系为20 μL:cDNA 2 μL、2×SYBR Green Master Mix(爱必梦生物科技有限公司)10 μL、双蒸水7 μL、目的基因上/下游引物(1 μmol·L-1)各0.5 μL。PCR反应条件:95 ℃预变性3 min;95 ℃ 15 s,60 ℃ 1 min,40个循环。根据GenBank中收录的鸡相关基因序列,用NCBI设计引物,选择β-actin作为内部参照基因,用2- ΔΔCT法[10]进行计算,引物由南京擎科生物科技有限公司合成,引物序列信息见表 2。
|
|
表 2 基因的引物序列 Table 2 The primer sequence of genes |
采用SPSS 20.0软件对所得数据进行单因素方差分析(one-way ANOVA),使用Duncan’s法进行多重比较,采用多项式中的线性和二次分析对不同浓度梯度的效果进行分析。结果用“平均值±标准误”表示,P<0.05为差异显著, P<0.01为差异极显著。
2 结果 2.1 甜菜碱对产蛋后期蛋鸡生产性能的影响如表 3所示,与对照组相比,日粮中添加3 000 mg·kg-1甜菜碱可以使产蛋后期蛋鸡的产蛋率和平均蛋重提高10.98%(P<0.01)和4.69%(P<0.05),且产蛋率和平均蛋重与甜菜碱添加水平呈显著线性关系(PL<0.01);对料蛋比无显著影响(P>0.05);日粮中添加1 000 mg·kg-1甜菜碱对产蛋率、平均蛋重和料蛋比均无显著影响(P>0.05)。
|
|
表 3 甜菜碱对产蛋后期蛋鸡生产性能的影响 Table 3 Effect of betaine on production performance of late-phase laying hens |
如表 4所示,与对照组相比,日粮中添加3 000 mg·kg-1的甜菜碱使蛋白高度、蛋黄颜色、蛋黄重量分别提高了19.18%、15.04%、8.08% (P<0.05),且蛋白高度、蛋黄颜色和蛋黄重量与甜菜碱添加量呈显著线性关系(PL<0.05),而其他指标与对照组比均无显著差异(P>0.05);日粮中添加1 000 mg·kg-1的甜菜碱对产蛋后期蛋品质无显著影响(P>0.05)。
|
|
表 4 甜菜碱对产蛋后期蛋鸡蛋品质的影响 Table 4 Effect of betaine on egg quality of late-phase laying hens |
如表 5所示,与对照组相比,日粮中添加1 000、3 000 mg·kg-1的甜菜碱,均极显著提升了产蛋后期蛋鸡血清中FSH和LH的水平(P<0.01), 且FSH分别提高了53.51%、97.37%,LH分别提高了47.12%、68.27%;与对照组相比,添加3 000 mg·kg-1甜菜碱组血清中Prog含量提高了35.08%(P<0.01), 且血清中E2水平有提升的趋势(0.05<P<0.1), 同时Prog水平与甜菜碱添加量呈显著线性关系(PL<0.01),FSH和LH水平与甜菜碱添加量呈显著线性和二次关系(PL<0.01;PQ<0.05)。
|
|
表 5 甜菜碱对产蛋后期蛋鸡血清激素水平的影响 Table 5 Effect of betaine on serum hormone levels of late-phase laying hens |
如表 6所示,与对照组相比,日粮中添加1 000、3 000 mg·kg-1的甜菜碱,极显著提升了产蛋后期蛋鸡血清中的T-AOC水平和SOD、GSH-Px、CAT的酶活性(P<0.01),且T-AOC分别提升了41.17%、61.31%,SOD分别提升了33.30%、48.56%,GSH-Px分别提升了19.83%、36.97%,CAT分别提升了53.63%、69.92%;极显著降低了血清中的MDA水平(P<0.01),分别降低了45.24%、53.86%。与对照组相比,日粮中添加3 000 mg·kg-1的甜菜碱产蛋后期蛋鸡卵巢中T-AOC水平和SOD、CAT的酶活性显著提升,分别提升了48.31%、86.52%、75.69%,MDA水平显著降低(P<0.05),显著降低了33.71%。但对卵巢中GSH-Px酶的活性无显著影响(P>0.05)。同时,血清中SOD、GSH-Px活性和卵巢中T-AOC、MDA水平、SOD、CAT活性与甜菜碱添加量呈显著线性关系(PL<0.05);血清中T-AOC、MDA水平、CAT活性与甜菜碱添加量呈显著线性和二次关系(PL<0.01;PQ<0.01)。
|
|
表 6 甜菜碱对产蛋后期蛋鸡血清和卵巢抗氧化指标的影响 Table 6 Effect of betaine on serum and ovary antioxidant index of late-phase laying hens |
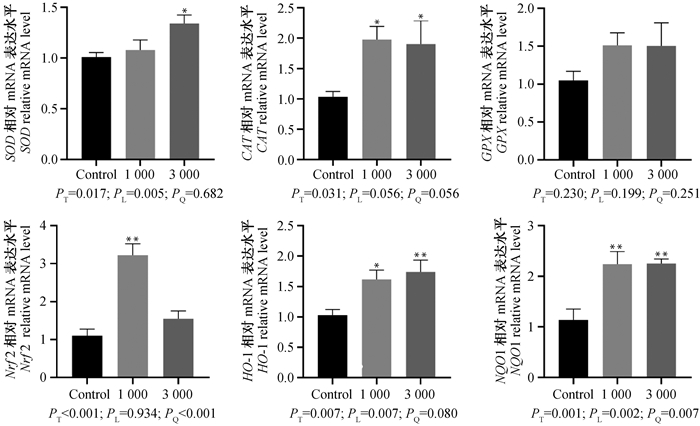
如图 1所示,与对照组相比,日粮中添加甜菜碱线性提高颗粒细胞中SOD、HO-1基因表达量(PL<0.01),且3 000 mg·kg-1甜菜碱组颗粒细胞SOD基因的表达量显著高于对照组(P<0.05),1 000和3 000 mg·kg-1甜菜碱组均可以提高小黄卵泡颗粒细胞HO-1基因的表达水平(P<0.05或P<0.01);日粮中添加甜菜碱,Nrf2基因的表达水平呈二次曲线升高(PQ<0.01),且与对照组相比,日粮中添加1 000 mg·kg-1可以极显著提升Nrf2基因的表达水平(P<0.01);日粮中添加甜菜碱线性和二次曲线升高NQO1基因的表达水平(PL<0.01;PQ<0.01),且与对照组相比,添加1 000、3 000 mg·kg-1甜菜碱可以极显著提高提高NQO1基因的表达水平(P<0.01);此外,日粮中添加甜菜碱可以显著提升CAT基因的表达水平(P<0.05),但对GPX基因的表达量无显著影响(P>0.05)。
|
*表示与对照组相比差异显著(P<0.05);**表示与对照组相比差异极显著(P<0.01) * mean significant difference compared with the control group (P < 0.05); ** mean highly significant difference compared with the control group (P < 0.01) 图 1 甜菜碱对产蛋后期蛋鸡小黄卵泡颗粒细胞抗氧化相关基因表达的影响 Fig. 1 Effect of betaine on expression of antioxidant related genes in granulosa cells of small yellow follicles of late-phase laying hens |
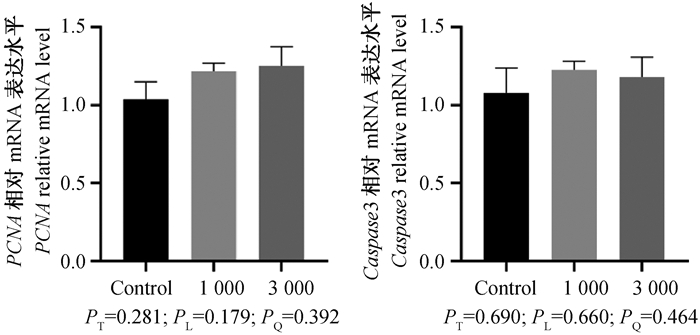
如图 2所示,与对照组相比,日粮中添加1 000、3 000 mg·kg-1甜菜碱对颗粒细胞PCNA和Caspase3基因的表达水平均无显著影响(P>0.05)。
|
图 2 甜菜碱对产蛋后期蛋鸡小黄卵泡颗粒细胞增殖凋亡相关基因表达的影响 Fig. 2 Effect of betaine on the expression of genes related to proliferation and apoptosis of small yellow follicle granulosa cells of late-phase laying hens |
甜菜碱是一种高效的饲料添加剂,在提升畜禽生长性能,提高畜禽产品品质等方面发挥重要作用[11-12]。Alagawany等[13]研究发现,日粮中添加甜菜碱可以提高产蛋后期蛋鸡的产蛋率、蛋品质和免疫机能。本试验结果表明,日粮中添加3 000 mg·kg-1甜菜碱显著提升了产蛋后期蛋鸡的产蛋率和平均蛋重。
类固醇激素对于卵泡的生长、成熟、排卵具有重要作用,是衡量蛋鸡产蛋性能的关键指标[14]。FSH可以促进卵泡的生长、发育和成熟,LH诱导卵泡排卵,两者协同作用,调节卵泡E2的生成,进而影响动物的繁殖性能[15]。在蛋鸡衰老过程中,血清中激素水平的下降,降低蛋鸡的繁殖性能,在本试验中,日粮中添加1 000、3 000 mg·kg-1的甜菜碱,极显著提升了产蛋后期蛋鸡血清中的FSH和LH的水平;日粮中添加3 000 mg·kg-1的甜菜碱极显著提升了产蛋后期蛋鸡血清中Prog的水平,这与产蛋率的增加相一致。故甜菜碱可以通过增加激素水平促进卵泡发育,改善产蛋后期蛋鸡的繁殖性能。
3.2 甜菜碱对蛋品质的影响随着蛋鸡日龄的增加,产蛋后期蛋鸡蛋品质逐渐下降,如蛋壳厚度降低、蛋白高度下降等[16],调节基础日粮的组成或使用添加剂可以改善产蛋后期的蛋品质。曲昆鹏等[17]研究表明,日粮中添加500 g·t-1甜菜碱可以提升海兰褐壳蛋鸡的蛋黄颜色和蛋黄比重;Zaki等[18]研究发现,蛋鸡日粮中添加甜菜碱可以显著增加蛋黄颜色;乔淑文等[19]研究表明,日粮中添加甜菜碱可以缓解热应激下蛋壳强度、蛋壳厚度、哈氏单位等指标的下降。
蛋鸡日粮中的叶黄素被载脂蛋白转运至卵黄中沉积,影响蛋黄颜色[20],产蛋后期蛋鸡卵黄前体物质和载脂蛋白合成能力减弱,卵黄合成和积累能力降低,降低产蛋性能和蛋品质[21]。甜菜碱可以作为甲基供体促进肝载脂蛋白的合成[17],促进卵黄蛋白原(VTG)和饲料中的叶黄素的运输及其在蛋黄中的沉积,本研究添加3 000 mg·kg-1的甜菜碱显著提高蛋黄颜色、蛋黄重量和蛋白高度可能与此有关,但具体的内在机制还需进一步研究。
3.3 甜菜碱对产蛋后期蛋鸡卵巢抗氧化能力的影响衰老引起的氧化应激是产蛋后期蛋鸡生产性能下降的主要原因[22]。ROS的积累打破了机体正常的氧化剂和抗氧化系统间的平衡[23],过量的ROS会破坏生物大分子,产生MDA,导致细胞凋亡和组织损伤[24]。CAT、GSH-Px、SOD等抗氧化酶可以维持体内的氧化平衡状态,保护机体免受氧化损伤[25]。研究表明甜菜碱可以增加血清中抗氧化相关酶的水平[26]。本试验中,日粮中添加1 000、3 000 mg·kg-1甜菜碱均显著提升了血清中的T-AOC水平和SOD、GSH-Px、CAT的酶活性,显著降低了血清中MDA含量;日粮中添加3 000 mg·kg-1的甜菜碱显著提升了产蛋后期卵巢的T-AOC水平和SOD、CAT的酶活性且显著降低了卵巢中MDA水平,与杨密等[27]和Cai等[28]的研究结果一致,即日粮中添加甜菜碱可以提高畜禽的抗氧化能力。
增龄或衰老伴随的氧化损伤会导致卵巢功能不断下降[29]。在卵巢衰老过程中,颗粒细胞受到氧化应激的影响发生凋亡,使得卵泡闭锁,最终导致产蛋后期蛋鸡的繁殖性能降低[30]。基于血清和卵巢中抗氧化酶活性的提升,本试验进一步研究了小黄卵泡颗粒细胞中抗氧化相关基因的表达水平。核因子E2相关因子2(Nrf2)在抗氧化系统中发挥关键作用,它可以激活抗氧化反应元件(ARE),促进下游抗氧化基因例如HO-1、NQO1、CAT、SOD和GPX的表达[31]。蛋鸡衰老过程中,卵巢氧化应激加强,Nrf2/HO-1通路活性降低[22]。Chen等[32]研究表明,高剂量甜菜碱通过上调Nrf2和HO-1在胸肌中的mRNA表达水平,改变Nrf2信号通路来提高肌肉的抗氧化能力。本研究在日粮中添加1 000、3 000 mg·kg-1甜菜碱,均显著提升了CAT、HO-1、NQO1基因的表达水平,与Cai等[28]发现湖羊日粮中添加甜菜碱,可增加湖羊睾丸CAT、SOD和GSH-Px的mRNA表达水平,增强湖羊睾丸的抗氧化能力结果一致。因此,甜菜碱可能通过激活Nrf2通路,提升产蛋后期蛋鸡卵泡颗粒细胞的抗氧化水平。
越来越多的证据表明,氧化应激诱导的颗粒细胞凋亡,卵泡闭锁加剧可能是老年蛋鸡繁殖力下降的根本原因[33-34]。先前的研究表明,甜菜碱可以通过增加人前列腺癌细胞的凋亡和炎症来抑制细胞增殖[35];Samie等[36]发现,甜菜碱可以抑制高糖条件下小鼠颗粒细胞的凋亡,促进颗粒细胞的增殖,而Cai等[28]发现湖羊日粮中添加甜菜碱,睾丸PCNA基因的表达降低,本试验发现,日粮中添加甜菜碱PCNA和Caspase3基因表达水平与对照组相比无显著差异,由于物种和组织的差异,与前人研究结果不同,甜菜碱是否可以改变产蛋后期颗粒细胞的增殖水平还需进一步研究。
4 结论综上所述,产蛋后期蛋鸡日粮中添加甜菜碱,可以通过增加血清激素水平和血清、卵巢中抗氧化酶的活性,促进小黄卵泡颗粒细胞中抗氧化相关基因CAT、SOD、Nrf2、HO-1、NQO1的表达,提高颗粒细胞的抗氧化能力,进而延缓蛋鸡衰老,提升产蛋后期蛋鸡的生产性能。
| [1] |
TONG L Y, CHUANG C C, WU S Y, et al. Reactive oxygen species in redox cancer therapy[J]. Cancer Lett, 2015, 367(1): 18-25. DOI:10.1016/j.canlet.2015.07.008 |
| [2] |
WU H Y, YUAN J, YIN H X, et al. Flammulina velutipes stem regulates oxidative damage and synthesis of yolk precursors in aging laying hens by regulating the liver-blood-ovary axis[J]. Poult Sci, 2023, 102(1): 102261. DOI:10.1016/j.psj.2022.102261 |
| [3] |
LIU X T, LIN X, MI Y L, et al. Grape seed proanthocyanidin extract prevents ovarian aging by inhibiting oxidative stress in the hens[J]. Oxid Med Cell Longev, 2018, 2018: 9390810. |
| [4] |
HE W Z, WANG H, TANG C H, et al. Dietary supplementation with astaxanthin alleviates ovarian aging in aged laying hens by enhancing antioxidant capacity and increasing reproductive hormones[J]. Poult Sci, 2023, 102(1): 102258. DOI:10.1016/j.psj.2022.102258 |
| [5] |
戴宏健, 吕增鹏, 黄振吾, 等. 山楂叶黄酮对产蛋后期种鸡蛋壳品质的影响[J]. 畜牧兽医学报, 2021, 52(4): 1010-1019. DAI H J, LV Z P, HUANG Z W, et al. Effects of hawthorn-leaves flavonoids on the quality of eggshells of breeder hens in late egg-laying period[J]. Acta Veterinaria et Zootechnica Sinica, 2021, 52(4): 1010-1019. (in Chinese) |
| [6] |
OMER N A, HU Y, HU Y, et al. Dietary betaine activates hepatic VTGⅡ expression in laying hens associated with hypomethylation of GR gene promoter and enhanced GR expression[J]. J Anim Sci Biotechnol, 2018, 9: 2. DOI:10.1186/s40104-017-0218-9 |
| [7] |
OMER N A, HU Y, IDRISS A A, et al. Dietary betaine improves egg-laying rate in hens through hypomethylation and glucocorticoid receptor-mediated activation of hepatic lipogenesis-related genes[J]. Poult Sci, 2020, 99(6): 3121-3132. DOI:10.1016/j.psj.2020.01.017 |
| [8] |
SHAKERI M, COTTRELL J J, WILKINSON S, et al. Betaine and antioxidants improve growth performance, breast muscle development and ameliorate thermoregulatory responses to cyclic heat exposure in broiler chickens[J]. Animals (Basel), 2018, 8(10): 162. |
| [9] |
ALAM M H, MIYANO T. Interaction between growing oocytes and granulosa cells in vitro[J]. Reprod Med Biol, 2019, 19(1): 13-23. |
| [10] |
LIVAK K J, SCHMITTGEN T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCT method[J]. Methods, 2001, 25(4): 402-408. DOI:10.1006/meth.2001.1262 |
| [11] |
CHENG Y T, SONG M T, ZHU Q, et al. Impacts of betaine addition in sow and piglet's diets on growth performance, plasma hormone, and lipid metabolism of Bama mini-pigs[J]. Front Nutr, 2021, 8: 779171. DOI:10.3389/fnut.2021.779171 |
| [12] |
SUN C Y, LIU W C, XIAO M, et al. Effects of graded levels of betaine supplementation on growth performance and intestinal morphology in indigenous young yellow feather broilers[J]. Pak J Zool, 2019, 51(6): 2323-2328. |
| [13] |
ALAGAWANY M, ELNESR S S, FARAG M R, et al. Betaine and related compounds: chemistry, metabolism and role in mitigating heat stress in poultry[J]. J Therm Biol, 2022, 104: 103168. DOI:10.1016/j.jtherbio.2021.103168 |
| [14] |
JOHNSON A L, WOODS D C. Dynamics of avian ovarian follicle development: cellular mechanisms of granulosa cell differentiation[J]. Gen Comp Endocrinol, 2009, 163(1-2): 12-17. DOI:10.1016/j.ygcen.2008.11.012 |
| [15] |
张玲, 钟光, 顾文婕, 等. 饲粮添加大豆黄酮对产蛋后期蛋鸡产蛋性能、蛋品质和血浆激素指标的影响[J]. 动物营养学报, 2020, 32(9): 4110-4115. ZHANG L, ZHONG G, GU W J, et al. Effects of dietary daidzein on laying performance, egg quality and plasma hormone indices of laying hens during late laying cycle[J]. Chinese Journal of Animal Nutrition, 2020, 32(9): 4110-4115. (in Chinese) |
| [16] |
周建民, 武书庚, 王晶, 等. 产蛋后期蛋鸡生理特点与营养调控[J]. 中国家禽, 2021, 43(3): 74-82. ZHOU J M, WU S G, WANG J, et al. Physiological characteristics and nutritional regulation of aged laying hens[J]. China Poultry, 2021, 43(3): 74-82. (in Chinese) |
| [17] |
曲昆鹏, 张倩, 张魏魏, 等. 日粮添加格氏碱对海兰褐蛋鸡生产性能、蛋品质、血液生化指标和生殖激素的影响[J]. 中国家禽, 2016, 38(12): 31-34. QU K P, ZHANG Q, ZHANG W W, et al. Effect of dietary betaine on production performance, egg quality, serum biochemical indexes and serum reproductive hormone of Hy-Line brown laying hens[J]. China Poultry, 2016, 38(12): 31-34. (in Chinese) |
| [18] |
ZAKI A, JIANG S Q, ZAGHLOUL S, et al. Betaine as an alternative feed additive to choline and its effect on performance, blood parameters, and egg quality in laying hens rations[J]. Poult Sci, 2023, 102(7): 102710. DOI:10.1016/j.psj.2023.102710 |
| [19] |
乔淑文, 王芳. 日粮添加甜菜碱对夏季高温蛋鸡生产性能、蛋品质及血液理化特征的影响[J]. 中国饲料, 2022(4): 25-28. QIAO S W, WANG F. Effects of betaine on performance, egg quality and blood physicochemical characteristics of laying hens in high temperature[J]. China Feed, 2022(4): 25-28. (in Chinese) |
| [20] |
PAPADOPOULOS G A, LIOLIOPOULOU S, ORDOUDI S A, et al. Xylanase supplementation in wheat-based diets of laying hens affects the egg yolk color, carotenoid and fatty acid profiles[J]. Foods, 2022, 11(15): 2209. DOI:10.3390/foods11152209 |
| [21] |
LIU X T, LIN X, MI Y L, et al. Age-related changes of yolk precursor formation in the liver of laying hens[J]. J Zhejiang Univ Sci B, 2018, 19(5): 390-399. DOI:10.1631/jzus.B1700054 |
| [22] |
LIU X T, LIN X, ZHANG S Y, et al. Lycopene ameliorates oxidative stress in the aging chicken ovary via activation of Nrf2/HO-1 pathway[J]. Aging (Albany NY), 2018, 10(8): 2016-2036. |
| [23] |
ZHU Y W, LU L, LI W X, et al. Effect of dietary manganese on antioxidant status and expressions of heat shock proteins and factors in tissues of laying broiler breeders under normal and high environmental temperatures[J]. Br J Nutr, 2016, 116(11): 1851-1860. DOI:10.1017/S0007114516003822 |
| [24] |
XU Y L, YU Y, SHEN Y Y, et al. Effects of Bacillus subtilis and Bacillus licheniformis on growth performance, immunity, short chain fatty acid production, antioxidant capacity, and cecal microflora in broilers[J]. Poult Sci, 2021, 100(9): 101358. DOI:10.1016/j.psj.2021.101358 |
| [25] |
XIE T, BAI S P, ZHANG K Y, et al. Effects of Lonicera confusa and astragali radix extracts supplementation on egg production performance, egg quality, sensory evaluation, and antioxidative parameters of laying hens during the late laying period[J]. Poult Sci, 2019, 98(10): 4838-4847. DOI:10.3382/ps/pez219 |
| [26] |
EGBUNIWE I C, UCHENDU C N, OBIDIKE I R. Ameliorative effects of betaine and ascorbic acid on endocrine and erythrocytic parameters of sexually-maturing female Japanese quails during the dry season[J]. J Therm Biol, 2021, 96: 102812. DOI:10.1016/j.jtherbio.2020.102812 |
| [27] |
杨密, 宋宇朵, 陈瑞, 等. 饲粮甜菜碱水平对雪山草鸡腿肌肉品质、糖酵解水平和抗氧化能力的影响[J]. 南京农业大学学报, 2022, 45(3): 578-586. YANG M, SONG Y D, CHEN R, et al. Effects of dietary betaine levels on meat quality, glycolysis level, antioxidant ability of Xueshan chicken[J]. Journal of Nanjing Agricultural University, 2022, 45(3): 578-586. (in Chinese) |
| [28] |
CAI Y, DENG M T, ZHANG Q F, et al. Effects of dietary betaine supplementation on biochemical parameters of blood and testicular oxidative stress in Hu sheep[J]. Theriogenology, 2021, 164: 65-73. DOI:10.1016/j.theriogenology.2021.01.006 |
| [29] |
LIM J, LUDERER U. Oxidative damage increases and antioxidant gene expression decreases with aging in the mouse ovary[J]. Biol Reprod, 2011, 84(4): 775-782. DOI:10.1095/biolreprod.110.088583 |
| [30] |
MURPHY M P. How mitochondria produce reactive oxygen species[J]. Biochem J, 2009, 417(1): 1-13. DOI:10.1042/BJ20081386 |
| [31] |
BAO L P, LI J S, ZHA D, et al. Chlorogenic acid prevents diabetic nephropathy by inhibiting oxidative stress and inflammation through modulation of the Nrf2/HO-1 and NF-κB pathways[J]. Int Immunopharmacol, 2018, 54: 245-253. DOI:10.1016/j.intimp.2017.11.021 |
| [32] |
CHEN R, YANG M, SONG Y D, et al. Effect of anhydrous betaine and hydrochloride betaine on growth performance, meat quality, postmortem glycolysis, and antioxidant capacity of broilers[J]. Poult Sci, 2022, 101(4): 101687. DOI:10.1016/j.psj.2021.101687 |
| [33] |
王新兴. FHC对鹅卵泡颗粒细胞氧化应激、细胞增殖和凋亡的影响[D]. 成都: 四川农业大学, 2019. WANG X X. Effect of FHC on oxidative stress, cell proliferation and apoptosis in follicular granulosa cells of geese[D]. Chengdu: Sichuan Agricultural University, 2019. (in Chinese) |
| [34] |
WANG J P, JIA R, GONG H J, et al. The effect of oxidative stress on the chicken ovary: involvement of microbiota and melatonin interventions[J]. Antioxidants (Basel), 2021, 10(9): 1422. DOI:10.3390/antiox10091422 |
| [35] |
MANDOULAKANI B A, EYVAZPOUR E, GHADIMZADEH M. The effect of drought stress on the expression of key genes involved in the biosynthesis of phenylpropanoids and essential oil components in basil (Ocimum basilicum L.)[J]. Phytochemistry, 2017, 139: 1-7. DOI:10.1016/j.phytochem.2017.03.006 |
| [36] |
SAMIE K A, TABANDEH M R, AFROUGH M. Betaine ameliorates impaired steroidogenesis and apoptosis in mice granulosa cells induced by high glucose concentration[J]. Syst Biol Reprod Med, 2020, 66(6): 400-409. DOI:10.1080/19396368.2020.1811423 |
(编辑 范子娟)



