2. 岭南现代农业科学与技术广东省实验室茂名分中心, 茂名 525000;
3. 华南农业大学国家生猪种业工程技术研究中心, 广州 510642;
4. 广东海大畜牧兽医研究院有限公司, 广州 511400
2. Maoming Branch, Guangdong Laboratory for Lingnan Modern Agriculture, Maoming 525000, China;
3. National Engineering Research Center for Breeding Swine Industry, South China Agricultural University, Guangzhou 510642, China;
4. Guangdong Haid Animal Husbandry and Veterinary Research Institute Co. Ltd, Guangzhou 511400, China
猪繁殖与呼吸综合征(porcine reproductive and respiratory syndrome,PRRS)在全球范围内普遍流行,俗称蓝耳病,其病原是猪繁殖与呼吸综合征病毒(PRRSV),PRRSV是一种单股正链RNA病毒[1],直径50~65 nm[2],基因组长度约15 kb,编码至少10个开放阅读框(open reading frame, ORF)。PRRSV共分为两种基因型,分别为欧洲型毒株(EU genotype)和北美型毒株(NA genotype),欧洲型毒株即PRRSV-1,代表毒株为Lelystad;美洲型毒株即PRRSV-2,代表毒株为ATCC VR2332[3],两种基因型之间的相似性约为60%[4]。我国境内流行的毒株主要是PRRSV-2,根据ORF5基因分型主要分为4个谱系,即谱系1(NADC30-like毒株和NADC34-like毒株),谱系3(QYYZ和GM2),谱系5.1(VR2332和BJ-4),谱系8.7(CH-1a和JXA1)。1996年我国首次分离到PRRSV,命名为CH-1a,十年后在我国江西省暴发高致病性猪繁殖与呼吸综合征(HP-PRRS),代表毒株为JXA1,后证实为CH-1a的突变毒株[5]。2010年,QYYZ毒株首次在我国大陆地区发现;2012年, GM2毒株被发现并被推测为是疫苗毒株与QYYZ的重组毒株[6]。2013年,NADC30-like毒株在我国首次报道,自传入我国以来流行至今,我国流行的NADC30-like毒株表现为中等毒力,具备强大的遗传进化能力[7]。2018年,我国辽宁省首次检测到NADC34-like毒株,2020年该毒株以后在我国多个省份流行[8]。
PRRSV ORF5和ORF7基因长期以来一直被视为监测PRRSV遗传进化的重要靶基因。ORF5基因序列长度约为603 bp,编码GP5蛋白,该基因拥有重要的中和抗原表位,在诱导免疫应答过程中发挥重要作用,GP5蛋白存在多个潜在的N-糖基化位点,对病毒感染、免疫逃避有着非常重要的作用,因此ORF5是最常被用作分子流行病学监测的基因[9]。ORF7基因序列长度约372 bp,编码N蛋白,该基因相比ORF5较为保守,也常用于PRRSV的临床检测及毒株分型[10],近年来,PRRSV ORF5基因的变异程度日趋复杂,导致ORF5基因序列获取难度加大,因此ORF7基因具备替代ORF5基因作为PRRSV分子遗传变异分析的潜力。自2018年非洲猪瘟在我国暴发以来,不断扩大的疫情对我国养猪行业造成严重的打击,导致PRRSV流行的关注力度明显下降,进而导致我国PRRSV的分子流行病学数据相对较少。本研究在2021—2022年开展了PRRSV分子流行病学调查,通过获取PRRSV阳性样本的ORF5和ORF7基因序列分析PRRSV的主要流行谱系,所有样品涵盖13个省份,为了解近年来我国PRRSV的流行变异情况提供参考依据。
1 材料与方法 1.1 样品收集2021—2022年,本课题组在我国黑龙江、吉林、河北、山西、河南、四川、贵州、湖南、广西、广东、海南、江西和福建13个省的50个猪场收集了117份疑似PRRS症状样品,样品类型主要为肺、淋巴结、血清。患病猪临床表现为体温升高、厌食、呼吸道症状、生长迟缓、耳鼻发绀、死亡,以及妊娠母猪出现流产、死胎、产木乃伊胎等。
1.2 引物设计参考NCBI GenBank中收录的JXA1、VR2332、CH-1a等毒株序列,利用Oligo7.0软件分别设计PRRSV ORF5和ORF7基因引物(表 1),同时设计PRRSV-1毒株实时荧光定量PCR引物,参照福建省地方标准(DB35/T 1852—2019)设计PRRSV-2实时荧光定量PCR引物,不同基因型引物序列由北京睿博兴科生物技术有限公司合成。
|
|
表 1 PRRSV ORF5和ORF7引物及扩增片段长度 Table 1 PRRSV ORF5 and ORF7 primers and amplified fragment lengths |
所有PRRSV阳性样品保存于-80 ℃超低温冰箱,使用超低温组织研磨仪(JXFSTPRP-CLN-48,上海净信)将样品匀浆,使用RNA Fast200(Fastagen)试剂盒提取病毒总RNA,使用qRT-PCR酶(HiScript III U+ One Step qRT-PCR Probe Kit,南京诺唯赞生物科技股份有限公司)鉴定阳性样品及基因型,反应程序:55 ℃ 15 min;95 ℃ 30 s;95 ℃ 10 s、60 ℃ 30 s,共45个循环。将病毒RNA反转录制备cDNA,利用RT-PCR扩增样品ORF7和ORF5基因,反应程序:95 ℃ 3 min;95 ℃ 15 s、60 ℃ 15 s、72 ℃ 60 s,共35个循环;72 ℃ 5 min。PCR产物在10 g ·L-1琼脂糖凝胶中进行电泳,电泳结果在凝胶成像系统中进行可视化分析,将条带大小位置一致的扩增产物进行Sanger测序以获取目的序列。
1.4 系统发育学分析及基因变异分析应用DNA STAR 7.1软件和MAFFT 7将PRRSV ORF5和ORF7基因序列进行比对,利用Megalign软件分析不同毒株ORF5和ORF7基因的序列相似性。利用IQ-Tree软件构建最大似然系统发育树,应用Figtree v1.4.3软件将系统发育树进一步可视化分析。利用EditSeq软件将PRRSV ORF5基因核苷酸序列转换为氨基酸序列,利用Jalview软件分析PRRSV GP5氨基酸突变位点。
2 结果 2.1 2021—2022年我国部分地区PRRSV临床样品检测结果2021—2022年,本研究共收集疑似PRRS症状患猪样品117份,其中大部分样品来自于华南地区,部分样品来自于我国西南和中部及北部地区(表 2),经实时荧光定量PCR鉴定48份样品为PRRSV阳性,且均为PRRSV-2毒株,应用RT-PCR成功扩增出38份样本ORF5基因,使用ORF7引物成功扩增出剩余10份样品的ORF7基因。
|
|
表 2 2021—2022年PRRSV临床样品收集地分布表 Table 2 Geographic distribution of PRRSV clinical sample collections, 2021—2022 |
以PRRSV-2不同谱系代表毒株作为参考毒株,38条ORF5基因序列之间核苷酸相似性为77.1%~99.8%,与NADC30相似性为82.4%~95.2%,与NADC34相似性为81.9%~96%,与QYYZ相似性为81.1%~91.4%,与GM2相似性为80.4%~90.7%,与VR2332相似性为81.4%~99.3%,与CH-1a相似性为82.9%~96.5%,与JXA1相似性为82.3%~97.7%;其中,GDHZ29与IA/2014/NADC34的相似性高达96%(图 1A)。10条ORF7序列间核苷酸相似性为83.3%~98.7%,与NADC30相似性为86%~96.8%,与NADC34相似性为84.1%~96%,与QYYZ相似性为85.2%~89.8%,与GM2相似性为84.4%~88.4%,与VR2332相似性为87.9%~93.3%,与CH-1a相似性为86.8%~98.1%,与JXA1相似性为86%~98.9%(图 1B)。

|
图 1 PRRSV ORF5(A)及ORF7基因(B)与不同谱系参考毒株基因相似性分析 Fig. 1 Gene similarity analysis of ORF5 and ORF7 genes with reference strains of different lineages |
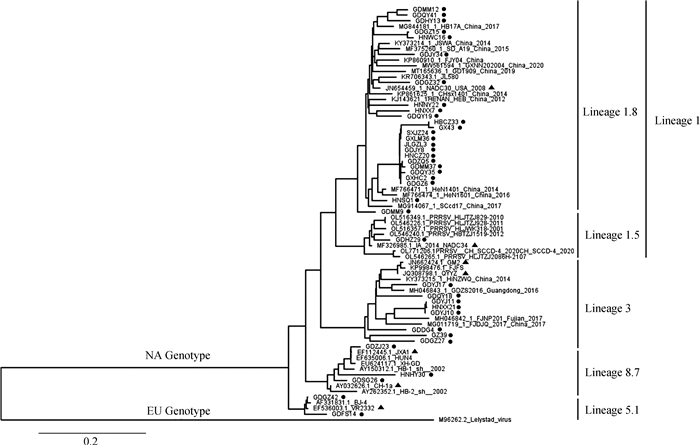
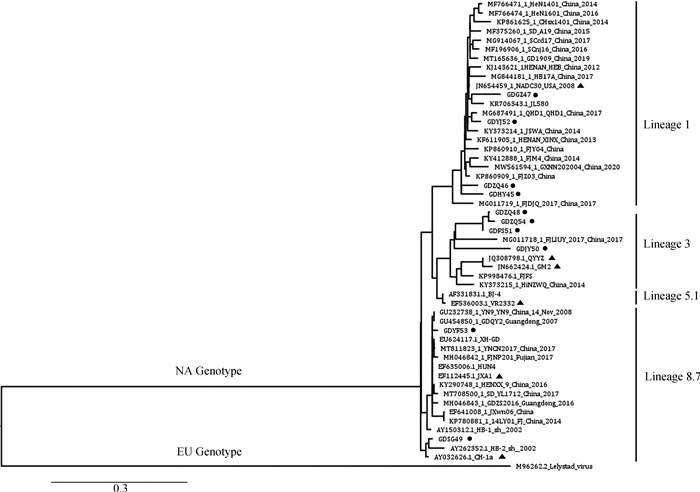
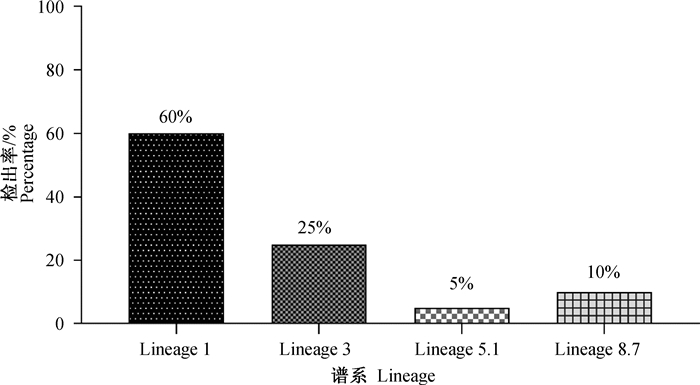
ORF5基因系统发育学分析表明,所有毒株均属于PRRSV-2,进而划分为4个分支:谱系1(谱系1.8 NADC30-like毒株24株,谱系1.5 NADC34-like毒株1株),谱系3(QYYZ-like毒株和GM2-like毒株8株),谱系5.1(VR2332-like毒株2株),谱系8.7(CH-1a-like毒株2株和JXA1-like毒株3株)(图 2)。ORF7基因系统发育学分析同样将所有毒株分为4个分支,其中4株属于谱系1,4株属于谱系3,2株属于谱系8.7(图 3)。根据ORF5和ORF7基因系统发育学分析可知,谱系1毒株共29株(60%),占比最高且地理分布最广,共在8个省份(8/9)均有检出;谱系3毒株12株(25%),主要在华南地区检出;谱系5.1毒株2株(5%),均在广东省检出;谱系8.7毒株5株(10%),均在华南地区检出(图 4,表 3)。
|
▲. 不同谱系代表毒株;●. 本研究中的毒株 ▲. Representative strains of different lineage; ●. The strains of this study 图 2 基于PRRSV ORF5基因的系统发育学分析 Fig. 2 Phylogenetic analysis based on PRRSV ORF5 gene |
|
▲. 不同谱系代表毒株;●. 本研究中的毒株 ▲. Representative strains of different lineage; ●. The strains of this study 图 3 基于PRRSV ORF7基因的系统发育学分析 Fig. 3 Phylogenetic analysis based on PRRSV ORF7 gene |
|
图 4 2021—2022年PRRSV不同谱系毒株的检出率 Fig. 4 Detection rates of different strains of PRRSV lineage from 2021 to 2022 |
|
|
表 3 PRRSV不同谱系毒株地理分布表 Table 3 Geographical distribution of different strains of PRRSV |
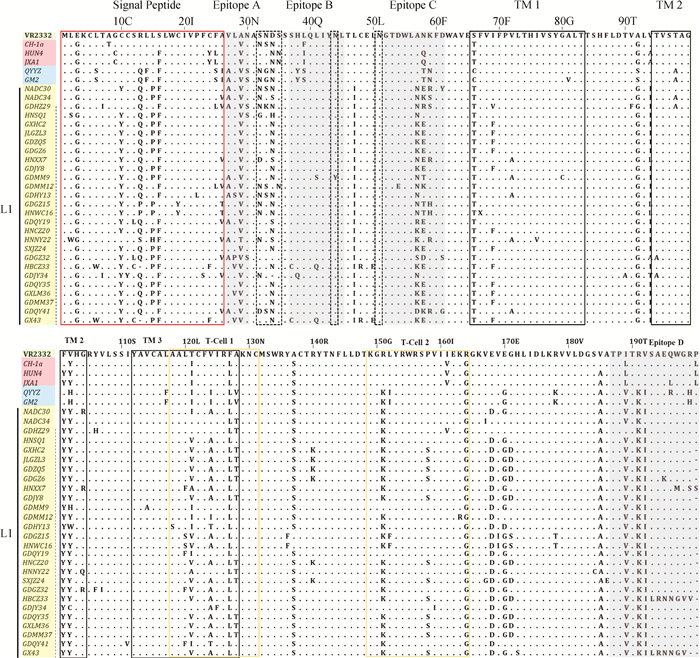
GP5氨基酸序列分析表明信号肽(aa 1—26)、潜在N-糖基化位点(aa 32—35、aa 44、aa 51)及表位C(aa 52—61)区域氨基酸突变程度最复杂,其他区域的氨基酸突变均具有谱系一致性(图 5、6)。以VR2332为参考毒株,不同谱系毒株存在个别氨基酸位点相似性(谱系1、谱系3、谱系8.7毒株大部分均为E3G、S16F、A29V、D34 N、F127 L、A137S、R165 G、V185A)。GP5潜在的N-糖基化位点共有6个,其中2个N-糖基化位点44和51相对保守,4个N-糖基化位点32、33、34、35处于高变区,谱系5.1毒株存在2种点突变(S32 N、D34 G),谱系8.7毒株存在6种点突变(S32 N、N33S、D34S/N、S35 N/H),谱系3毒株存在6种点突变(S32 N/E、N33 G/Q/T、D34 N),谱系1毒株存在5种点突变(S32 G/D、N33K、D34 H、S35 N),在表位C区域(aa52-61中和表位),谱系5.1存在3种点突变(D54E、A57 G、K59 N),谱系8.7存在5种点突变(A57 N、N58Q/D、K59 H、D61S),谱系3存在11种点突变(A57 N、N58 T/K/D/S/E、K59 N/R/S、D61E/Y)。

|
红色框. 信号肽;黑色框. 跨膜区;黄色框. T细胞表位;黑色曲线框. 潜在的N-糖基化位点;黑色阴影框.非中和表位和中和表位区域 Red box. Signal peptide; Black box. Transmembrane region; yellow box. T cell epitope; Black curved box. Potential N-glycosylation site; Black shaded box. Non-neutralizing epitope and neutralizing epitope region 图 5 谱系3、谱系5.1和谱系8.7 PRRSV GP5氨基酸位点变异分析 Fig. 5 Analysis of amino acid residue variants in PRRSV GP5 in lineage 3, lineage 5.1 and lineage 8.7 |
|
红色框. 信号肽;黑色框. 跨膜区;黄色框. T细胞表位;黑色曲线框. 潜在的N-糖基化位点;黑色阴影框.非中和表位和中和表位区域 Red box. Signal peptide; Black box. Transmembrane region; yellow box. T cell epitope; Black curved box. Potential N-glycosylation site; Black shaded box. Non-neutralizing epitope and neutralizing epitope region 图 6 谱系1 PRRSV GP5氨基酸位点变异分析 Fig. 6 Analysis of amino acid residue variants in PRRSV GP5 of lineage 1 |
自PRRSV首次在我国检出以来已有20余年流行史,其遗传进化历程总体分为三个阶段: 第一阶段为1996—2006年,优势流行毒株为CH-1a;第二阶段为2006—2013年,优势流行毒株为JXA1;第三阶段为2013年至今,优势流行毒株为NADC30-like[6]。尽管我国进行了广泛的疫苗免疫,由于PRRSV基因组的高度变异性导致新毒株层出不穷,使得常规疫苗的交叉保护效力并不理想。2018年以来,非洲猪瘟疫情的暴发给我国生猪养殖业带来了严重打击,同时使我国养猪业生物安全防护意识极大提高。然而,由于PRRSV自身遗传进化、对外频繁引种、疫苗使用不当等原因导致猪群免疫选择压力增大,使PRRSV得以传入并迅速发生遗传变异;此外,非洲猪瘟大流行背景下使养殖户对PRRSV防控意识下降,伴随着全国范围内生猪大批量复养,猪存栏数量剧增,使PRRSV得到了再一轮的流行[11]。因此,即便在非洲猪瘟流行的大背景下,PRRSV的流行力度未能降低[12]。同时,由于对PRRSV关注力度下降,导致PRRSV分子流行病学调查的数据相对较少。开展PRRSV流行病学调查研究有重要意义,流行病学调查将有助于了解PRRSV最新的遗传变异情况。在2021—2022年,本研究共收集了117份临床疑似PRRSV感染样品,经实时荧光定量PCR检测均为PRRSV-2,总体阳性率为41%(48/117),ORF5和ORF7基因系统发育分析将所有的序列分为4个谱系(谱系1、谱系3、谱系5.1、谱系8.7),谱系1毒株数量最多(29/48),其次是谱系3(12/48),谱系8.7(5/48)和谱系5.1(2/48)少量检出。有研究表明NADC30-like毒株已成为华中地区PRRSV主要流行谱系[13];福建省PRRSV主要流行毒株是以NADC30-like毒株为主要亲本的重组病毒[14];综合本研究结果显示NADC30-like毒株已代替HP-PRRSV成为全国范围内PRRSV主要流行毒株,NADC30-like毒株基因组变异程度极高,表现出强大的基因重组能力,有报道称NADC30-like毒株极易与HP-PRRSV发生重组,从而增加了田间流行毒株的复杂性,导致不同毒力的新毒株出现[3, 15],NADC30-like毒株的广泛流行是当下我国PRRSV防控需要迫切关注的问题。谱系3毒株目前依旧在华南地区广为流行,有研究表明谱系3毒株的核苷酸变异率为9.85×10-3 位点·年-1,近几年与谱系8.7毒株重组导致的高毒力毒株在华南地区广泛流行[16]。谱系5.1毒株多为疫苗毒株,与临床疫苗(Resp PRRS MLV)广泛使用有密切的联系。NADC34-like毒株在我国出现时间相对较晚,但2020年以来在全国范围内波及的区域越来越广[17],本研究于2021年在广东省惠州市检出一株NADC34-like毒株,与IA/2014/NADC34相似性为96%,证明NADC34-like毒株由我国北方地区(辽宁省、黑龙江省、河南省)[8]传入华东(福建省)和华南地区(广东省),结合相关报道可知NADC34-like毒株已经在广东省发生潜在流行[18]。
PRRSV GP5与病毒免疫逃避及免疫保护密切相关,GP5蛋白区域的突变影响信号肽的裂解、N-糖基化位点的数量以及中和抗体对PRRSV变异体的识别[19-20]。GP5氨基酸突变分析表明,广泛的突变位点分布在整个基因,信号肽、中和表位C及潜在的N-糖基化位点三个区域的突变程度最显著,不同数量的N-糖基化位点可能会影响病毒复制和诱导中和抗体的能力,并可能有助于病毒通过聚糖屏蔽逃避抗体中和[21], 表位C区域的氨基酸突变可能导致同源中和失效[22]。
综上所述,当下我国PRRSV的流行谱系以谱系1为主,同时谱系3和谱系8.7共存。其中,NADC30-like毒株检出率最高且流行区域最为广泛,NADC34-like毒株已经在华南地区出现并流行,多谱系毒株共存及谱系1毒株的广泛流行的现状给国内PRRSV的防控工作带来了巨大的挑战。NADC30-like毒株传入我国以来,遗传进化速度极快,极易与不同谱系毒株发生基因重组,导致PRRSV不同毒株的基因分型更加难以定性[23-24]。同时,我国PRRSV常规疫苗大多基于谱系8毒株研制,对于复杂多变的谱系1毒株的交叉保护效果不佳,不同疫苗的滥用也使得PRRSV控制难度加大[25]。同时,本研究发现谱系3毒株依然局限在华南部分地区流行,但流行率逐年增高,需要我们重视该谱系毒株的流行程度并及时加以控制。面对国内PRRS流行日趋复杂的现状,需要人们更大力度建立生物安全防控,以及加强流行病学调查用以动态分析PRRSV的遗传变异情况。本研究为国内PRRS流行现状给出了最新的数据支撑,也给未来临床防控策略制定提供了参考依据。
4 结论多个谱系猪繁殖与呼吸综合征病毒(PRRSV)同时在我国流行,谱系1已替代谱系8.7成为主要流行谱系,并分布于我国大多数省份;谱系3仅次于谱系1,主要在华南局部地区流行;谱系8.7毒株检出率较低。近几年来,PRRSV在我国的流行日趋复杂,谱系1毒株的广泛流行增加了PRRSV的遗传多样性。
| [1] |
BENFIELD D A, NELSON E, COLLINS J E, et al. Characterization of swine infertility and respiratory syndrome (SIRS) virus (isolate ATCC VR-2332)[J]. J Vet Diagn Invest, 1992, 4(2): 127-133. DOI:10.1177/104063879200400202 |
| [2] |
SPILMAN M S, WELBON C, NELSON E, et al. Cryo-electron tomography of porcine reproductive and respiratory syndrome virus: organization of the nucleocapsid[J]. J Gen Virol, 2009, 90(3): 527-535. DOI:10.1099/vir.0.007674-0 |
| [3] |
郭振华, 阮海宇, 耿瑞, 等. 1株类NADC30与类JXA1重组的猪繁殖与呼吸综合征病毒基因组遗传特征分析[J]. 畜牧兽医学报, 2020, 51(7): 1677-1687. GUO Z H, RUAN H Y, GENG R, et al. Genetic characteristics of a recombinant porcine reproductive and respiratory syndrome virus between NADC30-like and JXA1-like[J]. Acta Veterinaria et Zootechnica Sinica, 2020, 51(7): 1677-1687. (in Chinese) |
| [4] |
HAN K, SEO H W, PARK C, et al. Comparative virulence of reproductive diseases caused by type 1 (European-like) and type 2 (north American-like) porcine reproductive and respiratory syndrome virus in experimentally infected pregnant gilts[J]. J Comp Pathol, 2014, 150(2-3): 297-305. DOI:10.1016/j.jcpa.2013.11.205 |
| [5] |
CHEN J, LIU T, ZHU C G, et al. Genetic variation of Chinese PRRSV strains based on ORF5 sequence[J]. Biochem Genet, 2006, 44(9-10): 421-431. DOI:10.1007/s10528-006-9039-9 |
| [6] |
XIE J, WANJUN Z, YE C, et al. Molecular epidemiology of PRRSV in South China from 2007 to 2011 based on the genetic analysis of ORF5[J]. Microb Pathog,, 2013, 63: 30-36. DOI:10.1016/j.micpath.2013.05.013 |
| [7] |
SUN Y F, YU H, JIANG X, et al. Novel ORF5 deletion of NADC30-like porcine reproductive and respiratory syndrome viruses circulating in Northern China from 2016 to 2018[J]. J Vet Diagn Invest, 2020, 32(6): 928-932. DOI:10.1177/1040638720954543 |
| [8] |
BAO H Y, LI X D. Emergence and spread of NADC34‐like PRRSV in China[J]. Transbound Emerg Dis, 2021, 68(6): 3005-3008. DOI:10.1111/tbed.14316 |
| [9] |
PIRZADEH B, GAGNON C A, DEA S. Genomic and antigenic variations of porcine reproductive and respiratory syndrome virus major envelope GP5 glycoprotein[J]. Can J Vet Res, 1998, 62(3): 170-177. |
| [10] |
YOON S H, SONG J Y, LEE C H, et al. Genetic characterization of the Korean porcine reproductive and respiratory syndrome viruses based on the nucleocapsid protein gene (ORF7) sequences[J]. Arch Virol, 2008, 153(4): 627-635. DOI:10.1007/s00705-007-0027-0 |
| [11] |
张洪亮, 张文立, 许浒, 等. 2014年~2019年PRRSV主要流行毒株在我国的变化[J]. 中国预防兽医学报, 2020, 42(5): 512-516. ZHANG H L, ZHANG W L, XU H, et al. The changes of mainly endemic PRRSV in China during 2014-2019[J]. Chinese Journal of Preventive Veterinary Medicine, 2020, 42(5): 512-516. (in Chinese) |
| [12] |
杨汉春, 黄芳芳, 郭鑫, 等. 猪繁殖与呼吸综合征病毒(PRRSV)BJ-4株全基因组序列测定与分析[J]. 农业生物技术学报, 2001, 9(3): 212-218. YANG H C, HUANG F F, GUO X, et al. Sequencing of genome of porcine reproductive and respiratory syndrome virus isolate BJ-4[J]. Journal of Agricultural Biotechnology, 2001, 9(3): 212-218. (in Chinese) |
| [13] |
GUO Z H, CHEN X X, LI X, et al. Prevalence and genetic characteristics of porcine reproductive and respiratory syndrome virus in central China during 2016-2017:NADC30-like PRRSVs are predominant[J]. Microb Pathog, 2019, 135: 103657. DOI:10.1016/j.micpath.2019.103657 |
| [14] |
刘建奎, 徐叶, 刘辰, 等. 基于全基因组分析2017—2021年福建省猪繁殖与呼吸综合征病毒基因组特征[J]. 畜牧兽医学报, 2023, 54(4): 1579-1589. LIU J K, XU Y, LIU C, et al. Genomic characteristics of porcine reproductive and respiratory syndrome virus in Fujian Province from 2017 to 2021 based on whole genome[J]. Acta Veterinaria et Zootechnica Sinica, 2023, 54(4): 1579-1589. (in Chinese) |
| [15] |
ZHAO H J, HAN Q G, ZHANG L, et al. Emergence of mosaic recombinant strains potentially associated with vaccine JXA1-R and predominant circulating strains of porcine reproductive and respiratory syndrome virus in different provinces of China[J]. Virol J, 2017, 14(1): 67. DOI:10.1186/s12985-017-0735-3 |
| [16] |
SUN Y K, HAN X L, WEI Y F, et al. Phylogeography, phylodynamics and the recent outbreak of lineage 3 porcine reproductive and respiratory syndrome viruses in China[J]. Transbound Emerg Dis, 2019, 66(5): 2152-2162. DOI:10.1111/tbed.13269 |
| [17] |
XU H, SONG S J, ZHAO J, et al. A potential endemic strain in China: NADC34-like porcine reproductive and respiratory syndrome virus[J]. Transbound Emerg Dis, 2020, 67(4): 1730-1738. DOI:10.1111/tbed.13508 |
| [18] |
蒋智勇, 楚品品, 陈天宝, 等. 广东省猪繁殖与呼吸综合征病毒ORF5基因遗传变异分析[J]. 广东农业科学, 2022, 49(4): 97-105. JIANG Z Y, CHU P P, CHEN T B, et al. Genetic variation analysis of ORF5 genes of porcine reproductive and respiratory syndrome virus in Guangdong Province[J]. Guangdong Agricultural Sciences, 2022, 49(4): 97-105. (in Chinese) |
| [19] |
CHEN N, TRIBLE B R, KERRIGAN M A, et al. ORF5 of porcine reproductive and respiratory syndrome virus (PRRSV) is a target of diversifying selection as infection progresses from acute infection to virus rebound[J]. Infect Genet Evol, 2016, 40: 167-175. DOI:10.1016/j.meegid.2016.03.002 |
| [20] |
THAA B, SINHADRI B C, TIELESCH C, et al. Signal peptide cleavage from GP5 of PRRSV: a minor fraction of molecules retains the decoy epitope, a presumed molecular cause for viral persistence[J]. PLoS One, 2013, 8(6): e65548. DOI:10.1371/journal.pone.0065548 |
| [21] |
CHEN N H, XIAO Y Z, YE M X, et al. High genetic diversity of Chinese porcine reproductive and respiratory syndrome viruses from 2016 to 2019[J]. Res Vet Sci, 2020, 131: 38-42. |
| [22] |
POPESCU L N, TRIBLE B R, CHEN N H, et al. GP5 of porcine reproductive and respiratory syndrome virus (PRRSV) as a target for homologous and broadly neutralizing antibodies[J]. Vet Microbiol, 2017, 209: 90-96. |
| [23] |
黄锦柳. 我国猪蓝耳病类NADC30毒株的研究进展[J]. 广东畜牧兽医科技, 2019, 44(5): 13-16. HUANG J L. Research progress of NAD30 strains of PRRS in China[J]. Guangdong Journal of Animal and Veterinary Science, 2019, 44(5): 13-16. (in Chinese) |
| [24] |
胡栋, 徐煜琳, 朱迎春, 等. 山东及周边部分地区猪繁殖与呼吸综合征病毒的变异与遗传演化分析[J]. 畜牧兽医学报, 2019, 50(6): 1249-1260. HU D, XU Y L, ZHU Y C, et al. The variations and analyses in genetic evolution of porcine reproductive and respiratory syndrome virus in Shandong Province and its neighboring areas[J]. Acta Veterinaria et Zootechnica Sinica, 2019, 50(6): 1249-1260. (in Chinese) |
| [25] |
梁俊超, 赵翔, 刘红祥, 等. 2020年我国部分地区猪繁殖与呼吸综合征分子流行病学调查[J]. 中国动物检疫, 2022, 39(8): 17-25. LIANG J C, ZHAO X, LIU H X, et al. Molecular epidemiological investigation on PRRS in 2020 in some regions of China[J]. China Animal Health Inspection, 2022, 39(8): 17-25. (in Chinese) |
(编辑 白永平)



