2. 江苏大学食品与生物工程学院,镇江 212013
2. School of Food and Biological Engineering, Jiangsu University, Zhenjiang 212013, China
耐甲氧西林金黄色葡萄球菌(methicillin-resistant S.aureus,MRSA)是一种高度且多重耐药的食源性致病菌,已被列为3大世界最难解决的感染性疾患之一。MRSA基因组中含有葡萄球菌染色体mec盒,后者携带mecA基因,其编码新的青霉素结合蛋白(penicillin binding proteins,PBPs)PBP2a,具有转糖基酶和转肽酶活力,通过催化转肽反应合成肽聚糖。PBPs是细菌细胞膜上能与β-内酰胺类抗生素结合的蛋白质,MRSA中包含6种PBPs(PBP1、PBP2、PBP3、PBP3’、PBP4和独特的PBP2a)。PBP2a和β-内酰胺类抗生素几乎没有亲和力,当其他PBPs与β-内酰胺类抗生素结合失去活性后,PBP2a仍可继续参与肽聚糖合成,因此MRSA对几乎所有β-内酰胺类抗生素均耐药[1]。此外,femX、femA 和femB等基因也对MRSA的耐药性起重要作用。MRSA是导致化脓性关节炎、皮肤和软组织感染、肺炎、脑膜炎和心内膜炎等严重感染的主要细菌病原体之一[2]。MRSA分泌的肠毒素热稳定性较好,100 ℃处理30 min后仍保持活性,是高温灭菌后引起食物MRSA中毒的主要原因[3-5]。
MRSA可通过食物链传播,近年来,世界范围内从肉类到乳制品等多种食品中都发现了MRSA[6-7]。易受MRSA污染的食物包括发酵制品、乳制品和肉鱼类制品等[3-4]。Jones等[8]在2002年首次报道了由社区获得性MRSA引起的食物中毒。检测美国5个城市的136份肉类样品发现,42%的猪肉感染了葡萄球菌(SA),其中,64%为MRSA感染[9]。在瑞士和日本的肉类产品中,SA的检出率分别为23%和65%。食用被MRSA污染的食物,极易引起呕吐、腹泻、肠胃炎等,严重时会引起食物中毒,甚至危及生命[12]。MRSA对食品安全构成了巨大威胁,占北美细菌性食物中毒的9.52%,每年约造成1.5亿美元的经济损失[13]。
目前,MRSA已发生转移,通过环境、畜牧业、食物链等进入人体,对人类健康造成严重威胁。2005年,首次证实猪源MRSA可通过猪传给人群。Boer等[13]在264/2217份样本中发现MRSA(11.9%),Neeling等[14]在荷兰9个屠宰场中抽取的209/540头猪鼻腔中有MRSA,每个屠宰场中均有生猪被检出带有MRSA。由于MRSA对四环素类、林可胺类、氨基糖苷类、大环内酯类和氟喹诺酮类等多种抗菌药物也有耐药性,使防治MRSA引起的牲畜感染非常困难,高效、安全的动物源MRSA新型抗菌药物急需开发[15-23]。
新型抗生素研发一般需要10~15年,而细菌耐药性产生仅需要2~3年,因此天然产物与抗生素联合抑菌被视作防治MRSA的研究热点之一。已发现的PBP2a天然产物抑制剂包括黄芩中的黄芩苷[24]、绿茶中的儿茶素[21]和表没食子儿茶素没食子酸酯(EGCg)[22]、大角莲中的柯里拉京[25]和玫瑰中的鞣质和特里马素[23]等。此外,小舌菊和四环素联用、黄连叶精油或姜花素D或刺苞菊醛和庆大霉素联用、鼠尾草酸和诺氟沙星等的联用皆能协同降低抗生素对MRSA的MIC,但协同抑菌机制并未得到清晰的阐明[30]。本研究从多种天然产物中进行抗MRSA筛选,并与抗生素进行联合抑菌试验,同时阐释天然产物与抗生素联合抑制MRSA的分子机制,为降低畜牧养殖中抗生素的使用、提高肉奶类食品安全奠定基础。
1 材料与方法 1.1 材料和仪器金黄色葡萄球菌(ATCC 6538)购自武汉大学菌种保藏中心,MRSA(ATCC 33591)购自美国模式菌种保藏中心(American type culture collection,ATCC),盐酸小檗碱(BBR)购自西安优硕生物科技有限公司,阿莫西林、左氧氟沙星、万古霉素、氯霉素、头孢唑林、青霉素、四环素均购自上海原叶生物有限公司;RNAprep Pure提取试剂盒、PrimeScriptTMRT reagent Kit with gDNA Eraser逆转录试剂盒、SYBRR Premix Ex TaqTM‖PCR试剂盒购自北京宝日医生物有限公司(TaKaRa),牛肉浸粉购自青岛海博生物技术有限公司,其他试剂均为分析纯,购自上海国药集团。
超净工作台购自苏净化设备有限公司,LRH系列生化培养箱购自一恒科学仪器有限公司,高压灭菌锅购自鸟取三洋电机,HYG-C型多功能摇床购自太仓试验设备厂。
1.2 试验方法 1.2.1 最低抑菌浓度(MIC)和最低杀菌浓度(MBC)检测1.2.1.1 天然产物配制 称取BBR 0.1 g,振荡后均匀溶解于1 mL水中,浓度为0.1 g·mL-1,过滤除菌后,4 ℃保存。
1.2.1.2 抗生素配制 称取7种抗生素0.012 8 g,溶解于1 mL无菌水中,浓度为12.8 mg·mL-1,过滤除菌后,-20 ℃避光保存。
1.2.1.3 MIC/MBC测定 按照微量肉汤稀释法进行。96孔板横排前十孔每孔加入10 μL水解酪蛋白培养基(MH培养基)后,在第1孔内加入10 μL BBR或者抗生素,均匀震荡后,吸出10 μL加入至第2孔,依次梯度稀释,直至第10孔。之后,每孔加入90 μL细菌培养液,使终体积为100 μL,细菌终浓度为5×105 CFU·mL-1。第11孔中加入100 μL的菌液作为阳性对照,第12孔采用空白NB培养基作为阴性对照。将96孔板在37 ℃培养24~48 h,以24 h无菌生长的最低浓度为MIC,48 h后肉眼无细菌生长的试管中取100 μL菌液涂平板;过夜培养后平板无菌生长的对应肉汤管中的最低药物浓度,即是MBC。每个试验重复3次,每次3个平行。
1.2.1.4 联合抑菌和FIC测定 采用棋盘法进行[26-27],96孔板中每横排从左至右依次加入5 μL抗生素(终浓度为2MIC~1/64MIC),每纵列从上至下依次加入5 μL BBR(终浓度为1/2 MIC~1/32 MIC),再加入90 μL菌液(终浓度为5×105 CFU·mL-1),终体积100 μL。分别加入100 μL的菌液和空白培养基为阳性和阴性对照。37 ℃培养24 h,无菌生长的最低浓度为抗生素和BBR联合抑菌MIC。
抑菌浓度指数(fractional inhibitory concentration, FIC)计算方法:
FIC=MIC(联合)/MIC(BBR)+MIC(联合)/MIC(抗生素)
协同:FIC≤0.5;相加:0.5 < FIC≤1;无关:1 < FIC≤2;拮抗:FIC>2。
1.2.2 时间杀灭曲线测定 设置BBR组(1/4 MIC BBR、1/2 MIC BBR和MIC BBR)、MIC抗生素组和联合组(1/8 MIC BBR+1/32 MIC抗生素),以无药物加入的NB培养液为对照,分别加入细菌培养物,使终浓度为1×107CFU·mL-1。7组试管于37 ℃振荡培养,定时取样,稀释后,涂NB平板,37 ℃培养12~24 h后计数。以时间为横坐标,以菌落总数的对数为纵坐标绘图,即时间杀灭曲线。
1.2.3 电导率测定 取100 μL细菌过夜培养物,稀释50倍后,分别加入BBR、抗生素和联合抑菌液,37 ℃振荡培养。于0、1、2、4、6、8 h分别定时取样,5 000 r·min-1离心10 min,吸取上清液,无菌水均匀稀释,测定电导率。每个试验重复3次,每次3个平行。
1.2.4 膜电位测定 细菌于NB培养基中37 ℃培养12 h,取100 μL过夜培养物分别转接到含有BBR、抗生素和联合抑菌液的培养基中,混合均匀,取100 μL混合液加入96孔板中,过夜培养。用5 μmol·L-1 DiBAC4(3) 缓冲液清洗96孔板3次,加入180 μL 5 μmol·L-1 DiBAC4(3)的缓冲液进行染色,37 ℃孵育30 min,多功能酶标仪3 min检测一次荧光强度。以无细菌的培养基为空白对照。
1.2.5 碱性磷酸酶(AKP)的测定 取100 μL细菌过夜培养物加入5 mL NB培养基中,再分别加入BBR、抗生素和联合抑菌液,37 ℃下振荡培养,0、1、2、4、6、8 h定时取500 μL样品,5 000 r·min-1离心10 min,用试剂盒测定AKP含量。
1.2.6 荧光实时定量PCR(RT-PCR) 细菌过夜活化,1∶100的比例转接到分别含有BBR、抗生素和联合抑菌液的NB培养基中,37 ℃培养12 h,提取mRNA,再逆转录成cDNA。以cDNA为模板,16S rRNA为内参基因,使用荧光定量试剂盒,测定mecA的表达水平。反应程序:95 ℃预变性30 s;95 ℃变性5 s,50~60 ℃退火30 s,72 ℃延伸30 s,40个循环;熔解曲线从65 ℃升至95 ℃,每5 s升温0.5 ℃。
1.2.7 转录组学检测 送北京诺禾致源有限公司协作完成。具体操作为提取样品的总mRNA,使用fragmentation buffer随机将其打断成短片段,按照链特异性建库的方式建库。在M-MuLV逆转录酶体系中,将片段化的mRNA作为模板,随机寡核苷酸作为引物,合成cDNA第一条链,随后用RNaseH降解RNA链,将dNTPs(将dNTP中的dTTP用dUTP取代)作为原料在DNA polymerase I体系下合成cDNA第二条链(使第二条链中包含A/U/C/G),再用AMPure XP beads筛选250~300 bp的cDNA,通过cDNA末端修复、加A尾、连接测序接头,并借助USER酶降解含U的cDNA第二链,再进行PCR扩增并获得文库。
库检合格后,根据有效浓度及目标下机数据量的需求对不同文库pooling后,再按照边合成边测序(sequencing by synthesis)的原理进行Illumina测序。添加4种荧光标记的dNTP、DNA聚合酶以及接头引物于测序的flow cell中进行扩增,当测序簇延伸互补链时,每添加一个被荧光标记的dNTP即可释放出相对应的荧光,并利用软件将测序仪接收到的荧光信号转化为测序峰,从而获得待测片段的序列信息。
1.2.8 生物信息学分析 对转录组学测序结果进行GO富集、KEGG富集和差异基因筛选。Q值≤0.05的通路定义为在显著差异表达基因中显著富集的通路。应用DESeq2方法计算不同样本之间基因表达量的差异,具有统计学显著差异的确定为差异表达基因。P值< 0.05,FDR≤0.01和差异表达倍数≥2的基因即显著差异表达基因。
2 结果 2.1 抗生素和BBR单独作用于SA/MRSA的MICBBR与抗生素单独作用于SA/MRSA的MIC/MBC见表 1。7种抗生素对SA/MRSA均有抑菌效果,但对MRSA的MIC显著高于SA,除万古霉素和氯霉素以外,其他5种抗生素对MRSA的MIC比SA高了100倍~2 000倍之多。其中,阿莫西林对SA的抑菌效果最佳,MIC为0.5 μg·mL-1;万古霉素对MRSA的抑菌效果最佳,MIC为2 μg·mL-1。BBR对SA和MRSA的抑菌效果一致,均为1 250 μg·mL-1。
|
|
表 1 不同抗生素对SA/MRSA的MIC和MBC Table 1 MICs and MBCs of different antibiotics against SA/MRSA |
BBR和7种抗生素联用对SA均具有协同抑菌作用,但只与4种抗生素联用能协同抑制MRSA(表 2)。其中,1/32 MIC BBR+1/64 MIC青霉素联用对SA具有最小的FIC值0.047,但对MRSA却呈现无关作用;1/32 MIC BBR+1/32 MIC阿莫西林联用对MRSA具有最小的FIC值0.063,1/16 MIC BBR+1/4 MIC左氧氟沙星对SA和MRSA的FIC均为0.313。由于阿莫西林对MRSA的MIC太高,为5 120 μg·mL-1,而左氧氟沙星仅为128 μg·mL-1,因此选择左氧氟沙星进行之后的试验。联合抑菌结果表明,BBR不但能够直接抑制MRSA,而且与β-内酰胺类抗生素联合使用能够恢复其对MRSA菌株的敏感性。
|
|
表 2 BBR与各抗生素联用对SA/MRSA作用对比 Table 2 Comparison of the effects of BBR combined with various antibiotics on SA/MRSA |
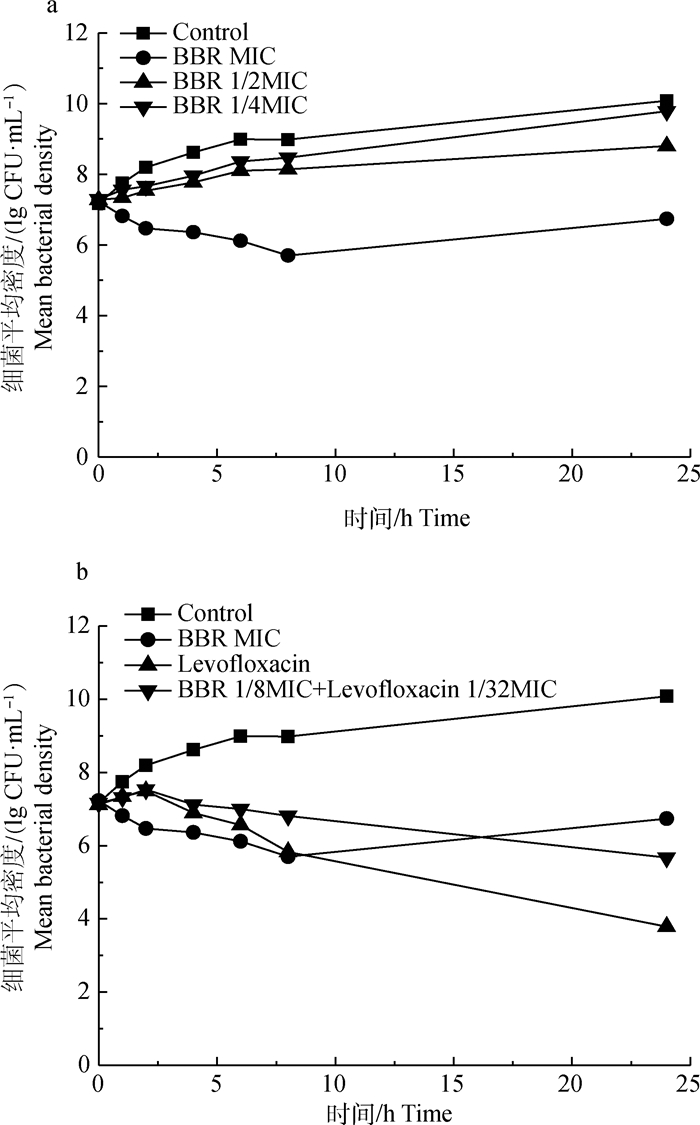
为了进一步评价BBR和左氧氟沙星的杀菌效果,作者测定了它们单独和联合分别作用于MRSA的时间杀灭曲线。当MRSA初始接种浓度为1×107CFU·mL-1时,24 h后MIC BBR组细菌显著下降,为(5.57±0.21)×106CFU·mL-1(P < 0.05);而1/4 MIC BBR组和1/2 MIC BBR组则分别为(6.17±0.15)×109和(6.3±0.2)×108CFU·mL-1,对照组细菌数可达(1.16±0.04)×1010CFU·mL-1 (图 1a)。24 h后,MIC左氧氟沙星组细菌数为(6.07±0.29)×103CFU·mL-1,而联合组则为(4.7±0.2)×105CFU·mL-1(图 1b)。联合组的抑菌效果不如左氧氟沙星单独作用,原因可能是因为复配浓度大幅度降低的原因,但两者联用依然可以抑制MRSA的生长繁殖,达到有效的MIC水平。
|
a.BBR;b. BBR和左氧氟沙星联合 a.BBR; b. The combination of BBR and levofloxacin 图 1 对MRSA的时间杀灭曲线 Fig. 1 Time-kill curve of drugs against MRSA |
电导率可以衡量细菌细胞膜的通透性,电导率越大,细胞膜被破坏越严重,因此可通过菌液电导率的变化判断细菌细胞膜的受损情况。结果表明,对照组菌液8 h内电导率无显著变化,BBR+左氧氟沙星联合组电导率变化率显著高于对照组但低于BBR组(P < 0.05)(图 2a)。

|
a.电导率变化;b.荧光强度变化;c.AKP活性 a. Conductivity change; b. Fluorescence intensity change; c. AKP activity 图 2 BBR和抗生素联用破坏MRSA细胞结构 Fig. 2 The combination of BBR and antibiotics destroyed the cell structure of MRSA |
DiBAC4(3)是一种亲脂性阴离子荧光染料,本身无荧光,但它能和细胞质中的蛋白质结合产生强烈荧光,当细胞膜受损,细胞荧光会大幅度增加。结果表明,对照组菌液30 min内荧光强度无显著变化,联合组的荧光强度显著高于对照组而低于BBR组(图 2b)。
AKP的活性表明细菌细胞壁的破损程度。8 h内,对照组AKP活性无显著变化,而联合组AKP活性显著高于对照组却显著低于BBR组(P < 0.05)(图 2c)。
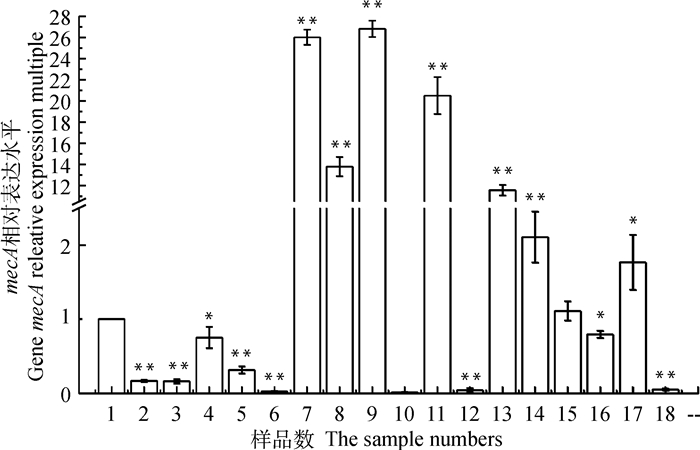
2.5 BBR和抗生素联用下调mecA表达图 3表明,BBR显著下调了mecA的相对表达水平,且呈现浓度依赖,与对照组相比,添加1/4 MIC、1/8 MIC和1/32 MIC BBR的mecA分别降低为对照组的16.69%、5.26%和75.19%(P < 0.05),说明mecA可能是BBR的作用靶点之一。左氧氟沙星组mecA表达上调26.82倍,而联合组却显著降低mecA的相对表达水平为对照的1.35%(P < 0.05)。BBR作用于mecA,使得MRSA细胞壁完整性降低,而左氧氟沙星作用于拓扑异构酶II,两者联用能大幅度协同下调mecA的表达。
|
1. 对照组; 2.1/4MIC BBR; 3.1/8MIC BBR; 4.1/32MIC BBR; 5.1/64MIC万古霉素;6.1/64MIC万古霉素+1/8MIC BBR;7.1/8MIC氯霉素;8.1/8MIC氯霉素+1/4MIC BBR;9.1/32MIC左氧氟沙星;10.1/32MIC左氧氟沙星+1/8MIC BBR; 11.1/32MIC阿莫西林;12.1/32MIC阿莫西林+BBR 1/8MIC; 13.1/16MIC红霉素;14.1/16MIC红霉素+BBR 1/8MIC;15.1/8MIC四环素;16.1/8MIC四环素+BBR 1/4MIC;17.1/64MIC磺胺甲恶唑;18.1/64MIC磺胺甲恶唑+1/32MIC BBR组 1. Control group; 2. BBR 1/4MIC group; 3. BBR 1/8MIC group; 4. BBR 1/32MIC group; 5. Vancomycin 1/64MIC group; 6. Vancomycin 1/64MIC+BBR 1/8MIC group; 7. Chloramphenicol 1/8MIC group; 8. Chloramphenicol 1/8MIC +BBR 1/4MIC group; 9. Levofloxacin 1/32MIC group; 10. Levofloxacin 1/32MIC+BBR 1/8MIC group; 11. Amoxicillin 1/32MIC group; 12. Amoxicillin 1/32MIC+BBR 1/8MIC group; 13. Erythromycin 1/16MIC group; 14. Erythromycin 1/16MIC+BBR 1/16MIC group; 15. Tetracycline 1/8MIC group; 16. Tetracycline 1/8MIC+BBR 1/4MIC group; 17. Sulfamethoxazole 1/64MIC group; 18. Sulfamethoxazole 1/64MIC+BBR 1/32MIC group 图 3 mecA基因表达变化 Fig. 3 The mecA expression change of MRSA |
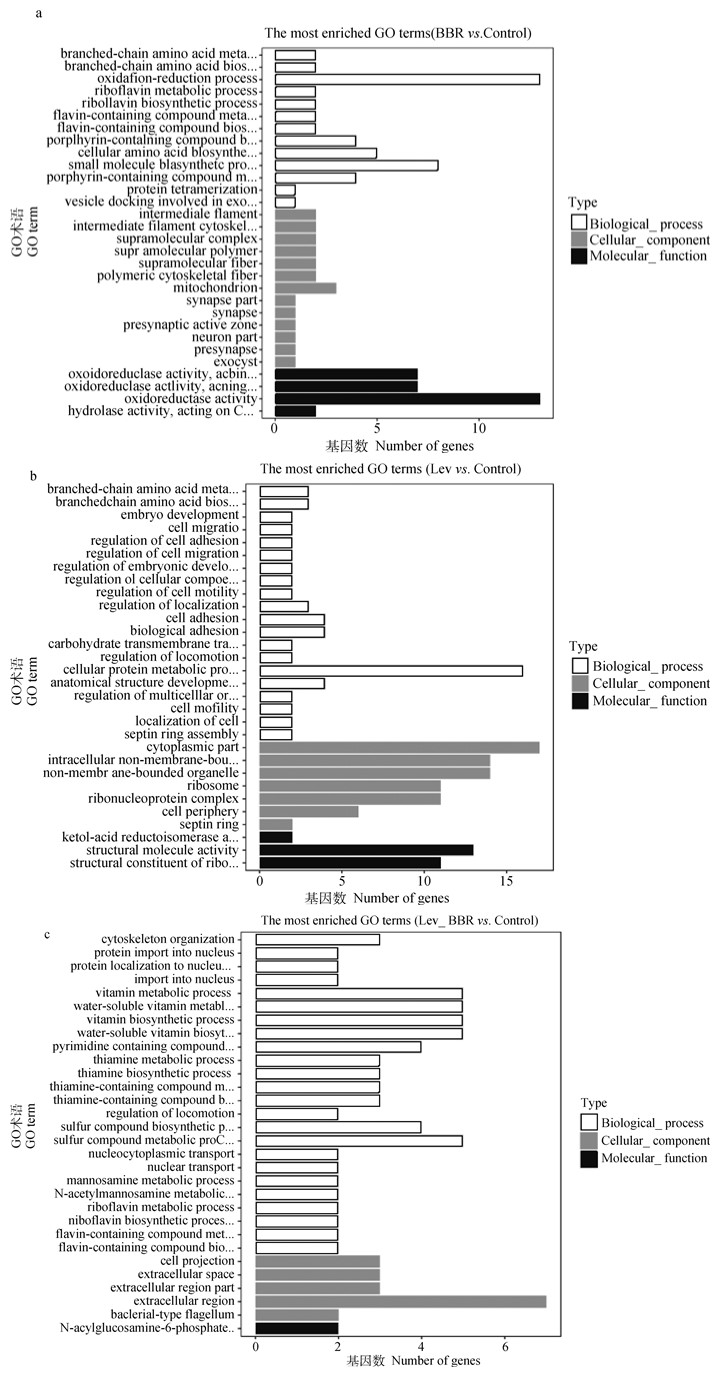
GO富集结果(图 4)表明,BBR影响MRSA 73个基因的表达,重要的上调基因功能包括氧化还原、氨基酸和维生素的合成与代谢,重要的下调基因功能包括转录和同化。
|
a. BBR; b. 左氧氟沙星;c. 联合组 a. BBR; b. Levofloxacin; c. Combination group 图 4 差异表达基因GO富集 Fig. 4 Go enrichment of differentially expressed genes |
左氧氟沙星影响MRSA 114个基因的表达,重要的上调基因功能包括有机氮化合物的合成和代谢、细胞酰胺合成和代谢过程以及碳水化合物跨膜转运,重要的下调基因功能包括药物反应、发展过程、对化学物质的反应和磷脂生物合成过程。细胞膜由磷脂双分子层构成,左氧氟沙星使得磷脂合成受到抑制,则细胞膜更易受到破坏,细菌细胞膜通透性增加、细胞形态难以维持。这可能是两者联用导致mec A表达下调的原因之一。
联合组影响MRSA 95个基因的表达,重要的上调基因功能包括维生素合成和代谢、细胞骨架组织、嘧啶化合物代谢过程和硫化合物的生物合成过程,重要的下调基因功能主要包括氨基酸、阴离子、有机酸和羧酸的运输和跨膜转运。
表 3~5总结了BBR、左氧氟沙星和联合组的KEGG富集结果。其中,与BBR抑菌有关的可能为维生素B2代谢、β-内酰胺抗性、双组分系统和多样环境中的微生物代谢,与左氧氟沙星组抑菌有关可能为甘油磷脂代谢,与联合组抑菌有关的代谢通路可能为维生素B2代谢和ABC转运体。
|
|
表 3 BBR KEGG富集汇总 Table 3 KEGG enrichment summary of the BBR group |
|
|
表 4 左氧氟沙星组主要代谢通路的KEGG富集汇总 Table 4 KEGG enrichment summary of the levofloxacin group |
|
|
表 5 联合组KEGG富集汇总 Table 5 KEGG enrichment summary of the combination group |
与对照组相比,BBR、左氧氟沙星和联合组的重要差异表达基因如表 6。BBR组seaR和seaS基因表达量与对照组相比分别下调为对照的42.92%和44.05%;BBR组、左氧氟沙星组及联合组中msc L基因表达量均显著下调,分别下调为对照组的46.73%、36.63%和43.67%;ribA在BBR组和联合组均表现为上调,上调倍数分别为2.69和3.64倍。
|
|
表 6 重要差异表达基因 Table 6 Important differentially expressed genes |
β-内酰胺类抗生素的β-内酰胺核能不可逆地与PBPs的Ser 403位点结合,竞争转肽酶的活性位点从而阻止肽聚糖合成,抑制细胞壁合成,导致细菌死亡。当正常PBPs与β-内酰胺类抗生素结合失去活性时,PBP2a可以代替它们合成继续肽聚糖,从而维持MRSA的生长繁殖[17]。
虽然阿莫西林、青霉素和头孢唑林均作用于MRSA的细胞壁,但它们和BBR联用产生的抑菌效果不同,推测可能是由于它们对MRSA细胞壁的作用靶点不同。PBP2a在其余PBPs失去活性后仍能维持MRSA的细胞壁形态。研究认为,两种药物联用时,作用靶位相同会产生拮抗作用,当联用的两种药物分别作用于不同的PBPs时可产生协同作用;或者两种药物联用,而其中一种发挥β-内酰胺酶作用时,亦可产生协同作用[31]。青霉素作用位点为PBP1,头孢唑林抗菌的作用位点主要为PBP1和PBP3,低浓度的阿莫西林可使PBP4及PBP5达到部分饱和。当三者和BBR联用,头孢唑林和阿莫西林继续协同抑制SA和MRSA,青霉素则失去协同抑制MRSA的效果,这也许说明BBR对MRSA的一个作用位点可能是PBP1。左氧氟沙星主要作用靶位是拓扑异构酶II,因此和BBR具有协同作用。
BBR组的电导率和荧光强度显著高于抗生素组和联合组,可能是因为其能够增加细胞膜通透性,促进物质泄漏。细胞膜不是左氧氟沙星的作用靶点,而BBR可通过增加细胞膜通透性,从而与其产生协同抑菌作用。BBR与左氧氟沙星联用时,荧光强度显著大于对应抗生素组,表明MRSA细胞产生超极化现象,抗生素更易进入细胞内。BBR能提高提升细胞壁通透性,当其降低浓度与左氧氟沙星联用时,细菌AKP活性增高,表明联用后细胞壁进一步受到破坏,细胞形态完整性难以维持,抗生素更容易突破胞壁屏障,进入细胞体内,从而造成更好的杀菌效果[16]。
天然产物往往具有多种抑菌机制,mecA基因可能只是其中一个靶点,为了进一步寻找联合抑菌机制,作者对BBR组、左氧氟沙星组和联合组进行了转录学的研究,对其差异基因进行GO富集、KEGG分析和显著差异基因的比较。
ABC转运体中的fhuA是一种铬铁-铁受体,属于外膜蛋白家族,它与能量转换蛋白TonB一起,介导含铁载体通过革兰阴性菌外膜的主动转运。ABC转运体可催化脂双层的脂类在两层之间翻转,对膜的发生和功能具有重要的意义,还与细菌对药物的抗性有关, 其表达下调也许说明MRSA细胞内药物的聚集。
seaR和seaS基因调控MRSA中一种保守的双组分调节系统(two-component regulatory systems, TCSs),参与生物膜的生成、荚膜多糖的合成、自我分解、抗生素抗性及血红素毒素的抗性等[19]。seaR和seaS编码感应器蛋白(如Spa和Fnba)及细胞壁相关蛋白(如Eap和Emp)。seaS受到外界信号激活后发生自主磷酸化,随后磷酸化seaR,磷酸化的seaR结合到P1启动子区,和RNA聚合酶共同调控转录过程。BBR可通过下调seaR和seaS基因表达,抑制MRSA细胞膜、细胞壁合成和抗生素抗性基因的表达。
ribA 和Msc L可能是BBR和左氧氟沙星联合抑菌的重要差异基因。
维生素B2在生物氧化过程中发挥递氧的作用,参与糖、蛋白质和脂肪代谢。ribA基因表达上调不仅限制维生素B2的合成,其基因编码的双功能酶的催化还会导致下游产物5-氨基-6-(D-核糖氨基)尿嘧啶的积累,这种高活性嘧啶二酮化合物对细胞的毒害作用可造成细胞自溶。norA是MRSA的固有多药耐药外排泵,与MRSA的耐药性极度相关。受到左氧氟沙星的诱导后,norA的表达大幅度增加,从而使进入细胞内的药物被更多更快的泵出体内,最终造成细胞耐药[27]。很多文献已经证实这点,并以norA为调控靶点,寻找天然外排泵抑制剂[28-29]。
Msc L是一种机械敏感通道(mechanosensitive channels, MS),是一种跨膜通道蛋白,可感受细胞膜表面的张力。mscL起到“紧急释放阀”的作用,当细菌的外部环境渗透压急剧变化引起细胞膨胀,细胞膜上产生张力时,msc L直接感知张力形成一个直径约为3 nm的通道,释放胞内物质维持渗透压的平衡,从而避免细胞的裂解[20]。mscL基因的下调直接限制了这一调控机制,使得MRSA对外界渗透压变化的耐受能力显著降低,较小的渗透压变化即可使细胞破裂。
4 结论BBR不但能够直接抑制MRSA,且与β-内酰胺类抗生素联合使用时能够恢复其对MRSA菌株的敏感性,大幅度降低抗生素的使用水平。BBR和左氧氟沙星联用对MRSA效果最佳,可降低左氧氟沙星的MIC至原来的1/16。联合抑菌的靶点为细胞壁和细胞膜,包括破坏细胞壁,增加细胞膜的通透性,上调ribA和下调mec A和msc L表达水平,从而达到协同抑菌的目的。
| [1] |
ZEOUK I, OUEDRHIRI W, SIFAOUI I, et al. Bioguided isolation of active compounds from Rhamnus alaternus against methicillin-resistant Staphylococcus aureus (MRSA) and panton-valentine leucocidin positive strains (MSSA-PVL)[J]. Molecules, 2021, 26: 4352. DOI:10.3390/molecules26144352 |
| [2] |
MORATA L, MENSA J, SORIANO A. New antibiotics against gram-positives: present and future indications[J]. Curr Opin Pharmacol, 2015, 24: 45-51. DOI:10.1016/j.coph.2015.07.004 |
| [3] |
NORMANNO G, CORRENTE M, LA SALANDRA G, et al. Methicillin-resistant Staphylococcus aureus (MRSA) in foods of animal origin product in Italy[J]. Int J Food Microbiol, 2007, 117(2): 219-222. DOI:10.1016/j.ijfoodmicro.2007.04.006 |
| [4] |
CRAGO B, FERRATO C, DREWS S J, et al. Prevalence of Staphylococcus aureus and methicillin-resistant S. aureus (MRSA) in food samples associated with foodborne illness in Alberta, Canada from 2007 to 2010[J]. Food Microbiol, 2012, 32(1): 202-205. DOI:10.1016/j.fm.2012.04.012 |
| [5] |
李毅. 金黄色葡萄球菌及其肠毒素研究进展[J]. 中国卫生检验杂志, 2004, 14(4): 392-395. LI Y. Advancement in researches of Staphylococcus aureus and its enterotoxin[J]. Chin J Health Lab Technol, 2004, 14(4): 392-395. DOI:10.3969/j.issn.1004-8685.2004.04.003 (in Chinese) |
| [6] |
OLSEN S J, DEBESS E E, MCGIVERN T E, et al. A nosocomial outbreak of fluoroquinolone-resistant Salmonella infection[J]. N Engl J Med, 2001, 344(21): 1572-1579. DOI:10.1056/NEJM200105243442102 |
| [7] |
KÖCK R, BECKER K, COOKSON B, et al. Methicillin-resistant Staphylococcus aureus (MRSA): burden of disease and control challenges in Europe[J]. Euro Surveill, 2010, 15(41): 19688. |
| [8] |
JONES T F. An outbreak of community-acquired foodborne illness caused by methicillin-resistant Staphylococcus aureus[J]. Emerg Infect Dis, 2002, 8(1): 82-84. DOI:10.3201/eid0801.010174 |
| [9] |
WATERS A E, CONTENTE-CUOMO T, BUCHHAGEN J, et al. Multidrug-resistant Staphylococcus aureus in US meat and poultry[J]. Clin Infect Dis, 2011, 52(10): 1227-1230. DOI:10.1093/cid/cir181 |
| [10] |
SCHRAFT H, KLEINLEIN N, UNTERMANN F. Contamination of pig hindquarters with Staphylococcus aureus[J]. Int J Food Microbiol, 1992, 15(1-2): 191-194. DOI:10.1016/0168-1605(92)90148-V |
| [11] |
KITAI S, SHIMIZU A, KAWANO J, et al. Prevalence and characterization of Staphylococcus aureus and enterotoxigenic Staphylococcus aureus in retail raw chicken meat throughout Japan[J]. J Vet Med Sci, 2005, 67(3): 269-274. DOI:10.1292/jvms.67.269 |
| [12] |
KLUYTMANS J A J W. Methicillin-resistant Staphylococcus aureus in food products: cause for concern or case for complacency?[J]. Clin Microbiol Infect, 2010, 16(1): 11-15. DOI:10.1111/j.1469-0691.2009.03110.x |
| [13] |
DE BOER E, ZWARTKRUIS-NAHUIS J T M, WIT B, et al. Prevalence of methicillin-resistant Staphylococcus aureus in meat[J]. Int J Food Microbiol, 2009, 134(1-2): 52-56. DOI:10.1016/j.ijfoodmicro.2008.12.007 |
| [14] |
DE NEELING A J, VAN DEN BROEK M J M, SPALBURG E C, et al. High prevalence of methicillin resistant Staphylococcus aureus in pigs[J]. Vet Microbiol, 2007, 122(3-4): 366-372. DOI:10.1016/j.vetmic.2007.01.027 |
| [15] |
PEREIRA V, LOPES C, CASTRO A, et al. Characterization for enterotoxin production, virulence factors, and antibiotic susceptibility of Staphylococcus aureus isolates from various foods in Portugal[J]. Food Microbiol, 2009, 26(3): 278-282. DOI:10.1016/j.fm.2008.12.008 |
| [16] |
CHEN L J, WANG J, LEVIN R E. Effect of benzylpenicillin on the viability and osmotic sensitivity of Listeria monocytogenes[J]. Lett Appl Microbiol, 1996, 22(1): 10-12. DOI:10.1111/j.1472-765X.1996.tb01096.x |
| [17] |
WU S W, LENCASTRE H D, SALI A, et al. A phosphoglucomutase-like gene essential for the optimal expression of methicillin resistance in Staphylococcus aureus: molecular cloning and DNA sequencing[J]. Microb Drug Resist, 1996, 2(2): 277-286. DOI:10.1089/mdr.1996.2.277 |
| [18] |
ITO T, OKUMA K, MA X X, et al. Insights on antibiotic resistance of Staphylococcus aureus from its whole genome: genomic island SCC[J]. Drug Resist Updat, 2003, 6(1): 41-52. DOI:10.1016/S1368-7646(03)00003-7 |
| [19] |
GARDETE S, WU S W, GILL S, et al. Role of VraSR in antibiotic resistance and antibiotic-induced stress response in Staphylococcus aureus[J]. Antimicrob Agents Chemother, 2006, 50(10): 3424-3434. DOI:10.1128/AAC.00356-06 |
| [20] |
OU X R, BLOUNT P, HOFFMAN R J, et al. One face of a transmembrane helix is crucial in mechanosensitive channel gating[J]. Proc Natl Acad Sci U S A, 1998, 95(19): 11471-11475. DOI:10.1073/pnas.95.19.11471 |
| [21] |
TAKAHASHI O, CAI Z, TODA M, et al. Appearance of antibacterial activity of oxacillin against methicillin resistant Staphylococcus aureus (MRSA) in the presence of catechin[J]. Kansenshogaku Zasshi, 1995, 69(10): 1126-1134. DOI:10.11150/kansenshogakuzasshi1970.69.1126 |
| [22] |
SURESH B, SRIRAM S, DHANARAJ S A, et al. Anticandidal activity of Santolina chamaecyparissus volatile oil[J]. J Ethnopharmacol, 1997, 55(2): 151-159. DOI:10.1016/S0378-8741(96)01490-0 |
| [23] |
SHIOTA S, SHIMIZU M, MIZUSIMA T, et al. Restoration of effectiveness of β-lactams on methicillin-resistant Staphylococcus aureus by tellimagrandin I from rose red[J]. FEMS Microbiol Lett, 2000, 185(2): 135-138. |
| [24] |
LIU I X, DURHAM D G, RICHARDS R M E. Baicalin synergy with β-lactam antibiotics against methicillin-resistant Staphylococcus aureus and other β-lactam-resistant strains of S. aureus[J]. J Pharm Pharmacol, 2000, 52(3): 361-366. |
| [25] |
SHIMIZU M, SHIOTA S, MIZUSHIMA T, et al. Marked potentiation of activity of β-lactams against methicillin-resistant Staphylococcus aureus by corilagin[J]. Antimicrob Agents Chemother, 2001, 45(11): 3198-3201. DOI:10.1128/AAC.45.11.3198-3201.2001 |
| [26] |
GUO Q, ZHANG C Y, CAO Q G, et al. Synergistic inhibition effects of tea polyphenols as adjuvant of oxytetracycline on Vibrio parahaemolyticus and enhancement of Vibriosis resistance of Exopalaemon carinicauda[J]. Aquacult Res, 2021, 52(8): 3900-3910. DOI:10.1111/are.15234 |
| [27] |
SUNDARAMOORTHY N S, MITRA K, GANESH J S, et al. Ferulic acid derivative inhibits nora efflux and in combination with ciprofloxacin curtails growth of mrsa in vitro and in vivo[J]. Microb Pathog, 2018, 124: 54-62. DOI:10.1016/j.micpath.2018.08.022 |
| [28] |
TINTINO S R, OLIVEIRA-TINTINO C D M, CAMPINA F F, et al. Evaluation of the tannic acid inhibitory effect against the nora efflux pump of Staphylococcus aureus[J]. Microb Pathog, 2016, 97: 9-13. DOI:10.1016/j.micpath.2016.04.003 |
| [29] |
SHARIFI A, MOHAMMADZADEH A, MAHMOODI P, et al. Inhibitory effect of thymus daenensis essential oil on Staphylococcus aureus NorA efflux pump[J]. J Adv Med Biomed Res, 2016, 24(105): 67-77. |
| [30] |
彭勤, 凌保东, 蔺飞, 等. 中药单体与抗菌药物联合应用对抗泛耐药鲍曼不动杆菌的作用研究[J]. 中药药理与临床, 2020, 36(2): 140-145. PENG Q, LING B D, LIN F, et al. Research on the effects of traditional chinese medicine monomer combined with antibacterial drugs against extensively drug resistant Acinetobacter baumannii[J]. Pharmacology and Clinics of Chinese Materia Medica, 2020, 36(2): 140-145. (in Chinese) |
| [31] |
《抗菌药物临床应用指导原则》修订工作组. 抗菌药物临床应用指导原则(2015版)[M]. 北京: 人民卫生出版社, 2015.
|
| [34] |
Working group on revision of Guiding Principles for Clinical Use of Antimicrobial Agents. Guiding principles for clinical application of antibiotics (2015 Edition)[M]. Beijing: People's Medical Publishing House, 2015.
|
(编辑 白永平)



