2. 中国农业大学动物医学院,北京 100193
2. College of Veterinary Medicine, China Agricultural University, Beijing 100193, China
犬呼吸道冠状病毒(canine respiratory coronavirus,CRCoV)首次发现于2003年英国的某家大型流浪动物中心[1],CRCoV与犬肠道冠状病毒(canine coronavirus,CCoV,属于α冠状病毒属)的同源性低(在稳定的聚合酶基因上的核苷酸相似性仅为69%,而在可变区的氨基酸序列相似性仅为21%),但与牛冠状病毒同源性很高(90%以上)[2],因此被归类于β冠状病毒属。CRCoV主要侵害犬的呼吸道,尤其是咽扁桃体和气管[1]。单独感染通常只引起轻度的呼吸道症状,如喷嚏、鼻流分泌物和干咳[3-4]等。免疫力强的犬也可能表现为无呼吸道症状。该病的潜伏期为6~10 d,感染后6 d可通过口咽途径排毒[5]。迄今为止,尚无针对CRCoV感染的特异性疗法及针对该病毒的疫苗。
CRCoV在全球范围内多个国家和地区广泛流行[6-12],但国内的流行性研究报道较少。临床上,CRCoV还可与其他呼吸道病原体发生混合感染,这可能对犬类造成较为严重的健康威胁。本研究对CRCoV进行流行病学、致病特点等方面的调查,以期对CRCoV有更为深入的了解,从而有利于对犬传染性呼吸道疾病进行防治,保障动物健康。
1 材料与方法 1.1 试验材料2015年12月—2017年3月,于中国农业大学动物医院收集的487份犬咽鼻拭子。
病毒基因组DNA/RNA快速提取试剂盒Ⅱ购自北京艾德莱生物科技有限公司。AMV reverse transcriptase反转录试剂购自Promega公司(USA)。2×Taq PCR MasterMix试剂购自北京康润诚业生物科技有限公司。琼脂糖购自Biowest(西班牙)。Goldview核酸染料购自北京赛百盛基因技术有限公司。PCR引物及PCR产物序列测定由三博生物工程技术有限公司完成。采用PrimerPremier 5.0软件设计引物。
1.2 试验方法1.2.1 CRCoV RT-PCR检测方法的建立和临床样本的检测 ① 引物:选择Erles等[1]检测CRCoV所使用的巢式引物,经生物学软件Primer评估合格后进行合成。扩增序列位于S基因,引物序列及扩增片段长度见表 1。②核酸提取及PCR扩增:按照RNA提取试剂盒说明提取鼻咽拭子样本中的总RNA,使用反转录试剂进行RNA反转录,然后利用巢式PCR检测方法对CRCoV目的片段进行特异性扩增。扩增分为两步,第一步以反转录获得的DNA为模板,使用外围引物(CRCoV NO-up, CRCoV NO-down)进行CRCoV特异性PCR扩增;第二步以上述PCR产物为模板,用内围引物(CRCoV NI-up, CRCoV NI-down)进行CRCoV特异性PCR扩增。③凝胶电泳及成像:将PCR扩增产物加入1%琼脂糖凝胶中进行电泳,利用SIM成像系统进行观察,保存图像并记录试验结果。将阳性扩增产物送至三博生物工程技术有限公司进行进行序列测定和分析,并将测序鉴定结果为CRCoV阳性的样本于-20 ℃保存,作为阳性质控。
|
|
表 1 CRCoV检测用PCR引物 Table 1 PCR primer for detecting CRCoV |
此CRCoV巢式PCR方法验证成功后,收集有或无临床症状的临床样本进行CRCoV检测并记录检测结果,用于后续分析。
1.2.2 犬腺病毒Ⅱ型、犬副流感病毒和犬瘟热病毒PCR/RT-PCR检测 采用本实验室[13]已经建立的犬腺病毒Ⅱ型(canine adenovirus type 2,CAV-2)、犬副流感病毒(canine parainfluenza virus,CPIV)和犬瘟热病毒(canine distemper virus,CDV)的PCR/RT-PCR检测方法对部分样本进行检测,所用引物见表 2。阳性质控品为硕腾卫佳伍疫苗。CPIV、CAV-2和CDV的检测用引物序列及扩增片段长度见表 2。
|
|
表 2 CPIV、CAV-2、CDV检测用PCR引物 Table 2 PCR primer for detecting CPIV, CAV-2, CDV |
1.2.3 统计分析 利用Microsoft Excel 2007软件进行数据录入、整理和分析。本试验中涉及的分类资料间的差异性情况通过卡方检验进行比较,通过回归统计对CRCoV感染率与年龄的关系进行分析。P < 0.05表示差异显著,P < 0.01差异极显著。
2 结果 2.1 验证CRCoV检测方法的特异性及稳定性对临床样本进行CRCoV盲测,部分样品扩增后电泳得到了预期大小的目的条带,图 1为盲测的CRCoV阳性样本电泳图。

|
1. CRCoV第一轮扩增结果;2. CRCoV第二轮结果;N.阴性对照;M. DNA相对分子质量标准 1. CRCoV first round; 2. CRCoV second round; N. Negative control; M. DNA molecular weight marker 图 1 CRCoV阳性样本PCR扩增结果 Fig. 1 PCR results of CRCoV-positive samples |
将3个不同时间内获得的CRCoV阳性扩增产物进行核苷酸测序,测序结果在Nucleotide BLAST上比对,发现第一轮和第二轮扩增条带的核苷酸序列与已知的CRCoV毒株及牛冠状病毒毒株的符合率均在96%以上,而与CCoV毒株的符合率均低于50%。这与国外研究结论相同[1],可表明该CRCoV的检测方法特异性高。对硕腾卫佳伍疫苗(含CPIV、CAV-2、CDV)及临床中获得的CCoV阳性粪便样本进行CRCoV RT-PCR检测,结果为阴性,说明CRCoV可被特异检出。
用所设计的PCR方法对5个CRCoV阳性样本各进行3次重复性试验,均扩增出相应目的条带,无其他杂带,说明该引物和该方法稳定性良好,可长期使用。
2.2 CRCoV、CPIV、CAV-2、CDV检出情况对所有487份样品进行CRCoV巢式RT-PCR检测,其中有104份检出阳性,阳性率为21.36%;对2016年6月―2017年3月的321份样品进行CPIV RT-PCR检测,其中50份检出阳性,阳性率15.58%;对2016年11月―2017年3月的156份样品进行CDV RT-PCR检测,其中22份检出阳性,阳性率14.10%;对2016年11月―2017年3月的156份样品进行CAV-2 PCR检测,其中4份检出阳性,阳性率2.56%(表 3)。
|
|
表 3 CRCoV、CPIV、CAV-2、CDV检出情况 Table 3 The detection of CRCoV, CPIV, CAV-2, CDV |
CRCoV、CPIV混合感染的样本数为11,CRCoV、CAV-2混合感染的样本数为0,CRCoV、CDV混合感染的样本数为6。CRCoV与CPIV、CAV-2、CDV的混合感染率分别为3.43%(11/321)、0%(0/156)和3.85%(6/156)。
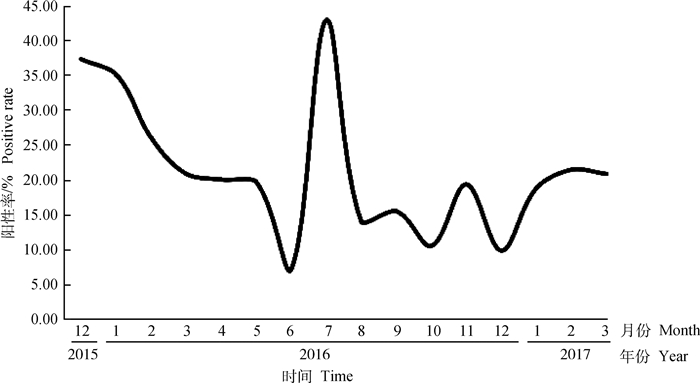
2.3 CRCoV流行趋势2015年12月—2017年3月病毒检出情况见图 2。整体而言,CRCoV在2015年末和2016年初的检出率较高,随着气候变暖,检出率逐渐下降(除7月份的检出率较高),在2016年11月气候转冷时又有上升趋势。
|
图 2 2015年12月―2017年3月各月份CRCoV检出率 Fig. 2 Positive rate of CRCoV from December 2015 to March 2017 |
在所有已检测CRCoV的样本中,有454份有年龄记录,年龄跨度为1月龄~15岁,感染犬的年龄跨度为2月龄~12岁。犬的体况和免疫力随年龄增长有一定变化规律,根据这种变化规律进行年龄段划分,每个分段均有CRCoV阳性犬分布。各年龄段犬感染CRCoV的情况见表 4。回归统计结果显示,犬的年龄与CRCoV感染之间无显著性趋势;卡方检验各年龄段间检出率无显著差异(P>0.05)。
|
|
表 4 各年龄段犬CRCoV检出情况 Table 4 The detection of CRCoV in dogs of different ages |
在呼吸道症状记录完整的455例样本中,有96例检出CRCoV阳性。在这些CRCoV阳性犬中,无呼吸道症状的有31例,占所有无呼吸道症状犬(455例样本中无呼吸道症状的有114例)的27.19%(31/114);呈现轻度呼吸道症状(鼻液、咳嗽)的有59例,占所有轻度呼吸道症状犬的19.73%(59/299);呈现中至重度呼吸道症状(肺炎)的有6例,占所有中至重度呼吸道症状犬的14.29%(6/42)(表 5)。
|
|
表 5 CRCoV感染犬的呼吸道症状严重程度分布情况 Table 5 Severity distribution of respiratory symptoms in CRCoV-infected dogs |
2016年11月—2017年3月,对156例样本进行了CRCoV、CPIV、CDV和CAV-2检测。在这156例中,呼吸道症状记录完整的有146例。在呈现无呼吸道症状的39只犬中,有8例为CRCoV阳性,此8例中有1例混合感染CPIV,混合感染率12.50%(1/8);在呈现轻度呼吸道症状的97只犬中,有17例为CRCoV阳性,此17例中有5例混合感染CPIV,2例混合感染CDV,混合感染率41.18%(7/17);在呈现中至重度呼吸道症状的10只犬中,有2例为CRCoV阳性,此2例均混合感染CDV,混合感染率100.00%(2/2)(表 6)。发生呼吸道病毒(CPIV、CDV、CAV-2)混合感染的CRCoV感染犬的无呼吸道症状发生率、轻度呼吸道症状发生率以及中至重度呼吸道症状的发生率分别为10.00%(1/10)、70.00%(7/10)和20.00%(2/10)(表 6)。
|
|
表 6 2016年11月—2017年3月CRCoV感染犬的呼吸道症状严重程度分布情况及混合感染情况 Table 6 Distribution of respiratory symptom severity and mixed infection in CRCoV-infected dogs from November 2016 to March 2017 |
一般来说,与人类一样,犬呼吸道疾病在冬春季更易流行,尤其是在北方地区[14]。如图 2所示,CRCoV检出率的整体趋势大致符合上述规律,但气候炎热的2016年7月份的检出率比冬季的检出率还高,这与部分地区人流感夏季暴发的情况相似[15],可能是室内空调使用过度导致,也可能和夏季气温高、体能消耗大,犬发生应激相关。
各年龄段犬的CRCoV的感染率与年龄并无的线性关系(R2=0.020 2 < 1),且卡方检验结果(P=0.870 8>0.05)也表明各年龄段犬的CRCoV感染率并无差异。虽然国外文献中提到2~8岁犬由于频繁与外界其他犬接触而呈现较高的CRCoV血清抗体阳性率[12],但病毒阳性率与血清抗体阳性率是两个不同概念。
据德国某文献报道,在2011年7月—2012年7月,CRCoV与CPIV、CDV、CAV-2、支气管败血波氏杆菌的混合感染率分别为1.32%(2/151)、0%(0/151)、0%(0/151)、2.65%(4/151)[16]。经卡方检验比较,本试验中CRCoV与CPIV、CDV、CAV-2的混合感染率与该文献所报道的感染率无显著差异(P>0.05),即北京地区CRCoV与CPIV、CDV、CAV-2的混合感染率和德国基本相同。
3.2 CRCoV感染犬的症状及CRCoV感染犬混合感染其他呼吸道病毒的症状分析为研究CRCoV的致病力强弱,将CRCoV感染犬的症状分为三类进行分析。从表 6来看,呈中至重度呼吸道症状的CRCoV感染犬有100.00%混合感染了其他呼吸道病毒,且这2例犬均混合感染了致病力强的CDV,故不能说明CRCoV致病力强。而呈无呼吸道症状和轻度呼吸道症状的CRCoV感染犬的混合感染率相对较低,分别为12.50%(1/8)和41.18%(7/17),且所有CRCoV感染犬有93.75%(90/96)表现无呼吸道症状及轻度呼吸道症状,无呼吸道症状的CRCoV感染犬占所有无呼吸道症状犬的比例较高(27.19%,表 5),这说明CRCoV单一感染多表现为无呼吸道症状或轻度呼吸道症状,CRCoV对呼吸系统的致病力较弱。
从表 6来看,CRCoV感染混合感染其他呼吸道病毒(CPIV/CDV/CAV-2)的患犬共10只,多表现轻度呼吸道症状(70.00%),其次是中至重度呼吸道症状(20.00%),较少表现为无呼吸道症状(10.00%)。
4 结论北京地区CRCoV的分子流行率较高,在冬春季节更易流行,且各年龄段犬的检出率差异不显著。该病毒与CPIV、CAV-2、CDV的混合感染率较低。该病毒的致病力较弱,感染犬通常无呼吸道症状或表现轻度呼吸道症状。
| [1] |
ERLES K, TOOMEY C, BROOKS H W, et al. Detection of a group 2 coronavirus in dogs with canine infectious respiratory disease[J]. Virology, 2003, 310(2): 216-223. DOI:10.1016/S0042-6822(03)00160-0 |
| [2] |
ERLES K, SHIU K B, BROWNLIE J. Isolation and sequence analysis of canine respiratory coronavirus[J]. Virus Res, 2007, 124(1-2): 78-87. DOI:10.1016/j.virusres.2006.10.004 |
| [3] |
ERLES K, BROWNLIE J. Investigation into the causes of canine infectious respiratory disease: antibody responses to canine respiratory coronavirus and canine herpesvirus in two kennelled dog populations[J]. Arch Virol, 2005, 150(8): 1493-1504. DOI:10.1007/s00705-005-0533-x |
| [4] |
ERLES K, DUBOVI E J, BROOKS H W, et al. Longitudinal study of viruses associated with canine infectious respiratory disease[J]. J Clin Microbiol, 2004, 42(10): 4524-4529. DOI:10.1128/JCM.42.10.4524-4529.2004 |
| [5] |
MITCHELL J A, BROOKS H W, SZLADOVITS B, et al. Tropism and pathological findings associated with canine respiratory coronavirus (CRCoV)[J]. Vet Microbiol, 2013, 162(2-4): 582-594. DOI:10.1016/j.vetmic.2012.11.025 |
| [6] |
AN D J, JEONG W, YOON S H, et al. Genetic analysis of canine group 2 coronavirus in Korean dogs[J]. Vet Microbiol, 2010, 141(1-2): 46-52. DOI:10.1016/j.vetmic.2009.09.002 |
| [7] |
DECARO N, DESARIO C, ELIA G, et al. Serological and molecular evidence that canine respiratory coronavirus is circulating in Italy[J]. Vet Microbiol, 2007, 121(3-4): 225-230. DOI:10.1016/j.vetmic.2006.12.001 |
| [8] |
ELLIS J, ANSEEUW E, GOW S, et al. Seroepidemiology of respiratory (group 2) canine coronavirus, canine parainfluenza virus, and Bordetella bronchiseptica infections in urban dogs in a humane shelter and in rural dogs in small communities[J]. Can Vet J, 2011, 52(8): 861-868. |
| [9] |
KANESHIMA T, HOHDATSU T, SATOH K, et al. The prevalence of a group 2 coronavirus in dogs in Japan[J]. J Vet Med Sci, 2006, 68(1): 21-25. |
| [10] |
KNESL O, ALLAN F J, SHIELDS S. The seroprevalence of canine respiratory coronavirus and canine influenza virus in dogs in New Zealand[J]. N Z Vet J, 2009, 57(5): 295-298. DOI:10.1080/00480169.2009.58624 |
| [11] |
MOCHIZUKI M, YACHI A, OHSHIMA T, et al. Etiologic study of upper respiratory infections of household dogs[J]. J Vet Med Sci, 2008, 70(6): 563-569. |
| [12] |
PRIESTNALL S L, BROWNLIE J, DUBOVI E J, et al. Serological prevalence of canine respiratory coronavirus[J]. Vet Microbiol, 2006, 115(1-3): 43-53. DOI:10.1016/j.vetmic.2006.02.008 |
| [13] |
朱军. 北京地区犬副流感病毒、腺病毒Ⅱ型分子流行病学调查[D]. 北京: 中国农业大学动物医学院, 2016: 14-19. ZHU J. The molecular epidemiology investigation of cannine parainflluenza virus and adenovirus type 2 in Beijing[D]. Beijing: College of Veterinary Medicine, China Agricultural University, 2016: 14-19. (in Chinese) |
| [14] |
中华人民共和国卫生部. 中国流行性感冒疫苗预防接种指导意见[J]. 国际呼吸杂志, 2006(1): 3, 7. Ministry of Health, PRC. Guidelines for influenza vaccine vaccination in China[J]. International Journal of Respiration, 2006(1): 3, 7. DOI:10.3760/cma.j.issn.1673-436X.2006.01.003 (in Chinese) |
| [15] |
CUNNINGHAM M J, LI W, ZI H R, et al. Analysis of epidemiological characteristics of influenza in Nanjing, from 2009 to 2013[J]. Chinese Journal of Disease Control & Prevention, 2017, 21(1): 3-7. |
| [16] |
SCHULZ B S, KURZ S, WEBER K, et al. Detection of respiratory viruses and Bordetella bronchiseptica in dogs with acute respiratory tract infections[J]. Vet J, 2014, 201(3): 365-369. |
(编辑 白永平)



