猪流感(swine influenza, SI)是由猪流感病毒(swine influenza virus, SIV)引起的一种急性、高度接触性呼吸道传染病。猪群中广泛流行的SIV主要有3种亚型H1N1、H1N2和H3N2,其中H1N1病毒又分为经典型、类人型、类禽型和2009/H1N1 4个基因谱系[1]。类禽型H1N1流感在20世纪70年代末首次出现于欧洲猪群,病原是由感染禽类传播到猪群中之后广泛流行[2],目前该类病毒在欧洲及亚洲多个国家的猪群中广泛流行,被称之为欧亚类禽型(Eurasian avian-like,EA)H1N1 SIV[3-4],并且出现了感染人的零星报道[5-6]。本实验室在2005年分离到第一株EA H1N1(A/swine/Henan/11/2005),近10多年SI的病原学监测结果发现EA H1N1已逐步成为主要的流行毒株,部分毒株已具备了在哺乳动物间高效传播的能力[7],大大凸显了EA H1N1病毒重要的兽医学及公共卫生学意义。
作为流感病毒重要的膜蛋白之一,血凝素(hemagglutinin,HA)具有与细胞表面病毒特异性受体结合、介导病毒外膜与细胞内体融合,以及刺激机体产生中和抗体等作用[8-9]。HA蛋白诱导机体产生的中和抗体作为抗病毒免疫的首要因素,能够在第一时间与病毒结合,从而抑制病毒对细胞的入侵,在抗病毒治疗及其免疫等方面都发挥着重要作用[10]。已有研究结果表明中和性单克隆抗体(monoclonal antibody, MAb)作为一种有效的技术手段可用于防制流感病毒感染的发生[11]。因此,本研究以纯化的全病毒蛋白作为免疫原,免疫BALB/c小鼠,利用杂交瘤技术筛选制备针对HA蛋白的、具有中和活性的MAb,并对其体内外中和病毒感染的活性进行了检测与分析。
1 材料与方法 1.1 病毒、细胞及实验动物等H1N1亚型SIV A/swine/Henan/11/2005(HN11,GenBank登录号为HQ541672~HQ541679)、A/swine/Guangxi/18/2011(GX18)、A/swine/Zhejiang/245/2013(ZJ245)、A/swine/Guangdong/306/2013(GD306)、A/swine/Liaoning/FS176/2015(FS176)、A/swine/Heilongjiang/44/2009(HLJ44)和H3N2亚型SIV A/swine/Guangdong/9/2005(GD5)均由本实验室分离、鉴定并保存。H5、H7及H9亚型禽流感病毒(AIV)HI试验抗原购自哈尔滨维科生物技术开发公司,表达病毒HN11 HA蛋白的重组质粒pCAGGS-H1HA、抗HN11毒株的小鼠多克隆血清、骨髓瘤细胞SP2/0和293T细胞由本实验室保存。6和8周龄的雌性BALB/c小鼠购自北京维通利华实验动物有限公司。
1.2 主要试剂DMEM培养基、标准胎牛血清购于Gibco公司;弗氏完全佐剂(FCA)、弗氏不完全佐剂(FICA),选择培养基HAT、HT,融合剂PEG2000,FITC-Mouse荧光二抗及羊抗鼠IgG-HRP酶标二抗均购于Sigma公司;Clonotyping Systerm/HRP Kit亚型鉴定试剂盒购自SBA公司;IRDye800CW羊抗鼠IgG抗体购自LI-COR公司,Protein G亲和层析柱购自GE healthcare公司。
1.3 免疫原制备将HN11毒株进行10倍倍比稀释,选取10-3、10-4、10-53个稀释度的病毒液接种10日龄的非免疫鸡胚,72 h后收取尿囊液测定其HA效价,收集HA效价在1:128以上的尿囊液,将其于4 ℃条件下8 000 r·min-1离心30 min;取上清液于4 ℃ 30 000 r·min-1离心2 h;弃上清,并取适量PBS(pH=7.4)悬浮沉淀。配制20%、40%、60%的蔗糖溶液,将上述得到的病毒液采用蔗糖密度梯度35 000 r·min-1离心3 h。取40%~60%的全病毒蛋白,取适量PBS再次溶解,35 000 r·min-1离心2 h进行脱糖。最后,用适量PBS重悬沉淀,β-丙内酯灭活,测定其蛋白含量,分装,-20 ℃保存,在后续试验中分别用作免疫原及MAb的筛选与鉴定。
1.4 动物免疫按照文献[12]的方法,将纯化的蛋白与等体积的FCA乳化均匀后,经皮下多点注射免疫6周龄雌性BALB/c小鼠,接种剂量为100 μg·只-1。之后每隔两周将FICA乳化的抗原经腹腔注射进行第2次与第3次免疫。融合前的3 d再次加强免疫。
1.5 杂交瘤细胞的制备与筛选将纯化的HN11全病毒蛋白、鼠抗HN11病毒多克隆阳性血清及阴性血清分别进行倍比稀释,采取棋盘法确定间接ELISA中抗原的最佳包被浓度与抗体的最佳反应浓度。判定标准:阳性血清孔OD450 nm接近1.0,阴性血清孔OD450 nm<0.2,且P/N>2.1时的反应条件,确定为最佳工作浓度。
参考文献[13]进行细胞融合、筛选、亚克隆。按照常规方法将免疫小鼠的脾细胞和SP2/0细胞在PEG2000的作用下按4:1比例进行融合。待细胞集落长到培养孔1/3~1/2大小时,通过ELISA和HI试验方法筛选阳性杂交瘤细胞。对筛选到的阳性孔细胞再进行2~3次亚克隆和检测, 直到所有细胞孔的培养上清ELISA和HI均为阳性为止。
1.6 腹水的制备与纯化采用8周龄的BALB/c小鼠腹腔注射FICA,每只0.5 mL。1周后,每只小鼠腹腔注射105个阳性杂交瘤细胞,密切观察小鼠腹部明显膨大,适时收集腹水,将收集的腹水以5 000 r·min-1离心10 min,取上清液,利用Protein G亲和层析法纯化抗体。具体步骤如下:取0.5 mL MAb 5 000 r·min-1离心10 min以去除油脂层,取上清;将所获上清用5倍体积的Binding Buffer (20 mmol·L-1 Na3PO4, pH=7.0)稀释,过亲和层析柱,流速约为1 mL·min-1;用10倍柱体积的Binding Buffer清洗柱子,以去除杂质;用5 mL的Elution Buffer (PBS,0.1 mol·L-1Gly,pH=2.7)洗脱结合在亲和层析柱上的抗体,流速约为0.5 mL·min-1,收集洗脱液;紫外分光光度计280 nm测定蛋白浓度,于-20 ℃保存备用。
1.7 MAbs生物学活性的检测 1.7.1 亚类鉴定将“1.6”中收集得到的MAbs腹水按照Clonotyping Systerm/HRP Kit试剂盒说明书中具体的步骤进行MAb亚类的鉴定。
1.7.2 ELISA和HI效价的测定将上述制备的HN11毒株作为ELISA包被抗原和HI检测抗原,对分泌MAbs的杂交瘤细胞上清以及MAbs腹水进行间接ELISA及HI试验,测定其ELISA及HI效价。
1.7.3 Western blot对MAbs活性分析将纯化的全病毒蛋白进行SDS-PAGE电泳,转印至硝酸纤维素膜(NC膜)上,并用制备MAbs作为一抗(1:1 000),以IRDye800CW羊抗鼠IgG抗体作为二抗(1:8 000),采用双色红外激光成像系统扫膜进行Western blot鉴定。
1.7.4 免疫荧光(IFA)对MAbs活性的检测将表达HN11 HA蛋白的重组质粒pCAGGS-H1HA转染293T细胞,48 h后用70%的冰乙醇固定细胞20 min,以获得的MAb作为一抗,二抗为羊抗鼠FITC-IgG,按照常规方法进行孵育,置于荧光显微镜下观察。
1.7.5 MAbs对不同分支H1亚型SIV及其他亚型流感病毒HI交叉反应活性的检测分别将制备的MAbs与EA H1N1、2009/H1N1、含有EA H1N1 HA基因的重配型H1N1、H3N2病毒及H5、H7、H9亚型AIV的HI试验抗原进行反应,测定MAbs对不同病毒的HI反应活性。
1.7.6 MAbs对不同分支H1亚型SIV中和活性的检测选取EA H1N1、2009/H1N1、含有EA H1N1 HA基因的重配型H1N1病毒,分别测定其TCID50,将MAbs按照1:10、1:20、1:40……1:10 240作2倍倍比稀释后与100 TCID50的病毒混合,37 ℃作用1 h,然后将其接种于80%铺满的MDCK单层细胞,37 ℃、5% CO2条件下继续培养,期间观察细胞病变情况,72 h后测定细胞上清的HA活性,根据结果再计算MAbs的中和效价。
1.7.7 MAbs对病毒感染小鼠的免疫保护性将MAbs分别按照小鼠体重20 μg·g-1的剂量接种6周龄BALB/c小鼠,24 h后,接种及未接种MAbs的小鼠分别再次分组(其中一组为正常对照),分别选取与制备MAbs时用到的免疫原病毒同源病毒株HN11与异源病毒株GD306进行滴鼻感染,感染剂量为106EID50,感染后14 d内每天称量小鼠体重,并在感染后第3天,随机剖杀其中的3只小鼠,取肺和鼻甲骨匀浆后接种10日龄的非免疫鸡胚,测定其病毒含量。
2 结果 2.1 杂交瘤细胞株的制备以纯化的HN11全病毒蛋白作为包被抗原,建立了间接ELISA方法。确定抗原的最佳包被浓度为8 μg·mL-1;血清最佳稀释度为1:1 600,最佳作用时间为37 ℃孵育1 h;二抗稀释度为1:5 000,最佳作用时间为37 ℃孵育1 h。免疫小鼠的脾细胞和SP2/0细胞经过融合,利用ELISA方法和HI试验筛选出阳性杂交瘤细胞,经3次亚克隆后,共获得两株能够稳定分泌抗HA蛋白MAb的杂交瘤细胞株,分别命名为2B6和4C7。
2.2 MAbs的亚类鉴定利用试剂盒Clonotyping Systerm/HRP Kit对两株MAbs的亚类进行鉴定,结果显示,单抗2B6和4C7的重链分别为IgG2a和IgG2b,其轻链均为κ链。
2.3 MAbs的ELISA及HI效价测定利用ELISA和HI试验分别检测MAbs的效价,结果显示2B6和4C7两株MAbs的细胞上清均检测到ELISA和HI效价,其制备腹水的效价均有所提高(表 1)。
|
|
表 1 两株MAbs的ELISA和HI效价 Table 1 The titers of ELISA and HI of two MAbs |
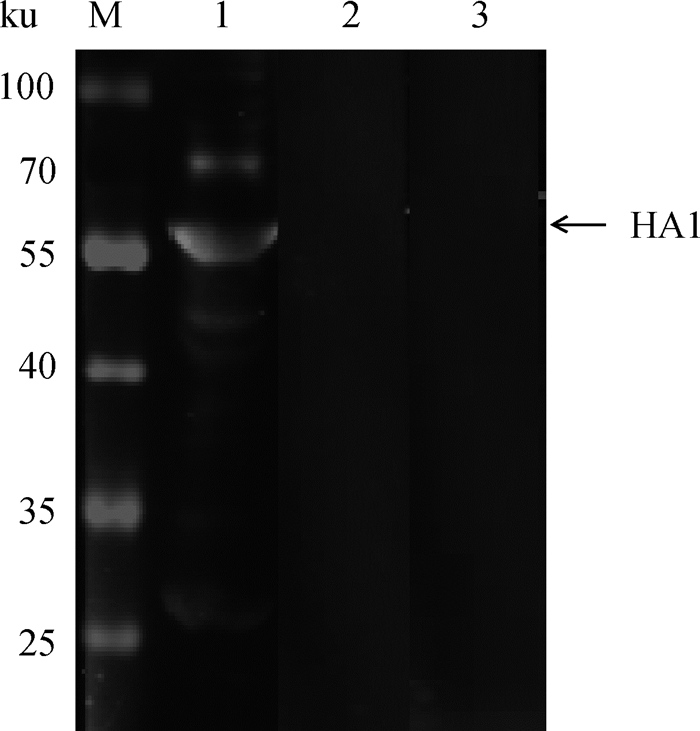
分别采用两株MAbs 2B6和4C7作为一抗,对纯化的HN11全病毒蛋白进行检测,同时用抗HN11病毒的阳性血清作为检测对照,结果显示用多克隆血清作为检测一抗,在56 ku处有明显的特异性条带,而两株MAbs检测时在相应的位置均未见反应条带(图 1),表明两株MAbs不能与HA蛋白发生反应,提示2B6和4C7可能为识别HA蛋白构象表位的MAbs。
|
M.预染的蛋白质相对分子质量标准;1.多克隆血清与纯化的全病毒蛋白反应;2.单抗2B6与纯化的全病毒蛋白反应;3.单抗4C7与纯化的全病毒蛋白反应 M. Prestained protein ladder; 1. Polyclonal serum reacted with the purified whole virus protein; 2. MAb 2B6 reacted with the purified whole virus protein; 3. MAb 4C7 reacted with the purified whole virus protein 图 1 Western blot对MAbs的活性检测 Figure 1 Activity analysis of MAbs by Western blot |
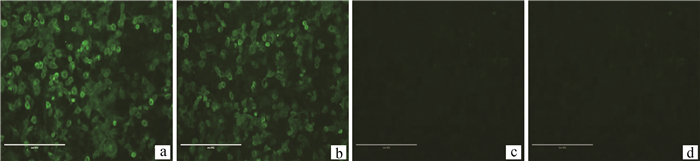
将重组质粒pCAGGS-H1HA转染293T细胞,IFA检测结果显示,两株MAbs与pCAGGS-H1HA在细胞中瞬时表达的HA蛋白反应均能出现亮绿色荧光,而转染空质粒pCAGGS的对照细胞未见荧光(图 2),表明两株MAbs与靶抗原HA蛋白均具有良好的反应活性。
|
a.单抗2B6检测pCAGGS-H1HA转染的293T细胞;b.单抗4C7检测pCAGGS-H1HA转染的293T细胞;c.单抗2B6检测pCAGGS转染的293T细胞;d.单抗4C7检测pCAGGS转染的293T细胞反应 a. MAb 2B6 detected 293T cells transfected with pCAGGS-H1HA; b. MAb 4C7 detected 293T cells transfected with pCAGGS-H1HA; c. MAb 2B6 detected 293T cells transfected with pCAGGS; d. MAb 4C7 detected 293T cells transfected wirh pCAGGS 图 2 IFA对两株MAbs的活性检测(200×) Figure 2 Activity analysis of the two MAbs by IFA(200×) |
选取不同的病毒及抗原分别配制4单位抗原,与MAbs分别进行HI试验,结果显示两株MAbs与EA H1N1病毒及含有EA H1N1 HA基因的重配型H1N1病毒HI反应效价较高,同时对H3N2病毒和H9抗原也有反应,而与HLJ44、H5和H7抗原不发生反应(表 2)。表明除了EA H1N1病毒外,MAbs对H3N2及H9N2亚型的病毒也具有一定的HI交叉反应活性。
|
|
表 2 两株MAbs对不同H1亚型SIVs及其他亚型流感病毒(或抗原)的HI效价 Table 2 The HI titers of the two MAbs against the different H1 subtype SIVs and other subtype influenza viruses |
将两株MAbs分别与100TCID50的病毒进行反应,结果显示2B6和4C7对HN11的中和效价显示较高,分别达到1:709.6和1:446.7;对其他两株EA H1N1和重配型病毒GD306也具有一定的中和活性,而不能中和病毒FS176和HLJ44(表 3)。表明MAbs对不同分支H1N1病毒的中和活性存在较大差异。
|
|
表 3 两株MAbs对不同H1亚型病毒的中和效价 Table 3 Neutralizing activity of two MAbs against the different H1 subtype SIVs |
在病毒感染前24 h,对部分试验小鼠分别接种两株MAbs。病毒感染后持续监测小鼠的体重,并于感染后第3天测定感染小鼠肺中的病毒含量。结果显示,未接种MAbs的小鼠,分别在感染HN11和GD306病毒后体重出现明显的下降,最大下降比率分别达到8.2%和10.7%;同时,肺中均检测到病毒复制,其滴度分别为3.23和3.58log10EID50·mL-1,鼻甲中的病毒复制滴度分别为1.25和2.5log10EID50·mL-1。而两组MAbs注射小鼠获得了对同源HN11病毒感染的完全保护,未见体重下降与病毒检出(图 3a);异源GD306病毒感染时,相比于对照组小鼠,注射MAbs的小鼠其体重下降的比例均显著降低,与此同时,肺和鼻甲骨中的病毒复制也得到了有效的抑制(图 3b)。上述结果表明两株MAbs可以对小鼠感染EA H1N1病毒提供完全保护,同时对含有EA H1N1 HA基因的重配型H1N1病毒也具有一定的抗感染免疫作用。

|
a.病毒感染小鼠的体重变化;b.病毒感染小鼠脏器病毒含量的测定 a. Weight changes of the infected mice; b. Viral titers in the organs of the infected mice 图 3 MAbs对病毒感染小鼠的免疫保护效果 Figure 3 Protection induced by MAbs in mice against infection with HN11 and GD306 viruses |
猪被称为流感病毒的“混合器”,其呼吸道上皮细胞含有唾液酸α-2, 3半乳糖苷(SA-α-2, 3-Gal)受体和唾液酸α-2, 6半乳糖苷(SA-α-2, 6-Gal)受体,在病毒种间传播和新型流感病毒的产生过程中发挥着重要的作用[14]。近年来,EA H1N1 SIV在猪群中广泛流行,给养殖业及人的生命健康构成了潜在威胁[7]。本研究选取一株EA H1N1 SIV作为免疫原,制备了两株针对病毒HA蛋白的MAbs,命名为2B6和4C7。进一步研究结果表明两株MAbs腹水效价较高,可特异性地识别病毒的HA蛋白,具有HI活性和病毒中和活性,可对小鼠提供抗同源EA H1N1病毒感染的高效预防,同时对含有EA HA基因来源的重配型病毒也具有一定的抗感染免疫效果。
本研究中,关于MAbs的抗原结合活性的检测结果发现,两株MAbs均不能在Western blot试验中与全病毒的HA蛋白发生特异性反应,可能是因为病毒蛋白样品在裂解过程中导致其抗原的结构发生了变化,导致抗体无法识别。进一步通过对病毒HA蛋白采用真核表达质粒转染细胞后进行表达,利用IFA检测结果发现两株MAbs均能够与蛋白发生特异性结合。提示本研究所制备的这两株MAbs可以识别接近天然活性的病毒HA蛋白,而对于经变性处理后的蛋白无法识别,由此推测此类抗体所针对的病毒抗原表位可能为构象表位。
近年来,中和性MAbs在流感病毒研究领域得到了广泛的应用,一方面是研究此类抗体作为流感的抗病毒药物用以探讨抗体治疗的疗效与机制,另一方面是分析确定MAbs特异性抗原结合表位,为新型疫苗的研发提供理论依据。研究表明针对流感病毒(H2N2)的一株中和性MAb C179,可以同时中和H1、H2、H5、H6、H9亚型的流感病毒的感染[15-16]。本研究结果表明2B6和4C7这两株MAbs的中和活性表现于对EA H1N1和携带有EA H1N1 HA基因的重配型H1N1病毒。鉴于HN11为实验室2005年分离的EA H1N1病毒,通过对两株MAbs与2011—2015年期间分离毒株反应情况的研究,结果发现,随着EA H1N1病毒在猪群中的流行与传播,病毒渐渐出现了抗原性的变化,即便是单纯的EA H1N1病毒,其抗原性的变化已经体现在抗体对病毒中和活性的差异,尤其是近年来猪群中又频频出现EA H1N1与2009/H1N1、经典型H1N1等地方性流行毒株之间发生基因重配而产生了多重重配型的病毒,给SI疫苗研发带来了更多的挑战。作为一种理想的疫苗种毒毒株,在选择上必须与流行毒株具有高度的抗原匹配性。由此,针对病毒诸如上述情况的出现,提示人们需要及时全面地掌握SIV流行毒株分子流行病学及其抗原性变异的情况,才能更好地防控SI。
4 结论利用EA H1N1 SIV全病毒蛋白作为免疫原,制备的两株MAbs具有较高的病毒中和活性,可有效保护小鼠抵抗同源及异源H1N1 SIV的感染,MAbs能够特异性识别病毒的HA蛋白。研究结果为进一步将中和性MAb应用于抗EA H1N1 SIV的感染及开展病原抗原性变异的分子基础研究奠定了重要的工作基础。
| [1] | BAUDON E, PEYRE M, PEIRIS M, et al. Epidemiological features of influenza circulation in swine populations:A systematic review and meta-analysis[J]. PLoS One, 2017, 12(6): e0179044. DOI: 10.1371/journal.pone.0179044 |
| [2] | PENSAERT M, OTTIS K, VANDEPUTTE J, et al. Evidence for the natural transmission of influenza A virus from wild ducts to swine and its potential importance for man[J]. Bull World Health Organ, 1981, 59(1): 75–78. |
| [3] | LIU J H, BI Y H, QIN K, et al. Emergence of European avian influenza virus-like H1N1 swine influenza A viruses in China[J]. J Clin Microbiol, 2009, 47(8): 2643–2646. DOI: 10.1128/JCM.00262-09 |
| [4] | VINCENT A, AWADA L, BROWN I, et al. Review of influenza A virus in swine worldwide:A call for increased surveillance and research[J]. Zoonoses Public Health, 2014, 61(1): 4–17. DOI: 10.1111/zph.2014.61.issue-1 |
| [5] | YANG H L, QIAO C L, TANG X, et al. Human infection from avian-like influenza A (H1N1) viruses in pigs, China[J]. Emerg Infect Dis, 2012, 18(7): 1144–1146. DOI: 10.3201/eid1807.120009 |
| [6] | ROVIDA F, PIRALLA A, MARZANI F C, et al. Swine influenza A (H1N1) virus (SIV) infection requiring extracorporeal life support in an immunocompetent adult patient with indirect exposure to pigs, Italy, October 2016[J]. Euro Surveill, 2017, 22(5): 30456. |
| [7] | YANG H L, CHEN Y, QIAO C L, et al. Prevalence, genetics, and transmissibility in ferrets of Eurasian avian-like H1N1 swine influenza viruses[J]. Proc Natl Acad Sci U S A, 2016, 113(2): 392–397. DOI: 10.1073/pnas.1522643113 |
| [8] | BYRD-LEOTIS L, CUMMINGS R D, STEINHAUER D A. The interplay between the host receptor and influenza virus hemagglutinin and neuraminidase[J]. Int J Mol Sci, 2017, 18(7): 1541. DOI: 10.3390/ijms18071541 |
| [9] | SHVARTSMAN D E, KOTLER M, TALL R D, et al. Differently anchored influenza hemagglutinin mutants display distinct interaction dynamics with mutual rafts[J]. J Cell Biol, 2003, 163(4): 879–888. DOI: 10.1083/jcb.200308142 |
| [10] | SKEHEL J J, WILEY D C. Receptor binding and membrane fusion in virus entry:The influenza hemagglutinin[J]. Annu Rev Biochem, 2000, 69: 531–569. DOI: 10.1146/annurev.biochem.69.1.531 |
| [11] | CHEN Y X, QIN K, WU W L, et al. Broad cross-protection against H5N1 avian influenza virus infection by means of monoclonal antibodies that map to conserved viral epitopes[J]. J Infect Dis, 2009, 199(1): 49–58. DOI: 10.1086/594374 |
| [12] | NAUNDORF S, PREITHNER S, MAYER P, et al. In vitro and in vivo activity of MT201, a fully human monoclonal antibody for pancarcinoma treatment[J]. Int J Cancer, 2002, 100(1): 101–110. DOI: 10.1002/ijc.v100:1 |
| [13] | BHAT S, BHATIA S, SOOD R, et al. Production and characterization of monoclonal antibodies against nucleoprotein of avian influenza virus[J]. Monoclon Antib Immunodiagn Immunother, 2013, 32(6): 413–418. DOI: 10.1089/mab.2013.0053 |
| [14] | CHEN L M, RIVAILLER P, HOSSAIN J, et al. Receptor specificity of subtype H1 influenza A viruses isolated from swine and humans in the United States[J]. Virology, 2011, 412(2): 401–410. DOI: 10.1016/j.virol.2011.01.015 |
| [15] | OKUNO Y, ISEGAWA Y, SASAO F, et al. A common neutralizing epitope conserved between the hemagglutinins of influenza A virus H1 and H2 strains[J]. J Virol, 1993, 67(5): 2552–2558. |
| [16] | EKIERT D C, WILSON I A. Broadly neutralizing antibodies against influenza virus and prospects for universal therapies[J]. Curr Opin Virol, 2012, 2(2): 134–141. DOI: 10.1016/j.coviro.2012.02.005 |



