2. 四川农业大学农学院,成都 611130
2. College of Agronomy, Sichuan Agriculture University, Chengdu 611130
植物在非生物胁迫和生物胁迫下会导致细胞活性氧(Reactive oxygen species,ROS)过量的积累,过量的ROS积累会非特异性的损害细胞组分,包括细胞核、核酸、蛋白质以及光合色素等,在生物体内抗氧化酶可以清除活性氧,维持细胞内ROS平衡,在抗氧化物酶中POD起着关键的作用[1]。在植物中广泛存在过氧化物酶,且具有多种功能[2]。过氧化物酶是多基因家族酶类,参与植物多种代谢途径,如植物的抗旱、抗盐、抗寒等多种抗逆功能[3-5]。烟草是中国非常重要的经济作物,烟草的产量与品质受到盐碱、冷害以及干旱等非生物胁迫的影响,因此在分子水平上研究POD对提高烟草非生物胁迫耐逆性具有重要意义。
POD是广泛存在于植物中的氧化还原酶,在植物生长发育和应激反应中发挥着重要的作用,是植物重要的保护酶类,最常见的是第Ⅲ类分泌过氧化物酶(Secretory peroxidase,POD),其功能是催化去除H2O2,参与木质部合成和降解、还原剂氧化和植物形态的形成,并参与环境胁迫相应[6-9]。目前,研究表明,POD家族基因与植物生长发育有关,如植物木质素聚合、栓化作用、细胞壁结构蛋白的交联等[10-11]。在许多植物中POD的作用都有过报道,而最主要的作用是利用H2O2为底物来参加各种还原物质的氧化。ROS是植物在胁迫刺激下产生的,并被POD还原为H2O和O2,因此POD是植物非生物胁迫下清除ROS的关键酶。Sierla等[12]研究表明,在植物胁迫下,POD活性增加,且参与了胁迫途径调控。Kumar等[13]和Neill等[14]研究表明,植物中的ROS可以被POD部分清除。目前,植物中POD基因研究取得了很大进展,在山楂、水稻、小麦等多种植物中成功克隆POD家族基因[15-17]。但植物中POD与ROS具体作用机制仍不明确。
本研究成功克隆到过氧化物酶家族基因NtPOD2,预测NtPOD2编码蛋白结构与功能,同时运用荧光定量测定NtPOD2在烟草各个组织中表达水平,以及在非生物胁迫处理下的表达模式,为进一步研究POD基因在烟草中与ROS作用机制提供科学依据。
1 材料与方法 1.1 材料挑选饱满均一的普通烟草(K326)种子,消毒(75%乙醇和20%NaClO),反复用无菌水清洗,播种于MS培养基培养2周,取大小均匀的幼苗进行ABA、H2O2、干旱、低温、低钾及高盐胁迫处理,每项处理设置3次重复,分别在0、3、6、12和24 h共5个时间点整株取样。ABA与H2O2非生物胁迫具体处理方法参照张雪薇等[18]。
1.2 方法 1.2.1 NtPOD2的克隆用Primer 5.0软件设计NtPOD2引物NtPOD2-F和NtPOD2-R(表 1)。以烟草叶片为材料,提取RNA,按照反转录试剂盒步骤进行反转录合成cDNA,将cDNA稀释10倍进行PCR扩增,PCR反应程序为95℃ 5 min;95℃ 30 s,55℃ 30 s,72℃ 3 min,35个循环。1%琼脂糖凝胶电泳检测,回收目的片段,将其与pMD19-T载体连接,转化,在含有Kn的LB固体培养基进行涂板,过夜培养后,挑取3个单克隆菌落进行测序。
参照王静等[19]方法进行NtPOD2的生物信息学分析。
1.2.3 烟草NtPOD2的表达分析采用Primer 5.0设计荧光定量引物,烟草18SrRNA为内参,引物序列为18S-F和18S-R(表 1)。每个样品重复4次,结果分析参考王静等[19]方法。
1.2.4 构建过表达载体重组克隆载体NtPOD2-pMD19-T与表达载体pBI121酶切反应,NtPOD2-pMD19-T进行37℃双酶切,酶切体系为10×T Buffer、1 µL;XbaⅠ 0.5 µL、SmaⅠ 0.5 µL、载体3 µL和ddH2O 5 µL。酶切过后产物与pBI121载体16℃连接过夜,连接后产物转化DH5α大肠杆菌感受态,在涂有Kn的LB培养基平板式上筛选,挑取单克隆菌株摇菌并送去测序公司进行测序,检测是否构建成功。
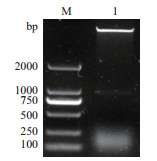
2 结果 2.1 NtPOD2的克隆以烟草叶片cDNA为模板进行PCR扩增,获得一条大小为750-1 000 bp条带。经回收和测序,片段大小为897 bp(图 1)。

|
| M:DL Marker 2 000 bp;1:NtPOD2 图 1 NtPOD2的克隆 |
通过对NtPOD2-pMD19-T质粒进行双酶切和测序,结果一致,目的片段大小为897 bp(图 2)。
|
| M:DL Marker 2 000 bp;1:NtPOD2 图 2 NtPOD2-pBI121重组质粒酶切 |
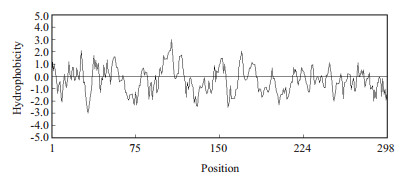
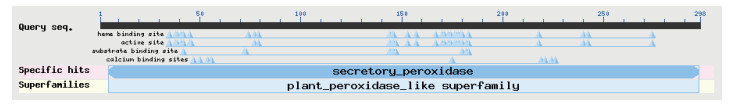
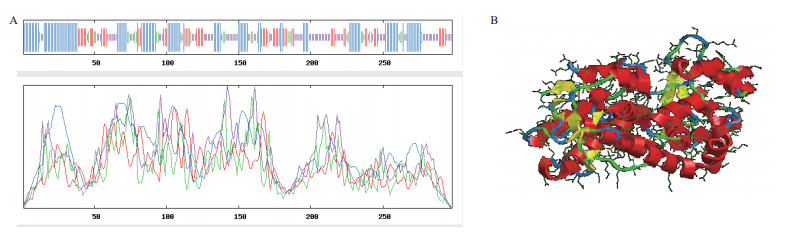
对NtPOD2蛋白进行生物学分析,理化性质分析结果表明,NtPOD2蛋白分子量为32.55 kD,等电点为5.78,不稳定系数为37.72。疏水性分析结果显示该蛋白属于亲水性蛋白(图 3)。NCBI在线分析NtPOD2蛋白保守功能域(图 4),该蛋白属于ClassⅢ型分泌性过氧化物酶。采用SMART和Scan Prosite分析NtPOD2蛋白理化性质,结果为NtPOD2蛋白含有6个蛋白激酶C磷酸化位点(67-69 SeK;70-72 TaR;77-79 SaR;183-185 TfR;200-202 SqR;235-237 SkK)、1个N-糖基化位点(75-78 NNSA)、5个酪氨酸激酶Ⅱ磷酸化位点(89-92 SevD;101-104 ScaD;183-186 TfrD;192-195 TniD;209-212 SggD)、1个氨基化位点(126-129 lGRR)、1个依赖于cAMP和cGMP的蛋白激酶磷酸化位点(128-131 RRdS)。NtPOD2蛋白信号肽预测结果显示,NtPOD2蛋白不存在信号肽,定位在细胞质中的概率最大(0.65)。二级结构分析表明,NtPOD蛋白二级结构的最大元件为α-螺旋,最小元件为β-转角(图 5-A)。三级结构分析结果表明,6个半胱氨酸残基48-53、102-294和181-206分别形成3个保守的二硫键桥(图 5-B)。
|
| 图 3 疏水性分析 |
|
| 图 4 保守结构域分析 |
|
| A:二级结构;B:三级结构 图 5 NtPOD2编码蛋白的结构预测 |
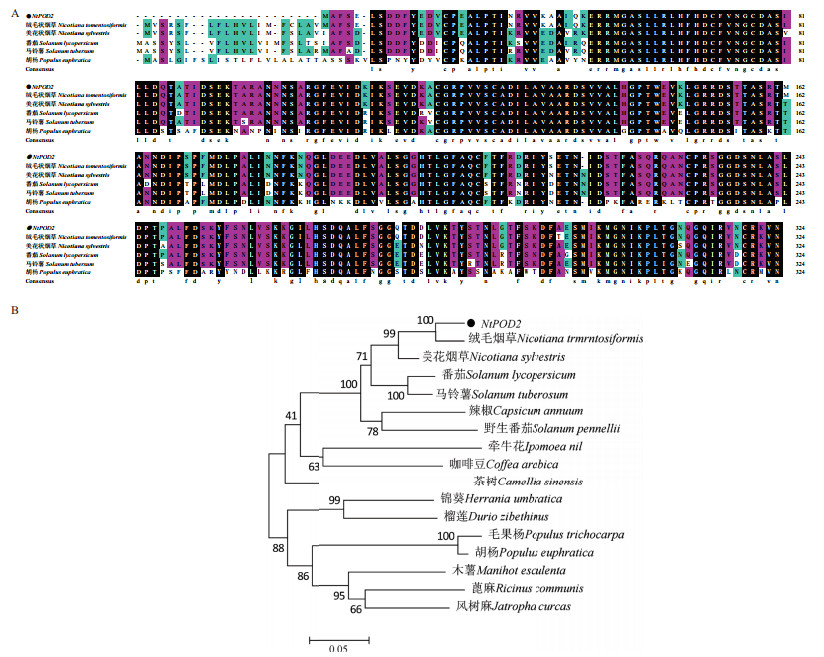
把NtPOD2编码氨基酸序列与绒毛状烟草、美花烟草、番茄、马铃薯以及胡杨POD2通过Dnaman多重序列比对(图 6-A),发现NtPOD2蛋白具有POD家族典型的结构特征,在N端都包含peroxidase活性位点GAslLRLhFHDC。把NtPOD2编码氨基酸序列通过Blast比对,选择不同物种POD2氨基酸序列下载,通过MEGA5构建系统进化树(图 6-B),结果表明,NtPOD2蛋白序列与绒毛状烟草POD2以及美花叶烟草POD2蛋白序列有较高同源性,分别为99%和94.65%。
|
| A:NtPOD2蛋白多重序列比对;B:NtPOD2蛋白系统进化树 图 6 NtPOD2同源性分析 |
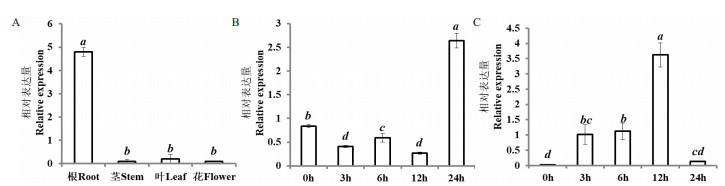
采用qRT-PCR对烟草K326各个组织进行表达分析,发现NtPOD2在根、茎、叶、花中均有表达,在根中表达量明显高于茎、叶、花(图 7-A)。
|
| A:NtPOD2组织表达分析;B:ABA胁迫下NtPOD2相对表达量;C:H2O2胁迫下NtPOD2相对表达量 图 7 NtPOD2的不同组织及信号分子处理下的表达模式 |
烟草K326幼苗上在培养皿上用ABA和H2O2处理,对处理后烟草幼苗NtPOD2表达分析表明,在12 h之前,ABA处理下NtPOD2的表达受到抑制,24 h时受到显著诱导,为对照的3.14倍(图 7-B);H2O2处理的早期,NtPOD2的表达受到强烈诱导,12 h时上升至最大,为对照的120.67倍(图 7-C)。以上结果表明NtPOD2能够响应逆境胁迫相关的信号分子调控。
2.7 NtPOD2在逆境胁迫下表达分析PEG和低温处理后,该基因分别在12 h和6 h时达到最大值,分别为对照的2.48倍(图 8-A)、8.60倍(图 8-B)。低钾处理下,NtPOD2表达量上升,NaCl处理下该基因下调(图 8-C-D)。结果表明,NtPOD2可能参与了PEG、低温等非生物胁迫。

|
| A:PEG胁迫下NtPOD2相对表达量;B:低温胁迫下NtPOD2相对表达量;C:低钾胁迫下NtPOD2相对表达量;D:盐胁迫下NtPOD2相对表达量 图 8 NtPOD2在非生物逆境胁迫下的表达模式 |
生物信息学分析表明,NtPOD2蛋白含有3个二硫键,属于分泌蛋白,含有活性位点(GAslLRLhFHDC),属于典型的ClassⅢ型分泌性过氧化物酶。信号肽预测显示NtPOD2蛋白定位在细胞质中,因此该基因可能在内质网加工成熟,进而通过高尔基体运输到细胞质。该蛋白与其他物种ClassⅢ型分泌性过氧化物酶相比含有相似的保守结构域(6A)以及二硫键桥[20]。该蛋白含有最大元件为α-螺旋,最小元件为β-转角。NtPOD2蛋白以Asp47、Val50、Gly52、Asp54和Ser56为中心的Ca2+结合位点构成远端的氧供体结构域,而Thr175、Asp219、Thr221和Asp226为中心的Ca2+结合位点构成近端的氧供体结构域,位于这两个结构域中间的血红素则由Fe2+与His46和His174形成共价键,构成活性中心。蛋白质空间结构影响其功能,NtPOD2蛋白特定的空间结构为其发挥功能奠定了基础。同源性分析表明,NtPOD2蛋白与其他植物POD蛋白含有较高同源性,其中与美花烟草POD2同源性为99%,可能与美花烟草POD2是POD家族的同一成员。通过对NtPOD2生物学分析,旨在为研究POD基因家族奠定基础。
烟草Ntpx在花中表达量最高,银杏GbPOD1和小桐子JcPOD73茎中表达量最高[21-22]。郭媖等[23]从陆地棉中克隆的GhPOD1和GhPOD2,两者相似性达99%,但表达模式相差很大。作为多基因家族的POD基因,具有功能多样性的特点。本研究表明NtPOD2在组织中都有表达,但根中表达最高,而茎、叶、花表达量相对较少,不同植物中POD基因在不同部位表达模式不同,说明POD家族基因表达存在特异性。NtPOD2在ABA处理下,表达量在3 h先下降,20 h又上升至最大,约为对照的3.14倍(图 5-B),说明NtPOD2受ABA诱导。Gao等[1]研究表明柽柳ThPODs参与非生物胁迫反应(PEG、ABA、NaCl等),并依赖ABA信号转导途径。钟新榕等[24]用不同浓度的ABA处理黄瓜幼苗,POD活性在短时间内可以提高。Anderberg等[25]研究结果表明低温胁迫、盐胁迫以及干旱胁迫下,能较短时间内增加植物体内ABA含量,进而诱导ABA调控相关基因的表达。司丛丛等[26]研究表明,烟草Ntpx在5% PEG6000胁迫下,Ntpx在最初无明显变化,在6 h后表达量上调在ABA和干旱胁迫下,表达量上调。本研究采用10 mmol/L H2O2处理烟草幼苗,NtPOD2的表达受到强烈诱导,12 h时上升至最大,为对照的120.67倍。苏亚春等[27]用100 μmol/L ABA处理甘蔗,结果表明,ScPOD02表达量在3 h显著增加,500 mmol/L H2O2处理下随着时间的延长,ScPOD02表达量基本不变。而这与苏亚春等在ABA、H2O2处理甘蔗后,ScPOD02表达模式不同,这可能是不同的浓度ABA、H2O2造成的。由此说明NtPOD2可能受干旱、ABA、NaCl、H2O2胁迫诱导,并依赖ABA信号转导途径进而参加植物生长发育。
在200 mmol/L NaCl处理下NtPOD2表达量呈现先下降后上升又下降的表达模式,在12 h表达量达到最大,约为对照1.12倍。苏亚春等[27]用250 mmol/L的NaCL处理下ScPOD02表达量先在6 h下降,而在12 h表达量又上升,约为对照的1.91倍。与苏亚春用NaCl处理甘蔗后ScPOD02表达模式一致,在6 h前表达量下降,在12 h时表达量上升为最大,之后又下降。程华等[21]用200 mmol/L NaCl喷洒银杏幼苗后,POD1表达量降低。Bae等[11]用200 mmol/L NaCl处理白杨后PoPOD1基因表达水平下调。低钾胁迫下,NtPOD2受到强烈诱导,NtPOD2表达量上调。王伟等[28]研究表明,大豆在低钾胁迫下,细胞内氧负离子O2-增加,超氧化物歧化酶催化O2-发生歧化反应生成H2O2-含量增加,进而引起过氧化物酶活性上升。在低温胁迫下,NtPOD2在6 h表达量达到最大,在12 h后又降低。Guo等[29]在4℃条件下处理柽柳叶和根,叶中ThPOD1表达量在6 h强烈诱导后又逐渐下降,根ThPOD1 6 h强烈诱导后在24 h达最大值后又下降。外源基因的表达增加宿主细胞的耐受性,植物受到生物胁迫以及非生物胁迫下,可以引起活性氧产生,进而破坏细胞稳态以及防御机制[30-31]。由此说明烟草NtPOD2,在不同胁迫下表达模式发生改变,以上均说明该基因在生物胁迫以及非生物胁迫中发挥着重要作用,由此推测,NtPOD2参与生物胁迫与非生物胁迫,可能引起活性氧的改变,进而参与植物生理调控与防御机制。
4 结论NtPOD2可能通过ABA信号通路来参与生物胁迫以及非生物胁迫。
| [1] |
Gao C, Wang Y, et al. Cloning of ten peroxidase(POD)genes from tamarix hispidaand charcterization of their responses to abiotic str-ess[J]. Plant Molecular Biology Reporter, 2010, 28(1): 77-89. DOI:10.1007/s11105-009-0129-9 |
| [2] |
Francoz E, Ranocha P, et al. Roles of cell wall peroxidases in plant development[J]. Phytochemistry, 2015, 112: 15-21. DOI:10.1016/j.phytochem.2014.07.020 |
| [3] |
Tognolli M, Penel C, Greppin H, et al. Analysis and expression of the class Ⅲ peroxidase large gene family in Arabidopsis thaliana[J]. Gene, 2002, 288(1/2): 129-138. |
| [4] |
Hiraga S, Yamamoto K, et al. Diverse expression profiles of 21 rice peroxidase genes[J]. FEBS Letters, 2000, 471(2): 245-250. |
| [5] |
Hiraga S, Sasaki KH, Ohashi Y, et al. A large family of class Ⅲ plant peroxidases review[J]. Plant & Cell Physiology, 2001, 42(5): 462-468. |
| [6] |
赵昶灵, 王树会. 剪叶对云南烤烟漂浮苗抗氧化酶活性和根系形态建成的效应[J]. 云南农业大学学报, 2014(1): 84-92. DOI:10.3969/j.issn.1004-390X(n).2014.01.016 |
| [7] |
梁艳荣, 胡晓红, 张颍力, 等. 植物过氧化物酶生理功能研究进展[J]. 内蒙古农业大学学报, 2003, 24(2): 110-113. |
| [8] |
刘莉, 孙虹丽, 程召阳, 等. 砀山酥梨褐皮芽变果皮中木质素生物合成相关基因克隆与表达分析[J]. 华北农学报, 2013, 28(6): 88-92. |
| [9] |
夏时云, 麦瑜玲, 等. 红掌叶片离体培养过程中酶活性及可溶性蛋白质含量的变化[J]. 华北农学报, 2007, 22(6): 195-198. |
| [10] |
Mohan R, Bajar AM, Kolattukudy PE. Induction of a tomato anionic peroxidase gene(tap1)by wounding in transgenic tobacco and activation of tap1/GUS and tap2 /GUS chimeric gene fusions in transgenic tobacco by wounding and pathogen attack[J]. Plant Mole Biol, 1993, 21(2): 341-354. DOI:10.1007/BF00019949 |
| [11] |
Bae EK, Lee H, Lee JS, et al. Molecular cloning of a peroxidase gene from poplar and its expression in response to stress[J]. Tree Physiology, 2006, 26(11): 1405-1412. DOI:10.1093/treephys/26.11.1405 |
| [12] |
Sierla M, Rahikainen M, et al. Apoplastic and chloroplastic redox signaling networks in plant stress responses[J]. Antioxidants & Redox Signaling, 2013, 18(16): 2220-2239. |
| [13] |
Kumar RR, Sharma SK, Rai GK, et al. Exogenous application of putrescine at pre-anthesis enhances the thermotolerance of wheat(Triticum aestivum L)[J]. Indian Journal of Biochemistry & Biophysics, 2014, 51(5): 396-406. |
| [14] |
Neill S. Interaction between abscisic acid, hydrogen peroxide and nitric oxide mediate survival responses during water stress[J]. New Phytologist, 2007, 175(1): 4-6. DOI:10.1111/j.1469-8137.2007.02112.x |
| [15] |
代红艳, 闫玉娇, 等. 山楂过氧化物酶基因的克隆及在烟草中异位表达分析[J]. 果树学报, 2015, 32(6): 1070-1076. |
| [16] |
Passardi F, Longet D, Penel C, et al. The class Ⅲ peroxidase multigenic family in rice and its evolution in land plants[J]. Phytochemistry, 2004, 65: 1879-1893. DOI:10.1016/j.phytochem.2004.06.023 |
| [17] |
Rebmann G, Hertig C, Bull J, et al. Cloning and sequencing of cDNAs encoding a pathogen-induced putative peroxidase of wheat(Triticum aestivum L.)[J]. Plant Mole Biol, 1991, 16(2): 329-331. DOI:10.1007/BF00020563 |
| [18] |
张雪薇, 刘仑, 等. 烟草NtCBL1基因的克隆、表达载体构建及表达分析[J]. 植物研究, 2017, 37(3): 387-394. |
| [19] |
王静, 彭双, 胡圣, 等. 烟草质膜ATPase4基因的克隆, 表达载体构建及表达分析[J]. 浙江农业学报, 2019, 31(2): 137-181. |
| [20] |
Veitch NC. Horseradish peroxidase:a modern view of a classic enzyme[J]. Phytochemistry(Amsterdam), 2004, 65(3): 249-259. DOI:10.1016/j.phytochem.2003.10.022 |
| [21] |
程华, 李琳玲, 王燕, 等. 银杏过氧化物酶基因POD1的克隆及表达分析[J]. 华北农学报, 2010(6): 44-51. |
| [22] |
王海波, 郭俊云, 赵志军, 等. 小桐子过氧化物酶73基因的克隆及表达分析[J]. 核农学报, 2017, 31(1): 29-36. |
| [23] |
郭媖, 郭旺珍, 张天真. 两个陆地棉过氧化物酶cDNA的克隆和鉴定[J]. 作物学报, 2007, 33(6): 891-897. DOI:10.3321/j.issn:0496-3490.2007.06.004 |
| [24] |
钟新榕, 郁继华, 颉建明, 等. NaCl胁迫及外源ABA和GA-3对黄瓜幼苗抗氧化酶活性的影响[J]. 甘肃农业大学学报, 2005, 40(4): 467-470. DOI:10.3969/j.issn.1003-4315.2005.04.010 |
| [25] |
Anderberg R J, Walker-Simmons M K. Isolation of a wheat cDNA clone for an abscisic acid-inducible transcript with homology to protein kinases[J]. Proceedings of the National Academy of Sciences of the USA, 1992, 89(21): 10183-10187. DOI:10.1073/pnas.89.21.10183 |
| [26] |
司丛丛, 刘好宝, 曲平治. 烟草钾离子通道及转基因烟草抗逆性的研究进展[J]. 中国农学通报, 2010, 26(2): 45-49. DOI:10.3969/j.issn.1007-7774.2010.02.022 |
| [27] |
苏亚春, 王竹青, 李竹, 等. 甘蔗过氧化物酶基因ScPOD02的克隆与功能鉴定[J]. 作物学报, 2017, 43(4): 510-521. |
| [28] |
王伟, 曹敏建, 王晓光, 等. 低钾胁迫对不同钾营养效应型大豆保护酶系统的影响[J]. 大豆科学, 2005(2): 101-105. DOI:10.3969/j.issn.1000-9841.2005.02.004 |
| [29] |
Guo XH, Jiang J, Wang BC, et al. ThPOD3, a truncated polypeptide fromTamarix hispida, conferred drought tolerance in Escherichia coli[J]. Molecular Biology Reports, 2010, 37(3): 1183-1190. DOI:10.1007/s11033-009-9484-8 |
| [30] |
Ying L, Dan C, Yizhi Z. Expression in Escherichia coli of three different soybean late embryogenesis abundant(LEA)genes to investigate enhanced stress tolerance[J]. Journal of Integrative Plant Biology, 2010, 47(5): 613-621. |
| [31] |
Yamada A, Sekiguchi M, Mimura T, et al. The role of plant CCTα in salt- and osmotic-stress tolerance[J]. Plant & Cell Physiology, 2002, 43(9): 1043-1048. |





