布鲁菌病是全球性人畜共患传染病,可引发家畜(猪、羊和牛)发热、流产及死亡,对农牧经济造成重大的损失并严重威胁人类的健康[1-2]。Rev.1、S19等减毒菌株是目前可用于控制动物布氏杆菌病的有效疫苗之一,但减毒疫苗存在一定的风险,安全性差[3]。布鲁菌抗原在激活宿主免疫时,特别是天然免疫的水平较低,不能形成稳定的免疫保护,因此提高蛋白免疫保护水平成为布鲁菌亚单位疫苗的热点[4]。Denoel等[5]研究表明胞间质结合蛋白(P39)作为T细胞免疫布鲁菌抗原可诱导Th1导向型的免疫反应,具有较高的免疫原性,因此P39成为很有前景的亚单位候选抗原。
近年来通过糖基化修饰改变蛋白质的生物学活性,提高蛋白免疫保护水平在疫苗领域备受关注,已有部分疫苗应用于临床[6-8]。有研究表明,通过糖基化修饰后的蛋白可激活宿主TLR4受体系统,提高宿主细胞天然免疫水平,从而提高抗原的免疫保护作用[9]。
本研究选取可进行糖基化修饰的毕赤酵母表达系统[10],对布鲁菌优势抗原蛋白P39进行分泌表达,探究其修饰后对巨噬细胞吞噬的影响。为进一步研究糖基化影响蛋白免疫原性的机理,开发新型糖基化布鲁菌亚单位疫苗提供理论和实验依据。
1 材料与方法 1.1 材料大肠杆菌Escherichia coli TOP10株购自全式金生物公司(北京,中国)毕赤酵母P. pastoris GS115由山东大学微生物实验室惠赠(山东,中国)、pPICZαA真核表达载体购自Invitrogen公司(长春,中国)、布鲁菌(B.melitensis 16M)DNA由军事医学科学院军事兽医研究所提供。
ExTaq DNA聚合酶、T4 DNA ligase、EcoR Ⅰ、Not Ⅰ、Sac Ⅰ、DNA marker均为TaKaRa公司产品(长春,中国),Zeocin为Invitrogen公司产品(长春,中国);Protein Find Anti-His Mouse Monoclonal Antibody、Protein Find Goat Anti-Mouse IgG(H+L),HRP Conjugate购自全式金公司(北京,中国)。PNGaseF糖苷酶购自NEB公司(上海,中国);PVDF膜、滤纸购自promega公司(上海,中国),引物合成及基因测序由上海华大基因有限公司完成(上海,中国)。
1.2 方法 1.2.1 毕赤酵母真核表达载体pPICZαA-P39的构建根据GenBank公布的Brucella melitensis 16M(Ge-nBank Accession ID:WP:087932960)序列,应用DMAMAN及primer 5.0基因分析软件,设计扩增P39基因序列,以布鲁菌基因组为模板进行PCR扩增。上游引物序列gaattc(EcoR Ⅰ)ATGGCACCTGT-TGCCAATGC,下游引物序列gcggccg(Not Ⅰ)TTTT-GCGGCTTCAACCGCC。将胶回收的PCR扩增产物P39基因与pPICZα-A质粒用Eco RⅠ、Not Ⅰ进行双酶切,将酶切后的P39基因片段用T4DNA连接酶连接pPICZα-A载体上,热激法转化大肠杆菌TOP 10感受态细胞中。经双酶切鉴定正确后送上海华大基因有限公司测序。
1.2.2 重组蛋白P39的诱导表达挑取生长在Zeocin抗性YPD平板上的阳性单菌落,接种于5 mL的BMGY液体培养基中,在50 mL三角瓶中培养,28℃、250 r/min摇床培养16-20 h,至OD600值约为2.0-4.0,此时酵母菌处于对数生长期。离心收集菌液,6 000 r/min,4℃离心,收集沉淀,重悬于5 mL的BMMY液体培养基,转入50 mL的BMMY液体培养基中,250 mL三角瓶继续震荡培养。每隔24 h加入1%的甲醇进行诱导表达。同时电转化空载体pPICZαA的GS115菌株作为阴性对照。培养96 h后收集样品,10 000 r/min,4℃离心2 min,取上清进行SDS-PAGE分析蛋白的表达情况。
1.2.3 重组蛋白P39的纯化将收集好的上清液进行真空冻干,10 mmol/L,pH 7.4的磷酸盐溶液(PBS)透析48 h,0.22 μm无菌过滤器过滤,利用Sephacryl S-100蛋白层析纯化柱纯化,20 mmol/L NaCl洗脱蛋白,每管3 mL,Nanodrop在280 nm处检测吸光值,SDS-PAGE鉴定各层析成分。
1.2.4 蛋白P39免疫印迹实验(Westen blot)鉴定通过Western blotting检验纯化后的重组目的蛋白。SDS-PAGE后100 V恒压转膜55 min。用5%脱脂奶粉室温封闭2 h,TBST漂洗3次,加入1:1 000稀释的抗his标签鼠单克隆抗体,37℃孵育45 min,TBST漂洗3次后,加入1:1 000稀释的HRP标记的羊抗鼠IgG抗体,室温孵育45 min,TBST漂洗3次后用DAB显色试剂盒进行显色(购自sigma公司),观察目的条带并记录结果。
1.2.5 发酵条件对蛋白表达量的影响 1.2.5.1 pH值对重组蛋白P39表达量的影响取阳性重组菌以1%的接种量分别接入pH值分别为3.0、5.0、6.0、8.0的200 mL BMGY培养基中,盐浓度0.05 M,28℃摇床培养,至OD600值为0.6-0.8时,1%甲醇诱导72 h。
1.2.5.2 磷酸盐浓度对重组蛋白P39表达量的影响取阳性重组菌以1%的接种量分别接入磷酸盐浓度分别为0.02 mol/L、0.05 mol/L、0.1 mol/L和0.2 mol/L的BMGY培养基进行培养,pH 6.0,OD600值为0.6-0.8时,1%甲醇诱导72 h。
1.2.5.3 甲醇浓度对重组蛋白P39表达量的影响取阳性重组菌以1%的接种量BMGY培养基中,28℃摇床培养,盐浓度0.05 mol/L,pH 6.0,OD600值为0.6-0.8时,分别以0.5%、1%、2%和3%不同浓度的甲醇诱导72 h。
1.2.5.4 诱导时间对重组蛋白P39表达量的影响取阳性重组菌以1%的接种量BMGY培养基中,28℃摇床培养,盐浓度0.05 mol/L,pH 6.0,OD600值为0.6-0.8时,以1%浓度的甲醇分别诱导24 h、48 h、72 h和96 h。
1.2.5.5 NanoDrop检测蛋白浓度以100 μg/mL牛血清白蛋白作为对照,对目的蛋白进行蛋白浓度标定。
1.2.6 酵母分泌表达的P39蛋白糖基化鉴定将纯化后10 μg的真核蛋白加入1 μL糖蛋白变性缓冲液,总体积10 μL。100℃变性10 min,加入2 μL的glycobuffer,10% NP-40和1 μL的PNGaseF糖苷酶,37℃,孵育1 h。500 MHz核磁共振氢谱检测重组P39蛋白糖基化修饰水平。
1.2.7 巨噬细胞RAW264.7吞噬荧光抗原实验将FITC与真核蛋白及原核蛋白进行混合反应,在4℃避光反应18 h后收集样品。复苏RAW264.7巨噬细胞后将其以105个每孔接种于24孔板中,加入FITC标记的真核蛋白和原核蛋白,PBS作为空白对照组,荧光显微镜观察巨噬细胞吞噬抗原蛋白情况,分别记录4 h、6 h不同时间巨噬细胞吞噬蛋白情况。
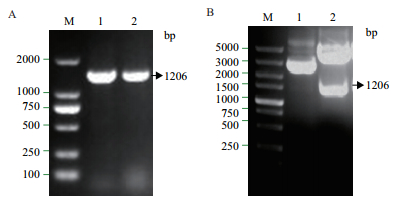
2 结果 2.1 构建真核表达载体pPICZαA-P39DNA核酸电泳显示成功构建pPICZαA-P39真核表达载体,电转化后挑选出的阳性菌株。条带大小与理论的片段大小一致为1 206 bp,如图 1所示。
|
| 图 1 真核表达载体pPICZαA-P39的构建 A:重组pPICZαA-P39质粒PCR(M:2000Marker;1-2:P39基因);B:重组质粒pPICZαA-P39酶切鉴定(M:2000Marker;1:重组质粒pPICZαA-P39;2:重组质粒pPICZαA-P39双酶切) |
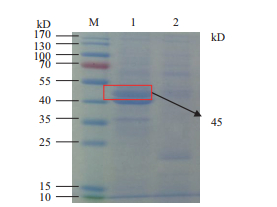
甲醇诱导阳性转化子表达,SDS-PAGE检测P39蛋白的表达,目的条带在45 kD处,如图 2。目的蛋白条带与理论值大小一致,纯化后的蛋白纯度较好,高效液相色谱检测纯化蛋白纯度,纯度可达93.77%,如图 3和图 4所示。经Western blot免疫印迹法检测确定该蛋白为P39蛋白,特异性良好,如图 5所示。
|
| 图 2 SDS-PAGE分析重组蛋白在毕赤酵母中的表达 M:蛋白相对分子质量标准;1:诱导后重组P39蛋白;2:诱导后空载体pPICZαA菌株 |

|
| 图 3 纯化后重组蛋白P39 M:蛋白相对分子质量标准;1-2:纯化后的重组P39蛋白 |

|
| 图 4 高效液相色谱(HPLC)检测纯化蛋白纯度 |

|
| 图 5 重组蛋白P39 western blot鉴定 M:蛋白相对分子质量标准;1-3:重组蛋白P39特异性条带;4:阴性对照 |
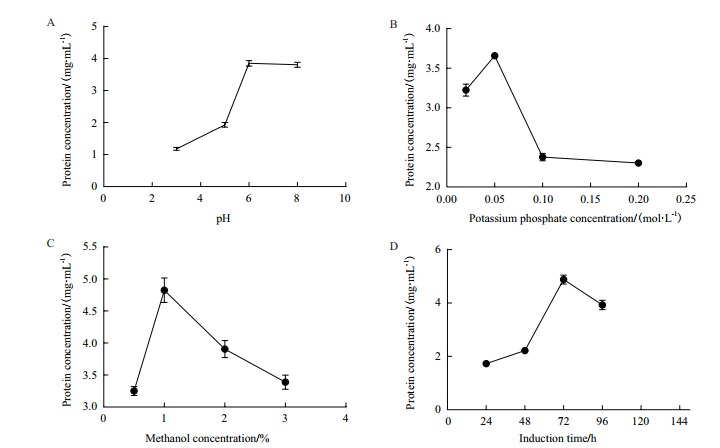
由图 6-A可以看出,蛋白得率随pH的升高先增高后降低,当pH至为6时,蛋白的得率最高,实验表明该重组蛋白在酸性或弱碱性的条件下表达条件较好,所以,最佳的发酵pH 6左右,最高得率为3.86 mg/mL。
|
| 图 6 不同因素对P39蛋白表达量的影响 A:不同pH值对P39蛋白表达的影响;B:不同磷酸钾盐浓度P39对蛋白表达的影响;C:不同浓度甲醇诱导对P39蛋白的影响;D:不同诱导时间对P39蛋白表达的影响 |
由图 6-B可见,随磷酸钾浓度的升高蛋白得率降低,在磷酸钾浓度为0.05 mol/L时,蛋白得率最高,过高的盐浓度可能会抑制蛋白的表达,所以,最佳的磷酸钾浓度为0.05 mol/L,最高得率为3.64 mg/mL。
2.3.3 甲醇浓度对重组蛋白P39表达量的影响由图 6-C可见,随甲醇诱导浓度的增加蛋白得率先增加后减少,在甲醇浓度1%时,蛋白得率最高,低浓度和高浓度的甲醇对蛋白的表达都有不利影响,最佳的甲醇诱导浓度1%,最高得率为4.96 mg/mL。
2.3.4 诱导时间对重组蛋白P39表达量的影响由图 6-D可见,随诱导时间的增加,蛋白得率出现先增加后下降的趋势,过长时间的诱导不利于目的蛋白的表达,实验表明,诱导72 h的条件下,长时间的诱导可能导致蛋白降解,所以,72 h蛋白得率最高,最高得率为5.05 mg/mL。
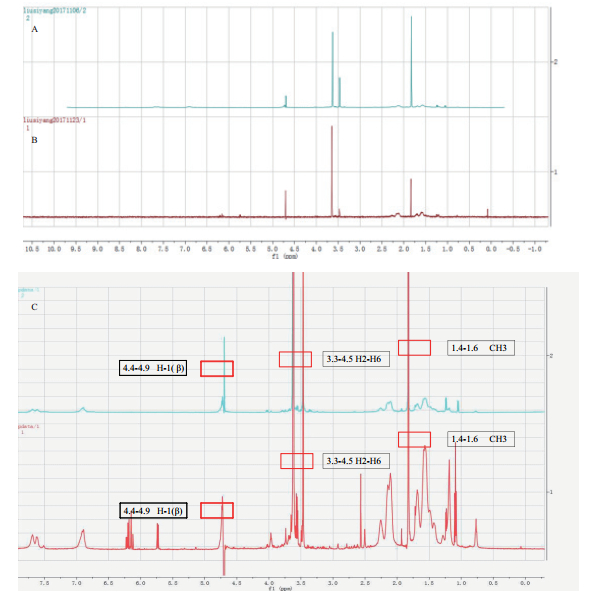
2.4 酵母分泌表达的P39蛋白糖基化鉴定本研究对酵母表达的P39蛋白和利用PNGaseF糖苷酶酶解的P39蛋白利用核磁共振氢谱进行了糖基化修饰分析,结果(图 7-C)表明,重组蛋白图谱在3.6-3.8 ppm处出现寡糖H信号,说明在纯化后的重组蛋白上存在糖信号,重组后的P39蛋白在毕赤酵母中发生糖基化修饰。同时利用PNGaseF糖苷酶酶解蛋白N-糖链后的重组P39蛋白糖信号未消失,P39蛋白存在潜在的糖基化修饰位点,但酶解后糖信号仍然存在,说明蛋白的糖基化形式不是理论上N-糖修饰类型,毕赤酵母表达系统对蛋白的糖基化修饰主要表现为N-糖修饰和O-糖修饰两种类型,综合上述结果表明该重组P39蛋白的糖基化形式可能是O-糖基化修饰[11-12]。
|
| 图 7 一维核磁共振氢谱(1H NMR)分析蛋白糖基化 A:PNGaseF糖苷酶酶解重组蛋白P39后核磁共振氢谱;B:重组蛋白P39核磁共振氢谱;C:对比A和B核磁共振氢谱 |
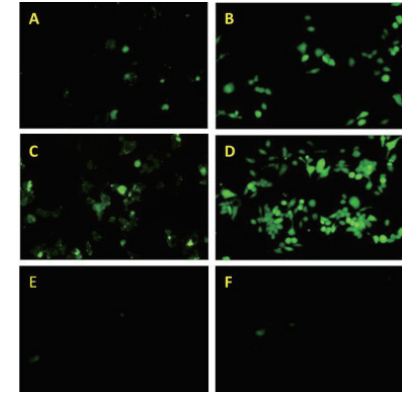
荧光显微镜观察实验结果显示,两种蛋白在2 h开始出现荧光,荧光强度随时间呈现增强趋势,真核蛋白出现荧光效果早于原核蛋白,在6 h时荧光现象明显,PBS空白对照组未见明显荧光细胞。根据图 8显示,巨噬细胞吞噬真核蛋白的荧光强度明显优于吞噬原核蛋白。说明糖修饰对巨噬细胞的吞噬作用具有一定的影响,可增强蛋白的免疫原性[13]。
|
| 图 8 检测巨噬细胞吞噬荧光蛋白情况 A:原核P39蛋白4 h吞噬荧光情况;B:原核P39蛋白6 h吞噬荧光情况;C:真核P39蛋白4 h吞噬荧光情况;D:真核P39蛋白6 h吞噬荧光情况;E:PBS组4 h空白对照;F:PBS组6 h空白对照 |
布鲁菌进入宿主细胞之后,可被宿主免疫系统分解,同时释放细胞质结合蛋白,这些蛋白质分子继续发挥免疫刺激与侵染的作用[14]。P39蛋白是布鲁菌优势抗原,其蛋白可以有效地诱导机体产生特异性免疫应答,而且P39基因在多个不同种型布鲁菌中高度保守,该成分可以在不同的布鲁菌中形成交叉保护作用,用于制备的新型布病疫苗具有较大优势[15-16]。近年许多研究表明,糖基化对蛋白的结构和活性有很大的影响,消除N-糖基化位点可延长IFN-α/Fc融合蛋白的半衰期[17],糖链长短的变化及不同糖型的修饰都会影响蛋白的生物活性[18-19],本课题组发现甘露六糖修饰后的布鲁菌AHCY蛋白的免疫性得到大幅度的提升[20],说明糖修饰会改变蛋白的生物功能,这为开发安全有效的布鲁氏菌亚单位疫苗提供了可能。
本实验中,为获得大量P39抗原,选择具有分泌优势的毕赤酵母表达系统,并在酵母体内对P39抗原蛋白进行天然的糖基化修饰。结果发现,糖基化后的P39蛋白更容易被巨噬细胞捕获,与原核表达的P39蛋白相比,其结合巨噬细胞的效率更好,也更有可能高效的激活巨噬细胞。重组后的P39蛋白显示出优于原核P39蛋白的免疫原性,这可能是由于糖链的存在及其结构引发的改变,在P39蛋白的理论N-端糖基化位点并为发生修饰作用,说明糖基化的修饰可能存在随机性,或是由于蛋白空间结构折叠后掩盖其理论的糖基化位点,使其潜在的糖基化位点未进行修饰。随着基因工程的发展,已经实现了在分子水平对酵母糖基化系统进行改造,从而更有利于生产人源糖蛋白药物及亚单位疫苗的开发[21-22]。
4 结论本研究成功在毕赤酵母中分泌表达P39抗原,优化发酵条件产量可达5.05 g/L,通过核磁共振氢谱结果表明P39抗原发生糖基化修饰,糖基化修饰后的P39抗原被巨噬细胞捕获的程度明显高于原核蛋白,说明糖基化修饰作用会在一定程度上影响蛋白的免疫原性。
| [1] |
Almariri A, Mahmoud NH, Hammoud R. Efficacy evaluation of live Escherichia coli expression Brucella P39 protein combined with CpG oligodeoxynucleotides vaccine against Brucella melitensis 16M, in BALB/c mice[J]. Biologicals, 2012, 40(2): 140. DOI:10.1016/j.biologicals.2012.01.002 |
| [2] |
Cannella AP, Tsolis RM, Li L, et al. Antigen-specific acquired immunity in human brucellosis:implications for diagnosis, prognosis, and vaccine development[J]. Frontiers in Cellular & Infection Microbiology, 2012, 2(2): 1. |
| [3] |
Scharp DW, al Khalaf SA, al Muhanna MW, et al. Use of mass vaccination with a reduced dose of REV 1 vaccine for Brucella melitensis control in a population of small ruminants[J]. Tropical Animal Health & Production, 1999, 31(3): 135. |
| [4] |
王真, HAN Gilsu, 吴清民. 动物布鲁菌病疫苗的来历及亚单位疫苗的研究概况[J]. 中国农业大学学报, 2014, 19(3): 169-174. |
| [5] |
Denoel PA, Vo TK, Weynants VE, et al. Identification of the major T-cell antigens present in the Brucella melitensis B115 protein preparation, Brucellergene OCB[J]. Journal of Medical Microbiology, 1997, 46(9): 801-806. DOI:10.1099/00222615-46-9-801 |
| [6] |
仲娜, 郝林华, 王小如. 糖蛋白药物的研究进展[J]. 中国新药杂志, 2005, 14(12): 1400-1403. DOI:10.3321/j.issn:1003-3734.2005.12.008 |
| [7] |
严钦, 俞慧清, 成国祥. 蛋白糖基化与免疫研究进展[J]. 现代免疫学, 2008, 28(2): 168-168. |
| [8] |
Durocher Y, Butler M. Expression systems for therapeutic glycopro-tein production[J]. Current Opinion in Biotechnology, 2009, 20(6): 700. DOI:10.1016/j.copbio.2009.10.008 |
| [9] |
许博然. TLR2和TLR4受体封闭肽对小鼠腹腔巨噬细胞细胞因子分泌的影响[D].呼和浩特: 内蒙古农业大学, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10129-1017212545.htm
|
| [10] |
Love KR, Shah KA, Whittaker CA, et al. Comparative genomics and transcriptomics of Pichia pastoris[J]. BMC Genomics, 2016, 17(1): 550. DOI:10.1186/s12864-016-2876-y |
| [11] |
Chaffey PK, Guan X, Chen C, et al. Structural Insight into the stabilizing effect of O-glycosylation[J]. Biochemistry, 2017, 56(23): 2897. DOI:10.1021/acs.biochem.7b00195 |
| [12] |
田媛, 张尊建. 糖类结构的核磁共振波谱及质谱分析[J]. 药学进展, 2003, 27(2): 78-80. DOI:10.3969/j.issn.1001-5094.2003.02.004 |
| [13] |
蒋春霞. Rab6在小鼠巨噬细胞RAW264. 7吞噬过程中的作用[D].杭州: 浙江大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10335-1013339816.htm
|
| [14] |
毛景东, 王景龙, 杨艳玲. 布鲁菌病的研究进展[J]. 中国畜牧兽医, 2011, 38(1): 222-227. |
| [15] |
Christopher S, Umapathy BL, Ravikumar KL. Brucellosis:Review on the recent trends in pathogenicity and laboratory diagnosis[J]. Journal of Laboratory Physicians, 2010, 2(2): 55. DOI:10.4103/0974-2727.72149 |
| [16] |
Blasco JM, Molina-Flores B. Control and Eradication of Brucella melitensis infection in sheep and goats[J]. Macedonian Academy of Sciences and Arts, Section of Biological and Medical Sciences, 2010, 31(1): 145-65. |
| [17] |
Hao J, Guo Y, Song X, et al. Elimination of N-glycosylation by site mutation further prolongs the half-life of IFN-α/Fc fusion proteins expressed in Pichia pastoris[J]. Microbial Cell Factories, 2016, 15(1): 209. DOI:10.1186/s12934-016-0601-9 |
| [18] |
Wang W, Lu B, Zhou H, et al. Glycosylation at 158N of the hemagglutinin protein and receptor binding specificity synergistically affect the antigenicity and immunogenicity of a live attenuated H5N1 A/Vietnam/1203/2004 vaccine virus in ferrets[J]. Journal of Virology, 2010, 84(13): 6570. DOI:10.1128/JVI.00221-10 |
| [19] |
Hossler P, Chumsae C, Racicot C, et al. Arabinosylation of recombinant human immunoglobulin-based protein therapeutics[J]. Mabs, 2017, 9(4): 715. DOI:10.1080/19420862.2017.1294295 |
| [20] |
许春晓.糖基化修饰对蛋白Rsα、AhcY免疫原性影响的研究[D].长春: 吉林农业大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10193-1016732706.htm
|
| [21] |
Ratanji KD, Derrick JP, Dearman RJ, et al. Immunogenicity of therapeutic proteins:Influence of aggregation[J]. Journal of Immunotoxicology, 2014, 11(2): 99. DOI:10.3109/1547691X.2013.821564 |
| [22] |
Mahan AE, Jennewein MF, Suscovich T, et al. Antigen-specific antibody glycosylation is regulated via vaccination[J]. PLoS Pathogens, 2016, 12(3): e1005456. DOI:10.1371/journal.ppat.1005456 |




