2. 国家食品质量安全监督检验中心,北京 100094
2. China National Food Safety Supervision and Inspection Center, Beijing 100094
铜绿假单胞菌(Pseudomonas aeruginosa)也称绿脓杆菌,属于假单胞菌属,革兰氏阴性菌,是一种重要的水源和食源性致病菌[1],广泛分布在自然界中,如水、土壤及空气中均有存在,能引起伤口、呼吸道以及泌尿道感染,甚至会引起败血症[2-3]。铜绿假单胞菌耐药能力强,在治疗时往往需要使用多种抗生素进行联合用药,但也不能保证将其完全根除。因此,如何快速而准确地鉴定出铜绿假单胞菌对保障食品安全具有重要的意义[4-9]。据世界卫生组织(WHO)统计,人类70%-80%的疾病都来源于不洁净的饮用水[10-11]。瓶装矿泉水中铜绿假单胞菌污染情况分析日渐受到重视。近年来,国内外均有在水源水或成品水中检出铜绿假单胞菌的报道[10, 12-17],甚至多批次样品的铜绿假单胞菌检出率大于10%[11]。
目前,国家标准GB 8538-2016天然矿泉水检验方法和GB/T7918.4-1987化妆品微生物标准检验方法中分别规定了矿泉水中铜绿假单胞菌的检验方法和化妆品种铜绿假单胞菌的检验方法[18-19]。VITEK 2 Compact全自动细菌鉴定系统用于微生物鉴定的准确率高,可用于微生物实验室的日常检测工作[20-21]。但根据日常检验工作经验,按照GB 8538.57-2016天然矿泉水中铜绿假单胞菌检验方法分离得到的部分阳性菌株,采用VITEK 2 Compact全自动细菌鉴定及药敏分析系统进行鉴定后为假阳性或假阴性。按照GB/T7918.4-1987化妆品微生物标准铜绿假单胞菌检验方法进行检验,同样会出现错误检验结果。
本实验以VITEK 2 Compact全自动细菌鉴定系统鉴定结果为参考,对GB 8538.57-2016天然矿泉水中铜绿假单胞菌检测方法和GB/T 7918.4-1987化妆品微生物标准检验方法中绿脓杆菌的检测方法进行分析与比较,研究并优化现行国家标准GB 8538.57-2016天然矿泉水中铜绿假单胞菌的检验方法,旨在提高日常样品检测的准确度。
1 材料与方法 1.1 材料 1.1.1 试验菌株(1)标准菌株:铜绿假单胞菌ATCC 27853(BZ-33)与杀鲑气单胞菌CICC 23564(BZ-34)为中国工业微生物菌种保藏中心保藏菌种,支气管炎博德特菌CGMCC 1.2418(BZ-38)、荧光假单胞菌CGMCC 1.0867(BZ-41),以及恶臭假单胞菌CGMCC 1.2309(BZ-42)为中国普通微生物菌种保藏管理中心保藏菌种,其中铜绿假单胞菌作为阳性对照,其余菌株为阴性对照。(2)实验室保藏菌株:YP-129、YP-131、YP-132、YP-141、YP-143、YP-170、YP-171、YP-190、YP-249、YP-250、YP-251、YP-252、YP-253、YP-254、YP-255、YP-256、YP-257、YP-258、YP-259、YP-260、YP-261及YP-269,22株实验室保藏菌株均分离自矿泉水,保藏菌种前初次乙酰胺试验结果均为阳性。
1.1.2 主要试剂及耗材假单胞菌琼脂基础培养基(CN琼脂)、营养琼脂斜面培养基、血琼脂平板、SCDLP液体培养基、十六烷三甲基溴化铵培养基、绿脓菌色素测定用培养基、金氏B培养基(King’s B)、明胶培养基、乙酰胺肉汤、氧化酶试剂、钠氏试剂、革兰氏染色液、生理盐水(0.45% NaCl和0.85% NaCl)等,以上试剂购买自北京陆桥技术有限公司。GN TEST革兰氏阴性杆菌鉴定卡与GP TEST革兰氏阳性杆菌鉴定卡购于北京威泰科生物技术有限公司、0.45 μm滤膜购于PEEL CORNER公司。
1.2 方法 1.2.1 菌株的活化将-80℃冻存的5株标准菌株与22株实验菌株划线接种于营养琼脂斜面上,36℃培养24 h,连续传代2-3次,得到活化菌株。
1.2.2 梅里埃VITEK 2 Compact全自动细菌鉴定系统鉴定方法(1)把活化好的菌株接种至血琼脂平板,36℃培养18 h,有刺激性味道、多数有溶血现象、边缘不整齐的墨绿色菌落或者扁圆形灰白色菌落为可疑菌落;(2)将可疑菌落进行革兰氏染色,普通光学显微镜下观察染色结果与菌体形态,根据结果准备相应的鉴定卡类型;(3)用无菌棉拭子挑取血平板上活性良好的待测菌落,将3 mL 0.45% NaCl溶液加入一次性悬浮液管,用生理盐水调配至麦氏浓度0.6左右,在真空填充舱内填充至革兰氏阴性杆菌鉴定卡或革兰氏阳性杆菌鉴定卡,采用梅里埃VITEK 2 Compact全自动细菌鉴定系统鉴定。
1.2.3 GB 8538.57-2016天然矿泉水中铜绿假单胞菌检验方法(1)将1.2.1得到的活化菌株与矿泉水混匀制备102 CFU/mL待测水样(因为人工污染水样,菌浓高于实际样品,省略掉GB 8538-2016中水样过滤操作)。(2)吸取1 mL待测水样至无菌平皿中,与冷却好的CN琼脂培养基混匀,(36±1)℃培养。(3)培养24 h和48 h后观察菌落的生长情况。计数所有显蓝色或绿色(绿脓菌素)疑似铜绿假单胞菌的菌落,并进行绿脓菌素确证性试验。在紫外线下检查所有发光不产绿脓菌素疑似铜绿假单胞菌菌落,并进行乙酰胺肉汤确证试验。将其它所有红褐色不发荧光的菌落进行氧化酶测试、乙酰胺液体培养基、金氏B培养基确证性试验。(4)确证性试验:营养琼脂;氧化酶试验;金氏B培养基;绿脓菌素试验;乙酰胺液体培养基产氨试验[18]。
1.2.4 GB/T 7918.4-1987化妆品微生物标准检验方法(1)取1 mL的1.2.3待测水样接种到体积为99 mL的SCDLP液体培养基中(因人工污染样品,加样体积区别于GB/T7918.4-1987),置于36℃下进行培养24 h;观察培养液颜色是否为黄绿色或蓝绿色以及培养液的表面是否有一层薄薄的菌膜;(2)挑取一环培养物,划线接种于十六烷三甲基溴化铵琼脂平板上,(36±1)℃培养24 h;(3)在非选择性培养基上挑取活性良好的可疑菌落进行涂片,并进行革兰氏染色,革兰氏阴性菌的可疑菌落需进行氧化酶实验;(4)氧化酶试验;(5)绿脓菌素试验操作;(6)硝酸盐还原产气试验;(7)明胶液化试验;(8)42℃生长试验[19]。
1.2.5 对GB 8538.57-2016铜绿假单胞菌检测方法的优化结合几种方法的测定原理与结果对GB 8538.57-2016铜绿假单胞菌检测方法进行优化,并且应用优化后的方法对27株试验菌株进行验证试验。
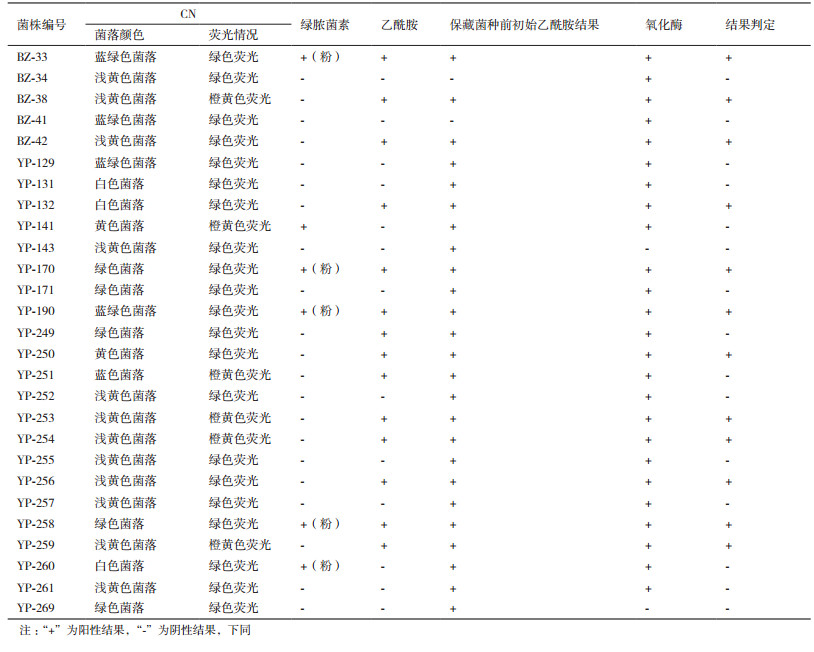
2 结果 2.1 梅里埃VITEK 2 Compact全自动细菌鉴定系统鉴定结果5株标准菌株与22株实验室保藏菌株经革兰氏染色,结果全部为阴性,采用VITEK 2 Compact全自动细菌鉴定系统鉴定结果如表 1所示。VITEK 2 Compact全自动细菌鉴定系统对5株标准菌株的鉴定结果符合率为100%,其中BZ-33为铜绿假单胞菌(Ps. Aeruginosa,94%),其余22株保藏菌株中YP-141(98%)、YP-170(97%)、YP-190(97%)、YP-249(99%)以及YP-258(97%)鉴定为铜绿假单胞菌,全部27株菌株中阳性菌株为6株,检出率为22.2%。阴性菌株为21株。以VITEK 2 Compact对所有标准菌株和试验菌株的鉴定结果作为其它两种检验方法检验结果的参考。
以VITEK 2 Compact鉴定结果作为检验结果的参考,27株试验菌株采用GB 8538.57-2016天然矿泉水中铜绿假单胞菌检验,检验结果如表 2所示,12株菌检测为铜绿假单胞菌阳性,阳性检出率为44.4%。假阳性的菌有8株,分别是BZ-38、BZ-42、YP-132、YP-250、YP-253、YP-254、YP-256、YP-259,假阳性检出率为29.6%。假阴性的菌株有2株,YP-141和YP-249,假阴性的检出率为7.4%。结果表明GB 8538.57-2016中铜绿假单胞菌的检验方法对铜绿假单胞菌检验结果的准确率较低。
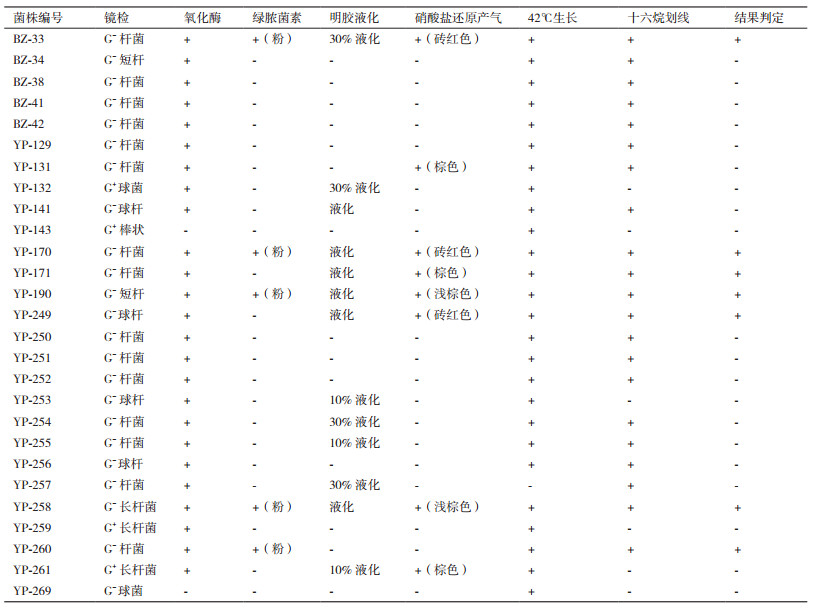
27株试验菌株采用GB/T 7918.4-1987化妆品微生物标准检验方法绿脓杆菌(铜绿假单胞菌)检验,结果如表 3所示,阳性检出率为26%。假阳性的菌株有2株,YP-171和YP-260。假阴性的菌株有1株,YP-141。假阳性的检出率为7.4%。假阴性的检出率为3.7%。结果表明GB/T 7918.4-1987检验方法对铜绿假单胞菌检验结果的准确度存在一定的误差,但是检验准确率高于GB 8538.57-2016方法。
综合3种对铜绿假单胞菌的检验程序与相应的检验结果,对其检验方法进行适当改进,以GB 8538. 57-2016矿泉水中铜绿假单胞菌检测方法为例,改进后的检验程序如图 1所示。检验程序中主要增加了3步:(1)将CN平板上生长出的蓝绿色菌落、360 nm紫外灯下产荧光(非蓝绿)菌落,转接到血琼脂平板36±1℃培养24-48 h并计数;(2)将可疑菌落进行革兰氏染色,镜检,铜绿假单胞菌为革兰氏阴性杆菌;(3)对血平板所有可疑菌落进行绿脓菌素试验。结果判定时菌体同时满足革兰氏阴性杆菌、氧化酶阳性、乙酰胺产氨阳性及绿脓菌素阳性,判定为铜绿假单胞菌阳性,其余反应为阴性。
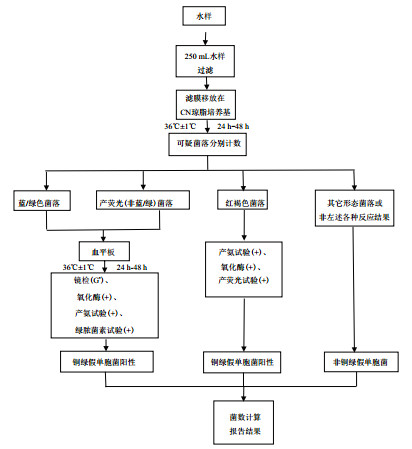
|
| 图 1 改进后的矿泉水中铜绿假单胞菌检验程序 |
采用改进后的GB 8538. 57-2016矿泉水中铜绿假单胞菌检测方法对27株试验菌株进行验证试验,试验结果如表 4所示,改进后的方法结果判定BZ-33、YP-141、YP-170、YP-190、YP-249及YP-258为铜绿假单胞菌阳性,全部27株菌株中阳性菌株为6株,检出率为22.2%,与VITEK 2 Compact的鉴定结果完全一致。
VITEK 2 Compact全自动微生物生化鉴定仪(包括药敏测试)是法国生物梅里埃公司推出的智能系统。适合用于微生物实验室的日常检测工作。该系统能简化日常复杂的生化实验操作,曾写进中华人民共和国国家标准GB/T4789-2016中,如GB/T4789.4-2016沙门氏菌中的生化鉴定[22]。孙燕萍等[23]采用VITEK 2 Compact全自动微生物分析系统仪对无锡市常见12种224株食源性致病微生物的鉴定结果与API鉴定系统鉴定结果的总体符合率为99.6%(223/224);何艳霞等[24]采用16S rRNA和rpoB基因序列分析在铜绿假单胞菌鉴定中的应用,用表型分类方法对VITEK自动微生物鉴定系统鉴定为铜绿假单胞菌的23株分离株进行再鉴定,结果表明表型再鉴定结果与自动微生物鉴定系统鉴定结果一致。宋逸萍等[25]研究发现VITEK 2 Compact对铜绿假单胞菌鉴定准确率在98%以上。但条件一般的检测机构,尤其偏远地区的不具备VITEK 2 Compact全自动微生物生化鉴定仪,采用其对样品鉴定的试验条件要求较高。基于VITEK 2 Compact的鉴定结果准确度高的原因,本实验选用VITEK 2 Compact全自动微生物生化鉴定仪鉴定结果作为其它检测方法的结果参照标准。
用GB 8538.57-2016矿泉水中铜绿假单胞菌检验方法的检测结果中与VITEK 2 Compact结果相比,假阳性的检出率为29.6%,分析原因是这8株菌在CN培养基上生长出黄色菌落,是产荧光(非蓝绿色)的菌落并且乙酰胺实验结果为阳性,依标准被判定为阳性检出铜绿假单胞菌。假阴性的检出率为7%,分别是YP-141和YP-249。一般阳性菌株的荧光多为绿色或黄色,与绿脓菌素的颜色相近。YP-249的菌株实验结果表现异常,分析为该菌为蓝绿色菌落并且绿脓菌素实验阴性,被判定为阴性未检出铜绿假单胞菌,然而乙酰胺试验和氧化酶试验均为阳性,符合铜绿假单胞菌的生化特性。因此,单纯根据GB 8538.57-2016中所设计的生化实验判定铜绿假单胞菌检验结果明显准确度不高。另外,所有参与试验的菌株在CN上的菌落颜色均无红褐色,故实验没有进行接种金氏B琼脂培养基的步骤,金氏B产荧光实验是不是判定阳性结果的必要条件,这一结论还需要实验的进一步验证。
综上所述,CN琼脂培养基上生长出蓝(绿)菌落加绿脓菌素试验和CN琼脂培养基上生长出的黄色产荧光菌落加乙酰胺试验的生化特性并不足以保证其结果的准确性。因此,标准GB 8538-2016中的试验方法是不严谨的,需要设计相应的补充生化实验进行验证。
采用GB/T 7918.4-1987中铜绿假单胞菌的检验结果中假阳性的菌株有2株,YP-171和YP-260,假阴性的菌株有1株,YP-141。十六烷三甲基溴化铵是标准中所规定的作为化妆品受测试样品增菌后的筛选分离培养基。实验是用实验室保藏的纯菌种进行检测,菌株增菌之后,划线于十六烷三甲基溴化胺琼脂,经培养观察,即便是标准菌株BZ-33在此培养基上生长状况不是很好。而此法的假阳性检测数量明显低于GB 8538.57-2016,分析原因为十六烷三甲基溴化胺琼脂选择性较强,同样因此出现了假阴性结果。
基于GB 8538.57-2016和GB/T 7918.4-1987检测方法的程序与实验判定不足,以GB 8538.57-2016天然矿泉水检验方法中铜绿假单胞菌检测方法为例,改进了检测方法,改进后的检测方法避免了单纯某种生化反应造成的结果误判,对27株试验菌株进行鉴定与鉴定仪的结果完全相符。产品检验方法的准确性对企业和消费者都尤为重要。国家食品质量安全监督检验中心每年检验工作量巨大,2015年GB 19298-2014包装饮用水国家标准实施后,以往不需要做铜绿假单胞菌的纯净水、蒸馏水等样品也需要做5份铜绿假单胞菌的检验[26]。2016年本检验中心的矿泉水样品检测量约300份,样品总检测量约2 000份。2016年阳性检出率约为5%,用改进后方法检出率降低到3%。改进后的GB 8538.57-2016铜绿假单胞菌检测方法结果判定依据更严谨,结果更准确、试验条件要求低、相对操作简单易行。当然,这一方法还需要后续大量的检测试验去验证其可行性与准确性。
4 结论本研究改进了GB 8538.57-2016铜绿假单胞菌的检测方法,改进后的方法增加了血琼脂平板培养、革兰氏染色及镜检和对血平板所有可疑菌落进行绿脓菌素试验。用改进后的GB 8538-2016铜绿假单胞菌检测方法对27株试验菌株进行验证试验,检验结果与VITEK 2 Compact一致。
| [1] |
闻玉梅. 现代医学微生物学[M]. 上海: 上海医科大学出版社, 1999.
|
| [2] |
Murray PR. Manual of clinical microbiology[M]. 9th ed. Washin-gton DC: American Society for Microbiology, 2007, 1762-1766.
|
| [3] |
何艳霞, 向诗非, 李浇. 基于16S rRNA和rpoB基因的分子系统发育分析在铜绿假单胞菌鉴定中的应用[J]. 微生物学杂志, 2016, 36(4): 27-35. |
| [4] |
Zamberlan da Silva ME, Santana RG, Guilhermetti M, et al. Compa-rison of the bacteriological quality of tap water and bottled mineral water[J]. International Journal of Hygiene and Environmental Health, 2008, 211(5-6): 504-509. DOI:10.1016/j.ijheh.2007.09.004 |
| [5] |
Varga L. Bacteriological quality of bottled natural mineral waters commercialized inhungary[J]. Food Control, 2011, 22(3-4): 591-595. DOI:10.1016/j.foodcont.2010.10.009 |
| [6] |
龙春平, 吴周健, 周秀萍. 2001-2002年吉首市桶装饮用水卫生微生物学分析[J]. 实用预防医学, 2004, 11(1): 140-141. |
| [7] |
武景福, 王文委, 武和平. 三门峡市区2002-2006年生活饮用水微生物学指标监测结果分析[J]. 中国预防医学杂志, 2008, 9(4): 298-300. |
| [8] |
周黎, 朱玫, 陈依江, 等. 生活饮用水和水源水微生物检测结果分析[J]. 应用预防医学, 2011, 17(2): 102-104. |
| [9] |
张辉, 吴陈, 刘怀志, 等. 德阳市饮用水微生物污染情况调查[J]. 环境卫生学杂, 2011, 1(6): 23-25. |
| [10] |
魏磊, 吴清平, 张菊梅, 等. 矿泉水和山泉水中铜绿假单胞菌污染调查及分离菌株毒力基因与耐药性分析[J]. 微生物学通报, 2015, 42(1): 125-132. |
| [11] |
邓梅清, 张菊梅, 郭伟鹏, 等. 矿泉水中铜绿假单胞菌污染状况调查研究[J]. 中国卫生检验杂志, 2009, 19(11): 2672-2673. |
| [12] |
马群飞, 陈伟伟, 杨毓环, 等. 瓶装饮用纯净水铜绿假单胞菌污染情况调查[J]. 食品科学, 2000, 21(2): 50-53. |
| [13] |
Nagaveni S, Rajeshwari H, Oli AK, et al. Widespread emergence of multidrug resistant Pseudomonas aeruginosa isolated from CSF samples[J]. Indian Journal of Microbiology, 2011, 51(1): 2-7. DOI:10.1007/s12088-011-0062-0 |
| [14] |
Fuentefria DB, Ferreira AE, Corção G. Antibiotic-resistant Pseudomonas aeruginosa from hospital wastewater and superficial water:Are they genetically related?[J]. Journal of Environmental Management, 2011, 92(1): 250-255. DOI:10.1016/j.jenvman.2010.09.001 |
| [15] |
张永清, 吴清平, 彭飞艇, 等. 矿泉水中铜绿假单胞菌及溴酸盐污染情况分析[J]. 食品与生物技术学报, 2012, 31(10): 1046-1050. DOI:10.3969/j.issn.1673-1689.2012.10.006 |
| [16] |
潘虹, 杨臣, 魏晓雪, 等. 五大连池天然矿泉水水源微生物污染调查[J]. 中国卫生检验杂志, 2012, 22(8): 1946-1949. |
| [17] |
王爽, 侯配斌, 刘静, 等. 山东省2014年矿泉水中微生物检测及铜绿假单胞菌分离株脉冲场凝胶电泳分型[J]. 中国卫生检验杂志, 2015, 25(23): 4104-4105. |
| [18] |
中华人民共和国国家质量监督检验检疫总局. 中国国家标准化管理委员会. GB 8538-2016天然矿泉水检验方法. [S]. 北京: 中国标准出版社, 2016.
|
| [19] |
中国预防医学科学院环境卫生监测所. 化妆品微生物标准检验方法绿脓杆菌[S]. GB/T7918. 4-87. 北京: 中国标准出版社, 1987.
|
| [20] |
杨晶, 王伟欢. VITEK 2 Compact系统的应用及鉴定结果分析[J]. 中国卫生检验杂志, 2016, 26(18): 2643-2645. |
| [21] |
乔宁, 喻华, 殷琳, 等. VITEK 2 COMPACT全自动微生物分析仪性能分析[J]. 淮海医药, 2012, 30(3): 211-213. |
| [22] |
中华人民共和国卫生部. 中国国家标准化管理委员会. 食品卫生微生物学检验沙门氏菌检验[S]. GB4789. 4-2016. 北京: 中国标准出版社, 2016.
|
| [23] |
孙燕萍, 彭浩, 凌霞, 等. VITEK 2 Compact全自动微生物分析系统的应用及鉴定结果分析[J]. 现代预防医学, 2010, 37(20): 3891-3893. |
| [24] |
何艳霞, 向诗非, 李浇, 等. 基于16S rNA和rpoB基因的分子系统发育分析在铜绿假单胞菌鉴定中的应用[J]. 微生物学杂志, 2016, 36(4): 27-35. |
| [25] |
宋逸萍, 宛传丹, 马月琴, 等. VITEK 2 Compact高级专家系统对肠杆菌科及铜绿假单胞菌中β-内酰胺酶耐药表型鉴别能力分析[J]. 江苏大学学报, 2012, 22(1): 77-79. |
| [26] |
中华人民共和国国家卫生和计划生育委员会. GB 19298-2014包装饮用水. [S]. 北京: 中国标准出版社, 2014.
|